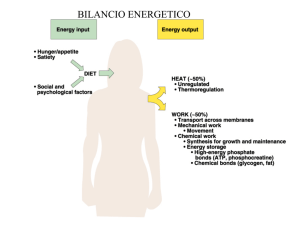
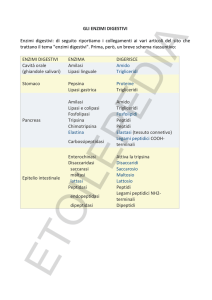
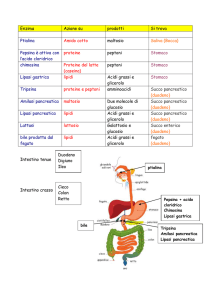
LIPASI
LIPASI
Cinetico Colorimetrico. Liquido.
Determinazione quantitativa della lipasi
Conservare a 2-8°C
IVD
PRINCIPIO DEL METODO
La lipasi pancreatica, in presenza di colipasi,desossicolato e ioni
calcio,idrolizza il substrato 1-2-O-dilauril-rac-glicero-3 ac.glutarico-6’metilresorufin)-estere,secondo la seguente serie di reazioni:
Lipasi
1-2-O-dilauril-rac-glicero-3 ac.glutar.-6’-metilresorufin)estere
1-2-O-dilauril-rac-glicerolo+Glutar-6’-metilresorufin-estere (instabile)
OH Acido glutarico + Metilresorufina
La velocità di formazione della Metilresorufina,misurata fotometricamente,
è proporzionale alla concentrazione catalitica della lipasi presente nel
campione.
SIGNIFICATO CLINICO
La Lipasi (LPS) è un enzima pancreatico necessario per l’assorbimento e la
digestione delle sostanze nutrienti, che catalizza l’idrolisi degli esteri di
glicerolo degli acidi grassi. La determinazione della LPS è utilizzata per la
diagnosi delle malattie del pancreas come la pancreatine acuta e cronica e
l’ostruzione del dotto pancreatico.
La diagnosi clinica non dovrebbe essere fatta sul risultato di un singolo
test;essa dovrebbe integrare i dati clinici e gli altri dati di laboratorio.
REAGENTI
R 1 Tampone
TRIS pH 8.3
Colipasi
Desossicolato
Taurodesossicolato
R 2 Substrato
Tartrato pH 4.0
Lipasi
Calcio Cloruro
Cal. Lipasi
40 mmol/L
> o = 1 mg/L
1.8 mmol/L
7.2 mmol/L
15 mmol/L
> 0.7mmol/L
0.1 mmol/L
Std.Siero umano liofilizzato.
L’attività della LPS ( U/L di
metilresorufina a 37°C) è
indicata sull’etichetta
PRECAUZIONI
Cal.Lipasi. Componente di origine umana,testato, è risultato negativo per la
presenza di HbsAg,ACV e anticorpi anti HIV(1/2).
Comunque,maneggiare con cura come potenzialmente infettivi.
PREPARAZIONE
R1 e R2 sono pronti all’uso. Una volta aperti i flaconi,sono stabili per 90 gg.
A 2-8°C. Mescolare bene il reagente R2 prima dell’uso.
Cal. LPS: scioglier con 1 ml di acqua dist..Tappare e mescolare
delicatamente per sciogliere completamente il contenuto.
Il reagente è stabile per 7 gg. a 2-8°C o 3 mesi a –20°C (in tal caso
aliquotare in piccoli volumi e congelare).
-R2 è una microemulsione torbida di color arancio; scartare se vira al
rosso.
MATERIALE ADDIZIONALE
-Spettrofotometro o colorimetro che misuri a 580 nm.
-Bagno termostatico a 37°C.
-Cuvette con cammino ottico di 1 cm.
-Attrezzatura generale di laboratorio.
CAMPIONI
Siero o plasma con sodio citrato, EDTA o eparina. Evitare ripetuti
congelamenti e scongelamenti.
Stabilità dei campioni: la lipasi è stabile 2 gg. a 2-8°C.
PROCEDIMENTO
1.Condizioni operative:
Lunghezza d’onda:
580 nm
Cuvette :
cammino ottico 1 cm
T. costante:
37°C
2. Azzerare lo strumento contro acqua distillata.
3. Pipettare in cuvetta:
R1 ( mL)
R2 ( μL )
Acqua dist(μL)
Standard (μL)
Campioni (μL )
Bianco
1.0
200
10
-------
Standard
1.0
200
---10
----
Campione
1.0
200
------10
4. Mescolare e incubare per 1 minuto a 37°C.
5. Leggere l’ assorbanza iniziale del campione,far partire il cronometro e
leggere le assorbanze a intervalli di 1 min. per altri 2 minuti. dopo 30 sec.
(A 1 ) e dopo 90 sec. (A 2 ).
5. Calcolare i valori di ΔA/min.
CALCOLI
(ΔA/min.) Camp. - (ΔA/min.) Bianco = (ΔA/min.) netto Camp.
(ΔA/min.) Stand. - (ΔA/min.) Bianco = (ΔA/min.) netto Stand.
(ΔA/min.) netto Camp. x Attività Calibr. = U/L Lipasi nel camp.
(ΔA/min.) netto Stand.
Unità: Una unità internazionale (IU) è la quantità di enzima che trasforma
1 μmol di substrato per minuto,in condizioni standards. La
concentrazione è espressa in unità per litro di campione (U/L).
CONTROLLO QUALITA’
Si consiglia di utilizzare dei sieri di controllo per monitorare le
performance del procedimento.
Se i valori dei controlli sono al di fuori del range definito, controllare lo
strumento, i reagenti e la tecnica per determinare i problemi.
Ciascun laboratorio dovrebbe stabilire un proprio schema di Controllo di
Qualità e le azioni correttive se i controlli non rientrano nei limiti di
tollerabilità.
VALORI DI RIFERIMENTO
< o = 38 U/L (U/L di Metilresorufina a 37°C)
CONSERVAZIONE E STABILITA’
Tutti i componenti del kit sono stabili fino alla data di scadenza indicata
sull’etichetta se conservati ben chiusi a 2-8°C,protetti dalla luce e se si
evitano contaminazioni durante l’uso.
Non utilizzare i reagenti oltre la data di scadenza.
Segnali di deterioramento dei reagenti:
-presenza di particelle e torbidità;
-assorbanza del bianco (A) a 580 nm > o = 1.00.
Questi valori sono orientativi;ciascun laboratorio dovrebbe stabilire
un proprio intervallo di riferimento.
CARATTERISTICHE DEL METODO
1. Range di misura: dal limite di detenzione di 5 U/L al limite di
linearità di 250 U/L. se i valori ottenuti sono superiori al limite di
linearità, diluire il campione 1/10 con NaCl 9 g/L e moltiplicare il
risultato per 10.
1
2.
Precisione:
Media(U/L)
SD
CV (%)
Intra-assay (n=20)
119
215
4.13
5.97
3.34
2.78
Inter-assay (n=20)
119
215
5.43
10.7
5.54
5.02
3.
Accuratezza: i risultati ottenuti con i reagenti di questo kit (y) non
mostrano differenze sistematiche se comparati con altri reagenti in
commercio (x).
I risultati ottenuti usando 100 campioni danno i seguenti risultati:
Coefficiente di correlazione ( r ): 0.997.
Equazione della regressione: y= 0.50054x + 3.9443.
I risultati delle caratteristiche dipendono dall’analizzatore utilizzato.
INTERFERENZE
I trigliceridi a 300 mg/dL interferiscono sulla determinazione, riducendo
l’attività dell’enzima del 6%. Concentrazioni di emoglobina più basse di 150
mg/dL e di bilirubina più basse di 20 mg/dL non interferiscono.
Un elenco di farmaci ed altre sostanze che interferiscono con la
determinazione della lipasi è stato riportato in letteratura da Young e al.
NOTE
1. In particolari condizioni di conservazione (ad es. a temperature più basse
di quella indicata), può apparire nel flacone un precipitato che non
influenza le performance dei reagenti.
2. Per evitare contaminazioni,si consiglia di usare materiale monouso.
3. Sono disponibili su richiesta le metodiche applicative per i più diffusi
analizzatori automatici.
BIBLIOGRAFIA
1.McNeeley M. Lipase. Kaplan A. et al. Clin.Chem. The C.V. Mosby Co.
St.Louis.Toronto.Princeton 1984; 1130-1134, 892.
2.Neumann U et al. Comptes Rend. 4 colloque de Pont-a-Musson,Masson 627-634
(1979).
3.Junge W et al. J.Clin.Chem.Clin.Biochem.,21 445-451 (1983).
4.Neumann U et al. Methods of Enzymatics Analysis,3rd ed. Vol.4,26-34 (1984)
2.Young DS. Effects of drugs on clin. Lab. test, 4th ed. AACC Press, 1995
3.Young DS. Effects of disease on clin. Lab. test, 4th ed. AACC Press, 2001.
4.Burtis A. et al. Tietz Textbook of Clin. Chem.,3rd ed. AACC 1999.
5.Tietz N.W. et al. Clin. Guide to Lab.Tests,3rd ed. AACC 1995.
CODICE PRODOTTO
CONFEZIONE LIPASI
8030305
4x10 + 1x8 mL. CAL: 1X1 mL.
INTERNAL CODE: 1001275
SIMBOLOGIA
8°C
2°C
Numero di
lotto
Conformità
Europea
Numero di
test
Per uso
diagnostico in
vitro
Numero di
catalogo
Leggere le
istruzioni
per l’uso
Attenzione,
vedere le
istruzioni
Non utilizzare se
la confezione è
danneggiata
Temperatura di
conservazione
Scadenza
Non riutilizzare
Fabbricante
PRODUTTORE
2