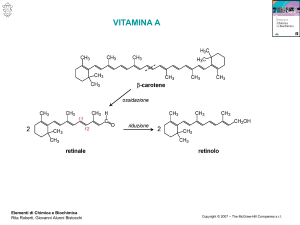
Vitamina A
o
retinolo
VITAMINA A o retinolo
(costituito da 4 unità isopreniche)
Si trova negli alimenti di origine animale (fegato, olio di pesce, pesce,
latte non scremato, burro, tuorlo)
CH2OH
Le linee rosse evidenziano le 4 unità isopreniche
anello β-iononico essenziale per l attività; è
presente nei carotenoidi con attività provitaminica
tutto-trans retinolo
(forma alcolica)
Vitamina
Il gruppo alcolico è esterificato da acidi
grassi (in genere acido palmitico) nella
forma di riserva (fegato e tessuto adiposo)
retinolo deidrogenasi + NAD (reazione reversibile): ossidazione ad aldeide)
CHO
retinale
(forma aldeidica)
Ruolo nella visione
retinaldeide deidrogenasi + NAD (reazione irreversibile) ossidazione ad acido)
COOH
acido retinoico
Ligando di fattori
di trascrizione
CAROTENI (costituiti da 8 unità isopreniche)
I carotenoidi sono presenti nelle piante; alcuni hanno attività vitaminica e
sono denominati provitamina A
Si trovano negli alimenti di origine vegetale (frutta, verdura, olio d oliva)
principale
provitamina:
beta carotene
Struttura chimica del beta carotene: dimero della vitamina A
Ma, da un punto di vista metabolico, la bioconversione si assume di 1:12
ASSORBIMENTO
Necessita dei sali biliari e della lipasi pancreatica
Retinolo assunto sotto forma di estere (in genere del palmitato)
Caroteni non esterificati
- β carotene esportato come tale
- scisso da una diossigenasi della mucosa intestinale Ú
2 molecole retinale Ú retinale reduttasi NADPH Ú retinolo
La scissione è inversamente proporzionale allo stato nutrizionale
in vit A (meccanismo omeostatico non noto)
Biodisponibilità (percentuale del nutriente assunto con la dieta che viene
effettivamente digerito, assorbito ed utilizzato dall organismo)
Vit A assorbita per il 70%
carotenoidi: assorbiti per il 2-50 % assorbiti, in base a vari fattori
es. cottura
ENTEROCITA
legati a CRBP (Cellular Retinol-Binding Protein) il legame alla proteina permette di
gestire la sostanza lipofila in ambiente acquoso
quindi l enzima LRAT (Lecitina Retinolo Acil Transferasi) forma l estere del
retinolo permette l incorporazione nei chilomicroni
PLASMA nei chilomicroni sotto forma di retinolo estere
EPATOCITA
Retinolo estere Ú scisso in retinolo e legato alla CRBP
CRBP-retinolo retinolo deidrogenasi + NAD (reazione reversibile di ox ad aldeide)
E
CRBP- retinale retinale deidrogenasi + NAD (reazione irreversibile di ox ad acido)
acido retinoico
IN ALTERNATIVA retinolo esterificato da LRAT ed esportato in circolo
- VLDL
- Legato alla RBP (Retinol Binding Protein)
A LIVELLO PERIFERICO captato dai vari organi tramite i Recettori per la RBP
Bioconversione
Produzione di un retinoide attivo da carotenoidi
precursori della vit A
Retinolo : β carotene : altre provitamine - 1:12 : 24
DRI 2001
Retinol activity equivalent RAE
1 RAE = 1 µg di retinolo
1 RAE = 12 µg di β carotene tutto trans presente in alimenti
1 RAE = 24 µg di altri caroteni provitamine presente in alimenti
1 RAE = 2 µg di βcarotene tutto trans in forma di supplemento
Deposito
300 -900 mg complessivi sotto forma di estere (palmitato)
90 % nel fegato,
10% in tessuto adiposo intraperitoneale, rene, polmoni
si lega a RAR
Recettore per l acido retinoico
tutto trans
si lega a RXR
Recettore per l acido 9 cis retinoico
Sintesi delle rodopsina a partire dalla vitamina A
RETINALDEIDE: PERCEZIONE VISIVA
Fotoisomerizzazione
11cis retinale è tutto trans retinale
molto veloce: 10-12 s
assorbe luce
di λ 500 nm
RODOPSINA: pigmento dei bastoncelli deputati alla visione notturna
opsina (apoproteina) + fotorecettore
legato tramite base di Schiff con lisina (Lys 296)
praticamente non vi è isomerizzazione spontanea e quindi il rumore di
fondo è molto basso; ciò permette di percepire anche pochi fotoni
Ciclo retinoide: via enzimatica che rigenera 11cis retinale
Rodopsina
luce
trasportatore
opsina
11 cis retinale
trans retinale
Deidrogenasi + NAD+
11 cis retinolo
trasportatore
La rigenerazione avviene al
buio, nelle cellule epiteliali
adiacenti ai fotorecettori
Per esportare il retinale dal
bastoncello alle cellule
epiteliali
MUTAZIONE:
degenerazione maculare
di Stargardt
Riduttasi +NADPH
trans retinolo
Isomerasi
trans retinolo estere
Lecitina retinol acil transferasi
MUTAZIONE : retinite pigmentosa
ACIDO RETINOICO: FUNZIONE TRASCRIZIONALE
Lega fattori di trascrizione: Recettori dell Acido Retinoico (RXR)
RXR forma eterodimeri con i recettori per
- PPAR
- calcitriolo
- ormoni tiroidei
.
Anche questi recettori sono fattori trascrizionali attivati dal legame con
l ormone e dalla dimerizzazione con RXR, con conseguente inibizione o
attivazione di specifici geni
Questo spiega i numerosi fenomeni biologici in cui è coinvolta la vit A
differenziamento
proliferazione
sviluppo embrionale e fetale
Ac 9cis retinoico
eterodimero RN- RXR
+
RXR
Forma
inattiva
RXR
attivo
RN
NUCLEO
RXR
promotore
gene bersaglio
mRNA
CITOPLASMA
proteina
RN – Recettore nucleare ( es per ormone steroideo)
RXR - Recettore dell acido 9cis Retinoico
I recettori attivati dal ligando sono denominati recettori nucleari
ASSUNZIONE 700 µg vit A/die (M adulto) (400 µg/die bambino)
CARENZA (malnutrizione, malassorbimento, alcolismo)
Nell’ordine si ha
1. cecità notturna e ipercheratosi (segni iniziali reversibili)
2. danno della cornea (xeroftalmia) e quindi cheratomalacia (irreversibile)
3. cecità
(bambini sotto i 3 anni nei paesi poveri: 70% delle cause di cecità).
- suscettibilità ad infezione per alterazioni del sistema immunitario
- carenza di ferro
- malformazioni fetali
ECCESSO non superare 3 mg vit A/die (M e F adulto)
- manifestazioni cutanee, apparato digerente, neuromuscolare, osso
- effetti teratogeni e malformazioni fetali
II. FUNZIONE TRASCRIZIONALE
quale ligando di fattori di trascrizione nuclari
recettore dell Acido Retinoico RXR forma eterodimeri con i recettori per
- PPAR
- calcitriolo
- ormoni tiroidei
.
Anche questi recettori sono fattori trascrizionali attivati dal legame con
l ormone e dalla dimerizzazione con RXR, con conseguente inibizione o
attivazione di specifici geni
Questo spiega i numerosi fenomeni biologici in cui è coinvolta la
vitamina A
Base molecolare per il ruolo fisiologico nel
differenziamento
proliferazione
sviluppo embrionale
III° - funzione immunitaria
Regola l espressione di enzimi per la sintesi di glicosamminoglicani e
glicoproteine epiteliali, sintesi mucina,
IV° funzione antianemica
Aumenta la disponibilità di Fe inorganico (forse contrastando l azione dei
fitati, composti vegetali presenti in particolare negli alimenti integrali, che
legando il ferro ne impediscono l assorbimento)
Fabbisogno
espresso come microgrammi /die se si tratta di vitamina A
oppure
RAE (Retinol activity equivalent)/die se si considera
vitamina A + provitamine A (in particolare il beta carotene)
LARN 2012
uomo adulto
donna adulta
gravidanza
allattamento
700 µg/die
600
700
1000
CARENZA
rischio nei paesi con povertà,
malnutrizione, basso peso alla nascita, parassiti,
fasce di età più a rischio 6 mesi- 6 anni
Carenza secondaria per
• malassorbimento dei lipidi,
• malattie epatiche ( bassi livelli di Retinol-Binding Protein -RBP)
• Alcolismo
Danni da carenza
• difficoltà della visione notturna
• xeroftalmia - principale causa di cecità nei bambini
• ipercheratosi della cute
• aumentata suscettibilità alle infezioni
• ritardo della crescita,
• deformazione delle ossa
• degenerazione organi riproduttivi ed epiteliali
Valutazione dello stato nutrizionale
test funzionale di percezione della luce
livelli plasmatici di retinolo
misura (immunoassay) del RBP (rapporto RBP/retinolo 1:1)
UL 3.000 µg (3 mg) di vitamina A preformata
TOSSICITA
Acuta anche mortale
Cronica
manifestazioni cutanee, apparato digerente, neuromuscolare
Ipotesi: azione simil-detergente degli esteri del retinolo
Più grave negli anziani che hanno una ridotta clearance postprandiale
delle lipoproteine
Ipervitaminosi A induce ipercalcemia, riassorbomento osseo ed inibisce
la formazione di nuovo osso
Effetto teratogeno
CAROTENOIDI
FUNZIONE dei carotenoidi nelle piante: assorbono la
luce solare favorendo la fotosintesi.
Hanno un diverso colore in base al numero di doppi
legami, captando le varie radiazione di diversa
lunghezza d onda della luce solare
In natura più di 600 carotenoidi di cui 50 consumati in modo significativo
con la dieta.
caroteni (α, β, γ,carotene, licopene) non contengono ossigeno
xantofille (luteina, zeaxantina, cantaxantina) contengono ossigeno
(presente come alcol o gruppo carbonilico)
vegetali contenenti ampio spettro di carotenoidi e xantofille
vegetali verdi - spinaci, broccoli
vegetali contenenti prevalentemene caroteni
vegetali e frutti giallo/rossi - pomodori, carote, albicocche
vegetali contenenti xantofille esterificate con ac. grassi (idrolizzati
prima di essere assorbiti)
vegetali e frutti giallo/arancione: arance, prugne, pesche
I carotenoidi hanno doppi legami coniugati che conferiscono la capacità di
assorbire la luce visibile (questo genera i rispettivi colori) e di eliminare
con efficienza i radicali liberi.
astaxantina
Supplemento per il colore rosa del salmone
Luteina e zeaxantina: per aumentare
pigmentazione del tuorlo d uovo
Carotenoidi usati comunemente anche come
supplementi nel mangime per animali
I carotenoidi sono assorbiti a livello intestinale e quindi si
trovano in circolo legati alle lipoproteine
Si accumulano prevalentemente nel fegato e nel tessuto
adiposo,
alte concentrazioni anche nei tessuti riproduttivi e nelle
ghiandole surrenali.
USA
assunzione giornaliera dalla dieta 6 grammi
a decrescere
licopene
β carotene
luteina e zeoxantina
I. Attività antiossidante
- L assunzione di licopene (pomodoro, carote, anguria, pompelmo
rosa) è inversamente correlata a cancro dell apparato digerente (cavo
orale, esafogo, stomaco, colon, retto)
- protezione da cancro della mammella, cancro della pelle
Luteina (spinaci, foglie verdi, broccoli, kiwi, tuorlo uovo) e zeaxantina
(mais, tuberi, patate, tuorlo uovo) si concentrano nella retina
Inversamente correlate alla progressione della cataratta
Si decompongono lentamente alla esposizione dei raggi UV e
proteggono i lipidi dalla ossidazione
II. Regolazione espressione genica
cantaxantina regola espressione della connessina, proteina che forma
legami fra cellule adiacenti
La perdita di comunicazione porta a proliferazione incontrollata delle
cellule
TOSSICITA
A differenza della vitamina A non è nota tossicità da carotenoidi.
probabilmente la trasformazione della pro-vitamina è regolata dallo
status nutrizionale in vitamina A:
non porta ad ipervitaminosi
La carotenodermia derivante da eccessiva assunzione non
sembrerebbe tossica
Cautela
• Studi su fumatori riportano effetti dannosi più che protettivi sul cancro
del polmone (maggiore incidenza di carcinoma polmonare)
• Riduzione dei livelli vit E con supplementazione a lungo termine
• Alte dosi della cantaxantina induce retinopatia reversibile
Il carotenoide rosso-arancio cantaxantina è stato propagandato negli USA
come pillola naturale abbronzante. Una supplementazione a lungo termine
può indurre retinopatia dovuta a formazione di cristalli nella retina: i cristalli
scompaiono dopo mesi dal termine della supplementazione.
Vitamina E (tocoferolo)
EEEE
EEEE
Vitamina E
Termine collettivo per:
tocoferoli (4 isoforme)
tocotrienoli (4 isoforme)
più importante antiossidante liposolubile
protezione acidi grassi polinsaturi
LOCALIZZAZIONE CELLULARE
zone ricche in lipidi: membrane cellulari, depositi di grassi
α-tocoferolo
STRUTTURA CHIMICA
anello funzionale fenolico
con una catena laterale isoprenica
scoperta nel 1922 nei vegetali verdi (è sintetizzata solo dalle piante
fotosintetiche) e denominata vit E
quindi messa in relazione con la fertilità e chiamata tocoferolo: tokos
(nascita) phero (porto) olo (alcol)
8 forme con diversa attività biologica
α-, β-, γ-, δ-tocoferolo
α-, β-, γ-, δ- tocotrienolo
Configurazione in base alla posizione dei metili rispetto all anello
2R,4 R,8 R α tocoferolo
(RRR α-Tocoferolo
oppure d-α-Tocoferolo
isomero naturale)
supplementi commerciali
forma sintetica - "all rac(emic) α-tocoferolo"
è formata dagli 8 differenti stereoisomeri dell' αtocoferolo derivanti dai tre centri chirali
stessa attività antiossidante in vitro ma diversa attività
biologica
esteri con acetato, succinato
più resistenti alla ossidazione con stessa biodisponibilità
FONTI: soprattutto in alimenti di origine vegetale
olio di oliva
oli vegetali (girasole, mais, soia)
germe di grano
noci, mandorle
vegetali verdi (spinaci freschi)
olio di fegato di pesce
cambia la % delle diverse forme
- α-tocoferolo: nell’olio di oliva, girosole, mandorle; nei prodotti
animali (parti grasse delle carne)
- γ- tocoferolo: nell’ olio di mais e di soia
suscettibile a calore, luce, esposizione all'aria
distrutta nei processi industriali di cottura e conservazione
ASSORBIMENTO
ad opera di
sali biliari,
enzimi pancreatici (idrolisi esteri del tocoferolo)
non vi è discriminazione fra le varie forme
BIODISPONIBILITA’
Aumentata da lipidi e acidi grassi a catena media
Diminuita da alti livelli di Vit A, alcol, pectine, crusca
Gli acidi grassi polinsaturi, assunti in elevata quantità possono degradare la
Vit E a livelli intestinale
TRASPORTO EMATICO
• chilomicroni,
• VLDL, LDL (la maggior parte di Vit E), HDL
BIODISCRIMINAZIONE
α - tocopherol binding protein (α TBP) Se-proteina
proteina epatica che lega selettivamente RRR- α -tocoferolo
negli alimenti soprattutto γ-tocoferolo; nel plasma solo il 10-20% rispetto all'α tocoferolo
attività biologica
dipende dalla differente struttura e dal differente
metabolismo
α : β : γ: δ - 1 : 0,2 : 0,1 : 0,01
1 mg RRR-α -tocoferolo = 1 α -TE (Tocoferolo Equivalente)
fonte naturale Vit E ha ≈ doppia bioattività della all rac
sintetica
FABBISOGNO: 15 mg/die
DEPOSITO
Tessuto adiposo, fegato, muscolo
ESCREZIONE
Bile (1% urina)
1. Catena isoprenica subisce ω-ossidazione e degradazione da parte del
sistema enzimatico epatico cit P450
2. coniugata all'acido glucuronico o solfati
forma all-rac aumenta livelli di cit P450 (riconosciuta come estranea)
Vit E naturale ritenuta più a lungo
Forma all-rac può interferire con il metabolismo dei farmaci: da tenere in
considerazione
LOCALIZZAZIONE: zone ricche in lipidi quali membrane cellulari,
lipoproteine, depositi di grasso
FUNZIONE
Antiossidante liposolubile
v protezione da auto-ossidazione degli acidi grassi polinsaturi.
v previene ossidazione lipoproteine (LDL)
MECCANISMO
ü Interrompe la catena di radicali che reagiscono più velocemente con la vit
E che con acidi grassi
ROO• + Vit E-OH Ú Vit E-O• + ROOH
Vit E-O• reagisce con vitamina C o altro donatore di idrogeno e ridiventa Vit EOH
ü α-tocoferolo si inserisce nei lipidi di membrana e le stabilizza
ü previene ossidazione LDL
LDL: 2700 molecole acido grasso : 5-9 Vit E : <1 β-carotene : <1 γ-tocoferolo
ü Regolatore di attività di enzimi di membrana e trasduzione del segnale
(protein chinasi C, ciclossigenasi) con effetti sulla aggregazione piastrinica,
risposta immunitaria, proliferazione di cellule muscolari liscie,..
ADDOTTI CON PROTEINE
Protezione da
malattie legate a radicali
aterosclerosi
malattia cardiovascolare
cancro (fumatori)
Alzheimer
infertilità
Vit E e Se sinergici (elimina idroperossidi tramite il
Se-enzima glutatione perossidasi)
gamma- tocoferolo
Manca rispetto all α-tocoferolo del metile in posizione 5.
Antiossidante più efficace verso i perossinitriti
O=N-O-O-
(che si formano dalla reazione dell NO con un
superossido)
e possono causare danni a DNA, proteine, lipidi
Tocotrienoli: catena laterale con tre insaturazioni
Minore biodisponibilità per minore affinita per la α-TBP
ü Proprietà neuroprotettive
ü Antiossidanti
ü Anticancro
ü Abbassano livelli di colesterolo (calo dell attività del
l enzima HMGCoA riduttasi).
La catena laterale isopronoide porta ad aumento
dei livelli di farnesolo cellulare e a conseguente
blocco della sintesi dell enzima (meccanismo
differente dalle statine che bloccano l attività)
Carenza alimentare rara data la distribuzione negli alimenti
e le riserve di deposito
necessari supplementi in carenza dovuta a
Ø soggetti con mancata sintesi apoproteina B ed incapacità a
formare chilomicroni (assorbimento) e VLDL (trasporto):
si ha neuropatia e retinopatia alla fine della prima decade di vita
Ø mutazioni αTBP: incapacità di incorporare in VLDL;
(dosi massicce di vit 2000 mg non raggiungibili con la dieta)
Ø malassorbimento
Ø malattie croniche epatiche
Ø neonati prematuri
UL
Studi clinici: sicura sino a 1600 UI (~ 1100 mg/die )
TOSSICITA’
> 3000 mg/die
diminuisce adesione piastrinica e quindi aumenta il
tempo di coagulazione