GOLIMUMAB (Indicazione: Spondilite Anchilosante) (05-04-2011)
Specialità: Simponi®(Centocor)
Forma farmaceutica:
•
•
1 PEN 50mg, 0,5ml - Prezzo: euro 1723.33
1 SIR 50mg, 0,5ml - Prezzo: euro 1723.33
ATC: L04AB06
Categoria terapeutica: Inibitore del TNF-alfa
Fascia di rimborsabilità: H
Indicazioni ministeriali:
Spondilite anchilosante (SA):
Simponi è indicato per il trattamento della spondilite anchilosante grave in fase attiva, in pazienti adulti
che non hanno risposto in modo adeguato alle terapie convenzionali.
Stato registrativo: Registrazione EMEA
data: 01-10-2009
data AIC: 30-08-2010
Stato registrativo FDA: SI
data: 24-04-2009
Decisioni PTORV
Data riunione: 05-04-2011
Decisione: Inserito
Commenti:
Golimumab rappresenta un’ulteriore opzione di trattamento per i pazienti con spondilite anchilosante che
non hanno risposto in modo adeguato alle terapie convenzionali, rappresentate soprattutto dai FANS. La
spondilite anchilosante è una patologia che colpisce soggetti anche molto giovani, con una prevalenza
dello 0,2% sulla popolazione generale. Golimumab è somministrato per via sottocutanea e ciò aumenta la
compliance dei pazienti, rispetto ai farmaci somministrati per infusione endovenosa.
File: RIUNIONE CTR DEL 05 APRILE 2011 _ GOLIMIMAB (SA).pdf
Caratteristiche del prodotto
Golimumab è un anticorpo monoclonale umano, IgG1κ prodotto da una linea cellulare di ibridomi murini
con tecnologia DNA ricombinante, che forma complessi stabili ad elevata affinità sia per la forma solubile,
sia per quella transmembrana bioattiva del TNF-alfa umano, impedendo il legame del TNF-alfa ai suoi
recettori. Il legame di golimumab al TNF umano ha mostrato di inibire l’espressione sulla superficie
cellulare delle molecole di adesione, selettina E, molecole di adesione alle cellule vascolari di tipo 1
(VCAM) e molecole di adesione intracellulare di tipo 1 (ICAM) da parte delle cellule endoteliali umane [1].
Per il trattamento della spondilite anchilosante Golimumab deve essere somministrato una volta al mese.
Inquadramento della patologia
La spondilite anchilosante (AS) è una malattia infiammatoria cronica, ad eziologia sconosciuta che
interessa principalmente lo scheletro assiale, ma anche le articolazioni periferiche e le entesi. Si tratta di
una patologia che fa parte delle spondiloartropatie. La percentuale di prevalenza della malattia è stimata
essere
compresa
fra
0.1%-1.1%
della
popolazione
[2].
La manifestazione di esordio, che generalmente compare tra i secondo e terzo decennio di vita, è di solito
un dolore sordo nella regione gluteo-lombare che dopo qualche mese diventa persistente e bilaterale. Si
possono inoltre manifestare artrite delle anche, delle spalle e di altre articolazioni periferiche ed altri
sintomi extra-assiali (ad es. uveite acuta anteriore, psoriasi e malattia infiammatoria dell’intestino). La
spondilite determina riduzione della motilità della colonna vertebrale nei movimenti di flessione e
limitazione dell’espansione del torace [3].
Trattamenti alternativi
Risultati d'efficacia delle alternative terapeutiche:
ASAS 20 alla 12° settimana [4]
Trattamento
Numero di studi e
disegno
(n. pazienti)
Durata
trattamento
Braccio
sperimentale
Braccio
di
controllo
35/151
Rischio
Relativo
Adalimumab vs.
placebo
2 RCT (n=397)
12 settimane
138/246
2.43
(1.76 a 3.35)
Etanercept vs
placebo
3 RCT (n=602)
12 settimane
231/353
73/249
2.13
(1.73 a 2.63)
Infliximab vs
placebo
2 RCT (n=348)
12 settimane
149/235
19/113
4.11
(2.62 a 6.44)
Durata
trattamento
Braccio
sperimentale
Braccio
di
controllo
Rischio
Relativo
ASAS 50 alla 12° settimana [4]
Trattamento
Numero di studi e
disegno
(n. pazienti)
Adalimumab vs.
placebo
2 RCT (n=397)
12 settimane
90/246
17/151
Etanercept vs
placebo
3 RCT (n=602)
12 settimane
162/353
32/249
3.53
(2.50 a 4.98)
Infliximab vs
placebo
1 RCT (n=69)
12 settimane
16/34
2/35
8.24
(2.05 a 33.13)
3.22
(1.98 a 5.23)
Linee guida di trattamento esistenti
Le linee guida per l'utilizzo degli anti TNF alfa nel trattamento della spondilite alchilosante sono state
sviluppate dalla British Society of Rheumatology [5] e dall'ASAS Intenational Working Group [6]. In
nessuno dei due documenti viene citato golimumab, in quanto entrambi sono stati pubblicati prima della
commercializzazione del farmaco. Entrambe le linee guida sono concordi nel riservare il trattamento con
anti TNF-alfa per quei pazienti con spondilite alchilosante attiva e persistente che non presentano risposta
adeguata al trattamento convenzionale con almeno due FANS.
Dati di efficacia
L'efficacia del golimumab nel trattamento della spondilite anchilosante (SA) è stata valutata in uno studio
clinico in doppio cieco, di fase III, verso placebo, denominato GO-RAISE [2,7].
Disegno dello studio: Dalla settimana 0 alla 14, studio a 3 bracci paralleli (golimumab 50 mg vs
golimumab 100 mg vs placebo); dalla settimana 16 alla 24, era permesso un interruzione con passaggio
al trattamento golimumab 50 mg (per i pazienti trattati con placebo), oppure al trattamento golimumab
100 (per i pazienti trattati con golimumab 50mg); dalla settimana 24 alla 104 tutti i pazienti trattati con
golimumab 50 mg o 100 mg.
Criteri d'inclusione: età>18 anni, SA da almeno 3 mesi definita secondo la Modified New York Criteria
del 1984, criteri radiografici (sacroiliti bilaterali di grado ≥2 o sacroiliti unilaterali di grado ≥3) almeno 1
criterio clinico (mal di schiena e rigidità da almeno 3 mesi; limitata mobilità delle vertebre lombari sia sul
piano sagittale che frontale; limitata espansione toracica).
Criteri d'esclusione: Altre patologie infiammatorie, controindicazioni o precedente utilizzo di anti TNFalfa, utilizzo di DMARDs ad eccezione del MTX, sulfasalazina nelle 4 settimane antecedenti la
randomizzazione.
End-point
I:
Risposta
ASAS
20
alla
settimana
14°
End-point II: Risposta ASAS 20 alla settimana 24°, variazione della BASFI (Bath Ankylosing Spondylitis
Functional Index) e della BASMI (Bath Ankylosing Spondylitis Metrology Index) alla settimana 14°.
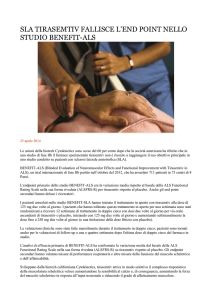
Risultati: La percentuale di pazienti che hanno raggiunto una risposta ASAS 20 alla 14° ed alla 24°
settimana è risultata significativamente maggiore con golimumab 50 mg e 100 mg rispetto al placebo.
Non sono disponibili dati di efficacia a lungo termine sebbene le linee guida EMEA raccomandano di
dimostrare l'efficacia anche nel lungo periodo (ad esempio 1 anno) [2]. La variazione del grado di
dipendenza funzionale (BASFI) è risultata maggiore nei pazienti trattati con golimumab versus placebo,
mentre non è stata osservata una variazione statisticamente significativa nell'attività di malattia con
indice metrologico BASMI.
Principali studi clinici:
Pazienti e
Referenza
trattamento
Disegno e fase
Misure di esito
356 pz con SA:
GO-RAISE
[7]
-PBO (n=78)
-GLM 50 mg ogni 4
sett. (n=137)
Jadad
score
ASAS 20:
RCT, doppio cieco,
ASAS 20 alla
fase III, random 1:2:2 settimana 14
-GLM 100 mg ogni 4
sett. (n=140)
GLM: golimumab
Criteria
Risultati
principali
PBO: placebo
-GLM 50 mg:
59.4% (p<0.001)
4*
-GLM 100 mg:
60.0% (p<0.001)
vs PBO 21.8%
ASAS 20: Assessment in Ankylosing Spondylitis Response
*Jadad Scale: strumento per la verifica della qualità della pubblicazione; si basa sulla considerazione che
i tre elementi principali che devono essere riportati per avere maggiori garanzie sulla buona qualità di
uno studio clinico siano la randomizzazione, la condizione di doppia cecità, e la gestione dei drop-out. Si
considerano buone le pubblicazioni che ottengono almeno 3 punti, mentre si considerano di scarsa qualità
quelle che raggiungono un punteggio uguale o inferiore a due.
Dati di sicurezza
Il tasso di eventi avversi seri, osservati durante le 16 settimane, è stato meno frequente nel gruppo
golimumab (4.3%) rispetto al gruppo placebo (5.2%). Fra i pazienti trattati con golimumab è stato
osservata una maggiore incidenza di disordini cardiaci rispetto al placebo, 2.2% vs. 0%. Molti di questi
pazienti avevano patologie cardiache pre-esistenti, pertanto la correlazione di questi eventi con il
golimumab è poco evidente [2].
Eventi avversi con frequenza ≥5% osservati nelle 16 settimane.
Placebo
(n=77)
Golimumab 50 mg
(n=138)
Golimumab 100 mg
(n=140)
Infezioni ed infestazioni
27.3%
38.4%
36.4%
Disordini gastrointestinali
19.5%
27.5%
16.4%
Disordini del tessuto muscoloscheletrico e
connettivo
20.8%
20.3%
14.3%
9.1%
16.7%
13.6%
11.7%
17.4%
10.7%
Evento avverso
Disordini del sistema nervoso
Disordini respiratori, toracici e mediastinici
Popolazione target
La ditta partendo da dati di letteratura e dalle indicazioni dei medici ha stimato una popolazione di
pazienti eleggibili al golimumab per tutte e tre le indicazioni (Artrite Reumatoide, Artrite Psoriasica e
Spondilite Anchilosante) pari a 450 pazienti. Utilizzando i dati disponibili in letteratura, le informazioni dei
clinici ed alcune informazioni presenti nel report della ditta, si è proceduto ad un nuovo calcolo della
popolazione eleggibile per singola indicazione. Le stime sono leggermente diverse da quanto
presentatoci.
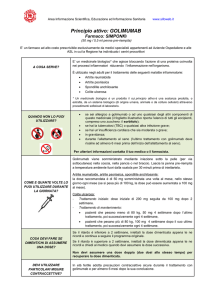
I dati di letteratura riportano una prevalenza della malattia in Italia di 0,37% [8]. Utilizzando questa
prevalenze e i dati Istat, che per il Veneto (anno 2010) riportano una popolazione adulta di circa
4.082.000 [9] abitanti, si può stimare una popolazione con spondilite anchilosante di 15.104 individui.
Dalle informazioni forniteci dai clinici globalmente circa il 10% di questi soggetti sarebbe candidato al
trattamento, mentre stime di mercato riportano che circa 8% viene effettivamente trattato con i farmaci
biologici. Considerando una percentuale del 10%, i malati candidabili alla terapia con biologici dovrebbero
essere 1.510. Infine in accordo con quanto sostenuto dai clinici, circa il 20% dei pazienti eleggibili per i
biologici, considerata anche la quota di switch da un altro farmaco anti-TNF, potrebbe essere eleggibile al
trattamento
con
golimumab,
ovvero
una
stima
di
302
pazienti
sul
Veneto.
Analisi dei costi (costi delle alternative, potenziale impatto di budget etc)
Il costo della terapia con goliumab è leggermente superiore rispetto alla terapia con etanercept e
adalimumab ma inferiore rispetto ad infliximab.
Prezzo del farmaco e delle alternative
Prezzo di cessione
ospedaliera (ex factory
incluso di sconti
obbligatori)
Principio attivo
Unità posologiche
GOLIMUMAB
1 pen o 1 sir 50 mg
€ 973,18
INFLIXIMAB
1 fl 100 mg
€ 466,25
1 fl 25mg
€ 119,70
€ 239,39
ETANERCEPT
1 fl 50 mg
ADALIMUMAB
1 pen o sir 40 mg
€ 465,88
Costo della terapia con il farmaco:
Principio
attivo
Costo
all'ospedale
Spreco
Tipo di
Somministrazioni per anno di
Dosaggio
per
Note
somministrazione in un anno
terapia
somministrazione
comprensivo
di spreco
GOLIMUMAB 50 mg
sc, 1 volta al mese
12
€ 11.668
---
Costo delle alternative:
Principio
attivo
INFLIXIMAB
ETANERCEPT
Costo
all'ospedale
Spreco
Tipo di
Somministrazioni per anno di
Dosaggio
per
Note
somministrazione in un anno
terapia
somministrazione
comprensivo
di spreco
€ 350
Il costo è stato
calcolato per un
pz di 65 kg, con
l'utilizzo di 4 fl
per ogni
somministrazione
€ 12.448
--
--
€ 12.113
--
--
5mg/kg
infusione alle
settim. 0,2,6, poi
ogni 6-8 settim.
8-9
€ 14.920 - €
16.785
50 mg
sc, 1 volta a sett
52
sc, 1 volta ogni 2
sett
26
ADALIMUMAB 40 mg
Ipotesi di impatto di budget:
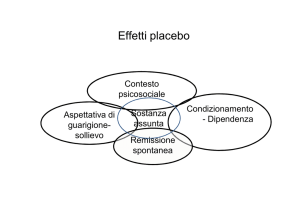
Sui 302 pazienti potenzialmente eleggibili, la ditta stima che il farmaco abbia una penetrazione del 30%
per un totale di 91 pazienti. Si può quindi stimare una spesa annua per il farmaco nella spondilite
anchilosante di €1.190.656. Essendo il costo del farmaco in linea con quello degli altri biologici
antagonisti del TNF (adalimumab, etanercept ed inflixibam) ed essendo golimumab un'alternativa agli
altri farmaci anti-TNF, si può presumere che l'introduzione del farmaco non comporterà un aumento della
spesa globale per gli anti-TNF.
Bibliografia
1. Riassunto caratteristiche del prodotto
2. EPAR - www.ema.europa.eu
3. Harrison-Principi di Medicina Interna, 17°Edizione
4.McLeod C. et al, Health Technology Assessment 2007; Vol. 11: No. 28
5. www.rheumatology.org.uk (accesso del 15/02/2011)
6. Braun J. et al, Ann Rheum Dis 2003; 62:817-824.
7. Inmand R.D. et al, Arthrit Rheum 2008; 58(11): 3402-3412.
8. Salaffi F. et al, Clin. Exp. Rheu. 2005; 23:819-828.
9. http://demo.istat.it
SINTESI
Caratteristiche del prodotto
Golimumab è un anticorpo monoclonale umano, IgG1κ prodotto da una linea cellulare di ibridomi murini
con tecnologia DNA ricombinante, che forma complessi stabili ad elevata affinità sia per la forma solubile,
sia per quella transmembrana bioattiva del TNF-alfa umano, impedendo il legame del TNF-alfa ai suoi
recettori. Per il trattamento dell'artrite psoriasica, Golimumab deve essere somministrato una volta al
mese.
Inquadramento della patologia
La spondilite anchilosante (AS) è una malattia infiammatoria cronica, ad eziologia sconosciuta che
interessa principalmente lo scheletro assiale, ma anche le articolazioni periferiche e le entesi. Si tratta di
una patologia che fa parte delle spondiloartropatie. La percentuale di prevalenza della malattia è stimata
essere compresa fra 0.1%-1.1% della popolazione.
Linee guida di trattamento esistenti
Le linee guida per l'utilizzo degli anti TNF alfa nel trattamento della spondilite alchilosante sono state
sviluppate dalla British Society of Rheumatology e dall'ASAS Intenational Working Group. In nessuno dei
due documenti viene citato golimumab, in quanto entrambi sono stati pubblicati prima della
commercializzazione del farmaco. Entrambe le linee guida sono concordi nel riservare il trattamento con
anti TNF-alfa per quei pazienti con spondilite alchilosante attiva e persistente che non presentano risposta
adeguata al trattamento convenzionale con almeno due FANS.
Dati di efficacia
L'efficacia del golimumab nel trattamento della spondilite anchilosante (SA) è stata valutata in uno studio
clinico in doppio cieco, di fase III, verso placebo, denominato GO-RAISE che ha arruolato pazienti adulti
con SA da almeno 3 mesi. La percentuale di pazienti che hanno raggiunto una risposta ASAS 20 alla 14°
ed alla 24° settimana è risultata significativamente maggiore con golimumab 50 mg e 100 mg rispetto al
placebo. Non sono disponibili dati di efficacia a lungo termine sebbene le linee guida EMEA
raccomandano di dimostrare l'efficacia anche nel lungo periodo (ad esempio 1 anno). La variazione del
grado di dipendenza funzionale (BASFI) è risultata maggiore nei pazienti trattati con golimumab versus
placebo, mentre non è stata osservata una variazione statisticamente significativa nell'attività di malattia
con indice metrologico BASMI.
Dati di sicurezza
Il tasso di eventi avversi seri, osservati durante le 16 settimane, è stato meno frequente nel gruppo
golimumab (4.3%) rispetto al gruppo placebo (5.2%). Fra i pazienti trattati con golimumab è stato
osservata una maggiore incidenza di disordini cardiaci rispetto al placebo, 2.2% vs. 0%. Molti di questi
pazienti avevano patologie cardiache pre-esistenti, pertanto la correlazione di questi eventi con il
golimumab è poco evidente.
Popolazione target
La ditta partendo da dati di letteratura e dalle indicazioni dei medici ha stimato una popolazione di
pazienti eleggibili al golimumab per tutte e tre le indicazioni (Artrite Reumatoide, Artrite Psoriasica e
Spondilite Anchilosante) pari a 450 pazienti. Utilizzando i dati disponibili in letteratura, le informazioni dei
clinici ed alcune informazioni presenti nel report della ditta, si è proceduto ad un nuovo calcolo della
popolazione eleggibile per singola indicazione. Le stime sono leggermente diverse da quanto
presentatoci.
I dati di letteratura riportano una prevalenza della malattia in Italia di 0,37%. Utilizzando questa
prevalenze e i dati Istat, che per il Veneto (anno 2010) riportano una popolazione adulta di circa
4.082.000 abitanti, si può stimare una popolazione con spondilite anchilosante di 15.104 individui.
Considerando una percentuale del 10%, i malati candidabili alla terapia con biologici dovrebbero essere
1.510. Infine in accordo con quanto sostenuto dai clinici, circa il 20% dei pazienti eleggibili per i biologici,
considerata anche la quota di switch da un altro farmaco anti-TNF, potrebbe essere eleggibile al
trattamento
con
golimumab,
ovvero
una
stima
di
302
pazienti
sul
Veneto.
Analisi dei costi (costi delle alternative, potenziale impatto di budget etc)
Il costo della terapia con goliumab è leggermente superiore rispetto alla terapia con etanercept e
adalimumab ma inferiore rispetto ad infliximab. Sui 302 pazienti potenzialmente eleggibili, la ditta stima
che il farmaco abbia una penetrazione del 30% per un totale di 91 pazienti. Si può quindi stimare una
spesa annua per il farmaco nella spondilite anchilosante di €1.190.656. Essendo il costo del farmaco in
linea con quello degli altri biologici antagonisti del TNF (adalimumab, etanercept ed inflixibam) ed
essendo golimumab un'alternativa agli altri farmaci anti-TNF, si può presumere che l'introduzione del
farmaco non comporterà un aumento della spesa globale per gli anti-TNF.