Morte Cellulare
Programmata
Classificazione classica delle
diverse modalità di morte cellulare
- Morte cellulare di tipo I: apoptosi
- Morte cellulare di tipo II: autofagia
- Morte cellulare di tipo III: necrosi
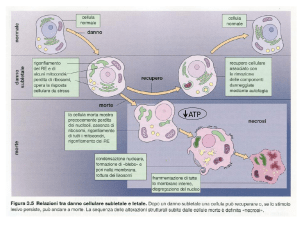
Necrosi
Apoptosi
Apoptosi:
morte cellulare programmata
Processo di morte attivo:
- richiede energia
- richiede sintesi proteica
- coinvolgimento di numerosi geni
Può essere indotta da:
- segnali interni (danni),
- segnali esterni
- assenza di segnali esterni di sopravvivenza
Ruolo dell’Apoptosi
• Sviluppo
- Es.: Sviluppo del sistema nervoso centrale
(morte neuronale dal 20 all’80% in differenti regioni del SCN)
• Mantenimento dell'omeostasi tissutale
- Es.: Intestino, Pelle, Sangue, cellule
danneggiate
(50 milardi di cellule muoiono ogni giorno nel nostro organismo)
• Sistema immune
- Eliminazione di cellule infette o cellule tumorali
Morte Cellulare e Patologie
• Diminuzione della Morte Cellulare
• Cancro
• Incontrollata proliferazione cellulare
– Infezioni Croniche
• Adenovirus e Papilloma virus
Morte Cellulare e Patologie
• Aumento della Morte Cellulare
• Neurodegenerazione
• Parkinson ed Alzheimer
• Ischemia Cerebrale, Infarto miocardio
• Morte per mancanza di ossigeno ma anche in
seguito a riperfusione
• Autoimmunità
• Lupus: Mancata morte di Linfociti B che
producono anticorpi che riconoscono il corpo
• Infezioni virali
• HIV
Fasi dell’apoptosi
Il processo apoptotico può essere diviso in
diverse fasi temporali:
- Iniziazione: cellule determinate alla morte
- Esecuzione: alterazioni morfologiche
- Riconoscimento e fagocitosi: eliminazione dei
resti cellulari da parte di cellule specializzate
Morfologia delle cellule apoptotiche
Modificazioni morfologiche
- Diminuzione del volume
- Arrotondamento (in cellule adese)
- Cambi a livello della membrana plasmatica (pur
rimanendo integra): esposizione di particolari lipidi,
perdita di estensioni e contatti
- Condensazione della cromatina, taglio del DNA e
perdita dell’involucro nucleare
- Distruzione del citoscheletro
- Frammentazione in corpi apoptotici
Meccanismi molecolari dell’apoptosi
Stimolo apoptotico
Caspasi iniziatrici
Caspasi effettrici
Taglio di numerose proteine.
citoscheletro, lamina nucleare, inibitori di DNAasi, enzimi di riparo del DNA
Cambi morfologici
che portano alla morte della cellula
Caspasi
(Cistein Aspartasi)
Proteasi: proteine che
digeriscono altre
proteine
Responsabili di molte
delle alterazioni
osservate nelle cellule
apoptotiche
Tagliano varie proteine
per inattivarle e
degradarle.
Tagliano anche loro
stesse per attivarsi
Caspasi Iniziatrici Caspasi Esecutrici
Attivazione delle Caspasi
16 Citologia, Istologia e Anatomia microscopica © Pearson Italia S.p.A.
Vie di attivazione dell’apoptosi
Via intrinseca:
- lo stimolo (il danno) insorge da dentro la cellula;
- il mitocondrio gioca un ruolo importante
Via estrinseca:
- lo stimolo arriva da fuori
- recettori di membrana giocano un ruolo importante
Via estrinseca
Ligandi e
Recettori di
Morte
Adattatori
Attivazione delle
caspasi iniziatrici
(caspasi 8)
tramite
dimerizzazione
Via intrinseca
Lo stimolo apoptotico
porta alla formazione di
pori nel mitocondrio che
rilasciano il Citocromo C.
Il Citocromo-C lega la
proteina APAF1 e ne
induce l’assemblaggio in
oligomeri.
Le caspasi legano APAF1
formando l’apoptosoma, e
si attivano tramite
dimerizzazione
L’aumentata
permeabilità della
membrana
esterna del
mitocondrio
(MOMP) è dovuta
alle proteine
proapoptotiche
Bak/Bax che si
assemblano a
formare dei pori.
Cosa regola l’attività di
Bax e Bak?
Ruolo delle proteine della
famiglia Bcl-2
- Proteine proapoptotiche
sono necessarie per
attivare Bax/Bak
- Proteine antiapoptotiche
con 4 domini (BH1-4)
legano e inattivano le
proteine proapoptotiche
Alcune vie intrinseche di attivazione dell’apoptosi iniziano
dal Reticolo Endoplasmatico o dal Nucleo
Stress del RE : Rilascio di calcio,
attivazione delle caspasi, sintesi
di attivatori delle caspasi
Danno al DNA: Attivazione del
fattore trascrizionale p53 e
sintesi di attivatori delle caspasi
Riconoscimento e fagocitosi
La morte cellulare è solo
metà del processo
• L’eliminazione dei corpi apoptotici è parte
fondamentale del processo in vivo
– Previene la risposta infiammatoria
– Ripulisce il tessuto
• L’eliminazione è un processo attivo
– Fagocitosi
Segnali che attivano la fagocitosi
Visione di insieme dell’Apoptosi
Necrosi:
Morte passiva
Indotta da
agenti non
fisiologici
La cellula si
rigonfia e
scoppia, con
conseguente
rilascio di
materiale
citoplasmatico
ad azione
infiammatoria
Autofagia
Il processo che permette di veicolare componenti
intracellulari nel lisosoma per la loro degradazione
AUTOFAGIA: caratteristiche morfologiche
AP: autofagosomi
AL: autolisosomi
AUTOFAGIA
Quando abbiamo la necessità di autodigerire
i costituenti delle nostre cellule?
Fare il tagliando alle cellule: sostituire i pezzi che si
‘’invecchiano’’ nel corso della vita (autofagia basale)
Rispondere agli stress (autofagia indotta):
- Eliminare rapidamente ciò che lo stress ha
danneggiato (aggregati proteici o organelli mal
funzionanti)
- Rimuovere corpi estranei all’interno della cellula
(contrastare le infezioni)
- Riciclare il materiale ottenuto dalla degradazione per
utilizzarlo per nuova sintesi in situazioni di emergenza
(carenza di nutrienti o energia)
L’autofagia è essenziale per superare
gli stress…fin dal primo: la nascita
GFP-LC3
Atg5 -/Topi mutanti per i geni autofagici muoiono
poche ore dopo la nascita
Autofagia e sviluppo
- Rimozione mitocondri negli
eritrociti
- Rimozione mitocondri
paterni nell’uovo fecondato
Autofagia e Patologia
Difetti di autofagia sono
associati all’insorgenza di
malattie neurodegenerative
Es.: Parkinson familiare
presenta mutazioni nei geni
Parkin e Pink che regolano la
rimozione di mitocondri
danneggiati
Autofagia e morte cellulare
In seguito a danno, la cellula induce molto rapidamente
l’autofagia come meccanismo di sopravvivenza, nel
tentativo di rimuovere il danno.
Se il danno è troppo grave, successivamente viene
indotta l’apoptosi che è anche in grado di inibire
l’autofagia (caspasi degradano proteine regolatrici
dell’autofagia)
L’autofagia diventa un «vero» meccanismo di morte
quando l’apoptosi non funziona. Solo in questo caso la
permanenza di un danno irreparabile porta ad una
attivazione troppo prolungata dell’autofagia che causa
l’autodigestione della cellula e la sua morte.