![(Microsoft PowerPoint - Respirazione [modalit\340 compatibilit\340])](//s1.studylibit.com/store/data/005389674_1-a26fad8be37ceeba30a7c27b4044a2d6-768x994.png)
RESPIRAZIONE
Ossidazione di composti organici per trarre
l’energia
necessaria
per
i
processi
endoergonici di sintesi. La demolizione
avviene tramite reazioni di ossido-riduzione.
Substrati: glucidi, acidi mono- (acidi grassi)
e bicarbossilici, amminoacidi, glicerina
Equivalenti
termici
(calorie
prodotte
dall’ossidazione totale di 1 g di sostanza): 4
kcal glucidi, 9,2 kcal per i lipidi, 5,7 kcal
per i protidi.
- Glicolisi (citosol)
- Ciclo di Krebs (mitocondri)
- Trasporto elettronico (mitocondri)
C6H12O6 + 6 O2 → 6 CO2 + 6 H2O
(∆
∆G0’ = -2.870 kJ mol-1)
Fattori che influenzano la respirazione:
- stadio di sviluppo
- organo
- grado di vitalità
- temperatura
- ossigeno (anossia terreno)
- luce
Quoziente respiratorio (QR) = CO2/O2
glucidi = 1 C6H12O6+6O2 → 6CO2+6H2O QR=6/6=1
lipidi, proteine < 1
C18H36O2+26O2 → 18CO2+18H2O QR=18/26=0,69
acidi ossigenati > 1
acido malico COOH-CHOH-CH2-COOH+3O2 → 4CO2+3H2O
QR=4/3=1,3
acido ossalico COOH-COOH+½ O2 → 2CO2+H2O
QR=2/0,5=4
Tanto minore è il QR tanto maggiore sarà il rendimento
energetico.
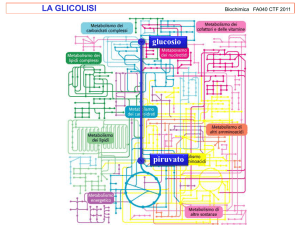
Glicolisi
glucosio + 2 Pi + 2 ADP + 2 NAD+ →
2 piruvato + 2 ATP + 2 H2O + 2 NADH + 2 H+
la fosforilazione attiva il glucosio e rende il
composto polare (non può uscire dalla
cellula)
ATP cede un gruppo fosforile
aldoso
chetoso
Pi = HPO42-
~
Composto ad alta energia
Fosforilazione a livello
del substrato
~
Composto ad alta energia
(forma enolica del piruvato)
Fosforilazione a livello
del substrato
(forma chetonica più stabile)
Regolazione della glicolisi (1)
Regolazione della glicolisi (2)
Fermentazione
La membrana esterna è relativamente permeabile ai soluti (presenza
di proteine-canale), mentre quella interna presenta trasportatori
specifici (trasporto attivo secondario). Il piruvato entra nella matrice
mediante un antiporto con ioni OH- (gradiente di ∆pH).
Complesso della piruvato deidrogenasi (matrice)
Ciclo di Krebs
Reazione netta del ciclo di Krebs
Acetil-SCoA + 3 NAD+ + FAD + GDP + Pi + 2 H2O
↓
2 CO2 + 3 NADH + FADH2 + GTP + CoASH + 3 H+
(dal punto di vista energetico GDP = ADP)
Catena respiratoria
Meccanismo di ossido-riduzione, consistente nella
ossidazione del composto iniziale (donatore) che
cede elettroni i quali, attraverso una serie di
trasportatori, riducono il composto finale, cioè
l’ossigeno (accettore) che li acquista.
Ogni trasportatore deve avere un potenziale redox
meno positivo di quello che viene ridotto, cioè di
quello che segue. La catena scorre quindi nel senso
di potenziali redox crescenti.
NADH dehydrogenase
FADH2
FAD
Succinate
dehydrogenase
Cytochrome
reductase
Cytochrome
oxidase
2
2
2H+
Gruppi Fe-S
2H+
2
2
Sistema navetta
Gli elettroni associati ai NADH prodotti
durante la glicolisi vengono ceduti alla catena
respiratoria mediante un ‘sistema navetta’ in
quanto i NADH citosolici NON sono capaci di
penetrare
all’interno
della
matrice
mitocondriale.
Inserimento a livello dell’ubichinone tramite un
complesso denominato NADH deidrogenasi
esterna.
Traslocazione di 6 H+
NADH deidrogenasi
esterna
Glicerolo 3-fosfato
NADH deidrogenasi
esterna
Teoria chemiosmotica
Le piante, trasferendo H+ attraverso la membrana
mitocondriale interna, stabiliscono un gradiente
elettrico, cioè una differenza di potenziale
elettrico (potenziale di membrana, ∆E), ed un
gradiente protonico, cioè una differenza di pH
(∆
∆H+, ∆pH).
Il gradiente elettrochimico ∆µ (forza motrice
protonica) conseguentemente originato può svolgere
un lavoro chimico, vale a dire che l’energia
liberata con il ritorno dei protoni alla condizione
originaria viene impiegata per fosforilare l’ADP ad
ATP.
∆G = RT ln [H+]B/[H+]A
gradiente protonico
∆G = nF ∆E
gradiente elettrico
Quando dalle due parti di una membrana
esiste un ∆E ed un ∆pH, la differenza di
energia libera derivante dagli H+ presenti ai
due lati della membrana (dovuta alla
concentrazione dei protoni e delle cariche) è
data dalla somma dei due ∆G secondo la
relazione:
∆G = 2,3 RT log10 [H+]B + nF ∆E
[H+]A
La differenza di energia libera ∆G può essere
espressa in termini di gradiente elettrochimico
∆µ.
∆µ Poiché ∆µ = ∆G/F, si ha che:
∆µ = ∆E - 2,3 RT ∆pH
F
Dal punto di vista energetico la sintesi di 1 ATP
richiede 3 H+.
NADH deidrogenasi
esterna
ATP sintasi
Dal punto di vista stechiometrico la sintesi di 1 ATP richiede
4 H+ (un quarto protone è richiesto per il trasporto del Pi
all’interno della matrice e non per motivi energetici).
Energetica della respirazione
NADH mitocondriale: H+/2e-=10 e H+/ATP=4 (ATP/2e-=2,5)
NADH citosolico, FADH2: H+/2e-=6 e H+/ATP=4 (ATP/2e=1,5)
Partendo da una mole di glucosio:
glicolisi
fosforilazione a livello del substrato 2 ATP
2 NADH
3 ATP (12 H+ traslocati)
complesso piruvato deidrogenasi e ciclo di Krebs
fosforilazione a livello del substrato 2 ATP
8 NADH
20 ATP (80 H+ traslocati)
2 FADH2
3 ATP (12 H+ traslocati)
30 ATP
Quoziente respiratorio (QR) = CO2/O2
glucidi = 1
lipidi, proteine < 1
acidi ossigenati > 1
Tanto minore è il QR tanto maggiore sarà il rendimento
energetico. Tanto più il composto è ricco di H (e quindi di
elettroni → formazione di equivalenti riducenti), tanto più
alta sarà la produzione di energia.
LA VIA DEI PENTOSI FOSFATO
Detta anche via dell’esoso monofosfato, si
svolge nel citosol e nei cloroplasti (al buio). Ha
la funzione di generare intermedi fosforilati ed
equivalenti riducenti (NADPH) per i processi
anabolici.
ribosio 5-fosfato ⇒ acidi nucleici
eritrosio 4-fosfato ⇒ amminoacidi, polifenoli
NADPH ⇒ sintesi acidi grassi
1 glucosio → 12 NADPH + 12 H+ + 6 CO2
Tranchetolasi: trasferimento
di un gruppo bicarbonioso da
un chetoso ad un aldoso
Transaldolasi: trasferimento
di un gruppo tricarbonioso da
un chetoso ad un aldoso
Importanza: possibilità di
interconversione dei glucidi
mediante
reazioni
non
ossidative.
*prodotti finali
![(Microsoft PowerPoint - Respirazione [modalit\340 compatibilit\340])](http://s1.studylibit.com/store/data/005389674_1-a26fad8be37ceeba30a7c27b4044a2d6-768x994.png)