Tossicità del MTX nell’artrite reumatoide
Il MTX è uno dei farmaci basilari nella cura dell’artrite reumatoide (AR), essendo uno dei farmaci
DMARDs che può fortemente incidere sul decorso della malattia (vedi sezione per approfondire),
tuttavia l’uso cronico anche a basse dosi del farmaco ha evidenziato diversi effetti tossici.
Recentemente sono stati pubblicati diversi articoli che focalizzano la loro attenzione sul
monitoraggio di tale immunosoppressore a basse dosi. Gilani e collaboratori (1) valutarono la
frequenza e la tipologia di eventi avversi attribuiti al MTX e la concentrazione minima tossica con
basse dosi di MTX in pazienti affetti da AR.
Lo studio
Si trattava di uno studio osservazionale cross-sectional o trasversale. I pazienti reclutati erano 140,
di cui 68 maschi (49%) e 72 femmine (51%), i quali ricevettero basse dosi di MTX (10 mg/a
settimana) per circa 3 mesi. Furono poi raccolti campioni di sangue dopo 2 h dalla
somministrazione orale del farmaco e valutati i livelli di GOT ,GPT e creatinina.
Dai risultati si notò che dei 140 pazienti trattati, 38 sviluppavano tossicità da MTX (27%), con
epatotossicità in 12 pz (8.6%), nefrotossicità in 3 (2.1%), anemia in 8 (5.7%), leucopenia in 2
(1.4%), trombocitopenia in 3 (2.1%), pancitopenia in 2 (1.4%), eventi avversi gastrointestinali in 5
(3.6%) e problemi cutanei in 3 (2.1%).
Il limite massimo di concentrazione minima tossica legata al MTX era di 0.71 μmol/l. Si evinse,
cosi, che la tossicità da MTX poteva essere rilevata solo con un monitoraggio costante della sua
concentrazione plasmatica che non doveva superare i 0.71 μmol/l (1).
Altro studio effettuato fu quello di Buhroo e collaboratori del 2006. Anche in tale studio si
analizzarono gli eventuali effetti avversi attribuibili al MTX a basse dosi in pazienti affetti da AR.
Vennero reclutati 295 pazienti affetti da AR dai 18 anni in su, nel periodo 1997- 2004. I pazienti
includevano sia nuovi casi di AR che non, con fallimento a continuare terapia con altri DMARDs
per un periodo minimo di 3 mesi dovuto alla non-effectiveness o non disponibilità (6).
Per approfondire
L’artrite reumatoide
L’artrite reumatoide è una malattia cronica autoimmune che colpisce circa 300.000 italiani e oltre
1.3 milioni di persone negli USA. Solitamente colpisce più le donne e si manifesta tra i 40-60 anni
di età. La malattia è difficile da diagnosticare in quanto i sintomi sono spesso modesti, almeno
nella fase iniziale, con rigidità articolare, affaticamento al mattino, perdita di energia, febbricola.
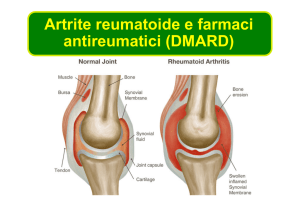
La causa della malattia ancora è sconosciuta. E’ caratterizzata da infiammazione della membrana
sinoviale. Si tende a pensare che un agente esterno (infettivo,forse) si leghi ai recettori delle cellule
dendritiche che si spostano nei linfonodi, attivando il sistema immunitario. Una volta attivati , i
linfociti T proliferano e migrano verso l’articolazione e il tessuto sinoviale. I linfociti T producono
interferone gamma e citochine pro infiammatorie che stimolano macrofagi, fibroblasti e monociti.
Essi generano a loro volta altre citochine coinvolte nella patogenesi dell’AR , quali il fattore di
necrosi tumorale alfa (TNF-alfa), l’interleuchina-1 e 6 nel tessuto sinoviale. Tali citochine hanno
un ruolo chiave in quanto inducono la liberazione di metalloproteasi della matrice ed attivano cosi
gli osteoclasti, che determinano l’infiammazione e danno irreversibile dei tessuti molli e delle ossa.
Dato la natura infiammatoria della malattia i segni più evidenti saranno il dolore, gonfiore e
tumefazione delle articolazioni (più colpite quelle di mani e piedi) (2,3,4).
Attualmente oltre ai FANS e corticosteroidi, la categoria di farmaci più usata è rappresentata dai
Lo studio
DMARDs(
disease-modifying antirheumatic drugs), ossia farmaci antireumatici che modificano il
decorso della malattia, prevenendo la progressione della malattia ed il danno articolare. Tra
questi ricordiamo il metotrexato che viene usato in monoterapia, anche.
Ma,oggi, l’evidenza supporta l’uso di MTX in combinazione con altri DMARDs:
idrossiclorochina
sulfasalazina
leflunomide
Sebbene il MTX fu sintetizzato nel 1948 come antitumorale ed il primo uso risale al 1951, il suo
utilizzo nella AR risale al 1970 (5).
Erano esclusi dallo studio:
soggetti con insufficienza renale ed epatica
soggetti con diabete mellito non controllato
soggetti con grave scompenso cardiaco, malattie polmonari,tumori
soggetti con leucopenia e/o trombocitopenia
donne incinte
Nei pazienti coinvolti venne somministrato MTX alla dose di 7.5 mg a settimana per via
intramuscolare. I pazienti vennero monitorati a 2 settimane, 3 settimane, 3 mesi e 6 mesi.
Il monitoraggio del paziente prevedeva la conta di GOT, GPT, albumina sierica ogni 4-8 settimane
e speciali indagini con gli ultrasuoni per valutare la funzionalità polmonare in caso di sintomi
sospetti.
Dei 295 pazienti reclutati alcuni furono poi esclusi: 27 non si presentarono più dal primo
monitoraggio e 23 non risposero al farmaco.
Rimasero cosi 245 pazienti. Qui di seguito riportiamo la suddivisione per genere ed età dei pazienti.
Età
21-30
31-40
41-50
51-60
>60
totale
Maschi
2
14
31
8
4
59
Femmine
12
34
84
43
13
186
Tab.1.1. Pazienti arruolati
L’osservazione
La maggioranza dei pazienti era già trattata con FANS (ben 204), 31 con corticosteroidi (prednisone
principalmente) e 25 con altri DMARDs .
Di questi ultimi 8 pazienti erano trattati con sulfasalazina, senza aver avuto grandi miglioramenti.
A tutti i gruppi di pazienti venne somministrato MTX, in quei pazienti che facevano già uso di
FANS per via orale si preferì dapprima la somministrazione intramuscolo del farmaco per poi
convertirla ad orale dopo 2 mesi. Negli altri pazienti il MTX veniva somministrato per via orale alla
dose di 7.5 mg a settimana, inizialmente, per poi aumentarla fino ad un massimo di 20 mg a
settimana.
Nei pazienti che facevano uso di FANS e corticosteroidi la dose di essi venne diminuita
gradualmente.
Dei 245 pazienti, 96 (39.2%) riportarono eventi avversi collegabili al MTX (2).
Evento avverso
Gastrointestinale (vomito,
diarrea e dispepsia)
Emato-tossicità
Aumento enzimi epatici e
(< 2 volte)
Aumento enzimi epatici e
(> 2 volte)
Eventi cutanei
Ulcerazioni al labbro
Noduli
Eventi avversi apparato
respiratorio
Numero
51
Percentuale
21
29
74
11.8
30
3
1.2
3
5
7
0
1.2
2.0
2.9
0
Tab.1.2 Eventi avversi sviluppati con MTX a basse dosi
Da come si evince dalla tabella 1.2, si notava come la gastrotossicità era più diffusa (21%), con
nausea in 38 pz (15.5%), vomito in 13 pz (5.3%) e diarrea in 6 pz (2.45%). L’utilizzo di acido
folico, anti-H2 e antiacidi riduceva tali effetti.
Solo due pazienti dovettero bloccare del tutto il farmaco e sostituirlo con altri DMARDs ,in quanto
gli effetti gastrici erano importanti.
Ematotossicità
Leucopenia
Pan citopenia
Anemia megaloblastica
Trombocitopenia
Femmine
21
2
1
0
Maschi
5
0
0
0
Tab 1.3. Ematotossicità
In 74 pz (30%) i livelli degli enzimi epatici si innalzarono; si trattava di un aumento temporaneo e
leggero (poco più del 15%). Solo in 3 pz l’incremento fu del doppio dei livelli normali ed in questo
caso si bloccò la terapia (2).
Tossicità in combinazione
Dato che nella maggior parte dei casi di AR , il MTX non viene somministrato da solo una review
pubblicata nel 2008 valutò l’efficacia e tossicità del MTX in combinazione con altri DMARDs in
tali pazienti.
Vennero analizzati 19 trials (2025 pz), molti dei quali avevano una durata che andava dai 6 ai 12
mesi. Il range della dose di MTX andava dai 5 ai 18mg/settimana e la somministrazione in tutti i
trials era orale.
I trials in pazienti naive a DMARDs non mostravano significativi vantaggi del MTX in
combinazione rispetto alla monoterapia.
Il MTX in combinazione con azatioprina aumentava il rischio di eventi avversi con RR=1.67.
La sulfasalazina e leflunomide in combinazione con MTX aumentava il rischio di eventi avversi
gastrointestinali con RR=1.67.
Mentre il MTX solo con leflunomide determinava un aumento del rischio di alterazioni della
funzionalità epatica con RR=4.3
Per quanto riguarda il rapporto rischio/beneficio era maggiore in uno studio che prevedeva l’uso di
MTX in combinazione con sulfasalazina e idrossiclorochina, rispetto a MTX da solo, con RR 0.3.
Ma casi di tossicità erano più significativi per MTX in combinazione con ciclosporina e azatioprina.
Ovviamente i trials analizzati erano effettuati su pazienti selezionati e spesso non riflettono la
pratica clinica; non solo, la dose di MTX usata nei vari trials analizzati era poco più bassa di quella
usata nella pratica corrente (6).
In conclusione
E’ bene perciò contestualizzare tali dati e in linea generale possiamo dire che:
1. la combinazione delle terapie DMARDs non migliora di molto l’efficacia e la tossicità spesso
aumenta, invece
2. solo uno studio di quelli valutati mostrava un miglior rapporto efficacia/tossicità, quello con
MTX, sulfasalazina e idrossiclorochina, rispetto al MTX da solo
3. aggiungendo la leflunomide ai pazienti non-responders al solo MTX ,invece, aumentava
l’efficacia ma anche i rischi di tossicità gastrointestinale ed epatica.
BIBLIOGRAFIA
1.
Gilani ST, Khan DA, Khan FA, Ahmed M.; Adverse effects of low dose methotrexate in
rheumatoid arthritis patients; J Coll Physicians Surg Pak. 2012 Feb;22(2):101-4.
2. Mohammad Buhroo, Baba; Adverse Effects of Low-Dose Methotrexate in Patients with
Rheumatoid Arthritis; IJPMR; October 2006; 17 (2) : 21-25
3. Ruderman E,Tambar S; Rheumatoid arthritis. ACR Education and Research Foundation.
4. Scott DL,Kingsley GH; Tumor Necrosis factor inhibitors for rheumatoid arthritis; N. Engl.J
Med;2006,355:704-721
5. Olsen NJ,Stein CM;New drugs for rheumatoid arthritis; N.Engl.J.Med.; 2004;305:21672179
6. Katchamart et al;Efficacy and toxicity of MTX monotherapy versus MTX combination
therapy with non-biological DMARds in rheumatoid arthritis:a sistematic review and metaanalysis;Ann Rheum Dis; 2009;1105-1112