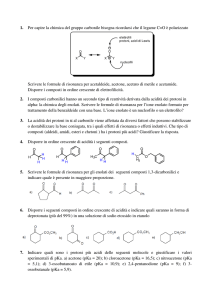
Sintesi degli esteri (1)
percorso 2
Sintesi degli esteri (1)
Materiale occorrente:
• una bilancia tecnica;
• un pallone a fondo sferico da 500 ml;
• una pipetta graduata da 5 ml;
• un refrigerante a ricadere (a bolle);
• un mantello riscaldante.
Reattivi:
• acido acetico glaciale;
• etanolo al 96%;
• acido solforico concentrato (96%).
Pericoli:
• fare attenzione alla manipolazione della soluzione al 96% di H2SO4, che è corrosiva.
• la reazione e le operazioni di separazione vanno condotte rigorosamente sotto cappa poiché
l’acetato di etile (estere) ha una certa tossicità e può produrre, inalandolo, mal di testa.
Principio
Gli esteri sono composti organici provenienti dalla reazione tra un acido carbossilico
(R-COOH) e un alcol (R’-OH).
Trattando, a caldo, l’acido acetico (acido etanoico) con l’alcol etilico (etanolo) in
ambiente acido per acido solforico (H2SO4) si ottiene acetato di etile (etanoato di
etile) e acqua:
Δ CH COOC H + H O
CH3COOH + C2H5OH "
3
2 5
2
Metodica
Si pesano 80 g (1 mole con eccesso) di acido acetico glaciale (CH3COOH) e si introducono in un pallone con il collo smerigliato da 500 ml.
Successivamente si aggiungono, pesandoli, 48 g (1 mole) di etanolo (C2H5OH) al 96%.
Si monta sul pallone con il collo smerigliato un refrigerante a bolle (condensatore di
Allihn).
Il condensatore è a sua volta collegato a un rubinetto e a uno scarico per garantire
l’afflusso di acqua (fluido refrigerante).
Si introduce il sistema pallone-refrigerante in un mantello riscaldante.
Il refrigerante deve essere collegato saldamente all’asta verticale del mantello mediante una pinza.
1
percorso 2
Sintesi degli esteri (1)
Si accende il mantello e si porta il miscuglio liquido all’ebollizione, mantenendovelo
per un’ora.
A questo punto si spegne il mantello e si fa raffreddare
il liquido, travasandolo in un imbuto separatore da 500
ml fino a che non si nota la separazione dell’acetato di
etile dalla fase acquosa.
L’acetato di etile (CH3COOC2H5) non è solubile in acqua e ha una densità minore di quest’ultima (quindi
galleggia).
L’acetato di etile (CH3COOC2H5) si separa dall’acqua e
dall’eccesso di acido acetico per mezzo di un imbuto
separatore.
Attenzione: la reazione e le operazioni di separazione vanno condotte rigorosamente sotto cappa poiché
l’acetato di etile (estere) ha una certa tossicità e può
produrre, inalandolo, mal di testa.
Figura 1
Apparecchiature per l'esterificazione
2