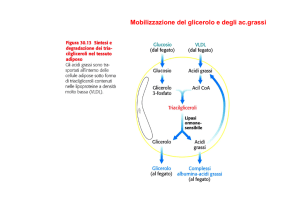
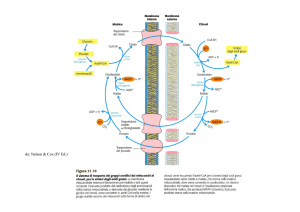
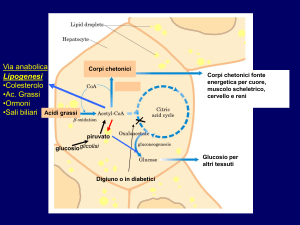
Biosintesi degli acidi grassi
1
Confronto tra b-ossidazione e biosintesi degli acidi grassi
2
Sistema di trasporto dei tricarbossilati:
con queste reazioni si trasferisce
l’acetil CoA dal mitocondrio al citosol
3
Prima tappa della biosintesi degli acidi grassi:
sintesi del malonil CoA
con una reazione catalizzata dall’enzima
Acetil-CoA carbossilasi (biotina dipendente)
4
HCO3- + ATP
E-biotina
E-biotina-CO2
O
CH3-C-SCoA
E-biotina-CO2
O
-O2C-CH2-C-SCoA
Malonil CoA
+ E-biotina
+
5
L’acetil CoA carbossilasi dei mammiferi
è sotto controllo allosterico
e ormonale
6
L’ acetil CoA carbossilasi è costituita da 21 protomeri
ciascun protomero è costituito da tre subunità
1. La biotina carbossilasi
2 . La carbossil trasferasi
3. Il carrier della biotina
Questo enzima è regolato da un duplice meccanismo:
1. depolarizzazione e polarizzazione
2. fosforilazione e defosforilazione
7
Regolazione dell’acil CoA carbossilasi
È attivo quando è defosforilato e polimerizzato
E’ inattivo quando è fosorilato e depolimerizzato
8
L’acetil CoA carbossilasi è sotto il controllo ormonale:
• L’ insulina – tramite la defosforilazione del sito
attiva l’enzima promuovendo la polimerizzazione
Glucagone
Adrenalina
Nor-Adrenalina
Stimolano la fosforilazione AMPdipendente di un sito dell’enzima
inattivando e depolimerizzando
l’enzima
INOLTRE
Il citrato favorisce la forma A polimerica dell’enzima
che è attiva
In presenza di
acetil CoA o in assenza di Citrato la
forma polimerica si dissocia, inattivandosi nei protomeri
9
costituenti
La sintesi degli acidi grassi richiede 7 reazioni
enzimatiche catalizzate dal complesso multienzimatico
acido grasso sintasi
e parte da
acetil CoA + malonil CoA
Il complesso contiene 7 attività enzimatiche e
una proteina trasportatrice degli acili
10
• La sintesi degli acidi grassi non è
semplicemente l’ inverso della via
degradativa
• Entrambe le vie sono sempre
distinte,hanno infatti sede diverse
• Gli intermedi nella sintesi degli acidi
grassi sono legati covalentemente ai gruppi
sulfidrilici di una proteina trasportatrice
di Acili ( ACP )
• La catena dell’acido grasso in crescita
viene allungata dall’addizione sequenziale
di unità bicarboniose derivate dall’ acetil
CoA
Il donatore attivato di unità bicarboniose è
la malonil ACP
11
RAPPRESENTAZIONE SCHEMATICA DELL’ACIDO
GRASSO SINTASI UN DIMERO CHE CONTIENE
TRE DOMINI
Primo dominio
Secondo dominio
( deidratasi )
Terzo dominio
( b-chetoacil riduttasi )
(ACIL- TRANSFERASI ) (MALONIL- TRANSFERASI)
( enoil reduttasi )
( tioesterasi )
( E NZIMA CONDENSANTE )
12
• traslocazione dell’acido grasso in allungamento tra il gruppo
solfidrilico del residuo di cisteina dell’enzima condensante
• il gruppo sulfidrilico della fosfopantoteina della ptoteina
trasportatrice di acili determinano la crescita della catena
• Le reazioni si ripetono finchè non viene sintetizzato il
prodotto palmitico
13
Reazioni catalizzate
Dall’acido grasso sintasi
14
L’allungamento è mediato da un altro
complesso multienzimatico, l’acido
grasso elongasi, situato sul reticolo
endoplasmatico.
Le unità a due atomi di C che si
aggiungono derivano dal malonil CoA.
15
ENZIMI LEGATI ALLA MEMBRANA DEL R.E.
- OSSIDASI A FUNZIONE MISTA GENERANO ACIDI GRASSI INSATURI
R-CH2-CH2-(CH2)7-COOH + NADH + H+ + O2
Stearoil CoA
R-CH-CH-(CH
2)7-COOH
oleoil CoA
+ NAD+ + 2H2O
doppio legame cis-D9
16
Allungamento mitocondriale degli acidi grassi
Anche i MT sono in grado di allungare gli
acidi grassi ma utilizzano acetil CoA come
donatore di unità bicarboniose.
17
SCHEMA RIASSUNTIVO
ALLUNGAMENTO DEGLI ACIDI
GRASSI
Sistema mitocondriale
• il palmitato attivato in palmitoil-CoA entra nel mitocondrio
• il sistema di trasporto è carnitina dipendente
• condensazione del palmitoil CoA con l’acetil CoA
• riduzione NADH(H)+ dipendente del chetoacil-CoA
• deidratazione dell’idrossiacil-CoA
• riduzione NADPH(H)+ dipendente del deidro acil -CoA
NAD(P)H(H)+
NAD(P)+
Palmitoil-CoA
Stearil-CoA
Acetil-CoA
CoA
18
SISTEMA MICROSOMIALE
• questo sistema utilizza maloni-CoA
• e gli equivalenti riducenti del NADPH(H)+
2 NADPH(H)+
2 NADP
Palmitoil CoA
Malonil-CoA
Stearil-CoA + CO2
CoA
19
REGOLAZIONE GLOBALE
• La sintesi e la degradazione degli acidi grassi sono
regolate reciprocamente
• Il malonil CoA inibisce la carnitina acil transferasi I
impedendo l’accesso degli acil CoA alla matrice
mitocondriale nei momenti di abbondanza
• Nello stato di digiuno la concentrazione degli acidi grassi
liberi aumenta poiché ormoni quali l’adrenalina e il glucagone
stimolano la lipasi delle cellule adipose
1 20
• Nel controllo a lungo termine si ha la modulazione della
sintesi degli enzimi coinvolti nella sintesi degli acidi grassi:
Citrato liasi,enzima malico,l’acetil-CoA carbossilasi,
l’acido grassi sintasi
Il contenuto epatico di questi enzimi, che hanno tutti una breve
emivita diminuisce a digiuno e nel diabete insulino privo, aumenta
in seguito a somministrazione di glucosio e insulina con:
aumento dei
glucidi
Stimola la biosintesi degli enzimi
della lipogenesi
conversione dei glucidi in lipidi
2
21
La desaturazione è attuata dalla stearoil-CoA desaturasi
ed è regolata a seconda delle necessità dell’organismo
Aumenta in seguito ad alimentazione
glucidica (questi formano ac. grassi
saturi) e in seguito all’azione
dell’insulina
Diminuisce dopo somministrazione di
ac. grassi insaturi
22
IMPORTANTI ACIDI GRASSI
Acido stearico
Acido oleico
Acido linoleico
Acido linolenico
18:0
18: 1(9)
18: 2(9,12)
18:3 (9,12,15)
L’acido linolenico è particolarmente importante poiché
viene convertito, attraverso una serie di allungamenti e
desaturazioni in acido arachidonico, un precursore della
sintesi delle prostaglandine e altri eicosanoidi
23
Desaturazione dell’acido linoleico
NAPH(H)+
18:2(9, 12)
acido linoleico
O2
NADP+
2H2O
2CO2
18:3 (6,9,12)
ac.-linoleico
20:3(8,11,14)
O2
2H2O
NADPH(H)+
NADP
Nell’uomo le desaturasi non sono in
grado di introdurre doppi legami tra
20:4(5,8,11,14)
l’atomo di C 10 e l’atomo di C del
ac.arachidonico
gruppo metilico terminale, per cui
devono essere introdotti con la
dieta e quindi sono essenziali:
L’acido linoleico
L’acido linolenico
24
L’ARACONOIDATO E’ IL PRINCIPALE PRECURSORE DEGLI
ORMONI EICOSANOIDI ( prostaglandine, prostacicline,
trombossani )
CORTICOSTEROIDI
-
-
FANS
ciclo-ossigenasi -
L’arachidinato può essere convertito in leucotrieni per azione
della lipossigenasi
Questi composti scoperti inizialmente nei leucociti, contengono tre
25
doppi legami coniugati
METABOLISMO DEL COLESTEROLO
26
Il colesterolo è un costituente vitale delle membrane cellulari,
il precursore degli ormoni steroidei e degli acidi biliari.
Il suo deposito nelle arterie è associato a malattie cardiovascolari.
In un organismo sano viene mantenuto un delicato equilibrio tra:
biosintesi, utilizzo e trasporto
27
Principalmente nel fegato
L’acetil CoA è il precursore di partenza
per la biosintesi del colesterolo.
l’acido mevalonico contiene 6 C che derivano da
3 molecole di acetil CoA
28
condensazione
29
reazione di condensazione
30
31
CONTROLLO DEL METABOLISMO
DEL COLESTEROLO
1)Attività dell’ HMG CoA reduttasi
2)velocità di sintesi del recettore per le LDL
3)velocità di esterificazione del colesterolo
da parte di ACAT
32
L’HMG-CoA reduttasi è il principale sito di controllo
della biosintesi del colesterolo.
Controllo retroattivo a lungo termine
meccanismo di controllo principale
Controllo a breve termine
fosforilazione reversibile
33
Due strategie per contrastare
l’ipercolesterolemia
1) ingestione di resine che legano gli acidi biliari
-conversione del colesterolo in acidi biliari
-aumento della sintesi dei recettori per le LDL
!!!!!
aumento di HMG-CoA reduttasi
2) trattamento con inibitori
competitivi dell’ enzima
HMG-CoA reduttasi (statine)
34
La concentrazione intacellulare del colesterolo è finemente regolata
35
REGOLAZIONE DELL’ HMG-CoA
• la velocità di sintesi è regolata dalla proteina che lega l’ elemento
di regolazione degli steroli ( SREBP )
• questo fattore di trascrizione si lega a una breve sequenza del
DNA denominata elemento di regolazione degli steroli ( SRE ), che
si trova sul lato 5’ del gene per la riduttasi
• nel suo stato inattivo la proteina SREBP è ancorata al reticolo
endoplasmatico o alla membrana nucleare.
• quando la concentrazione di colesterolo si abbassa , il dominio
amminoterminale viene rilasciato dalla sua associazione con la
membrana mediante due scissioni proteolitiche specifiche
36
1
La proteina libera migra fino al nucleo e lega l’SRE del gene per
la HMG-CoA riduttasi, ma anche altri geni coinvolti nella
biosintesi del colesterolo, e ne promuove la trascrizione
• quando la concentrazione di colesterolo sale, la liberazione da
proteolisi della proteina SREBP viene bloccata, mentre quella già
presente nel nucleo viene degradata rapidamente .
• la degradazione della riduttasi è strettamente regolata.
L’enzima è costituito da due domini: il dominio citosolico, che
porta avanti la catalisi e il dominio di membrana che è un
sensore dei segnali che determinano la sua degradazione
• la fosforilazione determina la riduzione dell’attività dell’enzima come
l’acetil-CoA-carbosilasi
2
37
La rimozione del colesterolo dai tessuti è un processo mediato dalle HDL
38
39
40
L’ossido di azoto secreto dalle cellule endoteliali è
importante per la funzione delle pareti dei vasi
sanguigni.
bassi livelli di NO: sviluppo dell’ipertensione
alti livelli di NO: effetto protettivo contro l’aterosclerosi
riduce l’adesione dei monociti all’endotelio
riduce la proliferazione delle cellule muscolari lisce
41
Fine
42
gruppo acetile
gruppo malonile
in seguito alla sua
decarbossilazione, al malonil
CoA si lega l’acetil CoA
acetoacetil - ACP
43
Due subunità multifunzionali, associate testa-coda, formano il dimero
44
Controllo del metabolismo del colesterolo
Endocitosi mediata da recettore per le LDL nelle cellule di mammifero
45
Acil-CoA: colesterolo acil trasferasi (ACAT)
O
R-C-
Colesterolo esterificato
trasportato dalle lipoproteine
46
47
L’allungamento e l’insaturazione degli acidi grassi
sono catalizzati da sistemi enzimatici accessori
I sistemi del reticolo endoplasmatico hanno la funzione di
introdurre doppi legami negli acil CoA a catena lunga
Nella conversione dello stearoil CoA in oleiol CoA, viene
inserito un doppio legame cis 9 da un’ossidasi che impegna
ossigeno molecolare
48