LE ESOFAGITI – LA MALATTIA DA REFLUSSO GASTRO-ESOFAGEO – L’ESOFAGO DI
BARRETT
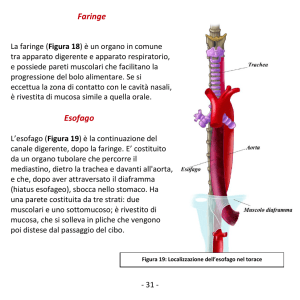
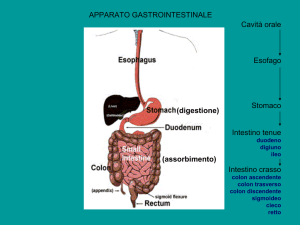
L’esofago è un organo tubulare muscolare, rivestito da epitelio malpighiano, che unisce il faringe allo
stomaco, e va dall’apertura del muscolo cricofaringeo (circa 20 cm dall’arcata dentale) alla giunzione
esofago-gastrica, nella zona dello iato diaframmatico (circa 40 cm dall’arcata dentale).
L’epitelio squamoso stratificato che ricopre tutto l’esofago presenta un colorito chiaro, grigio-roseo. Si
spinge fin oltre lo iato diaframmatico, dove incontra l’epitelio cilindrico monostratificato dello stomaco,
di colore roseo più intenso. La zona di passaggio fra i due tipi di mucosa assume l’aspetto di una linea
netta, ondulata, chiamata “ora serrata” o “linea z”.
Complesse sono l’anatomia e la fisiologia della giunzione esofago-gastrico. Il diametro esofageo è di 1,52 cm ed il lume presenta pliche longitudinali soffici, che si assottigliano gradualmente nel tratto distale; a
livello della giunzione esofago-gastrica tali pliche, nel numero di 4 o 5, assumono struttura simmetrica a
“rosetta”.
Le lesioni infiammatorie dell’esofago sono estremamente comuni e sono indicate con il termine generico
di esofagite. Per esofagite, dunque, si intende un processo infiammatorio, acuto o cronico, della mucosa
dell’esofago, causato nella maggior parte dei casi da reflusso acido dello stomaco, ma anche da cause
secondarie come l’ingestione di acidi e caustici, liquidi bollenti, da virus, batteri o funghi e da
radioterapia.
La causa più frequente è la malattia da reflusso gastro-esofageo (MRGE), caratterizzata dal passaggio
anomalo, per quantità e persistenza, di succo gastrico nell’esofago (il reflusso gastrico, entro certi limiti,
può essere considerato fisiologico). La patogenesi della MRGE è multifattoriale:
difetti del meccanismo antireflusso dello sfintere esofageo inferiore, che normalmente impedisce il
rigurgito, nell’esofago inferiore, delle secrezioni acide gastriche;
l’ernia iatale da scivolamento predispone significativamente all’esofagite da reflusso;
l’aumento del volume gastrico, qualunque ne sia la causa, contribuisce all’entità del reflusso;
i livelli di acido e di pepsina nel succo gastrico determinano il potenziale lesivo del reflusso;
un’inadeguata o rallentata clearance esofagea del materiale refluito è un importante fattore
predisponente. È implicata non soltanto la clearance del liquido rigurgitato ma anche il ripristino del
normale pH esofageo, che si attua principalmente con la deglutizione della saliva;
la stessa capacità ripartiva della mucosa esofagea è ridotta dall’esposizione protratta al reflusso
gastrico. La mucosa esofagea pluristratificata è impermeabile agli ioni H+ e, quindi, resistente alla
digestione peptica; con l’esposizione prolungata al reflusso gastrico essa diventa permeabile ad essi,
permettendo così il danneggiamento cellulare e, quindi, l’erosione e la desquamazione epiteliale.
I sintomi della MRGE sono molto vari: dalle forme tipiche, con pirosi retrosternale ascendente verso la
base del collo e spesso irradiato al dorso, dolore retrosternale e rigurgito acido entro tre ore dal pasto,
aggravati dalla posizione orizzontale, a quelle più severe, in cui il lungo tempo di contatto tra materiale
refluito e mucosa esofagea giunge e determinare sintomi dovuti a più o meno severe lesioni esofagee
(disfagia, emorragia..). Altri sintomi atipici, ma non infrequenti, sono le aritmie cardiache, la tosse
cronica specialmente notturna, l’asma bronchiale, la laringite, le polmoniti recidivanti, il singhiozzo
cronico. È da notare che non esiste un rapporto preciso fra gravità della sintomatologia e lesioni esofagee;
è possibile, cioè, che vi siano esofagiti, anche importanti, con pochi sintomi e, viceversa, una
sintomatologia importante con trascurabile danno esofageo.
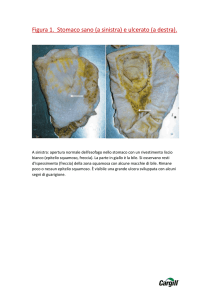
Morfologia ed anatomia patologica: le alterazioni anatomiche dipendono dalla gravità e dalla durata
dell’esofagite, nonché dall’agente etiologico causale. Macroscopicamente si può rilevare solamente una
lieve iperemia o irregolari lesioni superficiali o, in caso di malattia grave, un ispessimento della parete
conseguente all’edema o alla fibrosi che si producono in corrispondenza di erosioni superficiali confluenti
o anche di aree superficiali di necrosi e di ulcerazione della mucosa. Queste alterazioni sono più evidenti
nell’esofago distale, ma nei casi più gravi possono estendersi prossimalmente. La mucosa esofagea appare
1
rossastra, di aspetto granulare, ulcerata e può essere ricoperta di membrana infiammatoria
(pseudomembrana) bianco-grigiastra, simile a quella della candidiasi.
Il quadro istologico di un’esofagite causata dalla MRGE è caratterizzato da erosioni mucose o da
ulcerazioni più profonde, che si accompagnano ad infiltrato flogistico cronico. Macroscopicamente la
classificazione più utilizzata è quella di Savary – Miller – Monnier, che prevede cinque stadi:
GRADO
DESCRIZIONE
Unica, isolate (o spesso multiple) erosioni eritematose o eritemato1
essudative, interessanti una singola plica mucosa.
2
3
4
5
Erosioni multiple, interessanti più pliche mucose, parzialmente
confluenti, non circonferenziali.
Lesioni erosivo-essudative che confluiscono, circonferenziali, senza
stenosi.
a) una o più ulcere, con possibili stenosi o accorciamento
dell’esofago;
b) fibrosi stenosi o brachiesofago, con o senza erosioni o ulcere;
Presenza di metaplasia di Barrett.
A livello microscopico, negli stadi iniziali, modificazioni meno gravi includono iperplasia dello strato
basale e delle papille sottomucose, che possono estendersi fino al terzo superficiale dell’epitelio, con
presenza, in sede intraepiteliale, di granulociti eosinofili. Talora possono essere presenti sia alterazioni
displastiche delle cellule epiteliali squamose che fibrosi della parete, specie nelle forme di lunga durata.
L’esofagite cronica è un terreno fertile per lo sviluppo di un carcinoma.
Le lesioni elementari microscopiche riscontrabili, pertanto, nell’esofagite da reflusso sono:
1
2
3
4
5
6
7
8
Iperplasia basale, cioè espansione della zona basale per più del 15% dello
spessore dell’epitelio.
Allungamento delle papille della lamina propria per più del 15% dello
spessore dell’epitelio.
Venule intercapillari dilatate.
Granulociti neutrofili e eosinofili nella lamina propria.
Granulociti neutrofili, eosinofili e linfociti intraepiteliali (esocitosi).
Erosione - ulcerazione dell’epitelio.
Tessuto di granulazione.
Atipie epiteliali (d.d. con lesioni displastiche e/o carcinoma in situ).
In base ai riscontri microscopici si parlerà di:
esofagite da reflusso inattiva: coesistenza dei parametri 1, 2, 3;
esofagite da reflusso a basso grado di attività: presenza di almeno uno dei parametri 4, 5, anche
associati ai parametri 1, 2, 3;
esofagite da reflusso ad alto grado di attività: presenza dei parametri 6,7, anche associati ai
parametri 1, 2, 3, 4, 5.
Complicanze: le complicanze della MRGE sono le stenosi e la metaplasia di Barrett.
1. La stenosi da reflusso compare per l’estendersi della flogosi alla sottomucosa, provocando una
reazione fibrosa con genesi di tessuto cicatriziale. Il lume esofageo, così, si accorcia e si restringe.
Tali stenosi si verificano per lo più nell’esofago distale, ma se compare metaplasia di Barrett, essendo
2
la giunzione squamo-colonnare spostata prossimalmente, anche le stenosi sono più alte, a monte della
giunzione stessa. Le stenosi, di solito, sono brevi ma, talora, possono raggiungere anche i 10 cm.
2. L’esofago di Barrett è una metaplasia caratterizzata dalla sostituzione del normale epitelio squamoso
dell’esofago distale, al di sopra della giunzione esofago-gastrica, con epitelio colonnare, in soggetto
con reflusso severo e prolungato. A seconda dell’estensione del tratto di metaplasia di parlerà di:
long Barrett: quando l’area di metaplasia si estende per una lunghezza di almeno 3 cm dalla
giunzione esofago-gastrica;
short Barrett: quando l’area di metaplasia ha un’estensione inferiore ai 3 cm dalla giunzione
esofago-gastrica ed in quest’area si dimostri la presenza di epitelio di tipo intestinale specializzato.
L’esofago di Barrett è stato inizialmente considerato come un’alterazione congenita, ma studi
successivi hanno chiarito in modo inequivocabile che si tratta di una patologia acquisita. Esso sarebbe
l’esito di un processo adattivo della mucosa dell’esofago distale al reflusso cronico in quanto
l’epitelio colonnare offre maggiore resistenza all’aggressione del materiale refluito. Diversi costituenti
del succo gastrico contribuiscono alla patogenesi della metaplasia nei pazienti con MRGE. I principali
imputati sono la pepsina e l’acido cloridrico, ma la possibile insorgenza di esofago di Barrett dopo
gastrectomia suggerisce un potenziale ruolo patogenetico delle secrezioni biliari, intestinali o
pancreatiche. La grande importanza attribuita all’esofago di Barrett è legata alla sua potenziale
malignità, che comporta un rischio di evoluzione neoplastica fino a 350 volte superiore rispetto alla
popolazione generale. La prevalenza dell’esofago di Barrett nella popolazione generale, dimostrata in
corso di endoscopia, è di 22,6/100000 soggetti; tuttavia, indipendentemente dall’evidenza clinica e
sintomatologica di tale patologia, la reale prevalenza, che deriva da studi autoptici, risulta essere 17
volte superiore. La diagnosi di esofago di Barrett è endoscopica ma, soprattutto, istologica.
L’aspetto endoscopico di un esofago di Barret, di solito, è dato da mucosa prossimale normale, ora
serrata al terzo superiore o medio dell’esofago ed un tratto di colore rosa salmone di metaplasia sotto
l’ora serrata. Questo tratto si continua nella mucosa gastrica, di aspetto analogo. Nel tratto di
metaplasia sono assenti le pliche esofagee. Le stenosi, che vengono a complicare tale condizione, di
solito compaiono a livello della zona di passaggio tra epitelio squamoso ed epitelio colonnare; a valle
della stenosi, pertanto, si trova sempre epitelio colonnare, a meno che le stenosi non compaiano
sull’esofago distale per altre cause (ulcere o neoplasie). Le ulcere insorte su metaplasia di Barrett
possono comparire a qualsiasi livello del segmento interessato.
Dal punto di vista microscopico si possono riscontrare 3 diversi tipi di cellule:
epitelio tipo giunzionale o cardiale: è caratterizzato da un’architettura similfoveolare gastrica, con
epitelio superficiale colonnare e ghiandole mucose di tipo cardiale, talora dilatate. Vi possono essere
rare, sparse cellule caliciformi (NB: l’esofago di Barrett di tipo cardiale differisce, di solito, dalla
mucosa gastrica cardiale per la presenza di distorsione ghiandolare, edema ed infiltrati infiammatori
cronici);
epitelio gastrico fundico: è caratterizzato da architettura analoga alla mucosa ossintica, a superficie
foveolare, con epitelio superficiale mucosecernente e ghiandole costituite da cellule principali e
parietali; sono presenti rare ghiandole endocrine. Le ghiandole sono separate da abbondante tessuto
connettivo della lamina propria, che conferisce un aspetto atrofico alla mucosa. Non vi è
differenziazione di tipo intestinale. Il reperto di mucosa fundica non atrofica è suggestivo di ernia
iatale;
epitelio colonnare: è un epitelio specializzato, di tipo intestinale (metaplasia intestinale),
caratterizzato da una superficie villiforme, con epitelio costituito da cellule caliciformi (goblet cells) e
da cellule colonnari; in profondità sono presenti ghiandole simili alle cripte, rivestite da cellule
cuboidali, sieromucose, con cellule enterocromaffini. Rare le cellule endocrine, le cellule di Paneth e
di tipo assorbente con orletto a spazzola (NB: le ghiandole sono spesso contigue alla muscolaris
mucosae e poggiano su di esse con fibrocellule muscolari che sfioccano nella lamina propria. Questo è
3
un reperto suggestivo di una pregressa lesione ulcerativa con rigenerazione epiteliale sullo strato
muscolare).
L’epitelio colonnare di tipo intestinale presenta le stesse caratteristiche strutturali della metaplasia
intestinale dello stomaco, con due possibili aspetti di secrezione mucosa:
1. riconducibile alla mucosa ileale (metaplasia intestinale di tipo ileale, sia completa che incompleta,
con secrezione di mucine neutre e sialomucine);
2. riconducibile alla mucosa del grosso intestino (metaplasia intestinale di tipo colonico incompleta, con
secrezione prevalente di sialomucine e solfomucine).
Il sottogruppo dei pazienti con esofago di Barrett con metaplasia di tipo intestinale è quello a maggior
rischio di evoluzione in adenocarcinoma, con una frequenza di 1/88 pazienti per anno.
Questi tipi istologici possono essere presenti anche contemporaneamente, con i più vari mosaicisti; si
parlerà, in questo caso, di esofago di Barrett di tipo misto.
E’ importante che nei soggetti con esofago di Barrett, sia per l’inquadramento nosologico che a fini
prognostici, vengano effettuate biopsie multiple (sui 4 quadranti ogni 2 cm).
È importante segnalare che l’epitelio dell’esofago di Barrett può subire alterazioni displasiche ed avviare,
quindi, il processo di trasformazione maligna. La diagnosi di displasia su esofago di Barrett, si basa sulla
valutazione istologica delle alterazioni cellulari che permette una definizione in displasia di basso grado
(LGD), che corrisponde alla displasia di grado lieve, o di alto grado (HGD), che corrisponde alla
displasia di grado moderato-grave. Quest’ultima categoria include anche il carcinoma intraghiandolare
(cioè quello intraepiteliale e il carcinoma in situ).
4