Problemi
Termodinamica
1. Con una trasformazione isobara un gas ideale, inizialmente a 27°C è portato a 327°C. Se il
volume iniziale era di 2L quale sarà quello finale?
2. Un recipiente a tenuta termica contiene 80 g di acqua a 20 °C. Un proiettile di piombo di
massa 100 g e ad una temperatura di 90 °C viene velocemente immerso nell’acqua.
Nell’ipotesi che non vi siano perdite di calore verso l’ambiente, determinare il calore
specifico del piombo, sapendo che il sistema “acqua+proiettile” raggiunge una temperatura di
equilibrio finale di 22.6°C (il calore specifico dell’acqua è 4.186 Jg-1°C-1).
3. Una massa di gas occupa un volume di 400 cm3 alla temperatura di 27°C ed alla pressione di
1.0 atm. Essa viene riscaldata fino a che la sua temperatura è di 177°C ed il suo volume di
500 cm3. Qual è la pressione assunta dal gas in tali nuove condizioni? Se alla massa gassosa
in queste ultime condizioni si aggiungono altre 0.024 moli di gas, in modo che non cambi né
la temperatura né il volume, qual’ è la pressione assunta dal sistema?
4. Una macchina termica assorbe 100 cal ad ogni ciclo e ne cede 60. (a) qual è il suo
rendimento? (b) Se ogni ciclo si compie in 0.50 sec, qual è la potenza erogata dalla
macchina?
5. Un proiettile di massa 6.0 g viene sparato alla velocità di 300 m/sec in un tronco d’albero e vi
rimane infisso. Se la quantità di calore ottenuta dalla conversione dell’energia cinetica potesse
essere utilizzata per scaldare 10 g di acqua, di quanto si innalzerebbe la temperatura
dell’acqua?
6. Una massa m =1.0 kg di acqua, estratta allo stato solido da una cella frigorifera alla
temperatura t1 = -10°C, si va progressivamente portando in equilibrio termico con l’ambiente
esterno, alla temperatura t2 = 20°C. Sapendo che il calore specifico e il calore latente di
fusione del ghiaccio sono rispettivamente cg = 0.50 cal/g °C e L = 80 cal /g, calcolare la
quantità di calore assorbita dall’acqua in ciascuno dei processi che conducono dallo stato
iniziale a quello finale.
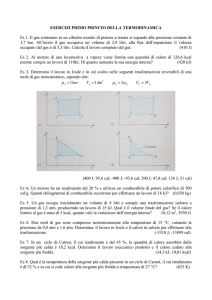
7. Nel diagramma in figura, 1 mol di gas perfetto è alla pressione atmosferica e alla temperatura
di 250K nel punto A. (a) si trovi il volume del gas in A. (b) Si raddoppia la pressione del gas
mantenendo costante il suo volume. Si trovi la temperatura del gas nel punto B. (c) Il gas è
lasciato espandere isotermicamente fino al punto C. Si trovi il volume del gas in C.
P
B
A
C
V
8. 0.12 mol di gas ideale in contatto con una sorgente termica alla temperatura costante T =
9.8°C hanno un volume iniziale di 1.3 litri e compiono 14 J di lavoro. Quali sono volume e
pressione finali?
9. Una certa massa di gas a pressione di 5 atm è contenuta in una bombola avente il volume di
30 dm3, quale sarebbe la pressione esercitata dal gas se questo venisse fatto espandere in un
recipiente sferico avente il raggio di 30 cm, supponendo di mantenere costante la
temperatura?
10. La sede stradale di un ponte ha una lunghezza di 1280 m. Durante l’arco dell’anno la
temperatura varia da -12°C a +38°C. Sapendo che la struttura del ponte è fatta di acciaio, qual
è la variazione di lunghezza della sede stradale in corrispondenza di quella variazione di
temperatura? α =12 x 10-6 °C-1.
11. Un grammo di acqua occupa il volume di 1 cm3 a pressione atmosferica. Quando quest’acqua
è fatta bollire diviene 1671 cm3 di vapore d’acqua. Calcolare la variazione di energia interna
per questa trasformazione. Le = 2.26 x 106 J/Kg
12. Un pezzo di metallo da 0.05 Kg viene riscaldato a 200°C e poi lasciato cadere in un secchio
contenente 0.400 Kg di acqua inizialmente a 20.0 °C. Se la temperatura finale di equilibrio
del sistema è 22.4 °C, trovare il calore specifico del metallo.
13. Una macchina a vapore ha un bollitore che opera a 500K. Il calore trasforma l’acqua in
vapore che fa funzionare un pistone.La temperatura di scarico è quella dell’aria esterna, circa
300 K. Calcolare il massimo rendimento di questa macchina.
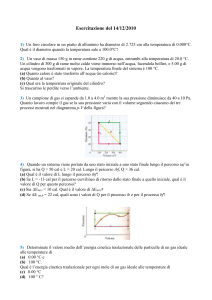
14. A 4 mol di gas perfetto viene fatto percorrere il ciclo ABCDA rappresentato in figura. Se
TD=100K, TAC= TA= TC=200K, TB=400K, PA=0.500x105 Pa e PD= 2.50x104 Pa, si
determinino i volumi VA e VB. Quali sono il lavoro compiuto, il calore ceduto o assorbito e la
variazione di energia interna lungo l’intero ciclo?cp = 4.97 cal/(mol·K); cV = 2.98
cal/(mol·K).
P
A
B
D
C
V
Risposte
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
4L
cp = 0.129 J g-1°C-1
a) p2 = 1.2 atm; b) p = 2.95 atm
a) η = 40% ; b) P = 334.8 watt
ΔT = 6.45 °C
Q1= 5 x 103 cal; Q2= 8 x 104 cal; Q3= 2 x 104 cal
a) VA = 20.5 L; b) TB = 500K; c) VC = 41.05 L
Vf = 1.36 L; Pf = 2.07 x 105Pa
p = 1.33 atm
ΔL = 0.768 m
ΔU = 2091 J
c = 452.5 J Kg-1°C-1 (acciaio)
η = 40%
VA=0.13 m3; VB=0.26 m3 W = 3.25 x 103 J; Q = 3.3 x 103 J; ΔU = 0 (trasf. ciclica)