Energia elettrica
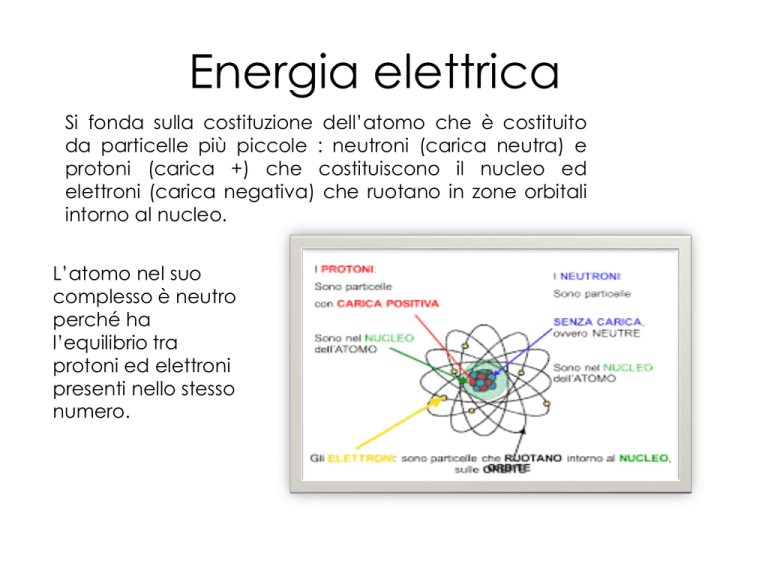
Si fonda sulla costituzione dell’atomo che è costituito
da particelle più piccole : neutroni (carica neutra) e
protoni (carica +) che costituiscono il nucleo ed
elettroni (carica negativa) che ruotano in zone orbitali
intorno al nucleo.
L’atomo nel suo
complesso è neutro
perché ha
l’equilibrio tra
protoni ed elettroni
presenti nello stesso
numero.
Le forze elettromagnetiche mantengono questo equilibrio tenendo
“insieme” le particelle.
Esistono alcuni materiali detti conduttori (i metalli appartengono a
questa categoria) nei quali, per determinate condizioni indotte
dall’esterno, un elettrone può abbandonare il suo atomo originario per
spostarsi ad un atomo vicino generando atomi con carica
positiva(quelli che perdono l’elettrone).
Questi ultimi si chiamano IONI POSITIVI- CATIONI.
Quelli invece che hanno carica negativa(perché guadagnano gli
elettroni si chiamano IONI NEGATIVI – ANIONI.
Il prossimo video è interessante perchè mostra quali infinitesime siano
le dimensioni dell’ atomo e quale rapporto di coesione è presente tra
gli elementi che lo costiuiscono.
https://www.youtube.com/watch?v=sxxbgcfPO3U
La causa di questo spostamento di elettroni si chiama
TENSIONE ELETTRICA O DIFFERENZA DI POTENZIALE
Unità di misura: VOLT
l’effetto conseguente è il flusso degli elettroni che ritornano agli
atomi originari e si chiama:
CORRENTE ELETTRICA O INTENSITA’
Unità di misura: AMPERE
Il conduttore oppone sempre una certa resistenza al flusso degli
elettroni in misura diversa a seconda del tipo di conduttore, della
lunghezza della sezione.
Questa grandezza è la RESISTENZA ELETTRICA
Unità di misura : OHM
Queste tre grandezze V,I,R sono in relazione secondo
la LEGGE DI OHM
LEGGE DI OHM
Enunciato:
Esiste una proporzionalità tra INTENSITA’ (I) E TENSIONE (V) .
Il fattore di proporzionalità è la R
Formule:
I = V/R
V=IxR
R = V/I
La resistenza R è direttamente proporzionale alla lunghezza del
filo conduttore e inversamente proporzionale alla sezione del
filo.
I = V/R
L’intensità è direttamente proporzionale alla tensione e
inversamente proporzionale alla resistenza.
Gli apparecchi elettrici trasformano l’energia elettrica in altre forme di
energia.
Generalmente producono sempre una trasformazione che produce
energia termica.
Questa trasformazione si chiama EFFETTO JOULE
cioè TRASFORMIAMO L’ENERGIA ELETTRICA IN LAVORO.
Se ne ottiene una POTENZA
Oppure
P=(VxV)/R P= (IxI) xR
P=V xI
L’unità di misura della POTENZA sono i WATT (w)
o meglio il suo multiplo è il Kilovatt (Kw)
La POTENZA esprime la capacità di compiere un lavoro.
Se rapportiamo il lavoro alla quantità di tempo impiegato a compierlo,
l’unità di misura che noi adoperiamo per quantificare questa
trasformazione dell’energia elettrica il lavoro è:
KWh (Potenza per l’unità di tempo).
Gli effetti della corrente elettrica sono:
EFFETTO JOULE
Effetto termico prodotto dal passaggio degli elettroni nel conduttore che
oppone resistenza .
Il prossimo video è interessante perché mostra alcune applicazioni
dell’effetto termico e l’utilizzo dei circuiti.
https://www.youtube.com/watch?v=D0SpXbCEXnw
EFFETTO CHIMICO
Si manifesta facendo passare gli elettroni in una soluzione liquida
chiamata elettrolisi ed è un processo che consiste nell’estrarre una
sostanza da una soluzione di un sale che la contiene,, attirandone gli ioni
su un elettrodo immerso nella soluzione. Questo processo avviene nella
cosiddetta cella elettrolitica.
Il prossimo video mostra un simpatico esperimento fatto in casa che
mostra come si fa una cella elettrolitica e come avviene il flusso di
corrente elettrochimico.
https://www.youtube.com/watch?v=6OXIw5KNucA
Nella soluzione elettrolitica
immergendo un catodo (polo negativo) e un
anodo (polo positivo) vedremo le particelle positive (cationi +) che
vanno verso il catodo e quelle negative (anioni -) che vanno verso
l’anodo (+)
Altre applicazioni dell’Effetto chimico:
Galvanostegia:
Collegando un elemento metallico all’estremità del catodo e
all’anodo un metallo che serve per ricoprire l’elemento, ed
immergendoli in una soluzione elettrolitica costituita da una soluzione
di sale del metallo con cui si vuole ricoprire, possiamo rivestire di uno
strato sottile l’intero elemento con un metallo a nostra scelta
(esempio placcare in oro, argento, cromare, stagnare, zincare,
nichelare).
Ramatura:https://www.youtube.com/watch?v=ZGnOutkEBNw
Galvanoplastica:
Analogo procedimento ma viene utilizzato su uno stampo in grafite.
Estrazione di metallo puro:
Usando una soluzione elettrolitica dal sale del metallo da trattare ed
inserendo nella soluzione un catodo e un anodo, il metallo puro si
deposita intorno al catodo(-) separandolo dal resto del materiale.
Si usa per l’alluminio, il nichel, il cobalto, il piombo, lo stagno, il rame
l’oro e l’argento.
Pila a secco(La clanchè)
.
La soluzione liquida viene
sostiuita da una pasta di
biossido di manganese +
cloruro di ammonio.
All’interno di questa
pasta è immerso un
cilindro di carbonio (che
è un elettrodo) ed il tutto
è inserito in un
contenitore esterno,
cilindrico, di zinco (che
costituisce l’altro
elettrodo). Principio delle
Pile ZINCO/CARBONE.
Pila alcalina: E’ analoga a Le clanchè ma utilizza come pasta
elettrolitica un composto di metalli alcalini di solito idrossido di potassio.
Pile all’ossido di argento: Pile di piccole dimensioni.