ELETTROSTATICA
STRUTTURA DELL’ATOMO
Democrito, IV sec. a.C., deduce l'esistenza di atomi (atomòs = indivisibile) da un processo logico e
puramente teorico attraverso il quale comprende che scomponendo la materia in parti sempre più
piccole non si può che arrivare a dei costituenti fondamentali e indivisibili.
Lo studioso inglese J.Dalton (1766-1844) all'inizio del XIX secolo dichiarò che la materia non é
continua, ma é composta da particelle che non possono essere ulteriormente divisibili né
trasformabili, gli atomi.
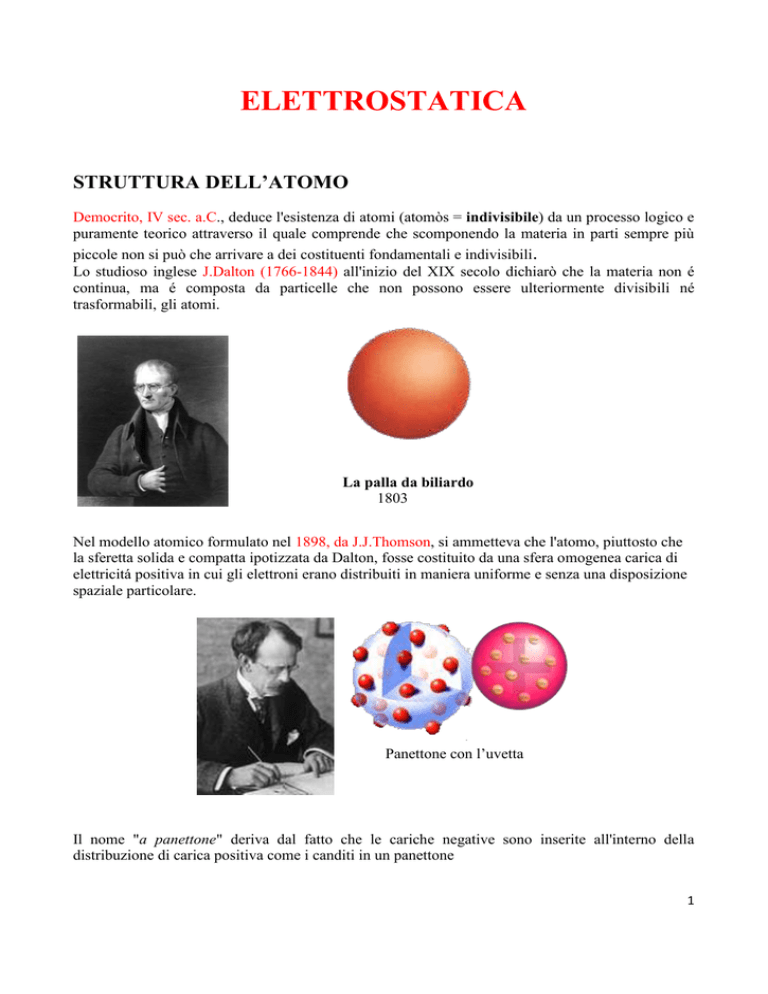
La palla da biliardo
1803
Nel modello atomico formulato nel 1898, da J.J.Thomson, si ammetteva che l'atomo, piuttosto che
la sferetta solida e compatta ipotizzata da Dalton, fosse costituito da una sfera omogenea carica di
elettricitá positiva in cui gli elettroni erano distribuiti in maniera uniforme e senza una disposizione
spaziale particolare.
Panettone con l’uvetta
Il nome "a panettone" deriva dal fatto che le cariche negative sono inserite all'interno della
distribuzione di carica positiva come i canditi in un panettone
1
Rutherford nel 1911 fece un esperimento in cui bombardò un foglio d'oro molto sottile con particelle alfa e
dedusse che l'atomo è in gran parte vuoto. Allora propose il modello planetario, in cui gli elettroni ruotano
attorno al nucleo a gran distanza da esso. L'atomo è così in gran parte vuoto.
Il nuovo modello proposto da Rutherford aveva delle caratteristiche che sono rimaste anche in
modelli successivi come la concentrazione della maggioranza della materia in un volume
relativamente piccolo rispetto alle dimensioni atomiche (ossia un nucleo atomico) e la presenza di
elettroni rotanti intorno ad esso, come i pianeti del sistema solare attorno al sole.
2












