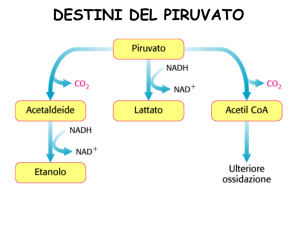
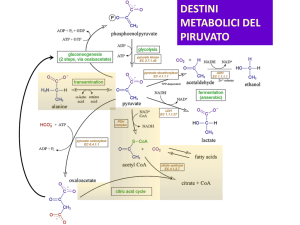
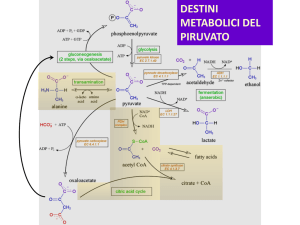
DESTINO DEL PIRUVATO
Il piruvato prende destini diversi a seconda di:
• tipo di organismo
• compartimento cellulare
• condizioni aerobiche o anaerobiche
Fermentazione etanolica
In condizioni anaerobiche, alcuni
organismi fermentanti come il lievito,
convertono il piruvato in etanolo e CO2.
Due tappe consecutive, che richiedono
l’intervento di 2 Enzimi:
1. Piruvato decarbossilasi:
decarbossilazione irreversibile del
piruvato ad acetaldeide e CO2
Tiamina pirofosfato (TPP) e ioni Mg2+
necessari per attività enzima
2. Alcol deidrogenasi: riduzione
acetaldeide ad etanolo tramite coenzima
NADH convertito a NAD+
Quindi la fermentazione alcolica
rigenera il NAD+, impedendo l’arresto
della glicolisi.
Fermentazione lattica
In anaerobiosi ad es. muscolo in intensa attività fisica, in
cui la richiesta di ATP è elevata ma il rifornimento di O2 è
scarso, quindi il destino aerobico del piruvato è, l’unico
modo per ottenere rapidamente ATP è attraverso la
glicolisi.
Glicolisi consuma NAD+, è necessario rigenerarlo a partire
dal NADH attraverso la fermentazione lattica.
Il piruvato viene ridotto a
lattato da Lattico
deidrogenasi (LDH) in
presenza del coenzima NADH
che viene ossidato a NAD+,
indispensabile per
continuare la glicolisi.
La conversione di piruvato in
lattato avviene anche in
aerobiosi.
Es . Eritrociti, in assenza di
mitocondri, la glicolisi è
l’unica fonte energetica.
Ciclo di Cori
Il lattato prodotto,
esce dalla cellula ed
entra nel flusso
sanguigno. Arriva
alle cellule epatiche
dove è riconvertito
a piruvato per
riformare glucosio
attraverso la
gluconeogenesi
(Ciclo di Cori).
Destino aerobico del piruvato
In condizioni aerobiche il piruvato viene
completamente ossidato ad CO2 ed acqua con
produzione di una grande quantità di composti ad
alto contenuto energetico.
L’inizio del destino aerobico del piruvato comporta la sua
trasformazione in Acetil-S-CoA, un intermedio chiave di
altri processi metabolici ad opera del complesso
enzimatico della piruvato deidrogenasi.
Complesso della piruvato
deidrogenasi
Il complesso multienzimatico della piruvato deidrogenasi,
localizzato nella matrice mitocondriale, catalizza in modo
irreversibile la decarbossilazione ossidativa del piruvato.
E’ costituito da tre attività enzimatiche e da cinque gruppi
prostetici/coenzimi, come mostrato nella figura
Complesso della piruvato deidrogenasi
Vedi slide successiva
1. E1 Piruvato deidrogenasi – TPP
Catalizza decarbossilazione del Piruvato, generando idrossietil- TPP
(reaz. 1); poi ossidazione di idrossietil a gruppo acetilico e
trasferimento di 2 e- per ridurre il disolfuro del lipoato legato ad E2
e ad esso trasferire il gruppo acetile da TPP, formando un un
acetiltioestere con SH (reaz. 2).
2. E2 Diidrolipoil transacetilasi – Lipoato
Catalizza la trans-esterificazione del gruppo acetilico dalla lipoillisina al CoA-SH, si forma l’Acetil-S-CoA, una forma attivata del
gruppo acilico (reaz. 3).
3. E3 Diidrolipoildeidrogenasi – FAD e NAD+ solubile
Catalizza la rigenerazione della forma ossidata della lipoil-lisina a
spese del FAD ridotto FADH2 quindi NAD+ riossida il FADH2 a FAD
(reaz. 4) trasformandosi in NADH+ H+ (reaz. 5).
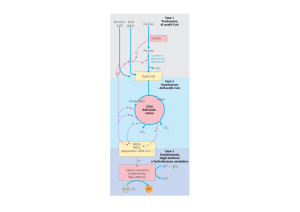
Condizione aerobiche: Respirazione
cellulare
•
Fase I: Produzione di AcetilCoA
Acetil-CoA è un intermedio chiave di altri processi catabolici,
deriva da glicolisi, ma anche da degradazione degli acidi grassi e
degli amminoacidi.
•
Fase II: Ossidazione di AcetilCoA
Acetil-CoA entra nel ciclo di Krebs dove è ossidato a CO2,
l’energia liberata è conservata come NADH+ H+ e FADH2.
•
Fase III: Trasferimento e- fosforilazione ossidativa
I coenzimi ridotti vengono riossidati e liberano e – che vengono
trasportati attraverso la catena respiratoria all’O2, ciò comporta
liberazione d’energia che viene conservata come ATP tramite la
fosforilazione ossidativa
Acido Citrico /Krebs
Nel mitocondrio il piruvato dopo la
trasformazione in AcetilCoA entra nel
ciclo dell’acido citrico (Krebs) dove viene
ulteriormente ossidato.
AcetilCoA +3NAD+ + FAD + GDP + Pi + 2H2O → 2CO2 + 3NADH + H+ + FADH2 + GTP+ CoA
Reazione 1
ossalacetato + acetil-CoA + H2O → citrato + CoA
CITRATO SINTASI
La prima reazione del ciclo è la condensazione dell’acetil-CoA con
l’ossalacetato per formare citrato
Durante la reazione si forma un intermedio transitorio (citril-CoA), un
tioestere con elevata energia di idrolisi.
L’idrolisi di questo intermedio fornisce energia per la reazione di
condensazione.
Reazione 2
citrato ⇆ isocitrato
ACONITASI
La seconda reazione del ciclo è l’isomerizzazione del citrato a
isocitrato
La reazione procede con la rimozione di una molecola di H2O dal
citrato, formazione di un intermedio (cis-aconitato) e aggiunta di
una molecola di H2O.
La reazione è catalizzata dall’aconitasi che possiede un centro
ferro-zolfo importante per il legame del substrato e per la catalisi
Reazione 3
N.B. Osserva sul testo le reazioni dallan.3 alla n. 8
isocitrato + NAD+ → α-chetoglutarato + CO2 + NADH + H+
ISOCITRATO DEIDROGENASI
coenzima NAD
•
•
La terza reazione del ciclo è la decarbossilazione
ossidativa dell’isocitrato per formare alfa-chetoglutarato e
CO2
Il NADH prodotto cede gli elettroni alla catena trasporto di
elettroni (complesso I).
Reazione 4
α-chetoglutarato + NAD+ + CoA → succinil-CoA + CO2 + NADH + H+
COMPLESSO MULTIENZIMATICO DELL’ALFA-CHETOGLUTARATO
DEIDROGENASI
molto simile per struttura e funzione al complesso della piruvato deidrogenasi
sono presenti tre enzimi (E1, E2, E3) e cinque coenzimi (TPP, acido lipoico, FAD,
NAD+, coenzima A).
La quarta reazione del ciclo è la decarbossilazione ossidativa dell’αchetoglutarato per formare succinil-CoA e CO2
Il succinil CoA è un tioestere ad alta energia di idrolisi.
L’energia liberata dall’ossidazione dell’ α -chetoglutarato è conservata
mediante la formazione del legame tioestere del succinil-CoA.
Il NADH prodotto cede gli elettroni alla catena trasporto di elettroni
(complesso I).
Reazione 5
succinil-CoA + GDP + Pi ⇆ succinato + GTP + CoA
SUCCINIL-COA SINTETASI
La quinta reazione del ciclo è la formazione del succinato
In questa reazione viene idrolizzato il legame tioestere del succinilCoA.
L’idrolisi del legame tioestere fornisce energia per la sintesi di GTP.
Il gruppo fosfato del GTP viene trasferito all’ADP per formare ATP.
GTP + ADP → GDP + ATP
Questa fosforilazione è una fosforilazione a livello del
substrato come quelle che si verificano nella glicolisi.
Reazione 6
succinato + FAD ⇆ fumarato + FADH2
SUCCINATO DEIDROGENASI
coenzima FAD.
La sesta reazione del ciclo è l’ossidazione del succinato a
fumarato.
La succinato deidrogenasi è legata alla membrana
mitocondriale interna; gli altri enzimi del ciclo si trovano
nella matrice mitocondriale.
Il FADH2 cede gli elettroni alla catena di trasporto degli
elettroni (complesso II).
Reazione 7
fumarato + H2O ⇆ malato
FUMARATO IDRATASI (FUMARASI)
La settima reazione del ciclo è l’idratazione del fumarato a malato.
Reazione 8
malato + NAD+ ⇆ ossalacetato + NADH + H+
MALATO DEIDROGENASI
coenzima NAD
L’ottava reazione del ciclo è l’ossidazione del malato a ossalacetato
Il NADH prodotto cede gli elettroni alla catena trasporto di elettroni
(complesso I).
Il ciclo dell’acido citrico è terminato.
L’ossalacetato, prodotto dell’ultima reazione, si condensa con un’altra
molecola di acetil CoA e il ciclo continua.
Ogni giro del ciclo dell’acido citrico produce:
2 CO2
1 GTP → ATP
3 NADH
1 FADH2
Nella figura sono evidenziate le reazioni in cui si ha formazione coenzimi ridotti.
Essi sono riossidati nella catena respiratoria, producendo ATP tramite
fosforilazione ossidativa.
Via anfibolica
Coinvolgimento sia in
processi catabolici che in
processi anabolici:
- da una parte, nel ciclo si
ha ossidazione di
acetilCoA proveniente da
carboidrati, ac. grassi ed
aa (catabolismo)
- dall’altra, gli intermedi
del ciclo costituiscono i
precursori per molte vie
biosintetiche
(anabolismo)
Reazioni anaplerotiche
esempi