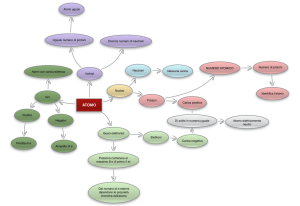
ELEMENTI E COMPOSTI
ELEMENTO
sostanza semplice non ulteriormente decomponibile
COMPOSTO
specie chimica a composizione definita e costante formata
dall’unione di due o più ELEMENTI
ATOMI E MOLECOLE
ATOMO
Particella infinitesima unitaria di dimensioni 2 - 5 Å
(2 - 5 10-10 m) costituita prevalentemente da:
PROTONI (Z) massa 1
NEUTRONI (N) massa 1
ELETTRONI (Z) massa 1/1837
carica +1
carica 0
carica -1
MOLECOLA
Aggregato di atomi capace di esistenza fisica autonoma
IONE
Atomo o molecola dotato di carica elettrica positiva
(catione) o negativa (anione)
ISOTOPO
Nuclide caratterizzato da un determinato valore di
NUMERO ATOMICO (Z) e di MASSA ATOMICA (A)
(con A = Z + N)
IDROGENO (H)
DEUTERIO (D)
TRIZIO (T)
Z=1
Z=1
Z=1
A=1
A=2
A=3
1
2
3
1H
1H
1H
PESO ATOMICO
Rapporto tra la massa media di un atomo e la dodicesima
parte della massa del nuclide 12 del carbonio
PESO MOLECOLARE
Rapporto tra la massa di una molecola e la dodicesima parte
della massa del nuclide 12 del carbonio
P.M. = somma dei P.A. degli atomi della molecola
PESO FORMULA
Somma dei P.A. degli atomi costituenti
l’ UNITA’ FORMULA (solidi ionici)
GRAMMO ATOMO
Quantità in grammi di un elemento pari al suo P.A.
GRAMMO MOLE (o mole)
Quantità in grammi di un elemento e/o composto pari
al suo P.M.
1 g atomo e/o 1 g mole di qualsiasi sostanza contiene sempre
6,023 . 1023 atomi e/o molecole di quella sostanza
6,023 . 1023 = NA = NUMERO DI AVOGADRO
Una MOLE di elettroni o di fotoni corrisponde ad un
NA di elettroni o di fotoni
g / PM = numero di moli di un elemento o di un composto
g / PA = numero di grammiatomi di un elemento
REAZIONI CHIMICHE
LEGGE DI CONSERVAZIONE DELLA MASSA
A. Lavoisier (1775)
“La somma delle masse delle sostanze reagenti è
uguale alla somma delle masse dei prodotti di reazione”
Una REAZIONE CHIMICA è un’equazione in grado di
soddisfare il principio di conservazione della massa e della
carica
CLASSIFICAZIONE DELLE REAZIONI CHIMICHE
Reazioni che non avvengono con trasferimento
di elettroni tra le sostanze coinvolte:
1) ASSOCIAZIONE (sintesi)
2) DISSOCIAZIONE (decomposizione)
3) SCAMBIO
1) CaO + CO2 CaCO3
2) CaCO3 CaO + CO2
3) AgNO3+ NaCl AgCl + NaNO3
Reazioni che avvengono con trasferimento di elettroni
tra le sostanza coinvolte (REAZIONI REDOX):
S + O2 SO2
H2 + ½ O2 H2O
N2 + 3H2 2NH3