LE BIOMOLECOLE
LE BIOMOLECOLE
DETTE ANCHE MOLECOLE ORGANICHE;
CARBOIDRATI
LE BIOMOLECOLE
LIPIDI
PROTEINE
sono
ACIDI NUCLEICI
molecole complesse
=
POLIMERI
formate dall'unione di
molecole semplici =
MONOMERI
1
I CARBOIDRATI
Sono chiamati anche GLUCIDI; sono fra i composti organici più abondanti sulla Terra e rappresentano la
prima sorgente di energia per l'uomo;
I Carboidrati sono formati da carbonio C, idrogeno H e ossigeno O;
Esse si suddividono in tre importanti gruppi:
MONOSACCARIDI [ 1 sola molecola] es.
CARBOIDRATI
DISACCARIDI
glucosio, fruttosio galattosio;
[ 2 molecole di monosaccaride unite] es.
saccarosio, lattosio;
POLISACCARIDI [ più molecole di monosaccaride unite] es. amido, cellulosa;
MONOSACCARIDI
2
3
DISACCARIDI
I DISACCARIDI sono formati dall'unione di due molecole di monosaccaridi che si uniscono eliminando
una molecola d'acqua (condensazione) reversibilmente.
4
POLISACCARIDI
Sono polimeri ad alta massa molecolare dei monosaccaridi naturali (da 100 ad oltre 3000 unità). fanno
parte dei polisaccaridi: l'amido, la cellulosa, il glicogeno.
5
6
I CARBOIDRATI NEI CIBI
I CARBOIDRATI sono presenti in molti cibi ma principalmente sono contenuti nella pasta e nel pane:
7
I LIPIDI
I LIPIDI insieme ai carboidrati rappresentano le principali molecole energetiche;
Sono costituiti principalmente da atomi di C, H, O, a volte sono presenti atomi di N, P;
CARATTERISTICHE:
Insolubili in H2O POLARE, sono solubili nei solventi organici come
ad esempio CCl4 tetracloruro di carbonio, (C2H5)2O etere C3H6O
acetone, ecc.. che sono APOLARI;
Sostanza di riserva ENERGETICA;
Funzione strutturale (presenti nelle membrane cellulari);
Essi vengono distinti in:
8
ACIDO GRASSO lunga catena di atomi di C (da 4 a 22 atomi) legati tra loro con all'estremità un gruppo
CARBOSSILICO
̶ COOH;
A secondo se gli atomi di Carbonio formano legami semplici o doppi si distinguono:
ACIDI GRASSI
SATURI
INSATURI
consideriamo i seguenti ACIDI GRASSI:
9
10
11
I LIPIDI NEI CIBI
I LIPIDI sono presenti in molti cibi ma principalmente sono contenuti:
12
LE PROTEINE
Sono composti organici quaternari formati da C, H, O, e N;
Si formano per polimerizzazione di AMINOACIDI. negli organismi viventi esistoni molti aminoacidi, ma
solo 20 si trovano in tutte le cellule e vengono utilizzati nella sintesi delle proteine.
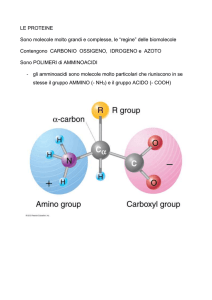
GRUPPO R
GRUPPO
AMMINICO
GRUPPO
CARBOSSILICO
Il gruppo ̶ NH2 prende il nome di gruppo amminico mentre il gruppo ̶ COOH è il gruppo carbossilico.
Tutti gli amminoacidi contengono questi due gruppi ma differiscono per il gruppo R che può essere
costituito da un solo atomo di carbonio o da una catena di atomi di carbonio.
13
Gli 8 aminoacidi essenziali sono tali perché l'organismo animale non riesce a sintetizzarli e devono essere
assunti attraverso la dieta.
IL LEGAME PEPTIDICO
Nelle proteine gli amminoacidi sono legati tra loro da un legame particolare chiamato LEGAME
PEPTIDICO che si forma quando il gruppo carbossilico di un amminoacido si lega con il gruppo
amminico di un altro amminoacido con eliminazione di una molecola di H2O. Un dipeptide è formato da
due amminoacidi legati tra loro; un tripeptide da tre amminoacidi legati tra loro; un polipeptide è una
molecola formata da più amminoacidi, anche parecchie centinaia.
14
PROTEINE NEL NOSTRO ORGANISMO
Tra le più importanti proteine fibrose abbiamo:
• il collagene che entra nella costituzione del tessuto connettivo, del tessuto osseo e cartilagineo;
• la cheratina che entra nella composizione dello strato più esterno della pelle, dei peli e delle
unghie;
• il fibrinogeno, che è una proteina plasmatica, responsabile della coagulazione del sangue;
• la miosina e l’actina, che sono responsabili della contrazione muscolare;
• l’albumina e le globuline, che sono contenute nelle cellule, nel siero del sangue;
• l’emoglobina, che trasporta l’ossigeno a tutti i tessuti;
• gli enzimi, che intervengono nei processi metabolici;
• gli ormoni, prodotti dalle ghiandole endocrine, che stimolano particolari organi bersaglio, che, a
loro volta, avviano e controllano fenomeni importanti;
• gli anticorpi o immunoglobuline, che vengono prodotti nel siero del sangue in seguito al
riconoscimento degli antigeni da parte delle cellule del sistema immuni
LA STRUTTURA DELLE PROTEINE
Esistono diverse possibili modalità con cui una lunga collana può essere disposta nello spazio:
linearmente,
avvolta su se stessa a gomitolo. a zig-zag, ecc. Così le lunghe catene proteiche possono assumere diverse
disposizioni spaziali, che dipendono dalla sequenza di amminoacidi di cui sono costituite; ogni proteina si
organizza nello spazio assumendo una specifica struttura, la quale garantirà una certa funzione.
LA STRUTTURA PRIMARIA
corrisponde alla semplice sequenza
lineare degli amminoacidi che è
determina dalle informazioni ereditarie
contenute nella molecola del DNA.
L’insulina, ad esempio, è una proteina
disposta nello spazio in modo
semplicemente lineare.
LA STRUTTURA SECONDARIA
La struttura secondaria è la forma che
la catena polipeptidica assume nello
spazio ripiegandosi su se stessa e che
può essere ad alfa elica, in cui la catena
di amminoacidi si avvolge come un
nastro attorno ad un asse, oppure a
lamine beta ( o più semplicemente a
foglietto ripiegato) come nelle proteine
fibrose che costituiscono i capelli, la
lana e la seta. Responsabili del
mantenimento di tale struttura sono i
legami a idrogeno che si vengono a
formare tra amminoacidi in posizioni
diverse della catena.
\
struttura secondaria
La cheratina o la miosina dei muscoli sono proteine con
struttura ad elica; il collagene, i cui sono costituiti i tendini,
risulta dall’attorcigliamento ad elica di tre catene proteiche. La
fibrina ha invece una disposizione a foglietto ripiegato.
15
LA STRUTTURA TERZIARIA
La struttura terziaria consiste in un ulteriore
avvolgimento della molecola, che si verifica
quando si stabiliscono legami a idrogeno o di
altro tipo tra i gruppi R degli amminoacidi, e
determina una struttura tridimensionale
complessa che spesso conferisce alla proteina
una forma globulare. Questa struttura è tipica
infatti delle proteine globulari, tra cui molto
importanti sono gli enzimi e gli anticorpi.
LA STRUTTURA TERZIARIA
Quando più molecole proteiche con una
struttura terziaria si uniscono tra di loro si
ottiene un ulteriore complessità strutturale,
detta struttura quaternaria, come nel caso
dell’emoglobina, che risulta sempre formata
da quattro catene uguali a due a due.
LE PROTEINE NEI CIBI
Le PROTEINE sono presenti in molti cibi ma principalmente sono contenuti:
16
GLI ACIDI NUCLEICI
IL NUCLEOTIDE:
17
DNA
STRUTTURA DEL DNA
18
RNA
STRUTTURA DEL RNA
19
DUPLICAZIONE DEL DNA
COSA SUCCEDE:
20
COSA SI OTTIENE:
21
FASI DELLA DUPLICAZIONE:
22
23