6
Le proteine sono composti organici quaternari; esse sono costituite infatti da C,H,N e O. Pertanto
rappresentano l'unica fonte di azoto del nostro organismo.
Le proteine si formano per polimerizzazione degli AMMINOACIDI. Negli organismi viventi esistono molti
tipi di amminoacidi, ma solo 20 si trovano in tutte le cellule e vengono utilizzati nella sintesi delle proteine.
Con questo numero relativamente piccolo di unità base si possono costruire le migliaia e migliaia di proteine
esistenti in natura, e questo sia perché gli amminoacidi possono concatenarsi in ordine diverso, sia perché
in una catena polipeptidica un amminoacido può comparire più volte ( in pratica è come se ci fossero 20
lettere dell’alfabeto con le quali possiamo costruire infinite parole: ecco perché esiste un numero
elevatissimo di proteine diverse! Ad esempio possiamo sostituire una lettera con un’altra per ottenere una
parola diversa; per esempio passare da foglia a voglia; analogamente in una catena polipeptidica basta
sostituire un amminoacido con un altro per ottenere una proteina del tutto diversa).
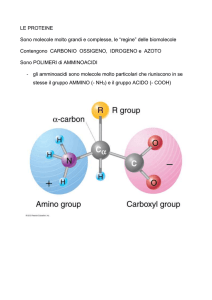
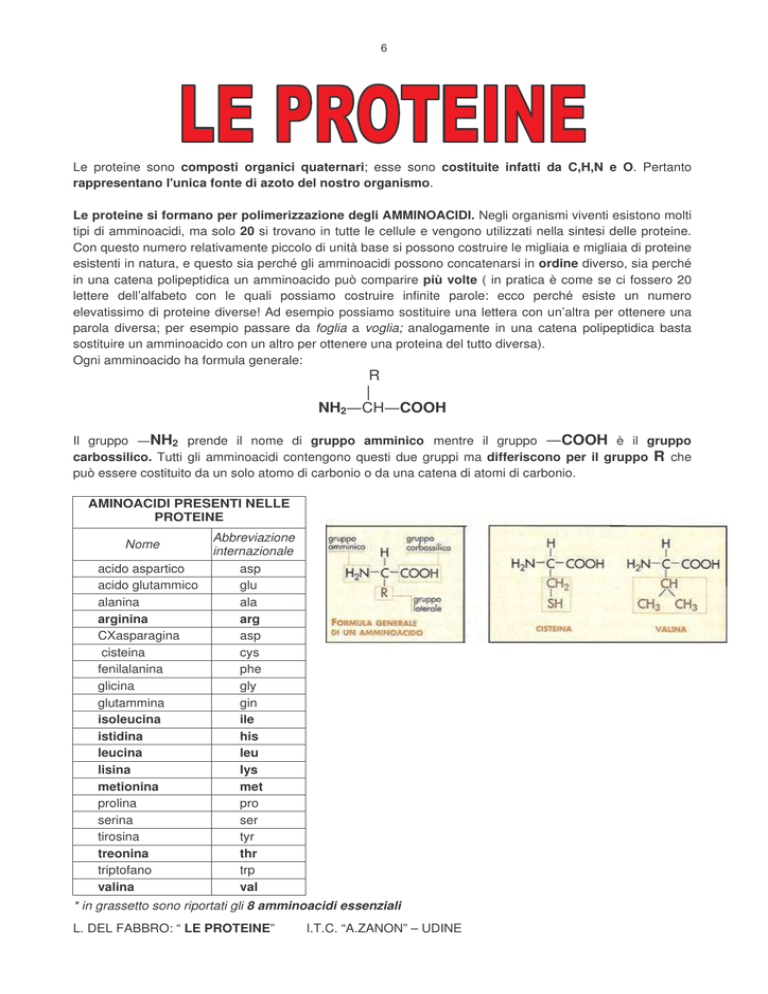
Ogni amminoacido ha formula generale:
R
NH2
CH
COOH
Il gruppo
NH2 prende il nome di gruppo amminico mentre il gruppo
COOH è il gruppo
carbossilico. Tutti gli amminoacidi contengono questi due gruppi ma differiscono per il gruppo R che
può essere costituito da un solo atomo di carbonio o da una catena di atomi di carbonio.
AMINOACIDI PRESENTI NELLE
PROTEINE
Nome
acido aspartico
acido glutammico
alanina
arginina
CXasparagina
cisteina
fenilalanina
glicina
glutammina
isoleucina
istidina
leucina
lisina
metionina
prolina
serina
tirosina
treonina
triptofano
valina
Abbreviazione
internazionale
asp
glu
ala
arg
asp
cys
phe
gly
gin
ile
his
leu
Iys
met
pro
ser
tyr
thr
trp
val
* in grassetto sono riportati gli 8 amminoacidi essenziali
L. DEL FABBRO: “ LE PROTEINE”
I.T.C. “A.ZANON” – UDINE
6
Gli 8 amminoacidi
essenziali
Dicevamo che in natura esistono 20 amminoacidi diversi ma otto di questi si dicono essenziali in quanto
l’organismo animale non riesce a sintetizzarli , ma li deve assumere attraverso la dieta. Gli aminoacidi
essenziali sono riportati nella figura in alto.
Nelle proteine gli amminoacidi sono legati tra loro da un legame particolare chiamato LEGAME PEPTIDICO
che si forma quando il gruppo carbossilico di un amminoacido si lega con il gruppo amminico di un
altro amminoacido con eliminazione di una molecola di H2O. Un dipeptide è formato da due
amminoacidi legati tra loro; un tripeptide da tre amminoacidi legati tra loro; un polipeptide è una molecola
formata da più amminoacidi, anche parecchie centinaia.
La formazione del legame peptidico nelle proteine
FUNZIONI DELLE PROTEINE
Le principali funzioni delle proteine sono:
PLASTICA o STRUTTURALE: servono cioè agli organismi come materiali da costruzione delle proprie
strutture e sono immagazzinate in siti specifici come ad esempio il seme e l’albume dell’uovo. Muscoli
del nostro corpo sono formati in gran parte da proteine e acqua. All’azoto si deve la funzione plastica
delle proteine, cioè la loro capacità di costruire e di rigenerare cellule e tessuti, nonché di favorire la
crescita.
L. DEL FABBRO: “ LE PROTEINE”
I.T.C. “A.ZANON” – UDINE
6
Intervengono inoltre:
a) nella costruzione di nuovi tessuti corporei nella adolescenza e nella infanzia
a)nella riparazione tissutale e in quelle situazioni che portano a logorio dei tessuti, ad esempio
febbre, ferite, ustioni…
c) nel mantenimento della struttura corporea: la scissione e la sintesi delle proteine
nell'
organismo umano avvengono sempre rispettando un equilibrio dinamico tra questi due
processi. La perdita di proteine nel corpo umano è costante e ha luogo sia a livello di epidermide
(le cui cellule si sfaldano e si rinnovano continuamente), sia a livello del sistema digerente e della
vescica, oltre a graduale logoramento di quelle di altri tessuti;
di MOVIMENTO e CONTRATTILITA’: l’attività dei muscoli, per esempio. è dovuta alla presenza di due
proteine,actina e miosina, che ne costituiscono le componenti principali
REGOLATRICE: specifica di alcune proteine che svolgono il ruolo di enzimi e ormoni, sostanze cioè
in grado di controllare importanti attività fisiologiche negli organismi superiori. Ne è un esempio l’insulina,
una proteina ormonale capace di regolare la concentrazione di glucosio nel sangue.
TRASPORTO: trasportano elementi essenziali, ad esempio l'emoglobina, proteina che lega il ferro e
trasporta ossigeno ai tessuti; altre provvedono al trasporto di peptidi fosforilati, calcio, fosforo, zinco.
di DIFESA: proteine come gli anticorpi difendono gli organismi animali da agenti estranei; in campo
vegetale vengono utilizzate proteine velenose: la ricina ad esempio, presente nei semi di ricino,
impedisce che gli insetti se ne cibino; altre proteine velenose sono la tossina prodotta dal batterio che
provoca il tetano e il veleno di alcuni ragni e serpenti:
ENERGETICA questa funzione viene svolta quando l'apporto energetico totale non è coperto
adeguatamente dai glucidi e lipidi e l'
organismo deve trarre la quota necessaria alla copertura del
fabbisogno energetico dalle proteine. Ne consegue che le proteine assunte a fini plastici non vengono
utilizzate, o solo in parte, con conseguenze sfavorevoli per l’organismo.
1 g proteine fornisce 4 kcal
FABBISOGNO
Il fabbisogno varia in rapporto all’età: in particolare l’infanzia e l’età dello sviluppo richiedono un elevato
apporto di proteine, in quanto queste sostanze svolgono un ruolo importantissimo nella costruzione di nuovi
tessuti e quindi nella crescita del corpo umano. In particolare:
il fabbisogno di un lattante è di circa 3 g per kg di peso corporeo
il fabbisogno di un bambino è di circa 1,5-2 g per kg di peso corporeo
il fabbisogno di un adulto è di circa 1 g per kg di peso corporeo
Razione ottimale = 10 - 15% dell’apporto calorico quotidiano totale (di cui il 65% deve essere di
origine vegetale)
Il processo di utilizzazione delle proteine, come vedremo in seguito, è presieduto dall’apparato digerente,
che scompone ( mediante enzimi contenuti nel succo digestivo dello stomaco e dell’intestino tenue) ) le
proteine contenute negli alimenti nei singoli aminoacidi che le compongono; questi poi si ricombinano in
modo differente sintetizzando le proteine necessarie per l’organismo.
Dal punto di vista alimentare esistono proteine ad alto valore biologico che sono le proteine di origine
animale e proteine a basso valore biologico che sono quelle di origine vegetale ( il valore biologico è
quantitativamente proporzionale al grado di utilità di una determinata proteina per l’organismo). entrambi i
tipi di proteine sono però importanti ed hanno la proprietà di essere complementari tra di loro se combinate
in modo opportuno. Per esempio, il valore biologico dei cereali aumenta notevolmente se vengono abbinati
ai legumi; questa proprietà, detta complementazione, spiega perché molti popoli sopravvivono
alimentandosi con una dieta povera di carne, pesce e latte.
Le proteine e gli aminoacidi eccedenti il fabbisogno dell’organismo vengono utilizzati come fonte di energia.
Una dieta alimentare che risulta invece povera di proteine può provocare gravi danni nei bambini
ostacolandone lo sviluppo psicofisico, mentre nell’adulto può tradursi in una minor resistenza alle malattie.
L. DEL FABBRO: “ LE PROTEINE”
I.T.C. “A.ZANON” – UDINE
6
LE LIPOPROTEINE E LE GLICOPROTEINE
Alcune molecole presenti negli esseri viventi sono degli ibridi, ossia sono combinazioni di vari tipi di molecole
biologiche finora visti. Le lipoproteine sono una combinazione di lipidi e proteine. rappresentano al
principale forma di trasporto di lipidi nel sangue e sono costituite da una capsula di proteina che avvolge un
bulbo di lipidi. due tipi di lipoproteine hanno una certa notorietà: le lipoproteine ad alta densità (HDL) e le
lipoproteine a bassa densità (LDL). Le LDL hanno la fama di essere lipoproteine “cattive” perché
trasportano il colesterolo ai tessuti periferici, comprese le arterie coronarie; qui il colesterolo può
depositarsi dando origine a “placche” che possono col tempo ostruire queste arterie impedendo l’afflusso di
sangue al cuore e provocando l’infarto. Invece , le HDL sono considerate proteine “buone” perché
trasportano il colesterolo dai tessuti periferici al fegato; pertanto un rapporto elevato di queste lipoproteine
rispetto al colesterolo viene considerato un fattore di protezione nei confronti delle malattie cardiache.
Le glicoproteine sono combinazioni di proteine e carboidrati. Molte sono recettori. Molte glicoproteine si
protendono come altrettante antenne dalla superficie delle cellule, in attesa dell’arrivo di una molecola che
abbia una forma che permetta di agganciarsi ad esse.
PROTEINE NEL NOSTRO ORGANISMO
Tra le più importanti proteine fibrose abbiamo:
il collagene che entra nella costituzione del tessuto connettivo, del tessuto osseo e cartilagineo;
la cheratina che entra nella composizione dello strato più esterno della pelle, dei peli e delle unghie;
il fibrinogeno, che è una proteina plasmatica, responsabile della coagulazione del sangue;
la miosina e l’actina, che sono responsabili della contrazione muscolare;
l’albumina e le globuline, che sono contenute nelle cellule, nel siero del sangue;
l’emoglobina, che trasporta l’ossigeno a tutti i tessuti;
gli enzimi, che intervengono nei processi metabolici;
gli ormoni, prodotti dalle ghiandole endocrine, che stimolano particolari organi bersaglio, che, a loro
volta, avviano e controllano fenomeni importanti;
gli anticorpi o immunoglobuline, che vengono prodotti nel siero del sangue in seguito al
riconoscimento degli antigeni da parte delle cellule del sistema immunitario
APPROFONDIMENTO
LA STRUTTURA DELLE PROTEINE
Esistono diverse possibili modalità con cui una lunga collana può essere disposta nello spazio: linearmente,
avvolta su se stessa a gomitolo. a zig-zag, ecc. Così le lunghe catene proteiche possono assumere diverse
disposizioni spaziali, che dipendono dalla sequenza di amminoacidi di cui sono costituite; ogni proteina si
organizza nello spazio assumendo una specifica struttura, la quale garantirà una certa funzione.
La struttura primaria corrisponde alla semplice sequenza lineare degli amminoacidi che è determina
dalle informazioni ereditarie contenute nella molecola del DNA. L’insulina, ad esempio, è una proteina
disposta nello spazio in modo semplicemente lineare.
struttura primaria
L. DEL FABBRO: “ LE PROTEINE”
I.T.C. “A.ZANON” – UDINE
6
La struttura secondaria è la forma che la catena polipeptidica assume nello spazio ripiegandosi su se
stessa e che può essere ad alfa elica, in cui la catena di amminoacidi si avvolge come un nastro attorno ad
un asse, oppure a lamine beta ( o più semplicemente a foglietto ripiegato) come nelle proteine fibrose
che costituiscono i capelli, la lana e la seta. Responsabili del mantenimento di tale struttura sono i legami a
idrogeno che si vengono a formare tra amminoacidi in posizioni diverse della catena.
La cheratina o la miosina dei muscoli sono proteine con struttura ad elica; il collagene, i cui sono costituiti i tendini,
risulta dall’attorcigliamento ad elica di tre catene proteiche. La fibrina ha invece una disposizione a foglietto ripiegato.
La struttura terziaria consiste in un ulteriore avvolgimento della molecola, che si verifica quando si
stabiliscono legami a idrogeno o di altro tipo tra i gruppi R degli amminoacidi, e determina una
struttura tridimensionale complessa che spesso conferisce alla proteina una forma globulare. Questa
struttura è tipica infatti delle proteine globulari, tra cui molto importanti sono gli enzimi e gli anticorpi.
Quando più molecole proteiche con una struttura terziaria si uniscono tra di loro si ottiene un ulteriore
complessità strutturale, detta struttura quaternaria, come nel caso dell’emoglobina, che risulta sempre
formata da quattro catene uguali a due a due.
a. Struttura terziaria delle proteine in cui sono messi in
evidenza i legami a idrogeno che si formano tar i gruppi R
b. Struttura quaternaria. Nell’emoglobina, ciascuna delle
quattro catene costituenti la struttura quaternaria è avvolta
attorno a un gruppo contenente ferro, il quale lega una
molecola di ossigeno. Ogni molecola di emoglobina trasporta
dunque quattro molecole di ossigeno.
Esempio di
terziaria de
Esempi di struttura
secondaria delle
proteine.
(a) Struttura ad alfa
elica. (b) Struttura a
lamine beta
Esempio di struttura
quaternaria di una
proteina. La proteina
raffigurata è costituita da
quattro catene
polipeptidiche.
L. DEL FABBRO: “ LE PROTEINE”
I.T.C. “A.ZANON” – UDINE
6
Poiché dalla struttura primaria dipende la possibilità di organizzazione delle strutture successive, si capisce
quale possa essere l’importanza della sequenza di amminoacidi nella catena proteica: una errata sequenza
comporta una errata struttura e quindi una funzione errata.
Esiste una malattia chiamata anemia falciforme, provocata dalla sostituzione di un amminoacido con un
altro in un determinato punto di una delle quattro catene che formano l’emoglobina. Le molecole di
emoglobina assumono una disposizione anomala, risultando più allungate e indurite; a loro volta i globuli
rossi, che contengono enormi quantità di questa proteina, risultano deformati, assumendo una forma a falce
anziché tonda. I globuli rossi si ostacolano a vicenda, finendo per formare degli ammassi che ostacolano il
passaggio di sangue nei vasi capillari.
La conformazione originaria di una proteina può essere alterata anche da fattori chimici o fisici: le alte
temperature, la presenza di sostanze acide o basiche o di metalli pesanti provocano la denaturazione delle
proteine, cioè la deformazione della sua organizzazione spaziale per rottura dei legami non covalenti tra
amminoacidi situati in posizioni diverse della catena.
Bibliografia
D.G. Mackean, Laura Masini “ I moduli di Scienze della Natura”V2 Ed. Scolastiche Bruno Mondadori
David Krogh “ Biologia – guida alla Natura” vol.A Le Monnier
E. Porzio, O.Porzio “Sistema natura – moduli di biologia” ed .
Valitutti, Tiffi,Gentile “ Le idee della Chimica” ed. Zanichelli
A. Post Baracchi A. Tagliabue “Chimica” ed. LAttes
A.Zullini, A. Sparsoli,F.Sparvoli “Scienze della natura” Atlas
L. DEL FABBRO: “ LE PROTEINE”
I.T.C. “A.ZANON” – UDINE