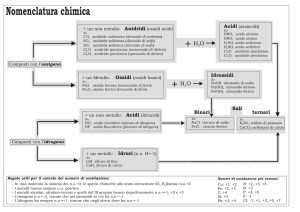
METALLO+OSSIGENO=OSSIDO BASICO
L’OSSIGENO E’ PRESENTE NELL’ARIA (O2: MOLECOLA FORMATA DA 2
ATOMI) E SI COMBINA FACILMENTE CON LE
ALTRE SOSTANZE NELLE REAZIONI DI:
-OSSIDAZIONE: REAZIONE LENTA SENZA
SVILUPPO DI LUCE E FIAMMA (ES DAL FERRO SI
FORMA LA RUGGINE CHE E’ OSSIDO DI FERRO)
4Fe +3O2 = 2Fe2O3
-COMBUSTIONE: TIPO PARTICOLARE DI
OSSIDAZIONE CHE AVVIENE VELOCEMENTE E
CON SVILUPPO DI LUCE E FIAMMA (QUANDO SI
BRUCIA QUALCOSA COME CARBONE, CARTA
ECC.).
ES, BRUCIAMO IL MAGNESIO: SI HA UNA LUCE
INTENSA CHE VENIVA UTILIZZATA UNA VOLTA
NEI FLASH. SI OTTIENE OSSIDO DI MAGNESIO
CHE E’ UNA POLVERINA FINISSIMA
INSOLUBILE IN ACQUA.
NON METALLO+OSSIGENO=OSSIDO ACIDO O ANIDRIDE
QUANDO UN NON METALLO COME IL CARBONIO O LO ZOLFO SI
COMBINANO CON L’OSSIGENO SI OTTIENE UN OSSIDO DETTO ANCHE
ANIDRIDE
C+O2=CO2
IL CARBONIO CON L’OSSIGENO FORMA ANIDRIDE
CARBONICA O BIOSSIDO DI CARBONIO
2C+O2 =2CO A VOLTE SI PUO’ FORMARE UN ALTRO GAS
VELENOSISSIMO CHE E’ L’OSSIDO DI
CARBONIO O MONOSSIDO DI CARBONIO
S+O2 =SO2 LO ZOLFO CON L’OSSIGENO
FORMA L’ANIDRIDE SOLFOROSA
OSSIDO (BASICO)+ACQUA=IDROSSIDO
ES. L’OSSIDO DI SODIO CON ACQUA FORMA L’IDROSSIDO
DI SODIO (SODA CAUSTICA, NaOH, USATA PER STURARE I
LAVANDINI PERCHE’ AGISCE SVILUPPANDO CALORE E
QUINDI DECOMPONENDO I RESIDUI CHE INTASANO GLI
SCARICHI).
Na2O + H2O = 2NaOH
IN ACQUA NaOH SI SEPARA NEI SUOI IONI Na+ E OH-.
LE SOSTANZE CHE IN ACQUA
RILASCIANO OH- SONO DETTE BASI:
RICONOSCONO CON LA CARTINA AL
TORNASOLE CHE SI COLORA DI
AZZURRO.
SI
ANIDRIDE+ACQUA=OSSIACIDO
QUANDO UN’ANIDRIDE REAGISCE CON ACQUA SI FORMA UN
OSSIACIDO.
ES. ANIDRIDE SOLFOROSA+ACQUA=ACIDO SOLFOROSO
SO2+H2O=H2SO3
UN ALTRO ACIDO IMPORTANTE E’ L’ACIDO SOLFORICO: H2SO4
QUESTE SOSTANZE SONO LA CAUSA DELLE PIOGGE ACIDE CHE
CORRODONO I MONUMENTI
ESPERIMENTI REALIZZATI IN LABORATORIO:
1. LA COMBUSTIONE DEL MAGNESIO
2. REAZIONE DI SCAMBIO FERRO-RAME (CHIODI METALLICI NEL
SOLFATO DI FERRO
3. REAZIONE DEL RAME METALLICO CON L’ACIDO NITRICO
4. IL SEMAFORO CHIMICO (REAZIONE DI OSSIDO-RIDUZIONE
TRA IL GLUCOSIO E UN COLORANTE BLU)