13
BOVINI
Large Animals Review, Anno 10, n. 5, Ottobre 2004
INFEZIONE DA BoHV-4
ASSOCIATA A METRITE-VAGINITE
IN UN ALLEVAMENTO BOVINO
MICHELE CAMERO1, ELVIRA TARSITANO1, GRAZIA GRECO1, COSTANTINA DESARIO1,
PIETRO GARGANO2, GIUSEPPE LUCIFORA2, MARIA TEMPESTA1
1
Dipartimento di Sanità e Benessere degli animali - Facoltà di Medicina Veterinaria di Bari
Strada provinciale per Casamassima km. 3 - 70010 Valenzano (BA)
2
Istituto Zooprofilattico Sperimentale del Mezzogiorno - Sezione di Cosenza - Via Panebianco, 301 - 87100 Cosenza
Riassunto
Viene descritto un focolaio di metrite e vulvo-vaginite da BoHV-4 (bovine herpesvirus-4) osservato in un allevamento bovino del sud Italia. Sono state interessate 14 vacche adulte che sono tutte risultate sieropositive per BoHV-4.
Nei secreti vaginali di due bovine è stato identificato BoHV-4 mediante la Polymerase chain reaction (PCR).
Summary
The authors report an outbreak of metritis and vulvo-vaginitis caused by BoHV-4 (bovine herpesvirus-4) occurred in a bovine herd in southern Italy. Fourteen adult cows were involved and resulted seropositive to BoHV-4.
BoHV-4 was detected by Polymerase Chain Reaction (PCR) in the vaginal discharge of two cows.
INTRODUZIONE
Bovine herpesvirus-4 (BoHV-4) è un virus cosmopolita
appartenente alla famiglia Herpesviridae1,2. In base all’analisi strutturale del genoma, BoHV-4 è classificato come γherpesvirus3,4.
Il primo isolamento risale al 1966 da un vitello con sintomatologia respiratoria5. In seguito il virus è stato isolato
ripetutamente da animali con una varietà di sintomi clinici
che includevano aborto, metrite, vaginite, enterite e polmonite, ma anche da animali apparentemente sani1,6,7.
Attraverso analisi del DNA con enzimi di restrizione sono stati identificati due tipi di BoHV-4 riconducibili rispettivamente ai due prototipi DN 599 e Movar 33/632,8,9.
Al contrario di BoHV-1 (virus della rinotracheite infettiva
del bovino) e BoHV-2 (virus della mammillite erpetica del
bovino), BoHV-4 non è mai stato riconosciuto come agente eziologico di una specifica malattia pertanto il suo ruolo
patogeno non è ancora chiaro9,10,11. Il virus è stato isolato
frequentemente da animali con concomitanti infezioni batteriche o in associazione ad altre infezioni virali, quali la
Diarrea Virale Bovina (BVD) e la Febbre Catarrale Maligna (MCF)12. Analogamente ad altri herpevirus, BoHV-4
determina nei suoi ospiti naturali un’infezione latente, e
può essere riattivato attraverso il trattamento con glucocorticoidi13 o, verosimilmente, in condizioni di immunodepressione dovuta anche ad altre infezioni.
Analogamente agli altri γ-herpesvirus3, BoHV-4 possie-
de tropismo per le cellule linfoidi sia negli ospiti naturali
che sperimentali14,15.
Nel coniglio, utilizzato come modello di infezione da
BoHV-4, è stata dimostrata un’ampia disseminazione del
virus nei tessuti. Nella coniglia gravida inoculata per via
intra-uterina sono stati osservati aborto, riassorbimento o
mummificazione fetale ed endometrite15,16,17.
BoHV-4 è stato isolato da una varietà di animali fra cui
il bisonte americano (Bison bison)18, il bufalo africano
(Syncerus caffer)19, la capra20 ma anche da alcuni carnivori
quali gatti e leoni10,21,22.
Il virus, solitamente viene isolato e coltivato su diverse
colture cellulari quali Bovine Embryo Kidney (BEK); Madin Darby Bovine Kidney (MDBK); Bovine foetal spleen
(BSF); Georgia Bovine Kidney (GBK). Oltre a linee cellulari bovine continue possono essere utilizzate cellule primarie di bovino ma anche di pecora, capra, cane, gatto,
coniglio, suino e pollo23. A differenza di altri herpesvirus
l’isolamento di BoHV-4 è abbastanza difficoltoso a causa
della lenta replicazione e dell’effetto citopatico poco evidente15,24. Le cellule endoteliali di arteria bovina sembrano
essere un ottimo substrato per la coltivazione del virus9.
Frequentemente BoHV-4 è stato isolato da bovine con
metrite o che avevano abortito7,25,26,27.
L’infezione sperimentale di bovini può indurre una malattia genitale13,28. Nella presente nota viene descritto un
focolaio di infezione da BoHV-4 in un allevamento di bovine da latte con problemi a carico della sfera riproduttiva.
14
Infezione da BoHV-4 associata a metrite-vaginite in un allevamento bovino
MATERIALI E METODI
Descrizione del focolaio
I casi clinici sono stati osservati in un allevamento di bovine da latte della provincia di Cosenza in cui si erano verificati diversi casi di aborto nell’arco dell’anno.
All’epoca dell’insorgenza del focolaio l’effettivo dell’allevamento comprendeva 370 bovini di cui 160 vacche in
lattazione. Nel settembre 2003, quattordici vacche hanno
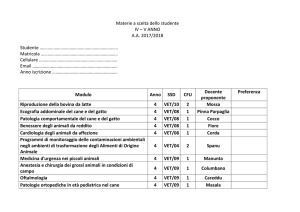
manifestato quasi contemporaneamente una sintomatologia caratterizzata da grave metrite e vaginite con profusa
essudazione muco-purulenta (Fig. 1). La mucosa vaginale
si presentava edematosa ed iperemica con presenza, in alcuni casi, di petecchie ed evidenti erosioni (Figg. 2, 3).
Dagli animali con sintomatologia in atto e da altri 10
soggetti apparentemente normali, sono stati prelevati campioni di sangue e di secrezioni vaginali.
FIGURA 1 - Scolo vaginale muco-purulento.
Isolamento virale
I campioni sono stati omogenati al 10% con terreno minimo essenziale di Dulbecco (D-MEM) e poi centrifugati a
5.000 x g per 10’ a +4°C. Il surnatante di ciascun campione, opportunamente antibiotato (penicillina 5000 UI/ml,
streptomicina 2500 µg/ml e fungizone 10 µg/ml) è stato
inoculato su monostrati di cellule renali bovine in linea
continua (MDBK) sviluppate in piastre a 24 pozzetti utilizzando per ciascun campione 2 pozzetti di cui uno con
vetrino.
Le colture cellulari, poste ad incubare a 37°C sono state
osservate quotidianamente al microscopio rovesciato per
evidenziare la presenza di effetto citopatico. Dopo 5 giorni
di incubazione, i monostrati cellulari inoculati sono stati
sottoposti a test di immunofluorescenza indiretta (IFI) utilizzando un siero bovino positivo per BoHV-4 e un siero
di coniglio anti-IgG di bovino marcato con fluoresceina
(Sigma-Aldrich, Milano).
I campioni sono stati considerati negativi in assenza di
effetto citopatico, e/o di fluorescenza dopo 3 passaggi seriali su cellule.
FIGURA 2 - Iperemia della mucosa vaginale con lesioni.
Esami per Mycoplasma spp.
I campioni sono stati sottoposti a test PCR per Mycoplasma secondo quanto riportato di seguito e, parallelamente, sono stati coltivati in brodo SP-4 e mantenuti a
37°C per una settimana.
Un’aliquota, pari a 100 µl delle colture, è stata trasferita
in terreno solido SP-4 e incubata a 37°C in camera umida
per un’ulteriore settimana mentre un’altra aliquota è stata
utilizzata per il test PCR.
Polymerase Chain Reaction (PCR)
Per l’estrazione del DNA virale dal criolisato delle cellule infette e dalle secrezioni vaginali è stato impiegato il kit
QIAamp Blood Kit (Qiagen GmbH, Germany). Duecento
microlitri di criolisato e/o secrezioni vaginali sono stati miscelati con 25 µl di proteinasi K e 200 µl di tampone di lisi
(AL). Dopo incubazione a 70°C per 10 minuti, sono stati
aggiunti 210 µl di alcool etilico assoluto. Il DNA è stato
quindi estratto su colonnine a matrice di resina, purificato
mediante 3 lavaggi con tampone AW a 6000 x g per 1’ ed
eluito in 100 µl di acqua distillata DNAse-free.
FIGURA 3 - Lesioni fibrinose ed emorragiche in sede vaginale.
La PCR è stata effettuata utilizzando una coppia di primer specifici per la regione non conservata E di BoHV-4 in
posizione 6153-6173 e 6423-6404 (nt)29, in grado di amplificare un frammento di 271 bp. La sequenza dei primer è la
seguente: P1 5’-TGAGACTATCTGGGAGTGCTTC-3’ e
P2 5’-CTCCTTCACTTCTGCCAGTG-3’.
La reazione è stata effettuata in 50 µl contenenti 5 µl di
DNA, 5 µl di buffer PCR II 10x, 4 µl di MgCl2 (1,5 mM),
2 µl di DNTPs (200 µM), 1 µl di ciascun primer (100 pM),
5 µl di glicerolo, 1 U di Amplitaq GOLD Polymerase (Applera, Italia, Monza). La reazione di amplificazione è stata
effettuata mediante attivazione della DNA polimerasi per
10 min a 94°, seguita da 35 cicli di 1 min a 94°C, 1,5 min a
55°C, 2 min a 72°C ed estensione finale per 10 min a
72°C.
Dieci microlitri di amplificato sono stati posti su gel di
agarosio al 2% in tampone TBE (0,09 M di acido borico,
0,09 M di Tris, 0,0025 M di EDTA, pH 8,3) e sottoposti
ad elettroforesi a 50V per 90’. Le bande di amplificazione
sono state visualizzate su transilluminatore a UV dopo colorazione con etidio bromuro (0,5 µg/ml). Nella prova è
stato incluso il DNA di BoHV-4 come controllo positivo e
un DNA estraneo come controllo negativo.
Per l’estrazione del DNA micoplasmico, 200 µl delle secrezioni vaginali sono state diluite con 200 µl di buffer AL
(Qiagen Tissue Kit GmbH, Hilden, Germany) e 20 µl di
proteinasi K.
Per l’estrazione del DNA micoplasmico dalle colture, 1
ml di terreno è stato centrifugato a 10000 x g per 20 minuti. Il pellet ottenuto è stato disciolto in 180 µl del buffer di
lisi ALT (Qiagen Tissue Kit GmbH, Hilden, Germany) a
cui sono stati aggiunti 30 µl di Proteinasi K.
Dieci µl di ciascun campione sono stati sottoposti a
PCR e nested-PCR basate sull’amplificazione della regione compresa tra i geni 16S e 23S dell’RNA ribosomiale
del DNA micoplasmico, secondo quanto già descritto da
Harasawa30.
Esami sierologici
I sieri delle 14 bovine con patologie e delle 10 bovine
apparentemente normali sono stati esaminati utilizzando
un test di immunofluorescenza indiretta (IFI) su vetrini
multispot (Biomerieux, Italia SpA) contenenti cellule di
polmone embrionale bovino (PEB) infettate con BoHV4. Ciascun siero è stato diluito a raddoppio partendo dalla diluizione 1:50. La reazione è stata visualizzata con siero di coniglio anti IgG di bovino marcato con fluoresceina (Sigma-Aldrich Co., Italia).
e 1.800. Quattro dei 10 animali apparentemente sani sono
risultati sieronegativi, mentre gli altri 6 soggetti hanno presentato titoli compresi fra 1:50 e 1:400.
DISCUSSIONE
Diverse indagini sierologiche condotte in Italia ed all’estero hanno evidenziato una significativa diffusione dell’infezione da BoHV-4 negli allevamenti bovini31,32,33,34,35.
Tuttavia non sempre è stata evidenziata una correlazione
diretta tra presenza di anticorpi per BoHV-4 e specifica
patologia. In bovine con disturbi della sfera riproduttiva è
stata ritrovata una più elevata positività sierologica per
BoHV-4 (17,2%) rispetto a bovine clinicamente sane
(10,0%)26. Occorre sottolineare che molto spesso è difficile confermare il sospetto clinico di infezione da BoHV-4
mediante l’isolamento del virus. In effetti anche nella presente indagine BoHV-4 è stato evidenziato solo con la
PCR mentre i tentativi di isolamento hanno fornito esito
costantemente negativo.
La esatta patogenesi dell’infezione da BoHV-4 nel bovino non è ancora perfettamente nota. Risulta pertanto difficile interpretare i risultati ottenuti nel presente studio. È
indubbio però che l’insorgenza di metrite e vaginite in un
discreto numero di bovine, alcune delle quali risultate positive al test PCR per BoHV-4, pone ulteriormente in evidenza il potenziale ruolo di questo virus nel determinismo
di patologie a carico della sfera riproduttiva.
Parole chiave
Bovino, herpesvirus tipo 4, metrite, vulvo-vaginite, PCR.
Key words
Bovine, herpesvirus type 4, metritis, vulvo-vaginitis, PCR.
Bibliografia
1.
2.
3.
4.
5.
RISULTATI
La PCR specifica per la regione non conservata E di
BoHV-4 ha prodotto amplificati di 271 bp in due dei
quattordici campioni di secreto vaginale esaminati.
Nei monostrati cellulari inoculati con i campioni e nei
successivi passaggi seriali non è comparso alcun effetto citopatico né è stato possibile osservare la presenza dell’antigene BoHV-4 mediante test IFI.
Sia il test PCR che le prove colturali per la ricerca di micoplasmi hanno fornito esito negativo.
Tutti i sieri delle bovine con sintomatologia hanno presentato anticorpi per BoHV-4 con titoli compresi tra 1:200
15
6.
7.
8.
9.
10.
Ludwig H. (1983) Bovine Herpesviruses: In: B. Roizman (Ed.). The Herpesviruses. Vol. 2. Plenum, New York, pp. 135-214.
Thiry E., Bublot M., Dubuisson J., and Pastoret P.P. (1989). Bovine Herpesvirus-4 (BHV-4) infections in cattle. In: Wittmann G. (Ed.), Herpesvirus
Diseases of Cattle, Horses and Pigs. Kluwer, Boston, Mass, pp. 96-115.
Bublot M., Lomonte P., Lequarre A.S., Albrecht J.C., Nicholas J., Fleckenstein B., Pastoret P.P. and Thiry E. (1992). Genetic relationships between
bovine herpesvirus 4 and the gammaherpesviruses Epstein-Barr virus
and herpesvirus Saimiri. Virology 190, 654-665.
Thiry E., Bublot M., Dubuisson J., Van Bressem M.F., Lequarre A.S., Lo
monte P., Vanderplasschen A., and Pastoret P.P. (1992). Molecular biology of bovine herpesvirus type 4. Vet. Microbiol. 33, 79-92.
Bartha A., Juhasz M., Liebermann H., Hantschel H. and Schulze P.
(1966). Isolation and properties of a bovine herpesvirus from a calf
with respiratory disease and keratoconjunctivitis. Archs. Exp. Vet. Med.
21, 615-623.
Buonavoglia C., Zicarelli L., Di Trani L., Orfei Z. (1984). Isolamento di un
virus herpetico e di Acholeplasma laidlawii da una bovina affetta da metrite post-partum. Selez. Vet. 25, 731-732.
Castrucci G., Frigeri F., Cilli V., Donelli G., Ferrari M., Chicchini U. and Bordoni E. (1986). A study of a herpesvirus isolated from dairy cattle with a
history of reproductive disorders. Comp. Immun. Microbiol. Infect. Dis. 9,
13-21.
Donofrio G., Cavirani S., Flammini C.F. Scatozza F. (2000). Molecular typing of a BHV-4 (bovine herpesvirus 4) field isolate. Vet. Res. Commun.
24, 411-422.
Lin TM, Shi GY, Tsai CF, Su HJ, Guo YL, Wu HL. (1997). Susceptibility of
endothelial cells to bovine herpesvirus type 4 (BHV-4). J. Virol. Meth. 63,
219-225.
Kruger J.M., Venta P.J., Swenson C.L., Syring R., Gibbons-Burgener S.N.,
Richter M., and Maes R.K. (2000). Prevalence of bovine herpesvirus-4 in-
BOVINI
Large Animals Review, Anno 10, n. 5, Ottobre 2004
16
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.
23.
24.
Infezione da BoHV-4 associata a metrite-vaginite in un allevamento bovino
fection in cats in Central Michigan. J. Vet. Intern. Med. 14, 593-597.
Staczek J. (1990). Animal cytomegaloviruses. Microbiol. Rev. 54, 247265.
Doyle L.G. and Heuschele W.P. (1983). Bovine viral diarrhea virus infection in captive exotic ruminants. J. Am. Vet. Med Assoc. 183, 1257-1259.
Dubuisson J., Thiry E., Bublot M., Thomas I., Van Bressem M.F., Coignoul
F. and Pastoret P.P. (1989). Experimental infection of bulls with a genital
isolate of bovine herpesvirus-4 and reactivation of latent virus with dexamethasone. Vet. Microbiol. 16, 339-349.
Osorio F.A. and Reed D.E. (1983). Experimental inoculation of cattle with
bovine herpesvirus-4: evidence for lymphoid-associated persistent infection. Am. J. Vet. Res. 44, 975-980.
Naeem K., Murtaugh M.P., Goyal S.M. (1991) Tissue distribution of bovid
herpesvirus-4 in inoculated rabbits and its detection by DNA hybridization
and polymerase chain reaction. Arch. Virol. 119, 239-255.
Naeem K., Caywood D.D., Werdin R.E., Goyal S.M. (1990) Evaluation of
pregnant rabbits as a laboratory model for bovid herpesvirus-4 infection.
Am. J. Vet. Res. 51, 640-644.
Tempesta M., Marsilio F., Tiscar P.G. Buonavoglia D., Abdi Farah A., Vitellozzi G. and Buonavoglia C. (1996): Evaluation of the pathogenicity to pregnant rabbits of a bovine herpesvirus-4 (BHV-4) strain. Eur. J. Vet. Path.
2, 83-85.
Todd W.J. and Storz J. (1983). Morphogenesis of a cytomegalovirus from
an American bison affected with malignant catarrhal fever. J. Gen. Virol.
64, 1025-1030.
Rossiter P.B., Gumm I.D., Stagg D.A., Conrad P.A., Mukolwe S., Davies
F.G. and White H. (1984). Isolation of bovine herpesvirus-3 from African
Buffaloes (Syncerus caffer). Res. Vet. Sci. 46, 337-343.
Moreno-Lopez J., Goltz M., Rehbinder C., Valsala K.V. and Ludwig H.
(1989). A bovine herpesvirus (BHV-4) as passenger virus in ethmoidal tumours in Indian cattle. J. Vet. Med. B. 36, 481-486.
Egyed L. (2000). Bovine herpesvirus type 4; a special herpesvirus. Acta
Vet. Hung 48, 501-513.
Fabricant C.G., Gillespie J.H., and Krook L. (1971). Intracellular and extracellular mineral crystal formation induced by viral infection of cell cultures. Infect. Immun. 3, 416-419.
Barahona H.H., Melendez L.V., King N.W., Daniel M.D., Fraser C.E.o: and
Preville A.C. (1973). Herpesvirus aotus type 2: A new viral agent from owl
monkeys (Aotus Trivirgatus). J. Infect. Dis. 127, 171-178.
Martin W.B., Castrucci G., Frigeri F., Ferrari M. (1990). A serological com-
25.
26.
27.
28.
29.
30.
31.
32.
33.
34.
35.
parison of some animal herpesviruses. Comp. Immun. Microbiol. Infect.
Dis. 13, 74-84.
Buonavoglia C., Zicarelli L., De Nardo P., Fioretti A., Orfei Z. (1986). Isolamento di un virus erpetico da una bovina affetta da metrite post-partum.
Riv. Zoot. Vet. 14, 169-174.
Czaplicki G. and Thiry E. (1998). An association exists between bovine
herpesvirus-4 seropositivity and abortion in cows. Prev. Vet. Med. 33,
235-240.
Van Opdenbosch E, Wellemans G, Ooms LA, Degryse AD. (1988). BHV4
(bovine herpes virus 4) related disorders in Belgian cattle: a study of two
problem herds. Vet. Res. Commun. 12, 347-353.
Wellemans G., Van Opdenbosch E., Mammerickx M. (1986). Experimental inoculation of bovine herpesvirus 4 (strain LVR 140) in pregnant and
nonpregnant cows. Ann. Rech. Vet. 17, 89-94.
Lin T.M., Jiang M.J., Eng H.L., Shi G.Y., Lai L.C., Huang B.J., Huang K.Y.,
Wu H.L. (2000). Experimental infection with Bovine Herpesvirus-4 enhances atherosclerotic process in rabbit. Labor. Invest. 1, 3-11.
Harasawa R. (1996). PCR: application of nested PCR to detection of mycoplasmas. In: Molecular and Diagnostic procedures in mycoplasmology,
vol II, eds. Joseph G. Tully and Shmuel Razin. London, Academic Press,
pp. 75-79.
Iovane G., Londrillo S., Tempesta M. (1988). Indagine sierologica (microtest di immunofluorescenza indiretta) sulla diffusione di anticorpi verso
Bovid Herpesvirus-4 (BHV-4) in bovine da latte della Campania. Acta
Med.Vet., 34, 423-434.
Wellenberg GJ, van Rooij EM, Maissan J, Van Oirschot JT. (1999). Evaluation of newly developed immunoperoxidase monolayer assays for detection of antibodies against bovine herpesvirus 4. Clin Diagn Lab. Immunol., 6, 447-451.
Marchot P., Thiry E., Jetteur P., Leroy P. (1991). Serological survey on the
prevalence of bovine type-4 herpesvirus infection in cattle in the Accra
plains of Ghana. Rev. Elev. Med. Vet. Pays. Trop. 44, 405-406.
Naeem K., Goyal S.M., Werdin R.E. (1989). Prevalence of bovid herpesvirus-4 and its antibody in cattle in Minesota. Am. J. Vet. Res. 50, 19311935.
Eyanga E., Jetteur P., Thiry E., Wellemans G., Dubuisson J., Van Opdenbosch E., Makumbu S., Pastoret P.P. (1989). Research on antibodies
against BHV-1, BHV-2, BHV-4, BVD-MD virus, bovine adenovirus A and
B, rotavirus and coronavirus in cattle in western Zaire: complementary results. Rev. Elev. Med. Vet. Pays. Trop. 42, 155-161.