Gennaio-Marzo 2014 • Vol. 44 • N. 173 • Pp. 20-24
endocrinologia pediatrica
L’ipertiroidismo in età pediatrica: una realtà rara
Giovanna Weber, Elena Peroni, Maria Cristina Vigone
Clinica Pediatrica, Istituto Scientifico Universitario, Ospedale San Raffaele, Milano
Riassunto
La malattia di Graves è la causa più comune di ipertiroidismo in età evolutiva, seguita dalla tiroidite autoimmune. Nella realtà europea, la terapia medica
con farmaci anti-tiroidei rappresenta la prima scelta terapeutica, nonostante il difficile controllo della funzionalità tiroidea, i noti effetti collaterali e il basso
rate di remissione. Per questi motivi è frequente il ricorso a una terapia definitiva chirurgica o con I-131, che però determina inevitabilmente una condizione
di ipotiroidismo iatrogeno permanente. Nessuna delle tre opzioni attualmente disponibili si è pertanto rivelata ottimale, evidenziando la complessità della
gestione terapeutica dell’ipertiroidismo autoimmune in età pediatrica.
Summary
Graves’ disease is the most common cause of thyrotoxicosis in children and adolescents, followed by autoimmune thyroid disease. In the European context,
antithyroid drug therapy is recommended as the initial treatment, despite the difficult control of thyroidal function, known side effects and the low rate of
remission. For these reasons a definitive therapy (surgery or radioactive iodine treatment with I-131) is commonly used as a second step, which is invariably
associated with the development of permanent hypothyroidism. None of the three options currently available has been shown to be clearly superior to the
others which further highlights the complexity of the therapeutic management of pediatric autoimmune hyperthyroidism.
Parole chiave: ipertiroidismo, età pediatrica, farmaci anti-tiroidei, tiroidectomia, radioiodio
Key words: hyperthyroidism, pediatric, antithyroid drug therapy, thyroidectomy, radioactive iodine
Obiettivo
Presentare le diverse forme di ipertiroidismo in età pediatrica, l’iter
diagnostico e le alternative terapeutiche.
Metodologia della ricerca bibliografica
La ricerca degli articoli è stata effettuata sulla banca dati bibliografica Medline utilizzando il motore di ricerca PubMed. Sono state
utilizzate le seguenti parole chiave: Hyperthyroidism, Pediatric, Antithyroid drug therapy, Thyroidectomy, Radioactive iodine. Sono stati
selezionati articoli originali, revisioni e linee guida recenti inerenti
l’età pediatrica.
Introduzione
L’ipertiroidismo è un’entità clinica rara in età pediatrica, caratterizzata da elevati livelli di ormoni tiroidei liberi associati ad inibizione del
TSH ipofisario. Nella maggioranza dei casi l’eziologia è autoimmune
e comprende principalmente la malattia di Basedow-Graves (MG) e
meno frequentemente la tiroidite autoimmune. In quest’ultimo caso
l’ipertiroidismo può esprimersi in fase iniziale con un transitorio e
per lo più lieve ipertiroidismo (fase di Hashitossicosi) secondario a
un aumentato rilascio di ormoni tiroidei preformati, conseguente
all’infiltrazione linfocitaria (De Luca et al., 2013).
Esistono inoltre condizioni cliniche rare associate all’ipertiroidismo
in età evolutiva, elencate in tabella I.
Malattia di Basedow-Graves
La MG è la causa più comune di ipertiroidismo in età pediatrica,
con un’incidenza dello 0,02%, a comparsa prevalentemente in età
adolescenziale. Sono a maggior rischio i soggetti di sesso femminile
(F:M = 5:1), affetti da altre patologie immunomediate e/o con anamnesi familiare positiva per tireopatia autoimmune.
Alla base della MG si osserva un’aumentata produzione di anticorpi
stimolanti diretti contro il recettore del TSH (Trab) che inducono iper-
Tabella I.
Cause di ipertiroidismo in età pediatrica.
PIÙ FREQUENTI
Cause autoimmuni
Malattia di Basedow-Graves (95%)
Tiroidite autoimmune (fase di Hashitossicosi)
RARE
Iperfunzione tiroidea autonoma
Adenoma tossico o nodulo solitario
Gozzo multinodulare
Cause esogene
Tireotossicosi factitia o accidentale
Ipertiroidismo iodio-indotto (farmaci, mezzi di contrasto iodati,…)
Cause genetiche
Mutazioni attivanti il TSHR
Sindrome di McCune-Albright
Mutazione del recettore degli ormoni tiroidei
Disfunzione ipofisaria
Adenoma TSH-secernente
MOLTO RARE
20
L’ipertiroidismo in età pediatrica: una realtà rara
plasia ghiandolare, aumento della vascolarizzazione, della sopravvivenza cellulare e della sintesi della proteina simporto sodio/iodio,
incrementando la formazione e la secrezione degli ormoni tiroidei
(Morshed et al., 2009).
Il meccanismo che porta alla produzione dei Trab è ancora poco
chiaro, verosimilmente di natura multifattoriale. Un ruolo fondamentale sembrerebbe svolto dalla suscettibilità genetica (probabilmente
di origine poligenica), dal sistema immunitario e dall’esposizione
a un trigger esterno (secondo alcuni Autori mediante un meccanismo di mimetismo molecolare conseguente a un processo infettivo)
(Wang et al., 2010). Secondo altri studi, un insulto al parenchima
tiroideo (esempio, un processo infettivo) sarebbe in grado di indurre
l’espressione di molecole del Complesso Maggiore di Istocompatibilità di classe II da parte dei tireociti, trasformando questi ultimi in
cellule presentanti l’antigene, capaci di contribuire all’innesco della
risposta autoimmune.
Studi di linkage in cluster familiari con storia di tireopatia autoimmune hanno dimostrato il coinvolgimento di numerosi loci, ma ad
oggi nessuno sembra essere in grado di spiegare completamente
la patogenesi della malattia (Ban et al., 2004). Con molta probabilità
esistono altri geni, ancora da scoprire, in grado di modulare la penetranza della MG nei pazienti affetti.
All’esordio della MG, in alcuni studi effettuati su pazienti adulti, oltre
alla tireomegalia è riportata la presenza di iperplasia timica, che regredisce dopo il trattamento con farmaci anti-tiroidei; molto più rare
sono le segnalazioni in ambito pediatrico (Chiu et al., 2013; Kawano
e Kohno, 2011; Kubicky et al., 2010). Sebbene il meccanismo patogenetico dell’iperplasia timica sia attualmente dibattuto, sembra
esserci alla base un processo immunologico. È importante ricordare
questa associazione che, se misconosciuta (sospetto di massa mediastinica anteriore), può portare a una diagnostica inutile e spesso
invasiva (biopsia o timectomia).
Cause minori di ipertiroidismo
Iperfunzione tiroidea autonoma
Il sospetto diagnostico viene posto all’esame obiettivo in caso di palpazione di nodulo solitario o noduli multipli e a livello laboratoristico
in presenza di un quadro di ipertiroidismo non autoimmune. L’ecografia rappresenta il primo step diagnostico; la scintigrafia tiroidea
viene effettuata in seconda battuta. La terapia è in genere chirurgica.
Eccessiva ingestione di ormone tiroideo o eccessiva
esposizione a iodio
L’ipertiroidismo causato dall’assunzione esogena di ormone tiroideo
(definito factitio) può verificarsi durante l’adolescenza, quando l’abuso di ormone è legato al tentativo di perdere peso, sfruttandone il
potere regolatore sulla termogenesi e sulla lipolisi.
L’esposizione a quantità di iodio tali da indurre tireotossicosi può derivare dall’uso di antisettici topici o farmaci a base di iodio e dall’impiego di mezzi di contrasto iodati.
Cause genetiche
Mutazioni nel gene che codifica per il recettore del TSH: il recettore mutato (in genere a livello del dominio transmembrana) causa
un’attivazione costitutiva del pathway di trasduzione intracellulare
e, quindi, una costante stimolazione della crescita e dell’attività dei
tireociti (Alberti et al., 2001).
Sindrome di McCune-Albright: la mutazione interessa il gene GNAS1,
che codifica per la subunità α della proteina Gs compresa nel sistema
recettoriale di molti ormoni proteici (TSH, ACTH, gonadotropine, GHRH,
MSH). La proteina anomala, collocata sulla membrana cellulare, attiva
il complesso recettoriale, causando un’autonoma ed eccessiva proliferazione cellulare ed ipersecrezione ormonale che, se interessanti
la tiroide, determinano un quadro di ipertiroidismo non autoimmune.
Resistenza agli ormoni tiroidei: la mutazione interessa il gene β codificante per il recettore degli ormoni tiroidei. Si tratta di una sindrome ereditaria caratterizzata da una ridotta risposta agli ormoni
tiroidei, che si presenta con un quadro di elevati livelli di fT3 e fT4
associati a TSH normale o lievemente aumentato.
Adenoma pituitario TSH-secernente (Rabbiosi et al., 2012): può manifestarsi con elevati livelli ormonali non associati ad inibizione del
TSH; nel sospetto di tale condizione diventa importante il riscontro di
elevate concentrazioni sieriche della subunità α del TSH e di un’alterata risposta allo stimolo con TRH. La conferma viene dall’imaging
(RM encefalo con studio della regione ipotalamo-ipofisaria), mentre
la chirurgia rappresenta il gold standard terapeutico.
Malattia di Basedow-Graves
Presentazione clinica
In età pediatrica l’esordio dei sintomi tipici dell’ipertiroidismo è spesso
insidioso. Il più delle volte occorrono alcuni mesi prima che si arrivi
alla diagnosi definitiva; infatti, il sospetto diagnostico viene spesso
ritardato sia nei primi anni di vita, per la rarità della patologia e l’aspecificità dei sintomi, sia in epoca peri-puberale, quando le alterazioni
dell’umore e del comportamento o le difficoltà scolastiche caratteristiche dell’ipertiroidismo possono essere del tutto sovrapponibili alle
manifestazioni tipiche dell’età adolescenziale (Shulman et al., 1997).
In tabella II sono indicati i principali sintomi dell’ipertiroidismo in età
pediatrica.
In età evolutiva l’ipertiroidismo non trattato è in grado di interferire
con lo sviluppo puberale, la crescita, la maturazione e la mineralizzazione ossea (Mora et al., 1999).
Diagnosi
In associazione ai dati anamnestici e al riconoscimento di segni e/o
sintomi caratteristici, la diagnosi di ipertiroidismo si basa sul riscontro
di elevati livelli di ormoni tiroidei liberi associati a inibizione del TSH.
È fondamentale il riscontro della positività dei Trab (diagnostici per la
MG e positivi in più del 90% dei soggetti affetti) e degli anticorpi antitireoperossidasi e anti-tireoglobulina (solitamente elevati nelle forme
Tabella II.
Elenco dei principali sintomi di ipertiroidismo in età pediatrica.
SINTOMO
FREQUENZA (%)
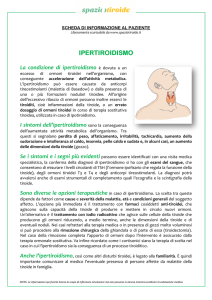
Gozzo (Fig. 1)
99
Tachicardia
83
Irritabilità
80
Ipertensione
71
Esoftalmo
66
Tremori
61
Aumento appetito
60
Perdita di peso
54
Palpitazioni
34
Mal di testa
15
Incremento nella frequenza dell’alvo
13
21
G. Weber et al.
fronte a un aumento degli ormoni tiroidei con TSH normale o lievemente aumentato, bisogna valutare la possibilità che si tratti di una
rara forma di resistenza agli ormoni tiroidei (è possibile riscontrare
simili livelli di fT3, fT4 e TSH anche in uno dei genitori) o di un raro
caso di adenoma TSH-secernente (l’imaging risulterà dirimente).
In caso di iperplasia timica, il riscontro di un quadro ormonale caratterizzato da TSH inibito e ormoni tiroidei elevati è fondamentale nella
diagnosi differenziale tra ipertiroidismo e miastenia gravis.
Figura 1.
Gozzo in paziente con ipertiroidismo autoimmune.
di tiroidite autoimmune, per quanto non patognomonici) in considerazione del fatto che le forme di ipertiroidismo in età pediatrica riconoscono nella quasi totalità dei casi un’eziologia autoimmune.
Nell’iter diagnostico molto informativo risulta essere l’esame ecografico; in caso di MG la ghiandola appare di volume aumentato,
in genere con struttura finemente disomogenea, prevalentemente
iporiflettente, con aumentata vascolarizzazione all’esame colorDoppler. L’ecografia è inoltre fondamentale nella diagnosi e caratterizzazione delle lesioni nodulari.
All’esordio dell’ipertiroidismo è opportuno eseguire alcuni esami a
completamento, elencati in tabella III.
La scintigrafia tiroidea viene effettuata nel sospetto di adenoma tossico ipercaptante.
Le cause non autoimmuni di ipertiroidismo, seppur rare, devono
essere prese in considerazione nella diagnosi differenziale. L’ipertiroidismo factitio è caratterizzato da un quadro ormonale che può essere sovrapponibile a quello della MG; tuttavia l’anamnesi, l’assenza
di anticorpi anti-tiroide, il riscontro di valori di tireoglobulina molto
bassi e un quadro ecografico normale ne permettono la diagnosi. Di
Alternative terapeutiche
Nella realtà europea il Metimazolo (MMI) è consigliato come trattamento di prima scelta dell’ipertiroidismo in età evolutiva, da continuarsi per 18-24 mesi, in grado tuttavia di garantire una ridotta
frequenza di remissione a lungo termine (20-30% dei pazienti in
fase peri-puberale e 15% dei pazienti pre-puberi) (Bahn Chair et
al., 2011). Il MMI è in grado di inibire la sintesi degli ormoni tiroidei,
interferendo con l’ossidazione dello iodio e la successiva iodinazione
dei residui di tirosina della tireoglobulina, azione mediata dall’enzima tireoperossidasi (Cooper, 2005).
In passato veniva utilizzato anche il Propiltiouracile (PTU), attualmente sconsigliato in età pediatrica per l’elevato rischio di epatotossicità (Rivkees et al., 2009). A questo proposito la FDA ha recentemente emesso un avviso di sicurezza: il PTU dev’essere utilizzato
limitatamente al primo trimestre di gravidanza (in quanto associato
a un minor rischio di anomalie congenite) o alla fase di bridge verso
una terapia definitiva in un paziente fortemente allergico al MMI.
Più controverso è il metodo block-and-replace, da utilizzarsi nei casi
di difficile controllo della funzionalità tiroidea, che consiste nell’utilizzo di alte dosi di tionamidi (ossia i farmaci antitiroidei), per bloccare la sintesi degli ormoni tiroidei, combinato alla L-Tiroxina, per
garantire uno stato di eutiroidismo, pur mantenendo la tiroide a riposo grazie all’inibizione della sintesi ormonale endogena (Abraham
et al., 2010).
Gli effetti collaterali delle tionamidi si differenziano in minori e maggiori (Tab. IV).
In caso d’instabilità ormonale durante il trattamento medico o di
fronte a una recidiva di malattia all’atto della sospensione terapeutica è possibile ricorrere a una terapia definitiva o, in assenza di
Tabella III.
Elenco degli esami da effettuarsi all’esordio dell’ipertiroidismo.
Esami consigliati
Valutazione cardiologica, ECG ed ecocardiogramma
Esoftalmometria e/o ecografia retro-orbitaria
Esami opzionali, da valutare caso per caso
Età ossea negli stadi pre/peri-puberali
DEXA per escludere una ridotta mineralizzazione ossea
Eventuale screening delle principali patologie autoimmuni
Tabella IV.
Principali effetti collaterali associati alla terapia con tionamidi, distinti in minori e maggiori.
REAZIONI AVVERSE MINORI
(5-25% dei pazienti trattati)
Reazioni cutanee minori (orticaria, rash, edema)
Lieve leucopenia
Modesto e transitorio movimento degli indici di funzionalità epatica
Artralgia e mialgie
Cefalea
Alterazioni del gusto
Disturbi gastro-intestinali
REAZIONI AVVERSE MAGGIORI
Agranulocitosi farmaco-indotta
Vasculite ANCA-associata
Epatotossicità
22
L’ipertiroidismo in età pediatrica: una realtà rara
effetti collaterali, è possibile proseguire la terapia farmacologica
fino al raggiungimento dell’età migliore per il ricorso a chirurgia o
radioiodio.
Attualmente la tiroidectomia viene scelta come terapia definitiva in
considerazione dell’età del paziente (< 5-10 anni) e delle dimensioni
della ghiandola tiroidea (> 80 grammi) (Peroni et al., 2012).
La scuola statunitense utilizza la terapia radiometabolica come
prima scelta a partire dai 10 anni e come scelta alternativa (in caso
di fallimento della terapia medica) nei pazienti di età compresa tra
5 e 10 anni. Nella realtà europea ancora forti sono le perplessità
in merito all’utilizzo del radioiodio nei soggetti con meno di 18
anni; tuttavia, in considerazione dell’assenza di effetti collaterali
a lungo termine rilevati in letteratura e alla luce dell’esperienza
americana, l’introduzione della terapia radiometabolica è sempre
più oggetto di discussione tra i medici europei, almeno nei soggetti
post-puberi.
L’effetto collaterale più temuto della terapia radiometabolica è quello
relativo al potenziale cancerogeno delle radiazioni ionizzanti. È stato
però dimostrato che il rischio di neoplasia tiroidea è maggiore in
caso di esposizione a bassi livelli di radiazioni, ben lontani dalle alte
dosi utilizzate nel trattamento della MG (Read et al., 2004).
Un altro aspetto dibattuto è il possibile effetto dello I-131 sulle cellule germinali e le eventuali ripercussioni sulla progenie. In letteratura
ci sono dati su 500 nati da circa 370 soggetti sottoposti a terapia
radiometabolica durante l’infanzia o l’adolescenza; l’incidenza di
anomalie congenite in questi 500 bambini non differisce da quella
della popolazione generale.
Alla luce di questi dati, la terapia radiometabolica appare sicura ed
efficace se utilizzata nel modo corretto.
L’identificazione di fattori prognostici relativi all’evoluzione dell’ipertiroidismo autoimmune rappresenterebbe un importante traguardo
in campo medico, indirizzando il clinico nella scelta terapeutica più
adatta al singolo paziente, individuando già alla diagnosi coloro che
potrebbero giovarsi di un prolungamento della terapia medica o del
ricorso a una terapia definitiva. Purtroppo finora c’è disaccordo tra
i risultati dei differenti studi pubblicati in letteratura: nessun fattore prognostico è risultato confermato e condiviso da tutti gli studi.
Attualmente la decisione del trattamento più idoneo da seguire in
ambito pediatrico è frutto di una stretta interazione tra la figura del
medico, il paziente e la sua famiglia ed è fortemente influenzata
dalle strutture mediche di riferimento del territorio.
Box di orientamento
Che cosa si sapeva prima
L’ipertiroidismo in età pediatrica è un’entità clinica rara, ma insidiosa. Attualmente la terapia migliore da seguire rimane materia di dibattito: nessuna
delle tre opzioni disponibili (terapia medica con farmaci anti-tiroidei, tiroidectomia e trattamento radiometabolico con I-131) si è rivelata ottimale,
presentando tutte vantaggi e svantaggi.
Che cosa sappiamo adesso
Attualmente si ricorre come prima scelta al trattamento con Metimazolo, da continuarsi per 18-24 mesi, in grado tuttavia di garantire una ridotta
frequenza di remissione a lungo termine. In caso d’instabilità ormonale durante il trattamento o di fronte a una recidiva di malattia all’atto della sospensione terapeutica è possibile ricorrere a una terapia definitiva o, in assenza di effetti collaterali, è possibile proseguire la terapia farmacologica, fino al
raggiungimento dell’età migliore per il ricorso a chirurgia o radioiodio.
Quali ricadute sulla pratica clinica
L’identificazione di fattori prognostici relativi all’evoluzione dell’ipertiroidismo autoimmune rappresenterebbe un importante traguardo in campo medico, indirizzando il clinico nella scelta terapeutica più adatta al singolo paziente, individuando già alla diagnosi coloro che potrebbero giovarsi di un
prolungamento della terapia medica o del ricorso a una terapia definitiva.
Bibliografia
Abraham P, Avenell A, McGeoch SC, et al. Antithyroid drug regimen for treating
Graves’ hyperthyroidism. Cochrane Database Syst Rev 2010;1:CD003420.
Alberti L, Proverbio MC, Costagliola S, et al. A novel germline mutation in the TSH
receptor gene causes non-autoimmune autosomal dominant hyperthyroidism.
Eur J Endocrinol 2001;145(3):249-54.
Bahn Chair RS, Burch HB, Cooper DS, et al. Hyperthyroidism and other causes of
thyrotoxicosis: management guidelines of the American Thyroid Association and
American Association of Clinical Endocrinologists. Thyroid 2011;21(6):593-646.
** L’articolo illustra le più recenti linee guida americane sull’ipertiroidismo, con
una sezione dedicata all’età pediatrica.
Ban Y, Concepcion ES, Villanueva R, et al. Analysis of Immune Regulatory gene in
familiar and sporadic Graves’ disease. J Clin Endocrinol Metab 2004;89,9:4562-8.
Chiu HK, Ledbetter D, Richter MW, et al. Reversible left recurrent laringeal nerve
palsy in pediatric Graves’ disease. Pediatrics 2013;132(6):e1704-8.
Cooper DS. Antithyroid drugs. N Engl J Med 2005;352(9):905-17.
* L’articolo illustra il meccanismo di funzionamento e gli effetti collaterali dei
farmaci anti-tiroidei.
De Luca F, Santucci S, Corica D, et al. Hashimoto’s thyroiditis in childhood: presentation modes and evolution over time. Ital J Pediatr 2013;39:8.
Kawano A, Kohno H. Thymic hyperplasia associated with Graves’disease in a 10
year-old boy. Clin Pediatr Endocrinol 2011;20(3):61-4.
Kubicky RA, Faerber EN, de Chadarevian JP, et al. An adolescent with mediastinal mass, diagnosed with Graves disease and thymic hyperplasia. Pediatrics
2010;125(2):e433-7.
Mora S, Weber G, Marenzi K, et al. Longitudinal changes of bone density and
bone resorption in hyperthyroid girls during treatment. J Bone Miner Res
1999;14,11:1971-7.
Morshed SA, Latif R, Davies TF. Characterization of thyrotropin receptor antibody-induced signaling cascades. Endocrinology 2009;150(1):519-29.
Peroni E, Angiolini MR, Vigone MC, et al. Surgical management of pediatric Graves’
disease: an effective definitive treatment. Pediatr Surg Int 2012;28(6):609-14.
Rabbiosi S, Peroni E, Tronconi GM, et al. Asymptomatic thyrotropin-secreting pituitary macroadenoma in a 13-year-old girl: successful first-line treatment with
somatostatin analogs. Thyroid 2012;22(10):1076-9.
Read CH Jr, Tansey MJ, Menda Y. A 36-year retrospective analysis of the efficacy
and safety of radioactive iodine in treating young Graves’ patients. J Clin Endocrinol Metab 2004;89(9):4229-33.
* L’articolo evidenzia l’efficacia e la sicurezza dell’utilizzo del radioiodio in età
pediatrica; la forza dello studio è rappresentata dalla numerosità del campione
e dalla durata del follow-up.
23
G. Weber et al.
Rivkees SA, Mattison DR. Propylthiouracil (PTU) Hepatoxicity in Children and Recommendations for Discontinuation of Use. Int J Pediatr Endocrinol 2009;132041.
* L’articolo sottolinea la pericolosità del PTU in età pediatrica.
Shulman DI, Muhar I, Jorgensen EV, et al. Autoimmune hyperthyroidism in prepubertal children and adolescents: comparison of clinical and biochemical features
at diagnosis and responses to medical therapy. Thyroid 1997;7,5:755-60.
Wang Z, Zhang Q, Lu J, et al. Identification of outer membrane porin f protein
of Yersinia enterocolitica recognized by antithyrotopin receptor antibodies in
Graves’ disease and determination of its epitope using mass spectrometry and
bioinformatics tools. J Clin Endocrinol Metab 2010;95(8):4012-20.
Corrispondenza
Giovanna Weber, IRCCS San Raffaele Università Vita-Salute, Centro di Endocrinologia dell’Infanzia e dell’Adolescenza, via Olgettina 60, 20132 Milano.
Tel.: +39 02 26432624. E-mail: [email protected]
24