ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Relazione:
Classi 1^ALS e 1^BLS
MISSIONE BRACCIO DI FERRO
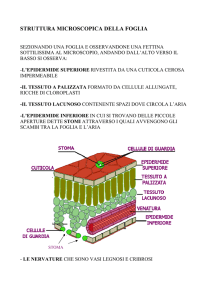
I pigmenti biologici:
sono generalmente classificati in base al tipo di molecola. I pigmenti piranici sono
derivati dalla molecola di pirano e si trovano soprattutto nelle piante. I più diffusi
appartengono al gruppo degli antociani che conferiscono colorazioni variabili dal blu al
rosso al viola (es: enocianina e clandinina).
Altri pigmenti piranici sono i flavoni, come la quercetina e la luteolina, di colori variabili
dall'arancio al giallo. I pigmenti pirrolici hanno molecole formate d un certo numero di
anelli dal pirrolo, ai quali sono legati anche atomi metallici, diversi in ciascun pigmento.
Fanno parte di questa categoria, che comprende molecole di grande importanza biologica,
la clorofilla e i pigmenti respiratori, molecole che si legano all'ossigeno e ne permettono il
trasporto e l'utilizzazione da parte delle cellule degli organismi animali.
Sono pigmenti respiratori l'emoglobina dei vertebrati, le eritocuorine dei protozoi, le
clorocruorine presenti in alcuni anellidi, le emocianine di molluschi e artropodi. I pigmenti
chinonici derivati da p-benzochinone, antrachinone e naftochinone, sono frequenti nei
funghi nelle muffe e in alcuni insetti; presentano colori molto vivaci, dal rosso al giallo.
I pigmenti polienici hanno struttura caratterizzata da doppi legami coniugati. I più
importanti sono i carotenodi, di colore giallo, arancione e rosso, presenti in molte piante e
animali; la crocetina che da il colore allo zafferano, il licopene ai pomodori, la zeaxantina
al mais e al tuorlo d'uovo.
Va infine considerato un gruppo dei pigmenti con struttura non riconducibile a nessuna
delle categorie citate; tra questi, la melanina, responsabile del colore della pelle e dei peli
nei vertebrati, che proteggono la pelle dalle radiazione ultraviolette.
I pigmenti delle piante:
Le piante verdi presentano nei diversi organi una diversità di colorazione, di tonalità di
colore, che rendono così vario e cangiante il paesaggio dei boschi e dei prati.
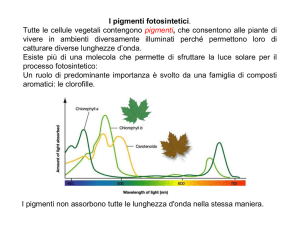
I vegetali sono dotati di pigmenti, cioè di sostanze colorate. I pigmenti principali delle
piante superiori sono le clorofille e i carotenoidi.
Le clorofille hanno colore verde, con due tonalità diverse. Si parla di colorofille, perchè
sono due: la clorofilla “a", che è l'artefice principale della fotosintesi cioè alla
trasformazione dell'energia luminosa in energia chimica, e la clorofilla "b", che è
considerata un pigmento acessorio. Un altro importante gruppo di pigmenti acessori è
quello dei carotenoidi di colore giallo-arancione.
I carotenoidi abbondano nei cloroplasti, ma normalmente il loro colore è mascherato dalla
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
clorofilla, per cui le foglie appaiono di norma verdi, e non gialle o arancioni. I carotenoidi,
quando sono contenuti in altri organuli, detti cromoplasti, sono invece ben visibili nei
petali dei fiori o nei frutti, ai quali danno i bei colori a tutti noti. In alcuni momenti dello
sviluppo della pianta, soprattutto in autunno, si verifica un cambiamento del rapporto
quantità di clorofilla/quantità di carotenoidi, i cloroplasti si trasformano in cromoplasti e
il colore delle foglie diventa rosso, arancione o giallo.
La clorofilla “b” e i carotenoidi sono in grado di assorbire la luce a lunghezze d'onda
diverse da quelle assorbite dalla clorofilla A e in altri casi, l'energia assorbita innesca
una reazione chimica.
Se avverrà o meno dipende dalle sue relazioni con le molecole vicine.
La clorofilla riesce a convertire l' energia luminosa in energia chimica, un processo che
inizia con una reazione di ossidoriduzione.
Quando i pigmenti assorbono la luce, gli elettroni,all'interno delle loro molecole,vengono
spinti a livelli di energia superiore; l'energia liberata può: essere assorbita da una
molecola vicina, in cui gli elettroni vengono spinti a livelli di energia più alti; essere
dissipata come calore; essere riemessa come energia luminosa di lunghezza d'onda
maggiore, un fenomeno detto fluorescenza.
I colori delle piante:
Domina il colore verde delle diverse clorofille che dal verde-blu vanno fino a un pallido
verde-giallo; è impressionante la costanza con la quale queste clorofille si presentano nei
grandi gruppi di piante e nelle alghe. Anche nelle colonie dei funghi microscopici e
batteri sono ben visibili le colorazioni verdi.
Il colore giallo è dovuto a varie quantità e combinazioni di pigmenti detti carotenoidi e
flavonoidi che danno delle spattacolari colorazioni ai paesaggi autunnali. Talora anche la
clorofilla tende al colore giallo e giallo-verde, specialmente in alcuni stadi iniziali
(protoclorofilla). Anche nei funghi e nei licheni si presentano colorazioni gialle, giallobrune, giallo-citrine. Il colore arancio è frequente, in numerosissimi fiori, nei frutti
(arancia), nelle radici (carota), ma anche nei funghi e nei licheni.
Il colore rosso è dovuto a sostanze (antocianine) in concentrazioni diverse. E' il caso di
ricordare la vasta categoria delle alghe rosse la cui colorazione è dovuta a particolari
pigmenti dell'apparato fotosintetico; i molti funghi e i licheni con intense colorazioni
rosse.
Il colore bruno è legato soprattutto alla colorazione autunnale e delle foglie morte
cadute al suolo. Nelle alghe, nei funghi e nei licheni si possono trovare colori rugginosi
dovuti a incrostazioni di ossido di ferro come anche in colonie batteriche delle acque
termali.
Il colore azzurro, anch'esso dovuto alle antocianine è frequentissimo nei fiori; si trova in
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
alcuni funghi del genere Boletus. Il colore violetto si presenta spesso nei fiori.
Non mancano screziature violette nelle foglie di alcune specie tropicali. Anche il colore
bianco è presente in molti fiori; si presenta anche nelle foglie tomentose, coperte di
lanosità candida.
Il colore nero o anche grigio si presenta per varie combinazioni, anzi accumuli di pigmenti
diversi. Interessanti sostanze però, dette fitomelanine, sono talora responsabili di
annerimenti di vari organi. I vegetali hanno costituito una fonte molto varia di coloranti
usati da tempi immemorabili per tingere le stoffe.
Struttura molecolare
Struttura molecolare della clorofilla a.
La clorofilla è una clorina. La molecola ha
una struttura ad anello, al centro del quale
c'è un atomo di magnesio, che ha la
funzione di mantenere la struttura rigida
per evitare che l'energia solare si disperda
sotto forma di calore prima che possa
essere utilizzata per il processo
fotosintetico. Dall'anello poi parte una
lunga catena idrofoba che serve per
ancorare la molecola di clorofilla alle
membrane dei tilacoidi. Vi sono alcune
forme differenti, ma la più universalmente
diffusa tra le piante terrestri è la clorofilla a, la cui struttura fu decodificata da Hans
Fischer nel 1940, e dal 1960, quando la stereochimica della clorofilla a era risaputa,
Robert Burns Woodward pubblicò una sintesi completa della molecola com'è ad oggi
conosciuta. Nel 1967, le residue delucidazioni stereochimiche furono perfezionate da Ian
Fleming, e nel 1990 Woodward e coautori pubblicarono una sintesi aggiornata.
Le differenti strutture della clorofilla sono sintetizzate sotto:
Clorofilla a
Formula molecolare
C55H72O5N4Mg
Clorofilla b
C55H70O6N4Mg
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Massa molecolare
893,51
907,49
Diffusione
Universale
Maggior parte delle
piante
Struttura della clorofilla a
Struttura della clorofilla b
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Nel momento in cui le foglie ingialliscono, la clorofilla è convertita in un gruppo di
tetrapirroli incolori conosciuti come cataboliti della clorofilla. Questi composti sono
anche stati identificati in vari frutti maturi.
Per questo motivo le foglie in autunno non mostrano il tipico colore verde, per il fatto che
gli altri pigmenti presenti non sono più mascherati dalla clorofilla e manifestano il loro
colore.
Estrazione e cromatografia dei pigmenti fogliari:
E’ possibile estrarre dalle foglie verdi i vari pigmenti e separarli utilizzando dei solventi e
un supporto (fase stazionaria) adeguati. A seconda del percorso compiuto da ogni
pigmento sul supporto, è possibile stabilire se una certa macchia corrisponde o meno a un
dato pigmento.
Per il procedimento VEDI SCHEDA TECNICA.
Fig.1 - Sminuzzare le foglie di spinaci e metterle nell’alcol e lasciare a riposo per alcuni
giorni.
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Fig. 2 - Preparare una soluzione di acetone ed etere di petrolio in rapporto di 1 a 9 (1 mL
acetone e 9 mL di etere).
Fig. 3 – Preparare striscioline di carta per cromatografia.
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Fig. 4 – Fare un segno con la matita a 2 cm da un’estremità.
Fig. 5 – Depositare una piccola goccia di liquido sul segno di matita.
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Fig. 6 – Versare nel cilindro un po’ della soluzione di etere e acetone fino ad un’altezza di
1,5 cm.
Fig. 7 – Immergere nel cilindro la strisciolina dalla parte della macchia.
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Fig. 8 – Aspettare che i solventi migrino lungo la strisciolina.
Fattore di ritenzione
Per le varie sostanze che si vanno via via separando è possibile calcolare il fattore di
ritenzione. Esso dipende:
- dal composto da separare;
- dalla fase stazionaria;
- dalla soluzione (eluente) usata;
- dalla temperatura.
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Rf= d (posizione della macchia)
d (fronte dell’eluente)
Abbiamo determinato tale fattore per i vari pigmenti trovati in quattro strisioline.
Striscioline di carta da cromatografia:
Pigmenti
Rf 1
Rf 2
Rf 3
Rf 4
carotene
0,99
0,98
0,98
0,99
xantofilla 0,52
0,51
0,57
0,54
chl-a
0,43
0,38
0,46
0,46
chl-b
0,35
0,28
0,35
0,38
Rf 3
Rf 4
Rf 5
Rf 6
Rf 7
Rf 5
Rf 6
Rf 7
Striscioline di gel di silice:
Pigmenti
Rf 1
Rf 2
carotene
chl-a
chl-b
xantofilla
Il fattore Rf per un dato composto è definito, e per questo è utilizzato per scopi
riconoscitivi.
Docenti referenti: Rita Mellere e Maria Marzi
Studenti: 1^ALS: Bedin Gialnuca, Bottarel Pierre, Buso Edoardo, Collavo Enrico, Donadel sara, Doumbia Damiano, Fornasier Sabrina, Frada Chiara,
Frezza Filippo, Gallina Patrik, Hassani Sophia, Michielon Sara, Miglioranza Mattia, Norbiato Nancy, Pozzobon Viviana, Safonchyk Karalina, Signor
Giulia, Tittoto Mirko, Vettoretti Valeria.
1^BLS: Berti Laura, Bovo Davide, Bronca Francesco, Campagnola Laura, Cecuta Roberto, Collanega Davide, Dal Din Alessandra, De Lazzari Elisabetta,
Geronazzo Marianna, Licini federico, Mognon Giacomo, Ortenzio Matteo, Pascotto Maria, Prosdocimo Alessandra, Rossetto Francesco, Sota Paola,
Stefani Irma, Ugwu Prince, Vettoretti Nicola
ISISS “G.Verdi” – Valdobbiadene
LABORATORIO “MISSIONE BRACCIO DI FERRO”
Classi 1^ALS e 1^BLS
Fig. 9 – Si osserva la formazione di alcune macchie di colore diverso.
Bibliografia
Smith I. “Cromatografia” Ed. Piccin-Nuova Libraria, 1976
Sitografia
http://madscientist.altervista.org/biologia/cromatografia/cromatog.htm