¾ fisiopatologia emopoiesi
¾ emocromo
¾ midollo osseo
¾ aspirato midollare
¾ biopsia ossea
1
Il sangue: 40% cellule; 60% acqua !
Valori normali di ematocrito:
maschio adulto
.42 - .54
femmina adulta .37 - .44
neonato(nascita)
neonato 3 mesi
.53 - .68
.30 - .38
bambino 10 anni .37 - .44
Hct varia con eta’ e sesso.
2
Composizione del sangue
Il sangue rappresenta il 5-7% del peso corporeo totale
a. Elementi cellulari
1. Globuli rossi (emazie), trasportano ossigeno e CO2,
non hanno nucleo
2. Globuli bianchi (leucociti), nucleate
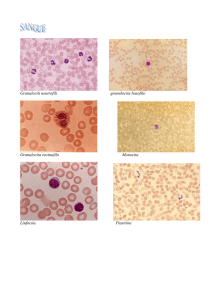
- Attività fagocitica, identificate tramite colorazione dei granuli
(granulociti - neutrofili, basofili ed eosinofili - ) o per le caratteristiche
del nucleo (cellule mononucleari – monociti nel sangue, macrofagi
nei tessuti
- Immunociti (linfociti B e T)
3. Piastrine, anucleate con emivita di circa 7 giorni
Vita media delle cellule del sangue
MIELOPOIESI 1.
Granulopoiesi e neutrofili: 10 h
monocItopoiesi
2. ErItropoiesi
emazie: 120 giorni
3. Trombocitopoiesi piastrine: 10 giorni
LINFOPOIESI 1. cellule B
2. cellule T
?
?
3
Composizione del sangue
b. Elementi plasmatici
Il plasma rappresenta la parte del sangue con la componente
cellulare sospesa, il siero è la parte senza elementi cellulari
1. Acqua >70%
2. Elettroliti (sodio Na+, potassio K+, Magnesio Mg, calcio, Ca++)
3. Proteine
- Coagulazione (pro ed anticoagulanti)
- Funzione immunologica (anticorpi)
- Funzione di trasporto (tarnsferrina, transcobalamina,
aptoglobina, lipoproteine)
Caratteristiche fisiche del sangue
CARATTERISTICHE FISICHE
Volume:
Totale = 66 + 7 ml/Kg
Eritrociti = 30 + 4 ml/Kg
Plasma = 36 + 4 ml/Kg
Viscosita’: 3.5 - 4.5 (relativa all’ H20)
pH: 7.35-7.45
Residuo secco: Sangue in toto = 19-23 g/dl
(di cui Hb = 90%, proteine 7%, sali/lipidi 3%)
4
Le proteine del sangue
PLASMA
Proteine Totali (g/dl): 6.5 - 8
Albumina (g/dl): 3.5-5 (= 55 - 70%)
Globuline (g/dl):
α1 = 0.15-0.25 (= 2 - 3.5%)
α2 = 0.4-0.7 (= 5 - 9%)
β = 0.5-1 (= 6 - 13%)
γ = 0.6-1.3 (= 8 - 18%)
Immunoglobuline (mg/dl):
IgA: 90-400
IgD: 0-30
IgE: 0-0.1
IgG: 650-1,700
IgM: 50-375
Fibrinogeno (mg/ml): 250-400
paziente ematologico: segni clinici
Anamnesi
- Emorragia
- Infezioni frequenti e linfoadenopatia
- sintomi aspecifici legati all’anemia
Esame fisico
- Cute ed unghie, mucose, ecchimosi, ittero,
pallore, cianosi
- Epato e splenomegalia, linfoadenopatia,
disturbi neurologici
5
Linfoadenopatia inguinale
Petecchie
6
L’emocromo
LEUCEMIA MIELOIDE ACUTA
7
PARAMETRI BIOMETRICI ERITROCITARI
GLOBULI ROSSI (RBC)
Ematocrito (Ht):
Emoglobina (Hgb)
Eritrociti (numero):
M. = 40-52%
F. = 36-48%
:media = 14.5 g/dl
M. = 13.2-17 g/dl
F. = 12- 15.5 g/dl
M. 4.5 - 6 (x 106/μL)
F. 4.2 - 5.2 (x 106/μL)
VOLUME CORPUSCOLARE MEDIO
(MCV) = Ht (%) : 90 fl (range 80 – 95)
RBC
EMOGLOBINA CORPUSCOLARE MEDIA
(MCH) = Hb (gr): 30 pg (range 27 - 33)
RBC
CONCENTRAZIONE EMOGLOBINICA CORPUSCOLARE MEDIA
(MCHC) = Ht (%) : 33 % (range 31 – 35)
Hgb(gr)
RETICOLOCITI: valore assoluto 25-80.000/μL (3-5/1000)
EMATOCRITO (HT)
• misura la percentuale dei globuli rossi rispetto alla frazione liquida del
sangue
• Valori normali 42 - 54% per l’uomo, 37 - 44% per la donna
•
•
•
•
•
Valori superiori:
Poliglobulia secondaria (fumo, BPCO, cardiopatie cianogene…)
Policitemia Vera
Uso di diuretici
Ustioni, vomito, disidratazione
Aumento eritropoietina
Valori inferiori:
• Anemie carenziali, emoglobinopatie, aplasie midollari, leucemie
• Emorragie
• Insufficienza renale cronica (carenza EPO, emolisi, emorragie, inibizione
midollare da sostanze tossiche)
• Infezioni croniche, neoplasie
8
Volume corpuscolare medio
9 E' il volume corpuscolare medio dei GR
9 Valori normali: 82-92 fl
Valori superiori a quelli normali da:
9 carenza vit.B12
9 carenza di folati
9 alcolismo
9 parassiti
Valori inferiori da:
9 emoglobinopatie (talassemia..)
9 carenza di ferro
9 sferocitosi
RDW: red cell distribution width (anisocitosi): 12,8 ± 1,2% (CV)
42,5 ± 3,5 fl (SD)
deficit di ferro RDW aumentato
tratta talassemico RDW normale
anemia megalobastica RDW aumentato
anemie macrocitiche RDW normale
9
Conta del sangue periferico
Globuli bianchi
La formula leucocitaria esprime il rapporto tra i vari
elementi della serie bianca (neutrofili segmentati, neutrofili a
banda, metamielociti, promileociti, blasti, basofili, eosinofili,
linfociti e monociti)
Piastrine
Le piastrine sono anucleate ed appaiono nel sangue
periferico come corpi blu con granuli rossi.
Volume Corpuscolare Medio (MPV). Piuttosto aspecifico,
serve correlato alla conta piastrinica per identificare la
presenza di piastrine giovani (grandi)
Esame del sangue periferico (vetrino)
Fornisce
informazioni
critiche
circa
la
morfologia degli elementi cellulari e delle
piastrine del sangue. Di routine, viene
usato un preparato fissato e colorato
(Giemsa)
10
Morfologia cellulare
1. Morfologia delle emazie (colorazione, corpi inclusi, contenuto
emoglobinico)
2. Morfologia dei globuli bianchi. Presenza di cellule immature
con shift verso sinistra (incremento dei neutrofili a banda),
iper- o iposegmentazione, inclusioni leucocitarie, linfociti
atipici, batteri
3. Morfologia delle piastrine. Presenza di piastrine giganti,
riduzione del numero piastrinico
Valutazione dei globuli rossi
¾ prelievo di sangue (emocromo e striscio periferico) per
poter evidenziare:
¾ una diminuzione di Hb e dei GR (anemia)
¾ Variazioni del colore dei GR (ipocromia)
¾ Dimensioni (microcitosi/macrocitosi)
¾ Grandezze differenti (anisocitosi)
¾ Forme bizzarre (poichilocitosi)
¾ Inclusioni eritrocitarie (corpi di HowelJolly…)
¾ L’entità delle malformazioni morfologiche è
proporzionale alla gravità dell’anemia
11
Forma delle emazie
Descrizione
Patologie associate
Acantociti
Poche spicole larghe
Cirrosi, uremia, HUS
Dacriociti
Forma a goccia
Talassemia, Mielofibrosi,
anemia emolitica
Drepanociti
Forma a falce
Drepanocitosi o altre
emoglobinopatie
Schistociti
Forma ad elmetto
DIC, TTP, protesi valvolari
Sferociti
Forma a sfera
Emolisi (ereditaria e non)
Stomatociti
Forma a “bocca” del pallore
centrale
Emolisi acquisita o
ereditaria
Forma anomala
Anomala distribuzione
Formazione di rouleau
“monete impilate”
MM, Waldenstrom
Inclusione di corpuscoli
Emazie nucleate
Nucleo picnotico
Sanguinamento acuto,
emolisi severa
Corpi di Howell-Jolly
Piccole formazioni
rotondeggianti
Anemia megaloblastica,
asplenia,emolisi
Corpi ad anello di Cabot
Anelli o figure a “8”
Emolisi severa
Inclusioni eritrocitarie
•
•
•
•
•
Corpi di Howell Jolly: frammenti nucleari, originanti da
frammentazione o incompleta espulsione del nucleo,
rimossi a livello splenico. Si osservano dopo splenectomia
Anelli di Cabot: residuo del fuso mitotico, visibili in
condizioni di diseritropoiesi
Punteggiatura basofila: aggregazione patologica di
ribosomi. Frequente nella intossicazione da piombo.
Residui di RNA nei reticolociti.
Corpi di Heinz: emoglobina denaturata che precipita in
caso di insulti chimici, di emolisi da carenza di G6PDH, o
per difetti di struttura globinica
Siderosomi: Granuli intracitoplasmatici di ferritina ed
emosiderina
12
Colorazione dei reticolociti:
Le cellule immature (reticolociti) sono identificate con colorazione
sopravitale di residui precipitati di RNA (blu di metilene).
le cellule che contengono il precipitato colorato sono contate
e riportate in percentuale (3-5/1000)
Colorazione dei Corpi di Heinz:
I corpi di Heinz (Heinz Body) sono precipitati di emoglobina
denaturata e vengono colorati con colorante sopravitale al
cristallo violetto.
Il test serve a identificare le emoglobinopatie instabili (HgH,
Talassemia, deficit di G6PD)
Fornula
leucocitaria
13
I globuli bianchi nel sangue periferico
formula leucocitaria
neutrofili 40 - 80 %
linfociti 20 - 40 %
monociti 2 - 10 %
eosinofili 1- 6 %
basofili <1- 2%
numeri assoluti
neutrofili
linfociti
monociti
eosinofili
basofili
2-7 x 109/L
1-3 x 109/L
0.2-1 x 109/L
0.02-0-5 x 109/L
0.02-0.1 x 109/L
monocita
neutrofilo
linfociti
eosinofilo
basofilo
LGL
piastrine
valori nel sangue: 150 - 450 x 109 /L.
circa 2/3 circolano, mentre 1/3 risiede nella milza o sedi extravascolari;
14
MPV: mean platelet volume;
aumentato piastrinopenia da distruzione periferica,
ridotto piastrinopenia iporigenerativa
PDW: platelet distribution width;
aumentato trombocitemia essenziale
normale trombocitosi reattiva
Le cellule del sangue sono prodotte nel midollo osseo
e negli organi linfatici secondari (milza e linfonodi)
Il midollo osseo nell’adulto occupa uno spazio di circa 4 litri;
la meta’ è composto da midollo emopoietico, il resto da
tessuto adiposo
Nei bambini il midollo occupa uno spazio di circa 1,6 litri,
ma è attivo al 100%
15
Periferico a bassa risoluzione
Periferico ad alta risoluzione
Piastrine
Emazie
16
Piastrine (normali)
Cluster di piastrine normali
17
Basofili
Linfocita (1), monocita (2), neutrofilo (3)
2
1
3
18
Monocita
Piastrine con molti aggregati
19
Linfocita reattivo
1
2
4
3
Monocita (1), linfocita (2), neutrofilo (3)
3
1
2
20
Talassemia-ß minor
Eritrofagocitosi
21
Cluster di piastrine patologiche
(trombositosi)
Indagini di laboratorio in ematologia
A)
VALUTAZIONE "DIRETTA"
dei parametri ematologici (composizione quantitativa e/o
qualitativa delle cellule del sangue e del midollo osseo)
Conteggi,
morfologia, funzione
1) generici
2) specifici
B)
VALUTAZIONE "INDIRETTA"
Effettuata su plasma/siero: dosaggio di
componenti del sangue quali vitamine,
proteine, minerali, metaboliti, etc...
22
Contatore di cellule
S IS T E M A DI CONT E G G IO
DE L L E PART ICE L L E DE L
S ANG UE
elettro d i
FL USS O
FL USS O
SIS TE M A D I
M IS UR A Z IO NE
DEL F L USS O
S C A R IC O
AP E RT URA
Sangue Periferico e Midollo
A) COLORAZIONI CITOCHIMICHE (PIU' O MENO SPECIFICHE):
Perl's = Ferro
LAP = Fosfatasi Alcalina Leucocitaria
- Linea differenziativa
PAS = Glicogeno
- Stadio maturativo
SUDAN Nero. = Lipidi
Perossidasi = Enzimi ossido-riduttivi
Esterasi = Enzimi esterasici aspecifici
B) CARATTERIZZAZIONE IMMUNOLOGICA:
- Linea differenziativa
- Stadio maturativo
- Monoclonalità
C) ESAME CITOGENETICO:
Valutazione di eventuali alterazioni cromosomiche
acquisite (utile a scopo diagnostico, prognostico e
terapeutico)
D) ANALISI MOLECOLARE:
Studio dei riarrangiamenti genetici noti (utile a
scopo diagnostico, prognostico e terapeutico)
E) ESAME ISTOLOGICO M.O. (+/- immunoistochimica)
23
Dove effettuare l’aspirato midollare
L’ago dell’aspirato
24
L’aspirato midollare
Dove effettuare la biopsia ossea
POSTERIOR SUPERIOR
ILIAC SPINE
25
Ago per biopsia (Jamshidi needle)
Il frustolo bioptico
26
Disturbi della milza: asplenia
La diagnosi di asplenia può sospettata in caso di:
1. Emazie nucleate o inclusioni eritrocitarie (corpi di
Howell-Jolly o Pappenheim)
2. Cellule bersaglio o acantociti in numero elevato
3. Aumento dei reticolociti
4. Aumento delle piastrine e dei granulociti
Cause di asplenia
Milza atrofica:
-
Rettocolite ulcerosa
Morbo celiaco
Tireotossicosi (malattia di Graves)
Sindrome di Sezary
GVHD
27
Disturbi delal milza: splenomegalia
Infezioni:
- Acute, subacute e croniche (mononucleosi,
endocardite, leishmaniosi, ecchinococcosi etc)
Malattie infiammatorie croniche:
- LES, sarcoidosi, AR
Neoplasie:
- LMC, LH, LNH, HCL, PV, mielofibrosi, LLC, metastasi
Malattie emolitiche:
- Talassemia, sferocitosi, AE immune
Malattie da deficit:
- Severa carenza marziale, anemia perniciosa
Ipertensione portale:
- Cirrosi, TV porta e VV splancniche
Valutazione del midollo osseo
Indicazioni all’aspirato midollare:
-
Riduzione di una singola linea cellulare
Riduzione di due linee cellulari
Pancitopenia
Leucemie acute
Valutazione delle riserve marziali (anemia
sideroblastica o anemie croniche)
- Diagnosi di infiltrazione midollare da neoplasia solida
- Infezioni intramidollari
- Disordini immunologici
- Diagnosi di malattie non ematologiche (Leishmaniosi,
tubercolosi, amiloidosi, sd di Gaucher, Kala-azar etc)
28
Valutazione del midollo osseo
Vantaggi rispetto all’aspirato: valutazione dell’osso
midollare con struttura conservata. E’ molto utile
perché mantiene il microambiente midollare; serve
per valutare la morfologia cellulare e/o infiltrati midollari.
Indicazioni alla biopsia ossea:
-
Incapacità di ottenere un buon aspirato
Valutazione di bi- o pancitopenia
Presenza di leucoeritroblasti nel periferico (mielofibrosi)
Mieloma multiplo
Staging tumorale
Grado di aplasia nella terapia delle leucemie
Definizione
L’ematopiesi è la (1) proliferazione delle cellule
progenitrici, che sono mantenute dalle cellule
staminali, e (2) la loro differenzazione nelle
componenti cellulari del sangue
29
L’emopoiesi
CFU -GM
NEUTROFILI
MONOCITI
LINFOCITO T
CFU -Eo
EOSINOFILI
CFU -Gemm
CELLULA
STAMINALE
LINFOIDE
CFU -Meg
PIASTRINE
CELLULA
STAMINALE
TOTIPOTENTE
CFU -Baso
LINFOCITO B
BASOFILI
BFU -E
CFU -E
ERITROCITI
30
Siti dell’ematopoiesi
Feto
0-2 mesi:
0-8 mesi:
5-9 mesi:
sacco vitellino
FEGATO, MILZA
MIDOLLO OSSEO (tutto)
Bambini
MIDOLLO OSSEO
(Tutte le ossa; poi progressiva
sostituzione con midollo giallo)
Adulti
MIDOLLO OSSEO
(Vertebre, costole, sterno, sacro
e pelvi, estremità prossimali dei
femori e degli omeri)
Timing dell’ematopoiesi
PRENATALE
POSTNATALE
CELLULARITA'
(%)
100
MIDOLLO OSSEO
SACCO VITELLINO
VERTEBRE
FEGATO
80
STERNO
60
40
MILZA
COSTOLE
TIBIA
20
0
FEMORE
1
2
3
4
5
6
7
8
9
10
NASCITA
20
30
40
ETA'
50
60
70
31
Ematopoiesi patologica
In presenza di patologie, i siti extramidollari possono
servire come siti primari per lo sviluppo delle cellule
ematiche
a. Siti ematopoietici fetali (milza e fegato) possono
diventare siti primari nell’adulto in alcune malattie
(mieloproliferative)
b. Siti midollari adulti, che sono normalmente non
ematopoietici, possono trasformarsi in siti ematopoietici
per aumentare la produzione di cellule de sangue
Vita media delle cellule ematiche
Processo di rinnovamento costante delle cellule
ematiche
vita media cellule mature
MIELOPOIESI
LINFOPOIESI
1) granulo-(mono)-poiesi:
2) eritropoiesi:
3) piastrinopoiesi:
10 ore
120 gg.
10 gg.
1) cellule B
2) cellule T
?
?
32
L’entità del fenomeno emopoiesi
• In condizioni normali, ogni ora sono prodotti:
1010 globuli rossi,
109 globuli bianchi
24/24 ore per tutta la vita.
• In condizioni di stress (perdita acuta di sangue,
infezione) i fabbisogni aumentano di 10 volte e oltre
• Inoltre le cellule prodotte dal midollo sono in grado di
funzionare in tutti i distretti dell’organismo in modo
autonomo
Struttura del midollo emopoietico
STROMA E PARENCHIMA
Cavità compartimentalizzate da trabecole ossee,
contenenti cellule adipose e parenchima (eritroblasti,
granuloblasti, megacariociti, cellule stromali), con un
complesso sistema vascolare (arteriole midollari e
corticali, rete sinusale, seno centrale)
Tale sistema vascolare è permeabile alle cellule ematiche
mature per la presenza di pori di migrazione beanti sulla
parete sinusale (passaggio per processo "attivo").
33
Istologia del midollo osseo
Osetoblasti e osteoclasti
34
Vasi midollari
Il microambiente emopoietico
• Il microambiente è composto da una multitudine di
cellule, mesenchimali ed emopoietiche che forniscono:
- Superfici
- Matrice extracellulare
- Fattori solubili che in concerto sono responsabili
della regolazione e proliferazione, quiescenza,
differenzazione, reclutamento ed accumulo dei
progenitori emopoietici e delle cellule staminali
35
La normale funzione del midollo
dipende da:
1.
Normalità del microambiente midollare specifico
2.
Normale funzione delle "cellule staminali"
3.
Vit. B 12, acido folico, ferro+ormoni, proteine+lipidi
+zuccheri
Fasi dell’emopoiesi
Cellula
Staminale
Totipotente
Automantenimento
Orientamento
"multip."
Mieloide
Linfoide
DIFFERENZIAZIONE
Eritroblasti
Granuloblasti
Megacariociri
B
T
Monoblast
i.
MATURAZIONE
linfociti
eritrociti
granulociti
piastrine
B maturi
T maturi
monociti
36
Il midollo delle CS pluripotenti
CS
CS
endodermiche CNS
Fegato
Pancreas
Cervello
Linee somatiche
CS
CS
Emopoietiche Cresta neurale
Midollo
Nervi periferici
Cellule neuro-endocrine
Cell. Schwann
Cellule pigmentarie
Cell. Musc. Liscie
ri
oAut ento
va m
nno
Cellule
Germinali
primitive
Creste
genitali
Protogameti
Vasi e CS CD 34+
37
La gerarchia delle cellule emopoietiche
• Il compartimento delle cellule staminali è costituito da rare
cellule multipotenti (che sono in gradi di trasformarsi in tutte
le cellule del sangue) e che possono automantenersi
(generare cellule identiche). [Capacità mitotiche limitate]
• Il processo denominato orientamento comporta la
transizione verso cellule denominate progenitori emopoietici
che hanno la capacità di differenziarsi verso una linea
emopoietica. [Capacità mitotica elevata].
• Le cellule riconoscibili nel midollo sono i precursori ; essi
hanno scarsa capacità di automantenersi ma elevatissima
capacità mitotica
Le CS: automantenimento
• Se la capacità di automantenimento del clone di CS
è illimitata e le CS sono immortali, esse possono
funzionare per tutta la vita
• Se così fosse la emopoiesi sarebbe un fenomeno
stabile nella vita
• Vi sono evidenze, invece, che indicano che solo una
parte delle cellule staminali è attiva in un certo
periodo e che per assicurare una emopoiesi
continua è necessaria la produzione di nuove SC
38
L’evoluzione delle CS ematopoietiche
LongTerm
HS
Automantenute
per tutta la vita
FlK-2Thy1.1low
CD34-
ShortTerm
HS
Automantenute
per 6-8 sett.
FlK-2+
Thy1.1low
CD34+
Progenitore
Linfoide
comune
T-cell
NK
B-cell
c-kitlow
Sca-1low
CD34+
IL-7R+
GMP
IL-7R-
Progenitore
Mieloide
comune
MEP
c-kit+
Sca-1CD34+
CS Pluripotente
(CFU-blast)
Unità formanti
Aggl. eritroidi
(BFU-E)
CS mieloide
(CFU-GEMM)
Prog. Eritr.
(CFU-E)
Megac.
(CFU-Meg)
Mono/gran.
(CFU-GM)
Prog. Eos.
(CFU-Eo)
Eritrociti
Piastrine
Monociti
Neutrofili
Basofili
Basofili
CS Linfoide
Linfonodi
Timo
Cellule B
Cellule T
39
I progenitori ematopoietici: proprietà
• AUTOMANTENIMENTO: capacità di generare cellule non
orientate che mantengono le stesse caratteristiche di
staminalità e che assicurano il rinnovamento costante
dell’ emopoiesi
• RICOSTITUZIONE: capacità di rigenerare il pool cellulare
di alcuni tessuti (nervoso, muscolare, epatico, vascolare
etc.) oltre a quello immune ed emopoietico
• ORIENTAMENTO E MATURAZIONE: capacità di generare
cellule di varie filiere differenziative
Le cellule staminali emopoietiche
Cellule capaci di ricostituire l’emopiesi linfoide e
mieloide quando trapiantate.
Caratteristiche fenotipiche:
1. assenza degli antigeni presenti nei progenitori
commissionati (lin-) e dell’ HLA-DR
2. positività dell’antigene CD34 (anche se vi sono
SC CD34-)
40
Le cellule staminali: orientamento
Il pool delle CS si automantiene e cloni di CS vanno
incontro a differenziazione. Vi sono due modelli teorici
per spiegare il comportamento delle CS:
1.
il modello stocastico (l’indirizzo verso
l’automantenimento o la differenziazione è basato
sulla probabilità)
2. la teoria della “induzione emopoietica indotta dal
microabiente”
Le cellule mesenchimali
• Fibroblasti, mio-fibroblasti, adipociti,
osteoblasti, cellule endoteliali e macrofagi
Citochine solubili
Osteoblasti
Cellula staminale
Macrofago
Fibroblasti
Citochine di membrana
Cellula endoteliale
Trabecola ossea
TNF, CSF, TGFβ, ILs
41
Spleen colony-forming unit (CFU-S) assay.
Macroscopic splenic hematopoietic colonies
arising from the CFU-S stem/progenitor cell
14 days after injection of murine bone
marrow into lethally irradiated mice
Reticolo normale: argirofilo
42
Proteine adesive (ligandi) e loro
recettori
• Ligandi
proteine della superficie cellulare con la funzione di
trattenere le cellule nel midollo:
- VCAM-1 ligando la cui espressione è ridotta da:
chemioterapia, G-CSF (Granulocyte Colony-Stimulating
Factor)
- ICAM-1
• Recettori adesivi
- Integrine
- Selettine
- CD34, CD43, CD45RA, CD164: importanti per il
processo di homing e di ritenzione delle CS al midollo
I fattori di crescita emopoietici (I)
L’ematopoiesi è regolata a diversi livelli:
-
le cellule emopoietiche hanno capacità
maturativa intrinseca
-
la matrice extracellulare svolge un ruolo importante
-
Gli ormoni di natura glicoproteica denominati
Fattori di Crescita Emopoietica (HGF,
Hematopoietic Growth Factor) regolano l’emopoiesi
43
Monocita
CS pluripotente
Endotossina
Azione dei fattori
di crescita
IL-3
T cell
CFUGEMM
Early
BFU
GM-CSF
EPO
Ipossia
Fibroblasto
IL-1
Late
BFU
Rene
Cellula endoteliale
EPO
EPO
EPO
CFU-Eo
CFU-G
CFU-M
Eosinofili Neutrofili
Monociti
EPO
CFUMeg
Piastrine
CFU-E
Eritrociti
I fattori di crescita emopoietici (II)
1. Controllano la differenzazione e moltiplicazione
giornaliera delle CS in cellule mature
2. Agiscono sulle cellule mature (leucociti) in risposta
alle infezioni
3. Vengono chiamati CSF (Colony-stimulating factors)
perché essi necessari allo sviluppo delle colonie
progenitrici dalle cellule multipotenti
4. Sono prodotti da: linfociti, monociti, macrofagi,
cellule endoteliali e fibroblasti
44
I fattori di crescita emopoietici:
classificazione
FC “non linea-specifici”
FC “linea-specifici”
Agiscono sulle cellue multi o totipotenti per l’automantenimento e
diffrenzazione
Agiscono sulle cellule “committed”
per la loro differenzazione e
differenzazione (stadi più avanzati)
Multi-CSF o IL-3
Per la formazione e differenzazione
di colonie di granulociti, macrofagi,
eosinofili, mast-cell, cellule eritroidi,
megacariociti
G (granulocyte)-CSF
M (monocyte)-CSF
Eo (Eosinophil)-CSF
GM-CSF
Formazione delle colonie
di granulociti e monociti
Linfociti e monochine, rispondono
all’infezione e risposta immune
(IL-1)
CSF, HGF e IL
• Il termine Colony Stimulating Factor (CSF) è un termine
generico utilizzato per significare sostanze ormonali
capaci di stimolare la crescita di colonie ematopoietiche in
vitro.
• Il termine Hematopoietic Growth Factor (HGF) indica
specifici ormoni capaci di agire in vivo a diversi livelli.
• Il termine Interleukina (IL), originariamente indicava
molecole che erano necessarie per le interazioni fra
cellule immuni. Oggi con questo termine si indica una
classe di molecole attive nella cascata emopoietica, multio mono-lineari appartenenti alla famiglia degli HGF
(citochine).
45
G-CSF come esempio della struttura di
una citochina
96
I numeri
indicano gli
amino-acidi
B
E 43
C
113
D
34
A
175
75
18
1-10
Sintesi ed effetti
• Molte citochine sono prodotte dalle cellule stromali del
midollo e agiscono a livello midollare e spesso agiscono in
siti ben precisi e specifici.
•
-
I fattori di crescita agiscono:
inducendo la proliferazione dei progenitori emopoietici
attivando le cellule mature
stimolando le funzioni delle cellule mature
stimolando la produzione di altri HGF
46
Espressione
• Non vi sono dati sperimentali certi sulla produzione degli HGF
in vivo. Unica eccezione è la trombopoietina (TPO) che è
prodotta costitutivamente ed i livelli regolati dal consumo.
• La trascrizione dei geni del GM-CSF (Granulocyte/Macrophage
CSF), G-CSF ed M-CSF (Macrophage CSF) è presente nella
grande maggioranza delle cellule analizzate, anche in assenza
di stimoli, ma i trascritti sono degradati rapidamente nel
traffico intra-citoplasmatico.
• In vitro, i fibroblasti e le cellule endoteliali producono
spontaneamente M-CSF.
• Gli effetti biologici delle citochine sono mediati dal legame a
rari (sulla superficie cellulare) ma specifici recettori ad alta
affinità.
Esempi di recettori di citochine
LIF receptor
gp130
C
LIF receptor
gp130
gp130
C
C
Azioni:
-Aumentata
sintesi proteine
fase acuta
-Induz. diff.
emopoietica
-Inibizione della
Lipoproteinlipasi
C
IL-6
LIF
= citochina
IL-11
47
Legame recettoriale (I)
• I recettori per le citochine consistono in un porzione
extracellulare deputata al legame ed in una porzione
intracellulare che serve ad attivare chinasi
citoplasmatiche che inducono la differenziazione e la
proliferazione.
• Le alterazioni dei domini intracitoplasmatici alterano
l’omeostasi cellulare favorendo la proliferazione senza
maturazione: il risultato può essere in una neutropenia
grave o in una LAM
Legame recettoriale (II)
• Il G-CSF esercita la propria azione tramite un recettore di
membrana che appartiene alla “superfamiglia “ dei
Recettori di citochine di Classe I ovv. Recettori
ematopoietinici.
• Dal punto di vista strutturale tali recettori sono
caratterizzati da residui cisteinici altamente conservati e da
una sequenza
triptofano-serina - x – triptofano-serina
circa 200 a.a. all’esterno della membrana cellulare
(Cytokine-Receptor-Homology, CRH) che è essenziale per il
ligando.
• Vi sono meccanismi comuni ma anche meccanismi specifici
per trasmettere i segnali caratteristici di ogni citochina
48
Produzione endogena di citochine (I)
• La EPO fornisce l’esempio più chiaro per quanto
riguarda la produzione endogena di citochine, in
quanto si conosce il sito esclusivo di produzione
(apparato iuxtaglomerulare)
• La TPO fornisce un altro esempio riguardante il
rapporto fra livelli sierici e produzione di piastrine
(unico agonista del suo recettore (c-MPL) ed è la
citochina regolatrice della produzione piastrinica.
Produzione endogena di citochine (II)
• Nel caso della mielopoiesi la situazione non è chiara:
il GM-CSF difficilmente si trova in circolo; si ritiene
che agisca a livello locale.
• Al contrario i livelli sierici di G-CSF aumentano in
svariate situazioni (infezioni, esposizione ad
endotossina): i livelli più elevati si riscontrano nelle
gravi neutropenie febbrili.
• Nei pazienti con neutropenia ciclica i livelli di G-CSF
fluttuano in modo concorde ed inverso alla conta dei
neutrofili.
49
Produzione endogena di citochine (III)
• L’ipotesi più accreditata per spiegare il
comportamento differente tra GM-CSF (az.
locale) e del G-CSF (az. sistemica) consiste nel
fatto che il G-CSF circola nel sangue e stimola la
neutropoiesi, mentre il GM-CSF agisce attivando
le cellule a livello locale
• Il controllo dei livelli è sulla base del
consumo/rimozione della citochina in seguito al
legame recettoriale
Ruolo fisiologico delle citochine (I)
• Gli studi sugli animali “knock-out” hanno contribuito
notevolmente a comprendere questo aspetto:
- Il topo carente in IL-7 ha una immuno-deficienza
molto più grave di quello carente in IL-2 o IL-4
- Il topo carente in GM-CSF ha una emopoiesi
relativamente normale, mentre quello carente in
G-CSG è gravemente neutropenico, con alterata
funzione dei neutrofili. Ciò significherebbe che il G-CSF
è la citochina di primaria importanza per la regolazione
dei livelli dei neutrofili in condizioni di emergenza
(infezioni, neutropenie)
50
Ruolo fisiologico delle citochine (II)
• Nel topo knock-out omozigote per la TPO (TPO-/-)
il numero delle piastrine e megacariociti è <20%
della norma (normale crescita, normale
riproduzione, normale emostasi), mentre nel topo
eterozigore (TPO-/+) i livelli delle piastrine sono
del 60% della norma.
• Poiché in assenza di TPO i megacariociti sono
presenti, si ritiene che il ruolo della TPO sia quello
di amplificare il sistema di produzione delle
piastrine.
Fattori di crescita e differenzazione
emopoietica
(Azione primaria sulla proliferazione e differenziazione e su
attività funzionali delle cellule emopoietici)
CLASSE
FATTORE
AZIONE
MULTILINEARE
IL3
(Interleuchina 3)
GM-CSF
(Granulocyte –
Monocyte Colony
Stimulating Factor)
51
Meccanismo autocrino di
trasformazione cancerogena
Fattori di crescita
mRNA
Proteina oncogena
3
4
Recettore attivato
dei Fattori di crescita
2
mRNA
1
Protoncogene
Il proto-oncogene (1) stimola (2)
proteine oncogene e la proliferazione
diretta (3) o mediata (4) di fattori di
crescita
MATURAZIONE
AMPLIFICAZIONE
ERITROBLASTI ERITROBLASTI
ERITROBLASTI
RETICOLITICI
ERITROBLASTI
ORTOCROMATOFILI
BASOFILI
POLICROMATPFOLI
ORTOCROMATPFOLI
ERITROBLASTI
ERITROCITI
72 h
ERITROBLASTI
40 h
POLICROMATOFILI
BASOFILI
BFU-E
CFU-Gemm
CELLULA
STAMINALE
TOTIPOTENTE
CFU-E
PROERITROBLASTI
ERITROPOIESI ACCELERATA
BFU
ERITROPOIESI
INEFFICIENTE
52
Lacuna vascolare paratrabecolare
Eritrone
53
Eritrone
G R A N U L O C IT O P O IE S I E M O N O C IT O P O IE S I
B F U -E
C F U -M K
C F U -S
C F U -G M
C F U -M
C F U -G
M IE L O B L A S T O
M ONOBLASTO
P R O M IE L O C IT O
M IE L O C IT O
P R O M O N O C IT O
M E T A M I E L O C IT O
M O N O C IT O
G R A N U L O C IT O
54
Megacariociti
Trombocitopoiesi
55
Organizzazione del sistema
immunocompetente
H
"helper" (T4)
T4
LINEA T
IMMUNITA'
CELLULARE
S
"suppressor" (T8)
T8
CELLULA
ANTICORPI
STAMINALE
LINFOCITOPOIESI
+
LINEA B
PLASMACELLULA
IMMUNITA'
UMORALE
FATTORI DI CRESCITA E
DIFFERENZIAZIONE EMOPOIETICA
(Azione su linfo-poiesi e altri sistemi
cellulari con effetto "mediato " tramite
cellule "accessorie“)
CLASSE
AZIONE MISTA
E INDIRETTA
FATTORE
IL 1
IL 2
IL 3
IL 4
IL 5 (Eosinofili)
56
AZIONE MONOLINEARE O RISTRETTA
G-CSF (Granulocyte Colony)
M-CSF (Monocyte Colony Stimulating Factor)
EPO
(Eritropoietina)
TPO
(Trombopoietina)
Azione dei vari FC sulle cellule emopoietiche
Pool
cellule staminali
LIF
IL-11
IL-12
IL-6
IL-1
SCF
G-CSF
Pool
proliferativo
IL-11
IL-9
IL-6
IL-3
SCF
GM-CSF
G-CSF
57
Azione dei fattori di crescita sulle popolazioni
midollari in rapporto alla maturazione
Pool maturativo
EPO
G-CSF
GM-CSF
M-CSF
Cellule mature
G-CSF
GM-CSF
IL-8
IL-5
58
59
CLASSE
FATTORE
AZIONE MISTA TNF
(Tumor Necrosis Factor)
E INDIRETTA
PDGF (Plateled Der. Growth
Factor)
EGF
(Epidermal
Growth Factor)
IFN α, β, δ
(Interferoni)
60