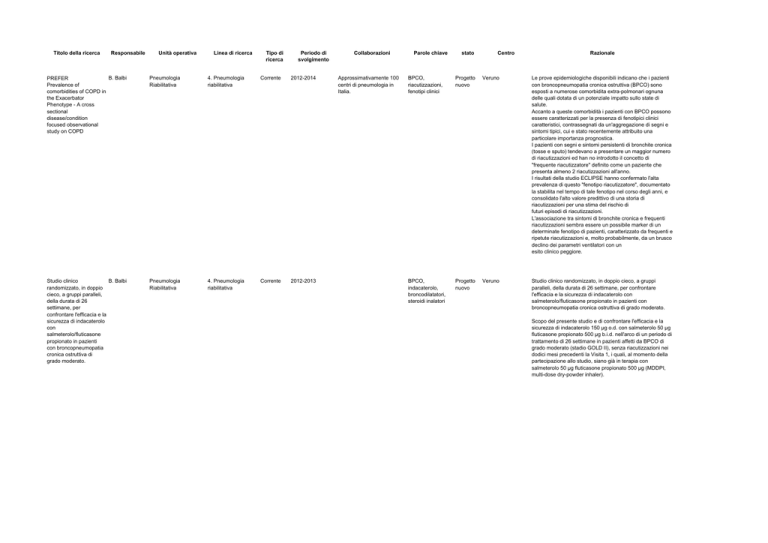
Titolo della ricerca
Responsabile
Unità operativa
Linea di ricerca
Tipo di
ricerca
Periodo di
svolgimento
B. Balbi
PREFER
Prevalence of
comorbidities of COPD in
the Exacerbator
Phenotype - A cross
sectional
disease/condition
focused observational
study on COPD
Pneumologia
Riabilitativa
4. Pneumologia
riabilitativa
Corrente
2012-2014
B. Balbi
Studio clinico
randomizzato, in doppio
cieco, a gruppi paralleli,
della durata di 26
settimane, per
confrontare l'efficacia e la
sicurezza di indacaterolo
con
salmeterolo/fluticasone
propionato in pazienti
con broncopneumopatia
cronica ostruttiva di
grado moderato.
Pneumologia
Riabilitativa
4. Pneumologia
riabilitativa
Corrente
2012-2013
Collaborazioni
Approssimativamente 100
centri di pneumologia in
Italia.
Parole chiave
stato
Centro
Razionale
BPCO,
riacutizzazioni,
fenotipi clinici
Progetto
nuovo
Veruno
Le prove epidemiologiche disponibili indicano che i pazienti
con broncopneumopatia cronica ostruttiva (BPCO) sono
esposti a numerose comorbidita extra-polmonari ognuna
delle quali dotata di un potenziale impatto sullo state di
salute.
Accanto a queste comorbidità i pazienti con BPCO possono
essere caratterizzati per la presenza di fenotipici clinici
caratteristici, contrassegnati da un'aggregazione di segni e
sintomi tipici, cui e stato recentemente attribuito una
particolare importanza prognostica.
I pazienti con segni e sintomi persistenti di bronchite cronica
(tosse e sputo) tendevano a presentare un maggior numero
di riacutizzazioni ed han no introdotto il concetto di
"frequente riacutizzatore" definito come un paziente che
presenta almeno 2 riacutizzazioni all'anno.
I risultati della studio ECLIPSE hanno confermato l'alta
prevalenza di questo "fenotipo riacutizzatore", documentato
la stabilita nel tempo di tale fenotipo nel corso degli anni, e
consolidato l'alto valore predittivo di una storia di
riacutizzazioni per una stima del rischio di
futuri episodi di riacutizzazioni.
L'associazione tra sintomi di bronchite cronica e frequenti
riacutizzazioni sembra essere un possibile marker di un
determinate fenotipo di pazienti, caratterizzato da frequenti e
ripetute riacutizzazioni e, molto probabilmente, da un brusco
declino dei parametri ventilatori con un
esito clinico peggiore.
BPCO,
indacaterolo,
broncodilatatori,
steroidi inalatori
Progetto
nuovo
Veruno
Studio clinico randomizzato, in doppio cieco, a gruppi
paralleli, della durata di 26 settimane, per confrontare
l'efficacia e la sicurezza di indacaterolo con
salmeterolo/fluticasone propionato in pazienti con
broncopneumopatia cronica ostruttiva di grado moderato.
Scopo del presente studio e di confrontare l'efficacia e la
sicurezza di indacaterolo 150 µg o.d. con salmeterolo 50 µg
fluticasone propionato 500 µg b.i.d. nell'arco di un periodo di
trattamento di 26 settimane in pazienti affetti da BPCO di
grado moderato (stadio GOLD II), senza riacutizzazioni nei
dodici mesi precedenti la Visita 1, i quali, al momento della
partecipazione allo studio, siano già in terapia con
salmeterolo 50 µg fluticasone propionato 500 µg (MDDPI,
multi-dose dry-powder inhaler).
Obiettivi
Lo Studio PREFER ha i seguenti obiettivi:
Stabilire la prevalenza di comorbidità in 3.000
pazienti italiani "frequenti riacutizzatori" (definiti
come pazienti con sintomi di bronchite cronica,
FEV-1 < 50% del valore teorico, 2: 2 riacutizzazioni
moderate/severe negIi ultimi 12 mesi)
Documentare I'appropriatezza dei test diagnostici
strumentali, come la spirometria, in questi pazienti,
poichè secondo un rapporto pubblicato di recente
questi test sono raramente eseguiti in Italia.
Obiettivo Primario:
Dimostrare la non inferiorità di indacaterolo (150
µg o.d.) verso salmeterolo 50µg/500 µg b.i.d. in
termini di trough FEV, (media dei valori di volume
espiratorio nel primo secondo dopo 23 are e 10
minuti e 23 ore e 45 minuti dall'inalazione della
dose mattutina del farmaco) dopo 12 settimane
(Giorno 85) di trattamento in pazienti affetti da
BPCD di grado moderato senza storia di
riacutizzazioni nell'anno precedente alla
partecipazione allo studio. In questo caso if trough
FEV, si definisce come la media dei valori del FEV,
misurato 23 ore e 10 rninuti e 23 ore e 45 minuti
dopo l'inalazione della dose mattutina del farmaco
al Giorno 84.
Obiettivi secondari
Confrontare l'effetto di indacaterolo 150µg o.d. con
quello di salmeterolo 50 gr ftuticasone propionato
500 µg b.i.d. sui trough FEV1 AUC5 min-4 h
standardizzata del FEV1 FEV e FVC, Transition
Dyspnea Index (TDI), St George's Respiratory
Questionnaire per i pazienti affetti da BPCO
(SGRQ-C), utilizzo di farmaci al bisogno, sicurezza
e riacutizzazioni nell'arco di un periodo di
trattamento di 26 settimane.
Fasi
Si stima un reclutamento di circa 3000 pazienti; 1.5
paziente/mese per centro che dovranno soddisfare i
seguenti criteri di inclusione:
- Eta: 45-85, entrambi i sessi;
- Consenso informato firmato;
- BPCO nota e documentata da esami spirometrici
che mostrano ostruzione non reversibile delle vie
respiratorie;
- FEV-1 < 50% in un test precedente (senza
restrizioni di tempo)
- Sintomi di bronchite cronica : tosse produttiva ed
escreato per almeno 3 mesi in ognuno dei 2 anni
precedenti la visita;
- In trattamento con broncodilatatori da almeno 12
mesi
- Con una storia di almeno 2 riacutizzazioni
(moderate/severe) negli ultimi 12 mesi prima della
visita
Ogni paziente sarà coinvolto un unica volta per una
singola visita durante la quale verranno raccolte le
seguenti informazioni:
- Età/Sesso fumatore(Si/No)
- BMI
- Riacutizzazioni negli ultimi 12 mesi
(lieve/moderato/severo)
- Sintomi di bronchite cronica
- Data della prima spirometria con FEV-1 < 50 %
- Data risultato di ogni successiva spirometria
- Risultato del test :6 minutes walking test (se
disponibile)
Studio clinico di non inferiorità multicentrico,
randomizzato, in doppio cieco, double-dummy, a
gruppi paralleli. I pazienti dovranno fornire consenso
informato scritto prima della Visita 1. I pazienti
eleggibili non devono aver assunto farmaci non
consentiti per il periodo specificato prima della Visita
1, come indicato nelle Tabelle 5-11 e 5-12 del
protocollo originale. I pazienti rimarranno in
trattamento con salmeterolo/fluticasone propionato
(MDDPI) in aperto fino alla Visita 2
(randomizzazione), e sarà loro consegnato del
salbutamolo da utilizzare come farmaco al bisogno.
Valutazioni di efficacia
- Spirometria (FEV1, FVC, rapporto FEV1/FVC)
- Capacità inspiratoria (in un sottogruppo di pazienti)
- Sintomi riportati dal paziente ed utilizzo di farmaci al
bisogno mediante eDiary
- BDI/TDI
- SGRQ-C
- Riacutizzazioni della BPCO
Valutazioni di sicurezza
- Eventi avversi
- Esame obiettivo
- Test di gravidanza sulle urine (nelle donne in età
fertile)
- Parametri vitali
- ECG
- Esami di laboratorio: ematologia, biochimica, urine
Popolazione
La popola ione dello st dio sarà costit ita da circa
Materiali e metodi
Risultati previsti
Studio osservazionale trasversale.
Saranno raccolti dati sensibili. Ogni paziente sarà oggetto di una
sola visita durante la quale saranno raccolti anche dati dalle
cartelle cliniche. Non e previsto un follow-up.
Verranno utilizzati metodi statistici epidemiologici.
L'approccio statistico sarà solamente esplorativo senza la
definizione di un'ipotesi a priori.
La prevalenza di ogni comorbidità considerata sarà calcolata
con i relativi intervalli di confidenza (CI) del 95%.
La percentuale di pazienti con test spirometrico annuale sarà
calcolata con i relativi Intervalli di confidenza (CI) del 95%.
Le differenze nelle caratteristiche demografiche e cliniche, tra cui
il numero delle riacutizzazioni nell'anno precedente la visita e il
numero annuale di test spirometrici, tra i sottogruppi di soggetti
saranno analizzate mediante un'analisi univariata. AI fine di
identificare i fattori associati in modo indipendente con la
presenza delle varie comorbidita, le variabili risultanti associate
alle comorbidita all'analisi univariata con un p <0,2 saranno
testati in un modello di regressione logistica multivariata. La
stessa analisi sarà effettuata al fine di identificare i fattori
associati alla presenza di almeno una spirometria 1 anno. Gli
odds ratio (OR) e gli intervalli di confidenza al 95% degli Odds
Ratio saranno calcolati.
Tutte le analisi saranno eseguite utilizzando il software SAS
(versione 9.2). Tutti i test saranno bilaterali, la significatività
statistica sarà fissata ad un valore di p< 0.05. Per i dettagli delle
analisi statistiche si rimanda allo Statistical Analysis Plan.
L'analisi dei dati ottenuti permetterà di valutare la
presenza dei diversi fenotipi tra i pazienti con BPCO.
Questo può essere un punto di partenza per meglio
adattare gli schemi terapeutici alle reali esigenze di
ogni paziente.
La variabile primaria è il trough FEV1 dopo 12 settimane di
trattamento (Giorno 85). Il trough FEV1 è definito come la media
dei valori di FEV1 misurati 23 ore e 10 minuti e 23 ore e 45
minuti dopo l’assunzione della dose mattutina di farmaco al
Giorno 84. Queste misurazioni saranno effettuate presso il
centro il Giorno 85. La variabile primaria (trough FEV1)
comprenderà il trattamento come effetto fisso con il FEV1 basale
ed il FEV1 prima dell’inalazione e 10-15 minuti dopo l’inalazione
di un SABA come covariate. Per riflettere lo schema di
randomizzazione, il modello includerà inoltre lo stato di
fumatore/ex-fumatore e il Paese come effetti fissi, con i centri
all’interno del Paese come effetto random. La non-inferiorità
sarà dimostrata se il 95% dell’intervallo di confidenza per la
media delle differenze dei valori di FEV1 di indacaterolo meno
salmeterolo/fluticasone si trova interamente a destra di -60 mL.
La valutazione principale di efficacia sarà effettuata sulla
popolazione per protocol. Tutte le valutazioni di tollerabilità
verranno effettuate sulla popolazione della full analysis (FAS),
costituita da tutti i pazienti che hanno ricevuto almeno una dose
di farmaco in studio. I pazienti saranno analizzati in base al
trattamento al quale sono stati randomizzati. Le valutazioni di
sicurezza verranno effettuate sulla popolazione safety, costituita
da tutti i pazienti che hanno ricevuto almeno una dose di
farmaco in studio. I pazienti saranno analizzati in base al
trattamento che hanno ricevuto, tranne se il paziente ha assunto
in maniera non corretta più di una dose di farmaco. Se ciò
dovesse verificarsi, il paziente sarà analizzato in base al
trattamento al quale è stato randomizzato.
Saranno riassunti e presentati i risultati relativi alle caratteristiche
demografiche ed anamnestiche, alla somministrazione di farmaci
d rante lo st dio alle ariabili di efficacia primarie e secondarie
La valutazione in questa popolazione di pazienti con
BPCO della non inferiorità o meno del
bronncodilatatore long-acting vs. il broncodilatatore di
generazione precedente associato allo steroide
inalatorio permetterà di definire meglio i criteri di priorità
tra le due classi di farmaci.