Reagente per bilirubina diretta
Metodo Acid Diazo
SCHEDA SINTETICA DEL PRODOTTO
Stabilità
:
fino alla scadenza a 2-25 °C
Intervallo lineare
:
fino a 340 µmol/l (20 mg/dl)
Tipo di campione
:
siero
Metodo
:endpoint
Preparazione del reagente :
pronto per l’uso.
USO PREVISTO
Questo reagente è destinato all’uso per la determinazione quantitativa in vitro della
bilirubina diretta nel siero umano.
SIGNIFICATO CLINICO
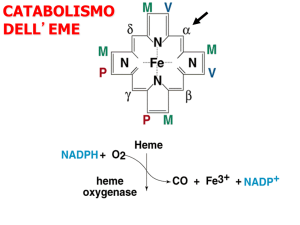
Al termine del loro ciclo di vita, gli eritrociti vengono degradati nel sistema
reticoloendoteliale, principalmente nella milza. L’eme che rimane, una volta
eliminato il ferro, è convertito in bilirubina. Questo processo è responsabile
dell’80% circa dei 500 µmol (300 mg) di bilirubina che si forma ogni giorno. Altre
fonti di bilirubina comprendono la degradazione della mioglobina e dei citocromi
e il catabolismo degli eritrociti immaturi nel midollo osseo.
Dopo essersi formata, la bilirubina viene trasportata nel fegato collegata ad
albumina, essendo idrosolubile. Questa frazione di bilirubina è detta bilirubina
indiretta o non coniugata. Nel fegato la bilirubina è coniugata in acido glucuronico
(monoglucuronidi e diglucuronidi) a formare la bilirubina coniugata ad opera
dell’enzima uridil difosfato glucuronil transferasi. La bilirubina coniugata o la
bilirubina diretta è escreta attraverso il sistema biliare nell’intestino, dove è
metabolizzata dai batteri in un gruppo di prodotti noti collettivamente con il nome
di stercobilinogeno. L’eliminazione è quasi completa e i livelli nel plasma rientrano
in un ordine normalmente trascurabile.
La bilirubina totale è la somma della frazione non coniugata e della frazione
coniugata. I livelli di bilirubina totale sono elevati in pazienti affetti da condizioni che
danno origine a un’ostruzione del dotto biliare, epatite, cirrosi, disordini emolitici
e numerose carenze enzimatiche ereditarie.
I livelli di bilirubina indiretta sono elevati per cause pre-epatiche come disordini
emolitici o disturbi epatici che comportano un’alterazione dell’ingresso, del
trasporto o della coniugazione all’interno del fegato.
Il monitoraggio della bilirubina nel neonato, soprattutto se prematuro, riveste
particolare importanza. Poiché la gestione epatica della bilirubina in tali casi è
spesso immatura, è comune l’insorgenza di ittero causato da un aumento dei livelli
di bilirubina non coniugata. La bilirubina non coniugata, se non legata all’albumina,
è in grado di attraversare la barriera ematoencefalica più facilmente, aumentando
il rischio di lesione cerebrale.1
METODOLOGIA
I metodi attualmente in uso per il dosaggio della bilirubina si basano per la maggior
parte sulla reazione tra la bilirubina e le soluzioni di acido solfanilico diazotato. In
soluzione acquosa reagisce in questo modo solo la bilirubina diretta (coniugata).
Questo reagente per bilirubina diretta utilizza un metodo con acido diazotato.
La bilirubina coniugata reagisce con l’acido solfanilico diazotato per produrre
azobilirubina acida, l’assorbanza della quale è proporzionale alla concentrazione di
bilirubina diretta nel campione e può essere misurata a 550 nm. Per gli analizzatori
bicromatici la lettura del bianco deve essere effettuata a 660 nm.
COMPOSIZIONE DEL REAGENTE
Principi attivi
Reagente per bilirubina diretta:
Acido idroclorico
Acido solfanilico
Reagente per nitrito di sodio:
Nitrito di sodio
Concentrazione
100 mmol/l
10 mmol/l
144 mmol/l
Simbolo di pericolo: Punto esclamativo e corrosione
Parola di segnalazione: Pericolo
Frasi di rischio
H314 Provoca ustioni della pelle e lesioni oculari gravi
H317 Può causare una reazione allergica a livello cutaneo
H318 Provoca gravi lesioni oculari
Indicazioni di prudenza - Prevenzione
Non respirare polvere/fumi/gas/nebbia/vapori/nebulizzato
Lavare accuratamente il viso, le mani e qualsiasi area cutanea esposta dopo la
manipolazione
Indossare guanti e abbigliamento protettivi nonché protezioni per gli occhi e il viso
Non portare fuori dal luogo di lavoro gli indumenti contaminati
Indicazioni di prudenza - Intervento
Consultare immediatamente un CENTRO ANTIVELENI o un medico
Trattamento specifico (vedere le istruzioni supplementari di primo soccorso su
questa etichetta)
Simboli sulle etichette del prodotto
Rappresentante autorizzato per
l’Europa
Per uso diagnostico in vitro
Codice partita/numero lotto
Limiti di temperatura
Utilizzare entro/data di scadenza
Numero catalogo
ATTENZIONE. Consultare le
istruzioni per l’uso.
Consultare le istruzioni per l’uso
Produttore
Corrosione
Punto esclamativo
Reagente per bilirubina diretta
Reagente per nitrito di sodio
Occhi
CONTATTO CON GLI OCCHI: Sciacquare con cautela con acqua per diversi minuti.
Rimuovere le lenti a contatto, laddove siano presenti e l’operazione sia facile da eseguire.
Continuare a risciacquare.
Consultare immediatamente un CENTRO ANTIVELENI o un medico
Pelle
CONTATTO CON LA PELLE (o i capelli): Rimuovere immediatamente tutti gli indumenti
contaminati. Sciacquare con acqua corrente o sotto la doccia.
Lavare gli abiti contaminati prima del riutilizzo.
In caso di irritazione o eruzione cutanea: rivolgersi a un medico
Inalazione
IN CASO DI INALAZIONE: Portare il soggetto infortunato all’aria aperta e tenerlo a riposo
in una posizione che favorisca la respirazione.
Consultare immediatamente un CENTRO ANTIVELENI o un medico
Ingestione
IN CASO DI INGESTIONE: Sciacquare la bocca. NON indurre il vomito.
Indicazioni di prudenza - Immagazzinamento
Conservare sotto chiave.
Indicazioni di prudenza - Smaltimento
Smaltire i contenitori e il contenuto in un centro autorizzato allo smaltimento dei rifiuti.
Pericoli non altrimenti classificati
Non applicabile
Tossicità non nota
Lo 0% della miscela consiste di ingredienti di tossicità ignota
Altre informazioni
Il contatto con la pelle ripetuto o prolungato può causare reazioni allergiche nei soggetti
sensibili
Interazioni con altre sostanze chimiche
Nessuna informazione disponibile
Per informazioni aggiuntive, consultare la scheda dati di sicurezza del prodotto (Safety
Data Sheet, SDS).
PREPARAZIONE DEL REAGENTE
Reagente per analisi:
Aggiungere il reagente per nitrito di sodio al reagente per bilirubina diretta con un
rapporto di 1:100. Ad esempio, a 10 ml di reagente per bilirubina diretta aggiungere
0,1 ml di nitrito di sodio (equivalente a circa 3 gocce, ma si raccomanda una verifica
da parte dell’operatore).
Reagente del bianco:
Usare il reagente per bilirubina diretta così come fornito.
STABILITÀ E CONSERVAZIONE
Se conservato a 2-25 °C, il reagente è stabile fino alla data di scadenza indicata sul
flacone e sull’etichetta della confezione del kit.
Reagente di lavoro:
Il reagente di lavoro è stabile per almeno 21 giorni a 2-8 °C.
Indicazioni di deterioramento del reagente:
• Torbidità;
• Assorbanza del reagente > 0,1 AU a 550 nm; e/o
• Mancato recupero dei valori di controllo entro il range assegnato.
RACCOLTA E MANIPOLAZIONE DEI CAMPIONI
Siero: usare siero non emolizzato.
Conservazione: I campioni devono essere tenuti al riparo dalla luce chiara poiché la
bilirubina è fotolabile. I campioni devono essere conservati refrigerati per 3 giorni.2
STRUMENTAZIONE ACCESSORIA NECESSARIA NON IN DOTAZIONE
• Se necessarie, pipette per un’erogazione accurata dei volumi misurati.
• Un analizzatore chimico-clinico in grado di mantenere costante la temperatura
(30/37 °C) e misurare l’assorbanza a 550 nm.
• Prodotti di consumo specifici per analizzatori, quali provette per campioni.
• Materiale di controllo normale e anomalo.
• Calibratore o adeguato standard acquoso per bilirubina diretta.
PROCEDIMENTO OPERATIVO
Si raccomanda di eseguire un bianco per ogni campione. Il bianco per ogni campione
può essere ottenuto semplicemente usando il reagente per bilirubina diretta così come
fornito senza aggiunta di nitrito di sodio.
Si consigliano i parametri di sistema elencati di seguito. Su richiesta del gruppo di
supporto tecnico sono disponibili singole applicazioni per gli strumenti.
•
PARAMETRI DI SISTEMA
Temperatura
Lunghezza d’onda primaria
Lunghezza d’onda secondaria
Tipo di dosaggio
cinetica
Rapporto Rapporto reagente
es. Vol. campione
Vol. reagente
Tempo di incubazione
Limiti del bianco del reagente
(550 nm, cammino ottico 1 cm)
Linearità
Sensibilità
(550 nm, cammino ottico 1 cm)
30/37 °C
550 nm
660 nm
Endpoint
Incremento
1 : 20
10 µl
200 µl
300 secondi
Inferiore 0,0 AU
Superiore0,1 AU
340 µmol/l (20 mg/dl)
2,5 DmAbs per µmol/l
(43 DmAbs per mg/dl)
CALCOLI
I risultati vengono calcolati di solito automaticamente dallo strumento nel seguente
modo:
Diretta
Assorbanza del campione sconosciuto
= ———————————————————————————–
Bilirubina
Assorbanza del calibratore
x valore calibratore
Esempio:
Assorbanza del calibratore (Test)
Assorbanza del calibratore (Bianco)
=
=
0,038
0,003
Assorbanza del campione sconosciuto (Test)
Assorbanza del campione sconosciuto (Bianco)
Valore del calibratore =
=
=
0,029
0,01
15 µmol/l (0,88 mg/dl)
Assorbanza del calibratore Assorbanza del campione sconosciuto
=
=
0,038 - 0,003 = 0,035
0,029 - 0,01 = 0,019
Diretta
0,019
= ————– x 15
Bilirubina
0,035
= 8,1 µmol/l
Diretta
0,019
= ————– x 0,88
Bilirubina
0,035
= 0,48 mg/dl
NOTE
1. I campioni con valori superiori a 340 µmol/l (20 mg/dl) devono essere diluiti e
rianalizzati. Moltiplicare i risultati per il fattore di diluizione.
2. Conversione unità: µmol/l x 0,0585 = mg/dl
CALIBRAZIONE
È necessaria la calibrazione. Si raccomanda un adeguato standard acquoso o
calibratore a base sierica.
Per la frequenza di calibrazione su altri strumenti automatizzati, consultare le
specifiche di fabbricazione dello strumento. Tuttavia, la stabilità della calibrazione
è subordinata alla migliore prestazione dello strumento e all’uso di reagenti che
siano stati conservati secondo le raccomandazioni della sezione di questo foglio
illustrativo relativa alla stabilità e alla conservazione. Si consiglia di ripetere la
calibrazione ogniqualvolta si verifichi uno dei seguenti eventi:
• Il numero di lotto del reagente cambia.
• Si esegue un intervento di manutenzione preventiva o si sostituisce un
componente fondamentale del dispositivo.
• I valori di controllo risultano alterati o fuori intervallo e l’uso di una nuova fiala
di controllo non risolve il problema.
CONTROLLO QUALITÀ
Per garantire un adeguato controllo di qualità, utilizzare come campioni sconosciuti
sia controlli normali che anomali con valori saggiati:
• Almeno ogni otto ore.
• Quando si utilizza un nuovo flacone di reagente.
• Dopo un intervento di manutenzione preventiva o di sostituzione di un
componente fondamentale del dispositivo.
Risultati dei controlli al di fuori dei limiti superiore o inferiore degli intervalli stabiliti
sono indicativi del fatto che l’analisi potrebbe essere fuori controllo.
In tali situazioni si consigliano le seguenti azioni correttive:
• Ripetere gli stessi controlli.
• Qualora i risultati della ripetizione dei controlli non rientrassero nei limiti,
preparare nuovo siero di controllo e ripetere il test.
• Nel caso in cui i risultati fossero ancora fuori controllo, ricalibrare con un nuovo
calibratore e ripetere il test.
Fisher Diagnostics
una divisione di Fisher Scientific Company, LLC
parte di Thermo Fisher Scientific, Inc.
Middletown, VA 22645-1905 USA
Telefono:800-528-0494
540-869-3200
Fax:540-869-8132
•
Nel caso in cui i risultati fossero ancora fuori controllo, eseguire una calibrazione
con del reagente appena preparato e ripetere il test.
Qualora i risultati fossero ancora fuori controllo, contattare il servizio di assistenza
tecnica o il distributore di zona.
LIMITI
1. Sono stati condotti studi per la determinazione del livello di interferenza da
emoglobina e lipemia. I risultati ottenuti sono stati i seguenti:
Emoglobina: Evitare l’uso di campioni emolizzati.
Lipemia: Nessuna interferenza da lipemia, con riferimento ai trigliceridi, fino
a 8,8 mmol/l (780 mg/dl).
2. Young DS3 ha pubblicato un elenco esaustivo di farmaci e sostanze che potrebbero
interferire con quest’analisi.
VALORI DI RIFERIMENTO2
Adulti e neonati (> 1 mese di vita): 0-3 µmol/l (> 0,2 mg/dl)
I valori citati sono rappresentativi dell’intervallo di riferimento per questo metodo e devono
essere usati a titolo puramente orientativo. Si raccomanda a ogni laboratorio di verificare
l’applicabilità di questo intervallo alla propria popolazione di pazienti e, se necessario,
di determinare intervalli di riferimento propri.4
DATI SULLE PRESTAZIONI
I dati riportati di seguito sono stati ottenuti usando il reagente per bilirubina diretta su un
analizzatore chimico-clinico automatizzato, regolarmente sottoposto a manutenzione.
Ogni operatore deve valutare le prestazioni del prodotto sul proprio analizzatore in uso.
IMPRECISIONE
Il livello di imprecisione è stato valutato usando due livelli di controlli commerciali sulla
base della procedura NCCLS EP5-T.5
Intra-analisi: LIVELLO I
LIVELLO II
Numero di punti dati 80 80
Media (µmol/l / mg/dl) 20,5 / 1,2 35,9 / 2,1
S.D. (µmol/l / mg/dl) 1,9 / 0,11 1,9 / 0,11
C.V. (%) <1 2,9
Totale:
LIVELLO I
LIVELLO II
Numero di punti dati 80 80
Media (µmol/l / mg/dl) 20,5 / 1,2 35,9 / 2,1
S.D. (µmol/l / mg/dl) 1,9 / 0,11 1,9 / 0,11
C.V. (%) 8,7 5,2
ACCURATEZZA
Sono stati condotti studi comparati usando un reagente per bilirubina diretta simile,
disponibile in commercio, come riferimento. Sono stati analizzati campioni di siero in
parallelo e i risultati confrontati con il metodo dei minimi quadrati. Si sono ottenuti i dati
statistici elencati di seguito.
Numero di coppie di campioni
51
Intervallo dei risultati per campione 5 - 488 µmol/l (0,3 - 28,6 mg/dl)
Media dei risultati di riferimento
107 µmol/l (6,3 mg/dl)
Media dei risultati relativi alla bilirubina diretta 111 µmol/l (6,5 mg/dl)
Pendenza0,96
Intercetta
8,5 µmol/l (0,5 mg/dl)
Coefficiente di correlazione
0,99
LINEARITÀ
Se l’analisi è corretta, il dosaggio risulta lineare fino a 340 µmol/l (20 mg/dl).
SENSIBILITÀ
Se l’analisi è corretta, la sensibilità di questo dosaggio è 2,5 DmAbs per µmol/l
o 43 DmAbs per mg/dl (cammino ottico 1 cm, 550 nm).
BIBLIOGRAFIA
1. Zilva JF, Pannall PR. “Liver Disease and Gall Stones” in Clinical Chemistry in
Diagnosis and Treatment”. Lloyd-Luke 1979; Chap XIII; 286-8.
2. Tietz Textbook of Clinical Chemistry, Second Edition. Burtis CS and Ashwood ER
(Eds), WB Saunders Company, 1994.
3. Young DS. Effects of Drugs on Clinical Laboratory Tests, Third Edition. AACC Press,
1990.
4. Watchel M et al, Creation and Verification of Reference Intervals. Laboratory Medicine,
1995; 26: 593-7.
5. National Committee for Clinical Chemistry Standards. User evaluation of Precision
Performance of Clinical Laboratory Devices NCCLS; 1984, NCCLS Publication EP5-T.
© 2012 Thermo Fisher Scientific Inc. Tutti i diritti riservati. Hitachi è un marchio commerciale registrato
di Roche Diagnostics, Indianapolis, IN 46250. ILab 600 è un marchio commerciale registrato di
Instrumentation Laboratory Company, Lexington, MA 02421. Tutti gli altri marchi commerciali sono di
proprietà di Thermo Fisher Scientific Inc. e delle sue affiliate.
Informazioni per gli ordini
N. di catalogo
WMDE
Bergerweg 18
6085 AT Horn
Paesi Bassi
JL840887-it (R0)
TR33321
2 x 125 ml
1 x 10 ml