
Microbiologia del terreno
Ciclo del Carbonio
Il carbonio rappresenta circa il 50% in peso della sostanza secca degli organismi sia animali sia vegetali.
Il ciclo inizia con le piante, le quali usano il Carbonio inorganico presente nell’atmosfera sottoforma di CO2, per
trasformarlo in Carbonio organico, il quale viene convertito nuovamente in forma inorganica per attività della
microflora presente nel terreno; durante la degradazione dei costituenti organici, non tutto il Carbonio viene
mineralizzato, poiché una parte dei prodotti intermedi andrà a formare la frazione umica, ossia la sostanza organica
tipica del terreno.
I materiali organici che arrivano al terreno sono molto diversi, e nell’ambito dei vegetali si hanno:
1. Componenti solubili in acqua che rappresentano dal 5 al 30% della sostanza secca (zuccheri, amminoacidi,
acidi organici).
2. Emicellulose, pectine e amido, che formano dal 15 al 30% della sostanza secca.
3. Cellulosa, che rappresenta dal 15 al 60% della sostanza secca.
4. Lignina, che rappresenta dal 5 al 30% della sostanza secca.
5. Prodotti solubili in solventi organici (lipidi, cere, resine).
6. Proteine
Degradazione dei glucidi
I glucidi arrivano al terreno dai residui vegetali, e subiscono un processo degradativo più rapido secondo la
complessità della loro molecola, essi, infatti, vengono distribuiti in:
• Glucidi semplici: esosi, pentosi
• Polisaccaridi: emicellulose, pectine e amido.
I glucidi semplici vengono degradati rapidamente dai microrganismi con produzione di H2O e CO2; durante questa
degradazione si vengono a formare diversi composti intermedi, in funzione delle condizioni del suolo, che a loro
volta vanno a regolare l’intervento microbico:
Batteri aerobi: originano acido lattico, acido acetico e acido piruvico come prodotti intermedi e H2O e CO2
come prodotti finali.
Batteri anaerobi: originano acido lattico, metano e CO2 come prodotti intermedi.
Funghi aerobi: originano acido citrico, acido ossalico, acido fumarico e acido succinico come prodotti
intermedi.
Funghi anaerobi: originano acido fumarico e alcol come prodotti intermedi.
La maggior parte dei microrganismi del terreno sono chemio-organotrofi, di conseguenza usano come fonte di
energia gli esosi, dalla cui ossidazione ottengono molecole di ATP; nel caso in cui l’accettore finale sia una molecola
organica (alcol etilico, ottenuto per riduzione dell’aldeide acetica), il prodotto di riduzione si accumula e contiene
molta energia, quindi il processo di mineralizzazione si svolge molto lentamente in quanto non è liberata tutta
l’energia potenziale; se invece l’accettore finale è l’O2 atmosferico, si ha la completa mineralizzazione con
liberazione di tutta l’energia.
Le vie che portano alla degradazione degli esosi, sono tre:
1. Glicolisi.
2. Ciclo dell’esoso-monofosfato o del pentoso-fosfato.
3. Via di Entner-Doudoroff, tipica dei batteri Pseudomonas.
1
Degradazione dell’amido
L’amido è un polisaccaride formato da 2 unità:
L’amilosio: formato da lunghe catene e semplici catene di
unità glucosidiche, tenute insieme da legami α-1,4
glucosidici
L’amilopectina: presenta una struttura ramificata, formata
da catene simili a quelle dell’amilosio ma legate alla
catena principale da legami α-1,6 glucosidici.
La degradazione dell’amido è operata da enzimi amilolitici, detti
amilasi, delle quali la forma α-amilasi produce destrine e un pò di
glucosio, mentre la forma β-amilasi produce β-maltosio.
Delle due unità costituenti l’amido, solo l’amilosio viene
degradato completamente dall’amilasi, la quale risulta invece
inefficace nei confronti dell’amilopectina, per la presenza dei
legami α-1,6 glucosidici, che verranno demoliti solo per attività di
enzimi come l’amilo-α-1,6-glucosidasi dei lieviti, unici
microrganismi amilolitici.
È bene ricordare che alcuni tra i microrganismi amilolitici,
esplicano anche attività cellulolitica e azotofissatrice, come:
Batteri aerobi facoltativi e aerobi stretti: Bacillus cereus e
subtilis
Batteri anaerobi: Clostridium butyricum e amylolyticum.
Degradazione delle emicellulose
Le emicellulose sono glucidi polimerizzati, formate da catene di
poliosi ed acidi poliuronici.
La loro degradazione nel terreno è eseguita da diversi
microrganismi:
Funghi: Penicillium spp Aspergillus
Attinomiceti: Streptomyces
Batteri anaerobi: Clostridium spp e alcuni batteri presenti
nel rumine
Batteri aerobi: Pseudomonas spp.
Tra i vari enzimi che partecipano al processo, il più importante è la xilanasi (solitamente, un enzima che attacca le
emicellulose, non attacca le cellulose).
Degradazione delle pectine
Le pectine si differenziano dalle emicellulose per due motivi:
1. sono ricche in acido galatturonico
2. sono ricche di gruppi carbossilici
La loro importanza è legata al fatto che costituiscono la forza cementante che unisce le cellule vegetali: rispetto alle
emicellulose sono dei costituenti più omogenei, poiché comprendono polimeri α-1,4 dell’acido galatturonico,
associato a pentosi ed esosi. La sua degradazione è regolata da 2 enzimi:
1. pectina-metil-esterasi che degrada la pectina, con produzione di acido pectico e alcool metilico
2. poligalatturonasi che degrada l’acido pectico liberando unità galatturoniche.
I principali microrganismi ad attività pectinolitica sono:
Batteri aerobi: Bacillus subtilis
Plectridi anaerobi: Plectridium pectinovorum.
Clostridi anaerobi stretti: Clostridium butyricum, pectinolyticum, onnivorum.
Funghi pectinolitici: Aspergillus e Penicillium.
2
Dalla degradazione delle pectine, i microrganismi liberano acidi organici, alcoli e zuccheri, i quali verranno
metabolizzati da altri microrganismi.
Degradazione della cellulosa
Strutturalmente, la cellulosa è formata da catene lineari di unità di β-D-glucopiranosio unite da legami β-1,4glucosidici. Le catene sono unite tra loro da ponti H e forze di Van der Waals.
La degradazione della cellulosa risulta essere regolata da un complesso enzimatico che agisce in successione,
denominato cellulasi.
Inizialmente si pensava che l’azione demolitiva si svolgesse in 3 tappe:
1. un enzima preparava la molecola all’attacco dell’enzima successivo
2. il secondo enzima degradava la molecola producendo unità più piccole
3. il terzo enzima, la cellulasi, idrolizzava queste unità liberando glucosio.
Oggi si sa che la cellulasi è formata da altri enzimi:
1. endoglucanasi: attacca le catene poliosidiche a caso, sino ad avere la rottura in frammenti più corti
2. esoglucanasi: liberano unità di cellobiosio
3. β-glucosidasi: agisce sui composti solubili (cellobiosio) liberando glucosio.
Vengono quindi definiti microrganismi cellulolitici autentici, solo quelli dotati di tutto il corredo enzimatico e
pertanto capaci di degradare la cellulosa naturale.
I microrganismi ad attività cellulolitica sono:
Batteri aerobi: genere Sporocytophaga, Cytophaga.
Batteri anaerobi: genere Clostridium, Plectridium, Caducens, Terminosporus ed Endosporus; sono i
principali agenti della fermentazione anaerobica, dalla quale si ha la produzione di gas (CO2 e H2), acidi
organici (acido acetico) e alcoli (alcol etilico).
Batteri cellulolitici termofili: sono presenti nel terreno e nelle deiezioni animali, hanno una temperatura
ottimale di sviluppo compresa fra 52 °C e 60 °C. Le specie più importanti sono due: Terminosporus
monocellus e Terminosporus thermocellulolyticus.
Batteri cellulolitici dell’apparato digerente degli erbivori: si trovano in diversi tratti del tubo digerente. Le
specie più importanti sono: Ruminococcus flavus, Ruminococcus albus, Ruminobacter flavescens. Sono tutti
microrganismi polifagi che producono acidi grassi volatili, glucosio e cellobiosio.
Funghi cellulolitici: sono molto importanti nei terreni acidi, dove i batteri hanno un’attività molto ridotta; i
generi principali sono: Trichoderma, Botrytis, Penicillium; degradano la cellulosa con produzione di
zuccheri in condizioni aerobiotiche.
Cellulolisi nel terreno
La cellulolisi è il processo di degradazione della cellulosa, che risulta essere influenzato da 3 fattori:
1. Potenziale di ossidoriduzione: è la capacità che ha il terreno di cedere o assumere elettroni; esso è
influenzato dalla temperatura e dall’umidità.
2. pH: influenza il tipo di microrganismo che si sviluppa (O2 = microrganismi aerobi, assenza di O2 =
microrganismi anaerobi; O2 e terreno acido = funghi).
3. Contenuto in N del substrato e Rapporto C/N: i bisogni di Azoto aumentano all’aumentare della velocità di
degradazione (estate).
Degradazione della chitina
La chitina è formata da lunghe catene, la cui unità fondamentale è un amino-zucchero, l’N-acetil- β-glucosammina,
la cui degradazione comporta la liberazione di N in forma di NH3.
I microrganismi più attivi in tal senso sono gli Attinomiceti, che producono chitinasi, l’enzima responsabile della
rottura delle catene di amino-zuccheri, con produzione di diacetil-chitobiosio, che viene attaccato da un altro enzima,
la chitobiasi, con produzione di 2 molecole di acetil-glucosammina. Alla fine, mediante l’intervento di altre reazioni,
si arriva alla produzione di glucosammina, acido acetico, glucosio e ammoniaca.
I principali batteri coinvolti nel processo appartengono ai generi Streptomyces e Bacillus.
3
Degradazione della lignina
La lignina è un composto fenolico condensato, estremamente resistente all’attacco microbico, che accumulandosi nel
terreno va a costituire la sorgente più importante dell’humus.
I microrganismi più attivi nella degradazione della lignina sono i funghi, soprattutto i Basidiomiceti, i quali sono
anche i principali agenti del Marciume del legno, distinguibile in:
Marciume molle: consiste in una decomposizione dei costituenti glucosidici.
Marciume bruno: consiste nella decomposizione dei polisaccaridi.
Marciume bianco: consiste nella decomposizione contemporanea di polisaccaridi e lignina e formazione di
composti solubili.
Esistono anche alcuni batteri che partecipano alla demolizione della lignina, come i generi Pseudomonas,
Flavobacterium, Xantomonas. È una demolizione che avviene lentamente e in assenza di O2.
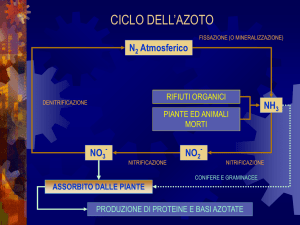
Ciclo dell’Azoto
L’azoto subisce nel terreno una serie di trasformazioni operate dai microrganismi, e alle quali partecipano composti
sia organici che inorganici. L’azoto organico viene trasformato in NH3 (mineralizzazione o ammonizzazione), la
quale può essere usata dalle piante oppure può essere ossidata a nitrato (nitrificazione), infine lo ione nitrico può
essere ridotto con produzione di N2 e N2O (denitrificazione). Contemporaneamente al processo di mineralizzazione, i
microrganismi assimilano azoto minerale trasformandolo in azoto organico.
Il ciclo dell’azoto comprende 5 fasi:
1. Fissazione: l’azoto elementare viene convertito in NH3 da parte di microrganismi sia liberi che in simbiosi
con le piante.
2. Mineralizzazione: l’azoto organico viene convertito in azoto inorganico:NH4+, NO3–.
3. Nitrificazione: ossidazione dell’NH4+ in ioni NO2– e NO3–
4. Riduzione assimilativa del nitrato: riduzione del nitrato a livello di NH4+ o di N amminico come costituente
della cellula
5. Denitrificazione: riduzione del nitrato e formazione di N2 e N2O.
Fissazione biologica dell’azoto
È il processo con il quale l’Azoto atmosferico viene convertito in NH3 da parte di microrganismi che possono essere
liberi o in associazione simbiotica con le piante. I vantaggi che essa comporta sono diversi:
• Avviene senza investimento di capitali
• L’energia necessaria è fornita dal sole
• Non si ha accumulo di NH3
• Non richiede combustibili fossili
Gli svantaggi sono:
• È un processo che non avviene nelle principali colture cerealicole
• Le leguminose presentano una minore resa
• Richiede molta energia
La fissazione biologica dell’Azoto, è possibile grazie al fatto che i microrganismi possiedono un sistema enzimatico
denominato nitrogenasi, che si presenta formato da due componenti:
1. enzima molibdeno–ferro: contenente 4 proteine che possono essere separate in due unità distinte
2. una ferro–proteina: composta da due sub–unità identiche. Essa combina Mg e ATP e trasferisce gli elettroni
all’altro componente che riduce il substrato.
La nitrogenasi è un enzima estremamente sensibile nei confronti dell’O2, inducendo quindi i microrganismi ad
elaborare apposite strategie atte ad evitare il contatto dell’enzima con l’O2. Tale problema non sussiste nel caso dei
microrganismi anaerobi obbligati e facoltativi, i quali non eseguono il processo di fissazione in presenza di O2.
4
Simbiosi ed associazioni azotofissatrici
Le interazioni tra piante e microrganismi azoto–fissatori, sono caratterizzate da relazioni complesse che portano alla
formazione di noduli radicali contenenti i batteri oppure da associazioni meno strette, nelle quali l’essudazione di
carboidrati da parte delle piante stimola la fissazione di batteri liberi nel suolo. La simbiosi possono essere distinte
in:
• ectosimbiosi: il microrganismo azoto–fissatore è extracellulare
• endosimbiosi: l’Azoto–fissatore è intracellulare
Affinché il processo di N–fissazione possa svolgersi, è necessario che siano soddisfatte alcune condizioni utili per il
funzionamento della nitrogenasi:
• presenza di Ferro e Molibdeno, necessari alla sintesi dell’enzima
• capacità di produrre ATP, necessaria per il funzionamento dell’enzima
• esclusione degli ioni H+, che vengono trasformati dalla nitrogenasi in H2, danneggiando sia l’ATP che la
stessa nitrogenasi
• temperature compatibili con la crescita di batteri mesofili, in quanto la nitrogenasi non è attiva a temperature
elevate o basse
• esclusione dell’O2 che inattiva l’enzima
L’azoto–fissazione richiede energia sottoforma di ATP, questa si lega alla ferro–proteina, abbassandone il potenziale
redox; l’ATP non è idrolizzata ad ADP finché la ferro–proteina non ha trasferito un elettrone alla Fe–Mo–proteina.
In generale la nitrogenasi non si forma quando è presente un’alta concentrazione NH3 o per l’aggiunta nel mezzo di
NH+4. Poiché il processo si verifica solo nel caso in cui si esauriscono le riserve azotate del mezzo, in modo da
evitare l’accumulo di Azoto fissato nell’ambiente.
I microrganismi azoto–fissatori
Azoto–fissatori liberi
1. Batteri eterotrofi aerobi:
•
Genere Azotobacter:
−
−
con microcisti:
Azotobacter chroococcum
Azotobacter vinelandi
senza microcisti:
Azotobacter agilis
Azotobacter insignis
Azotobacter macrocytogenes
•
Genere Beijerinckia: sono acido–tolleranti, di forma bastoncellare e con dimensioni minori
dell’Azotobacter. Vengono suddivisi in tre gruppi sulla base della morfologia e delle sorgenti di
Carbonio usate:
− mobili o immobili con attiva azoto–fissazione:
Beijerinckia indica
Beijerinckia lacticogenes
Beijerinckia mobilis
− mobile con lenta azoto–fissazione:
Beijerinckia fluminensis
− immobili con lenta azoto–fissazione:
Beijerinckia derxii
Beijerinckia acida
Beijerinckia congensis
•
Genere Derxia: sono batteri tropicali con un alto rendimento di azoto–fissazione (pH = 5~8,5).
5
•
Genere Clostridium: sono tutti batteri anaerobi, liberi, sporigeni:
•
Clostridium butyricum
Clostridium butylicum
Clostridium pasteurianus
Genere Bacillus:
Bacillus polymixa
Bacillus macerans
2. Batteri fotosintetici e chemiolitotrofi:
•
•
•
•
Genere Rhodospirillium: fotosintetici, l’azoto–fissazione è associata alla fotosintesi
Genere Chlorobium: fotosintetici, l’azoto–fissazione è associata alla fotosintesi
Genere Desulfovibrio: batteri chemiosintetici
Genere Desulfotomaculum: batteri chemiosintetici
3. Cianobatteri: sono i microrganismi più efficienti, essendo capaci di soddisfare le loro esigenze nutritive
a partire da N2, CO2, H2O e sali minerali, utilizzando l’energia solare. Essi possono svolgere l’azoto–
fissazione in 2 modi:
• condizioni aerobiche
• condizioni anaerobiche
Azoto–fissatori associati non nodulanti
•
Genere Azospirillium:
−
Azospirillium lypoférum: è capace di fissare N2 sia allo stato libero che in associazione con le radici
delle piante
Azoto–fissatori simbionti che formano noduli radicali
Abbiamo 3 tipi di simbiosi:
1. simbiosi radicali delle Leguminose: la famiglia Rhizobiaceae comprende 2 generi, Rhizobium e Agrobacterium,
che comprendono batteri aerobi obbligati che vivono in forma saprofitica nel suolo, associati alle radici delle
piante. I rizobi invadono le radici delle Leguminose, inducendo le cellule corticali ad attività meristematica ed a
formare una nuova struttura, il nodulo radicale, nella cui parte più profonda si insediano i batteri. Da questo
momento, tramite un processo non compreso, la pianta controlla il genoma batterico: tale processo è
accompagnato dalla formazione della leg-emoblobina, prodotto genetico dei due simbionti, in quanto la pianta
produce la globina e i batteri il cofattore ematico. Essa è responsabile del trasporto di O2 al sistema generatore di
ATP, richiesto dai batteroidi per la riduzione di N2. Morfologicamente, i Rizobi sono batteri Gram–, mobili, di
forma bastoncellare e con una parete formata da tre strati. Le cellule che penetrano nell’ospite sono quelle
batteroidi, di dimensioni maggiori e provviste di un involucro che le separa dall’ospite impedendo reazioni di
tipo immunitario. La quantità di azoto fissato dalla simbiosi Leguminose–Rhizobium può essere, in condizioni
favorevoli, assai elevata. Le specie coltivate possono fissare da 50 a 200 Kg di Azoto per ettaro all’anno.
L’infezione si svolge in 4 fasi:
a. preinfezione delle radici: Rhizobium specifici si moltiplicano nella rizosfera; deformazione dei peli
radicali
b. infezione e genesi del nodulo: i batteri penetrano nei peli radicali e si dispongono a “filo d’infezione”
(filamento continuo e mucoso, circondato da una guaina cellulosica sintetizzata dall’ospite) che
progredisce; formazione del tessuto del tubercolo
c. maturità del nodulo (fase intracellulare): il filo d’infezione libera i batteri, che assumono forma batteroide
e vengono circondati dall’involucro che li separerà dall’ospite; in questo stadio si ha la formazione di
emoglobina ed avviene la fissazione
6
d. degenerazione: si ha la degenerazione del nodulo accompagnata dalla lisi delle cellule batteriche e
conseguente liberazione dei batteri nel terreno, inoltre si ha la sostituzione dell’emoglobina con pigmenti
biliari.
2. simbiosi radicali di angiosperme non leguminose: genere Frankia. Oltre alle leguminose, anche altre piante
hanno la capacità di fissare l’Azoto atmosferico interagendo con batteri del genere Frankia, anche in questo caso
si vengono a formare dei noduli perenni, a partire dalle radici laterali, la cui crescita è completamente bloccata
dall’infezione. Inizialmente, i noduli sono molto simili a quelli formati dalle leguminose, in seguito però si
verifica una ramificazione estremamente spinta tanto che i noduli raggiungono dimensioni enormi. Con questo
metodo vengono fissati dai 60 ai 200 Kg di Azoto per ettaro all’anno.
3. simbiosi cianobatteriche.
Mineralizzazione
L’Azoto del terreno si trova combinato in composti organici, di origine sia animale che vegetale. L’Azoto minerale
rappresenta circa il 5%, quello organico il 95%. La mineralizzazione è il processo che porta alla trasformazione
dell’Azoto organico in NH4+, (ioni ammonio) e NO3– (nitrato), che si accumulano nel terreno in conseguenza di due
distinti processi:
1. ammonizzazione: l’NH4+ si forma a partire dai composti organici.
2. nitrificazione: l’NH4+ è ossidato a nitrato NO3–.
È possibile misurare la mineralizzazione sulla base della formazione
di NH4+ (primo composto inorganico che si ottiene), ricorrendo al
Potere ammonizzante potenziale, definito come la capacità che ha il
terreno di liberare NH4+ in seguito alla decomposizione di composti
azotati. Si ottiene l’NH3 svolta come:
NH3 libera = NH3 formata – NH3 assimilata o fissata dal suolo
Il Tasso di mineralizzazione (quantità di N mineralizzato nell’unità di
tempo) dell’Azoto organico del suolo, definito dalla conversione in NH4+ e NO3–, è in pratica la liberazione globale
di N inorganico, la cui quantità è data come differenza tra:
N inorganico = N organico – (N assimilato dalle piante + N assimilato dai m.o. + N perduto per lisciviazione + N
perduto per volatilizzazione durante la nitrificazione)
È molto importante notare come i processi di mineralizzazione del C e dell’N sono estremamente correlati e
avvengono con tassi paralleli (7–15:1). Un altro parametro che si può calcolare è il Rendimento della
mineralizzazione:
Rendimento =
NH3 svolta
N amminico nel terreno
Microrganismi ammonizzanti
Il processo di mineralizzazione è attuato da diversi m.o. che sfruttano l’N organico nel loro metabolismo. Il processo,
nel suo complesso, è influenzato da diversi fattori:
1. tipo di m.o. presente
2. caratteristiche fisico–chimiche del terreno
3. pH
4. temperatura
5. umidità
In relazione al tipo di terreno, si può dire che:
− nei terreni neutri o alcalini: predominano i batteri
− nei terreni acidi e aerati: predominano i funghi
− nei terreni asfittici: predominano i batteri anaerobi
In relazione all’umidità, la mineralizzazione procede più lentamente quando l’umidità del terreno è vicina al punto di
appassimento. Inoltre il processo è influenzato anche dal contenuto di N del terreno.
7
Degradazione delle proteine
Le proteine vengono inizialmente degradate, per attività di proteasi extracellulari microbiche, che scindono i legami
peptidici, originando lunghe catene polipeptidiche, che verranno ulteriormente idrolizzate con rilascio di
amminoacidi, i quali verranno utilizzati come fonte di C e di N di m.o. eterotrofi dopo che avranno subito processi di
deamminazione e decarbossilazione. Gli enzimi che possiedono attività idrolitica sono:
• esopeptidasi: idrolizzano i legami peptidici in prossimità dell’estremità della catena amminoacidica.
• endopeptidasi: idrolizzano i legami peptidici che si trovano lontani dall’estremità della catena amminoacidica.
Nitrificazione
La nitrificazione è l’ossidazione biologica dell’NH4+ a nitrato NO3–, avendo come intermedio il nitrito NO2–. I m.o.
che partecipano al processo vengono suddivisi in due categorie:
1. batteri nitrosi: ossidano l’NH4+ a nitrito NO2– :
• Nitrosomonas europaea: ha forma bastoncellare, mobile o immobile, ossida l’NH3 a nitrito NO2– e fissa la
CO2 come fonte di Carbonio. Si accresce bene con 5~30 °C e pH = 5,8~8,5
• Nitrosospira briensis: ha forma a spirale, mobile o immobile, ossida l’NH4+ a NO2– e fissano CO2 come
sorgente di Carbonio.
• Nitrosolobus multiformis: cellule suddivise in settori per l’invaginazione della membrana citoplasmatica e di
altri segmenti cellulari che formano regioni vescicolari; chemiolitotrofi obbligati, ossidano NH4+ a nitrito e
fissano CO2 come sorgente di Carbonio. Ottimi: 15~30 °C, pH = 6~8,2.
• Nitrosococcus nitrosus: cellule tonde, mobili o immobili; chemiolitotrofi obbligati, ossidano NH4+ a nitrito
NO2– e fissano CO2 come fonte di Carbonio. Ottimi: 2~30 °C, pH = 6~8.
2. batteri nitrici: ossidano i nitriti NO2– a nitrati NO3–:
• Nitrobacter winogradskii: ha forma bastoncellare, immobile, si sviluppano bene con 5~40 °C e pH = 6,5~8,5
• Nitrospira gracilis e Nitrospira mobilis: vivono nel mare.
Biochimismo della nitrificazione
La nitrificazione è un processo che si svolge in due reazioni. I m.o. principalmente coinvolti sono il Nitrosomonas e
il Nitrobacter:
NH4+ + 1,5 O2
6 e–
NO2– + ½ O2
NO2– + H2O + H2 [+64 Kcal/mole di NH4+]
2 e–
NO3– [+18 Kcal/mole di NO2–]
Entrambe le reazioni richiedono la presenza di O2 e sono esoergoniche. I fattori fisici che influenzano l’attività dei
batteri nitrificanti sono:
• richiedono molto O2
• vivono bene in terreni alcalini (pH = 8~8,5)
• il processo è sfavorito dalla luce
• la temperatura ottimale è di ~25 °C.
• essendo batteri chemiosintetici obbligati, richiedono O2.
Questo tipo di nitrificazione è detta nitrificazione autotrofa, per distinguerla da quella eterotrofa, attuata da m.o. che
partono da composti azotati ridotti come l’NH3, per ottenere i nitrati. Questi m.o. si sviluppano in condizioni avverse
per i batteri autotrofi, e possiedono un meccanismo di nitrificazione completamente diverso. Le specie interessate
sono:
• Aspergillus flavus, Nocardia e Agrobacterium.
8
Nitrificazione del terreno agrario
I fattori che si devono considerare sono:
• Ricchezza del terreno in batteri nitrificanti: i batteri nitrificanti sono presenti in tutti i terreni, eccetto in quelli
eccessivamente acidi; sono situati negli strati superiori.
• Tenore del terreno in nitrati: la presenza dei batteri nitrificanti varia con la stagione, con la profondità e a
seconda che il terreno sia coltivato o meno.
Denitrificazione
La denitrificazione è la riduzione del nitrato con produzione di gas e conseguente perdita dell’N fissato.
Biologicamente il processo si presenta come un insieme di processi di respirazione anaerobica, in cui il nitrato è
l’accettore finale in una catena di trasporto elettronico:
Nitrato
Nitrito
NO2–
NO3–
riduttasi
Ossido nitrico
NO
riduttasi
Ossido nitroso
N2O
riduttasi
N2
riduttasi
L’assimilazione dei nitrati come fonte di N è attuata da funghi, batteri e lieviti. La denitrificazione si divide in:
• denitrificazione assimilativa: l’NH4+ viene ottenuto dall’uso del nitrato come fonte di N per la sintesi delle
proteine. Non causa una perdita di N, ma una temporanea immobilizzazione
• denitrificazione dissimilativa: il nitrato NO3– viene usato come accettore di elettroni in reazioni di ossidazione. È
la vera denitrificazione, dove il nitrato sostituisce l’O2 in un meccanismo respiratorio. Specie Pseudomonas.
I batteri denitrificanti
Il processo di denitrificazione è attuato da diversi batteri, dei quali, alcuni partecipano a tutto il processo e altri solo a
determinate fasi; essi possono essere divisi in tre gruppi:
1. batteri che possono ridurre solo il nitrato NO3– a nitrito NO2–
2. batteri che possono ridurre il nitrito NO2– ma non il nitrato NO3– perché mancano della nitrato–riduttasi
3. batteri che riducono il nitrato NO3– a ossido nitroso N2O secondo tre vie:
a. in anaerobiosi per riduzione dei nitrati
b. in aerobiosi durante l’assimilazione del nitrato
c. in aerobiosi durante l’ossidazione di NH4+ a NO3–.
Denitrificazione del terreno
È l’ossidazione del nitrato NO3– con liberazione di Azoto in forma di N2 o di N2O. I fattori che aumentano tali
perdite sono:
• aumento di umidità che determina mancanza di O2
• alte temperature
• leggera alcalinità
• consumo di O2 nel terreno da parte di radici e m.o.
• disponibilità di composti organici ossidabili come donatori di elettroni.
I fattori che rallentano il processo sono:
• siccità
• aerazione
• acidità del suolo.
9
Ciclo dello Zolfo
Lo Zolfo è un elemento molto importante nella nutrizione delle piante e dei m.o., i quali lo usano principalmente
come solfato. Il ciclo dello S comprende reazioni di ossido–riduzione, che implicano il trasferimento di 8 elettroni
dalla forma più ossidata (solfato) a quella più ridotta (solfuro). I m.o. che partecipano al processo sono responsabili
delle reazioni di:
• Mineralizzazione.
• Organicazione.
• Ossido–riduzione.
A differenza dell’N, la cui fonte principale è rappresentata dall’atmosfera, lo S rientra nella composizione di rocce
sedimentarie. I due cicli, tuttavia, hanno in comune il processo di mineralizzazione delle forme organiche, affinché i
due elementi siano assimilabili.
Mineralizzazione dello Zolfo organico
Lo S organico si trova prevalentemente sotto forma di amminoacidi solforati liberi (cistina, metionina, taurina), di
solfati organici (solfato di colina), esteri solforici di glucidi e lipidi. La mineralizzazione è il processo che porta alla
trasformazione dello S organico in solfuri, e può avvenire sia in aerobiosi (operata dai batteri eterotrofi del genere
Pseudomonas e Proteus), che in anaerobiosi (operata dai batteri del genere Desulfovibrio). Anche i solfati vengono
ridotti in anaerobiosi, portando alla formazione di H2S, tramite reazioni di tipo autotrofo. Lo S mineralizzato può
essere usato dai m.o. come:
• donatore di H e sorgente di energia
• agente riduttore nell’assimilazione della CO2 atmosferica
• accettore di H
Riduzione ed ossidazione dello Zolfo minerale
La riduzione dello S può essere assimilativa o dissimilativa:
• la riduzione assimilativa del solfato in solfuro, porta alla formazione degli amminoacidi solforati, che entrano
nella composizione delle proteine
• la riduzione dissimilativa del solfato dipende dall’ossidazione combinata di composti ridotti di carbonio o
dall’idrogeno, ed è riferita a specie di Desulfovibrio che possono utilizzare come sorgenti ridotte di energia
soltanto lattato, piruvato, malato e idrogeno.
Ossidazione chemiotrofica
Gli ossidanti chemiotrofici costituiscono un gruppo alquanto eterogeneo di batteri, dei quali i più importanti sono i
Thioleucobacter, appartenenti alla famiglia Thiobacteriaceae, genere Thiobacillus, che comprende m.o. autotrofi che
dall’ossidazione dei composti ridotti dello S traggono l’energia per ridurre la CO2. A questo genere appartengono:
• Autotrofi stretti: ossidano solo i composti dello S:
o Aerobi stretti:
Thiobacillus thioparus: si sviluppa bene in ambiente neutro (pH = 6~8)
Thiobacillus neapolitanus: si sviluppa bene in ambiente neutro (pH = 6~8)
Thiobacillus thiooxidans: si sviluppa bene in ambiente acido (pH = 1~3,5)
o Anaerobi facoltativi: usano i nitrati in assenza di O2:
Thiobacillus denitrificans
• Autotrofi facoltativi:
Thiobacillus novellus
Thiobacillus intermedius
• Eterotrofi: usano contemporaneamente i composti dello S e i substrati organici:
Thiobacillus perometabolis
Ossidazione fototrofica
L’ossidazione fototrofica dei composti ridotti dello S avviene in ambienti completamente acquatici ed
intermittentemente nei suoli sommersi. In tali ambienti i batteri fototrofi si trovano nelle condizioni migliori (luce,
H2S e concentrazioni minime di O2) per la moltiplicazione.
10










![5\) batteri [modalità compatibilità]](http://s1.studylibit.com/store/data/000928299_1-28a224c15810efb654d8d9e4b207aa31-300x300.png)
