Lezione 7
Il metabolismo
terminale e la
produzione di ATP
1
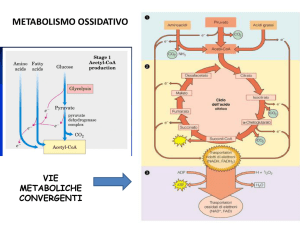
Il metabolismo terminale
Catabolismo Lipidi – Amminoacidi – Carboidrati
convergono sul metabolismo terminale,
e producono una stessa molecola: l’acetil-CoA
- ciclo di Krebs (o ciclo degli acidi tricarbossilici o
ciclo dell’acido citrico)
- fosforilazione ossidativa.
Entrambe le vie sono localizzate nei mitocondri
2
Relazione tra metabolismo
intermedio e terminale
© Zanichelli editore, 2014
3
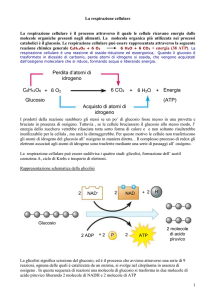
Respirazione
Cellulare
Respirazione
Cellulare
I mitocondri
Coenzima A
Il coenzima A è sintetizzato a partire dalla vitamina
B5 (o acido pantotenico) e dall’aminoacido cisteina,
spendendo 4 ATP. La vitamina B5 è presente in molti
alimenti, specialmente uova, carne e latte. Il CoA è il
cofattore essenziale per la sintesi dell’acetil CoA.
© Zanichelli editore, 2014
7
La piruvato deidrogenasi
1. Il piruvato è decarbossilato formato un derivato idrossietilico con la tiamina pirofosfato
(coenzima della piruvato deidrogenasi)
2. L’intermedio idrossietilico è ossidato alla forma disulfidrilica dell’acido lipoico (coenzima
della piruvato deidrogenasi)
3. Il gruppo acetilico è trasferito al CoA
4. La forma disulfidrilica dell’acido lipoico è ossidata dal FAD che diventa FADH2
5. FADH2 perde i due H tornando alla forma ossidata FAD. I 2 H sono acquistati da NAD+
La regolazione della piruvato
deidrogenasi
Il ciclo di Krebs (I)
Il ciclo di Krebs venne scoperto nel
1937 da H.A. Krebs, che lo
chiamò ciclo dell’acido citrico.
Successivamente, venne indicato
come ciclo degli acidi
tricarbossilici, dai tre intermedi
della fase di recupero dell’energia
(citrato, cis-aconitato e
isocitrato).
Hans Adolf Krebs ricevette il
premio nobel per la medicina
nel 1953
© Zanichelli editore, 2014
10
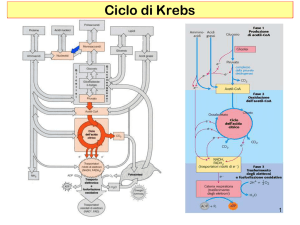
Il ciclo di Krebs (II)
A ogni giro del ciclo, un gruppo acetile (2C) entra
come acetil-CoA e si condensa con ossalacetato (4C)
per formare il primo acido tricarbossilico (citrato). Alla
fine del ciclo il gruppo acetile è ossidato a 2 CO2 e
viene rigenerato ossalacetato. Quindi, teoricamente,
una sola molecola di ossalacetato basterebbe per
ossidare un numero illimitato di acetil-CoA.
Questo in realtà non succede perché l’ossalacetato e
altri intermedi vengono utilizzati anche come
precursori di molte biosintesi.
© Zanichelli editore, 2014
11
La struttura del ciclo di Krebs
Nel ciclo di Krebs possiamo osservare:
• La via degli elettroni, ovvero la generazione di
potere riducente attraverso la generazione di NADH
e FADH2.
• La via dei carboni, ovvero il destino del gruppo
acetile attraverso le successive decarbossilazioni
ossidative.
• La via del Coenzima A, in cui una molecola di CoA
viene liberata all’inizio dall’acetil-CoA, per essere
poi utilizzata e nuovamente rigenerata nella
sequenza del ciclo:
a-chetoglutarato-> succinil-CoA -> succinato
© Zanichelli editore, 2014
12
La struttura del ciclo di Krebs
© Zanichelli editore, 2014
13
Le sequenze di reazioni del ciclo
di Krebs
Possiamo dividere idealmente il ciclo di Krebs in due blocchi
di reazioni:
1. La serie da citrato a succinato serve a operare le due
decarbossilazioni ossidative successive che rimuovono
i 2C entrati nel ciclo all’inizio come acetil CoA.
2. La serie da succinato a ossalacetato serve a
ripristinare il composto di partenza (ossalacetato) per un
nuovo giro.
3. In entrambe le serie di reazioni si ottiene energia sotto
forma di 4 coppie di elettroni e una molecola di GTP. Ma
solo nella prima serie viene prodotta CO2.
© Zanichelli editore, 2014
14
Ciclo di Krebs
15
1. Formazione del citrato
Acetil CoA reagisce con
l’ossalacetato (acido 2-oxo1,4-butandioico) per
formare il citrato (acido 3carbossi-3-idrossi-1,5pentandioico)
L’enzima citrato sintasi
inibita da succinil-CoA, il
prodotto della reazione 5.
16
La decarbossilazione ossidativa
L’ossidazione dell’acetil-CoA, che forma 2 molecole di
CO2 (con liberazione di una coppia di elettroni per
ciascuna molecola) avviene grazie a due
deidrogenasi che agiscono su
-isocitrato > a-chetoglutarato (reazione 3)
- a-chetoglutarato > succinil- CoA (reazione 4).
17
La decarbossilazione ossidativa
18
Ripristino Ossalacetato
Per formare il Succinato, si rompe il
legame alta energia del Succinil CoA,
fosforilando la GTP che poi forma ATP.
Succinato > Fumarato > Malato >
Ossalacetato.
Formazione di FADH2 e NADH + H+
19
Il ciclo di Krebs è una via
anfibolica (I)
Il ciclo di Krebs fornisce numerosi precursori per le
vie biosintetiche:
- ossalacetato e a-chetoglutarato per la sintesi di
amminoacidi,
- citrato come fonte di acetil-CoA per la biosintesi di
acidi grassi,
- succinil-CoA per la sintesi dell’eme,
20
Il ciclo di Krebs è una via anfibolica (II)
21
Reazioni anaplerotiche (I)
Continuamente vengono sottratti intermedi dal ciclo di
Krebs per la biosintesi. Questo potrebbe rallentare la
respirazione se non venissero rimpiazzati.
Le reazioni dedicate a fornire sempre sufficienti
intermedi al ciclo sono dette anaplerotiche (di
riempimento).
La principale è la carbossilazione del piruvato ad
ossalacetato ad opera della piruvato carbossilasi
mitocondriale:
piruvato+CO2+ATP -> ossalacetato + ADP+Pi
22
Destino del piruvato in condizioni
aerobiche: ossalacetato
- importante intermedio del ciclo di Krebs,
- substrato per la gluconeogenesi: forma il
fosfoenolpiruvato.
© Zanichelli editore, 2014
23
Il ciclo di Krebs genera elettroni
Nel ciclo di Krebs non viene prodotto direttamente
ATP. Un ATP è prodotto indirettamente a partire dal
GTP generato nella reazione 5.
Il ciclo invece genera 4 coppie di elettroni sotto
forma 3 NADH e 1 FADH2. Questi potranno essere
spesi per la sintesi di molte molecole di ATP.
il ciclo di Krebs è una specie di motore che usa
gruppi acetili come combustibile per trasformarli in
un flusso di elettroni.
24
La catena di trasporto degli
elettroni (I)
Le coppie di elettroni conservate nel NADH e FADH2
devono essere rese disponibili per la produzione di
ATP. Questo rigenererà le forme ossidate (NAD+ e
FAD) che potranno ricevere nuovi elettroni,
mantenendo in moto il ciclo. Gli elettroni sono ceduti
da NADH e FADH2 a un sistema di proteine presenti
nella membrana interna del mitocondrio, esposte
verso la matrice, dove si svolge il ciclo di Krebs e
quindi facilmente accessibili.
Queste proteine costituiscono la catena di trasporto
degli elettroni o catena respiratoria.
25
La catena di trasporto degli elettroni (II)
26
Flusso degli elettroni nella catena
(I)
La catena respiratoria comprende quattro complessi
proteici:
• Complesso I: NADH deidrogenasi
• Complesso II: succinato deidrogenasi
• Complesso III: Q-citocromo c ossidoreduttasi
• Complesso IV: citocromo c ossidasi
27
Flusso degli elettroni nella catena
(II)
Questi complessi contengono proteine specializzate
nell’accettare e donare elettroni (flavoproteine,
proteine Fe-S, citocromi).
La capacità di trasferire elettroni di queste proteine
dipende dalla presenza di particolari coenzimi
(ubichinone) o di gruppi prostetici, ovvero strutture
molecolari in grado di legare elettroni, quali il gruppo
eme (nei citocromi) i gruppi ferro-zolfo (nelle
corrispondenti proteine), il gruppo
flavinmononucleotide (nella NADH deidrogenasi).
28
La catena di trasporto degli
elettroni (III)
Ossido-riduzioni
La catena respiratoria è una sequenza di ossido-riduzioni, in
cui le proteine dei vari gruppi (nella sequenza I-IV) accettano gli
elettroni (riducendosi) e li cedono immediatamente al gruppo
successivo (ossidandosi).
30
Ossigeno: accettore finale di eÈ necessario che gli elettroni alla fine vengano
eliminati: è questa la funzione dell’ossigeno che
funziona da accettore finale.
Una molecola di O2 accetta 4 elettroni dal complesso
IV, formando 2 molecole di acqua.
Quindi gli elettroni generati in ogni ciclo di Krebs (8)
necessitano di 2 molecole di ossigeno per essere
smaltiti.
31
Funzionamento della catena di trasporto
La catena respiratoria non genera direttamente ATP, bensì
energia, sotto forma di forza proton-motrice, che servirà per
32
la fosforilazione ossidativa.
Il gradiente elettrochimico
protonico (I)
Il trasferimento degli atomi di idrogeno attraverso la
catena respiratoria comporta la separazione tra ogni
atomo di H e il suo elettrone. Gli ioni H+ così generati
vengono pompati verso lo spazio intermembrana.
L’ossidazione del NADH + H+ libera 2 elettroni e 2
protoni (H+). Gli elettroni entrano nella catena nel
complesso I e vengono trasportati dai complessi I-IV
all’ ossigeno.
I protoni vengono pompati attraverso la membrana
interna nello spazio intermembrana.
33
Il gradiente elettrochimico
protonico (II)
La presenza di una concentrazione elevata di H+ da un
solo lato della membrana farà sì che, nel momento in
cui lo spazio intermembrana (elevata concentrazione
di H+) venga messo in collegamento con la matrice
(bassa concentrazione di H+) si crei un gradiente
elettrochimico, in cui i protoni fluiscono dal
compartimento ad alta concentrazione verso quello a
bassa.
Il collegamento è creato da un complesso
transmembrana: l’ATP sintasi.
34
Il flusso elettronico attraverso la membrana interna dei mitocondri è
accompagnato da un pompaggio di protoni dalla matrice allo spazio
intermembrana.
Ciò genera una differenza di potenziale elettrico e una
differenza di pH tra i due lati della membrana rendendo
quello che guarda la matrice più alcalino.
Questa concentrazione protonica e questa separazione di cariche
determinano una energia elettrochimica che prende il nome di
forza motrice protonica che rappresenta la forma di
conservazione dell' energia prodotta e liberata nelle
ossidazioni biologiche.
La membrana mitocondriale è impermeabile ai protoni che non
possono così rientrare per annullare il gradiente elettrochimico.
Ma quando questi potranno fluire
attraverso i canali protonici
specifici posti nel complesso Fo dell'ATPsintetasi in direzione del
gradiente elettrochimico, si renderà disponibile una grande quantità
di energia.
Il complesso F1 dell'ATPsintetasi condenserà un fosfato
all'ADP per generare ATP.
Il gradiente di H+ è la forza che
permette la fosforilazione di ADP
che procede con la rimozione di
H2O.
ADP+Pi = ATP + H20
ADP + Pi = ATP + H+ (interno) + OH(esterno)
Fosforilazione ossidativa: ATP
sintasi
La teoria chemiosmotica (1962, P.Mitchell) spiega la
sintesi di ATP a partire dalla forza proton-motrice del
gradiente elettrochimico. Il flusso di protoni che ritorna
verso la matrice, infatti, passa attraverso un canale
costituito dalle proteine della subunità F0 del
complesso della ATP sintasi. Questo canale, in realtà è
un rotore, le cui componenti vengono mosse dal
flusso di H+.
© Zanichelli editore, 2014
38
Meccanismo della ATP sintasi
Questo movimento si
trasmette alle proteine della
testa (subunità F1) che
sporge verso la matrice e
dove ha sede la sintesi di
ATP a partire da ADP e Pi,
generando acqua. Gli
elettroni ceduti da una
molecola di NADH + H+
portano alla sintesi di 2
ATP, mentre quelli di un
FADH2 a 1,5 ATP.
© Zanichelli editore, 2014
39
Considerazioni finali sulla
produzione di ATP
La produzione di ATP (la moneta energetica della
cellula) quindi procede attraverso complesse
sequenze di reazioni connesse tra di loro:
1. Il catabolismo della macromolecole è connesso al
ciclo di Krebs grazie all’ acetil-CoA.
2. Il ciclo di Krebs è connesso alla catena
respiratoria grazie ai trasportati di elettroni ridotti
FADH2 e NADH+H+.
3. La catena respiratoria è connessa all’ATP sintasi
grazie alla forza proton motrice del gradiente
elettrochimico.
© Zanichelli editore, 2014
40
Resa energetica: 65% di 679 kcal
Emoglobina, O2, CO2 e
respirazione (I)
È possibile ora capire il nesso tra la respirazione
intesa come processo organo-meccanico di
inspirazione ed espirazione e la respirazione come
processo biochimico che porta alla sintesi di ATP.
Inspirando immettiamo l’ossigeno che viene captato
dall’emoglobina degli eritrociti e veicolato alle cellule,
dove funge da accettore finale degli elettroni della
fosforilazione ossidativa.
© Zanichelli editore, 2014
42
Emoglobina, O2, CO2 e
respirazione (II)
La quantità notevole di CO2 generata dalla
decarbossilazione ossidativa nel ciclo di Krebs e nelle
varie reazioni cellulari, viene ceduta all’emoglobina,
riportata ai polmoni ed emessa con l’espirazione.
La respirazione è quindi un bell’esempio di come
nell’organismo, ogni aspetto macroscopico sia
legato a precisi eventi molecolari.
© Zanichelli editore, 2014
43







![11. Ciclo di Krebs [modalità compatibilità]](http://s1.studylibit.com/store/data/001120215_1-23827c0a1e611852a5ba14474c14bb9c-300x300.png)