Biochimica
Molecole
a specchio
Nella chimica della vita gli amminoacidi
mancini sono la regola. Ma perché in natura
ci sono tante eccezioni?
di Sarah Everts
C
hi va a infastidire un ornitorinco maschio nella stagione riproduttiva rischia di finire intrappolato fra le sue tozze zampe posteriori, sotto la minaccia di una serie di aguzzi speroni e del loro veleno. Un veleno doloroso
capace di azzoppare un altro maschio nella competizione riproduttiva, ma
utile anche come difesa contro quegli scocciatori degli esseri umani e dei
cani. È anche un prodotto piuttosto insolito, che ben si addice a un mammifero così strano da deporre uova e avere un becco d’anatra. Il veleno
dell’ornitorinco contiene infatti una classe di molecole che un tempo i biologi ritenevano confinata al mondo microscopico dei batteri.
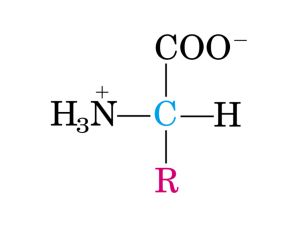
Queste molecole sono l’immagine speculare dei normali amminoacidi che le cellule uniscono
fra loro per costruire tutte le proteine della vita, essenziali per un funzionamento corretto. Le immagini speculari sono fatte degli stessi atomi della ventina di amminoacidi standard del corredo
biologico; e questi atomi sono legati fra loro nel medesimo ordine. Leggermente diverso, però, è
l’orientamento dei legami, e questo porta a strutture che differiscono dagli amminoacidi classici
più o meno come una mano destra differisce da una mano sinistra. Nelle reazioni biologiche, tuttavia, le due forme non sono intercambiabili. Si potrebbe dire, per semplicità, che gli amminoacidi classici sono «mancini» e le loro immagini speculari sono «destre». I termini corretti per identificarli sono «levogiro» e «destrogiro», dalle parole latine per mancino (laevus) e destro (dexter). Le
due forme sono dette anche L-amminoacidi e D-amminoacidi.
Per lungo tempo si è ritenuto che gli amminoacidi destrogiri dovessero avere un ruolo minimo negli organismi superiori, perché mal si accoppierebbero al macchinario molecolare della
In breve
Fotografia di Dan Saelinger
Gli amminoacidi, i mattoni fondamentali delle
proteine, possono esistere in due forme che, come le
mani, destra e sinistra, sono l’immagine speculare
l’una dell’altra. Quando è sorta sul nostro pianeta, la
vita ha favorito una sola delle due forme, quella
levogira, per lo svolgimento delle attività cellulari.
Per lungo tempo, le sole eccezioni a questa regola
68 Le Scienze
539 luglio 2013
www.lescienze.it
sono state trovate nei batteri. Di recente però sono
diventate sempre più numerose quelle individuate
negli organismi superiori, esseri umani compresi.
I ricercatori studiano possibili applicazioni
biomediche di questi amminoacidi insoliti per il
trattamento di condizioni come schizofrenia, fibrosi
cistica e degenerazione maculare.
Le Scienze 69
Un fortunato accidente
Come mai gli amminoacidi levogiri hanno assunto un ruolo dominante rispetto agli analoghi destrogiri, al punto che per molto
tempo le funzioni biologiche di questi ultimi sono sfuggite all’attenzione degli scienziati, anche se le loro molecole erano già state caratterizzate verso la fine dell’Ottocento? Alcuni ricercatori sostengono che all’origine della prevalenza delle forme mancine ci
sia l’equivalente cosmologico di un lancio di moneta. Semplicemente, è successo che le prime entità chimiche in grado di replicarsi con successo utsassero amminoacidi mancini, e questa distorsione si è poi consolidata, in un’eredità dei nostri lontani progenitori,
suggerisce Robert Hazen, geofisico della George Mason University,
che studia l’origine della vita. Un’altra popolare teoria ritiene che
la luce polarizzata emessa da una stella in rapida rotazione ai primordi della nostra galassia abbia in qualche modo distrutto selettivamente gli amminoacidi destrogiri, aumentando la probabilità
che come elementi costitutivi della vita emergessero quelli levogiri.
Una volta consolidatasi la scelta, l’evoluzione aveva un chiaro incentivo a mantenere la prevalenza di un tipo di ammino­
acido sull’altro, spiega Gerald Joyce, che studia le origini della vita allo Scripps Research Institute di La Jolla, in California. «Per
fare un’analogia, nei paesi occidentali per convenzione ci salutiamo stingendoci la mano destra. Funzionerebbe altrettanto bene se ci accordassimo tutti per stringerci la sinistra, ma se non
ci fosse nessuna convenzione certi incontri sarebbero piuttosto imbarazzanti». Quindi la maggior parte del macchinario delle
cellule viventi, dagli enzimi che producono gli amminoacidi alle
complesse strutture dette ribosomi che li allineano e poi li uniscono a formare le proteine, è compatibile solo con gli L-amminoacidi e non con i loro corrispondenti D-amminoacidi.
In effetti la primordiale decisione della vita di preferire gli amminoacidi mancini potrebbe aver favorito la scelta dell’orientamento di un’altra classe di composti organici, i carboidrati.
Nell’ultimo decennio numerosi gruppi di ricerca hanno dimostrato
70 Le Scienze
Un semplice test
Sarah Everts, nata a Montreal, è la
corrispondente da Berlino del settimanale
«Chemical and Engineering News». Cura inoltre il
blog Artful Science, che tratta di arte e scienza.
modo queste molecole per coordinare attività come accendere la fluorescenza o costruire biofilm. Capire come questi batteri
sfruttino i D-amminoacidi per comunicare è di grande interesse per lo sviluppo di
Della ventina di amminoacidi naturali, l’unico a essere achirale (cioè a non poter esistere in due
farmaci o prodotti con cui disperdere le
configurazioni diverse, «destra» e «sinistra») è la glicina (sopra). Se si sovrappone questa molecopellicole che si formano sui nostri denti,
la alla sua immagine speculare si ha una corrispondenza perfetta. L’amminoacido serina, invece, è
nei polmoni di chi soffre di fibrosi cistichirale: se lo si sovrappone alla sua immagine speculare non c’è corrispondenza.
ca, nei tubi degli oleodotti e su dispositivi
medici come i cateteri.
Achirale (Amminoacido: glicina)
Uno dei motivi per cui batteri e creatuSovrapposizione
re velenose usano D-amminoacidi è che
Immagine
Idrogeno
un peptide, o una proteina più lunga in cui
speculare
sia­no presenti, non è facile da degradare
Azoto
per gli enzimi dell’ospite. Tutti gli organiCarbonio
smi hanno enzimi proteolitici, che degradano e riciclano rapidamente gli L-ammiOssigeno
noacidi delle proteine, ma non quelli D.
Gli scienziati che sviluppano farmaci hanno cercato di aggiungere D-amminoacidi a
Chirale (Amminoacido: serina)
peptidi e proteine da usare a fini terapeutiForma levogira
Forma destrogira
Sovrapposizione
ci proprio per aggirare queste proteasi «da
guardia» e consentire ai farmaci di permaImmagine
Discrepanze
nere nel corpo più a lungo.
speculare
Ora che i ricercatori indagano su questo strano nuovo mondo degli amminoacidi destrogiri, esplorano anche una serie di
ulteriori ruoli che potrebbero avere questi
composti. Losick e altri, per esempio, ipotizzano che almeno qualcuno dei D-ammiKreil ha iniziato a interessarsi del veleno delle rane arboricole noacidi prodotti dai batteri che vivono sulla pelle, nel tratto digequando ha sentito parlare di un popolo indigeno del Perù, i Matsés, stivo e in altre parti del nostro corpo potrebbe essere importante
che sfrutta i peptidi contenenti D-amminoacidi presenti nella pel- per benessere, salute e forse comportamento degli esseri umani.
le di una rana arboricola chiamata Phyllomedusa bicolor come poUna delle grandi domande nel campo dei D-amminoacidi è
tente allucinogeno per i suoi rituali di caccia. I Matsés si praticano se ci sia qualche altra parte del corpo umano, a parte il cervello,
delle bruciature sul petto, su cui poi applicano un estratto di pel- che fabbrica questo genere di composti. Le prove preliminari sole di rana. Questo provoca immediatamente diarrea e palpitazioni, no suggestive. Il gruppo di Yoko Nagata, alla Nihon University di
e poi uno svenimento di breve durata. Al risveglio i cacciatori han- Tokyo, ha riferito di D-amminoacidi nella saliva umana, e i ricerno sensi più acuti e la sensazione di avere una forza sovrumana. Il catori guidati da Kenji Hamase alla Kyushu University, in Giappeptide della rana è composto quasi interamente di L-amminoaci- pone, hanno osservato nei ratti D-alanina immagazzinata ad alta
di, ma in mancanza del suo unico D-amminoacido risulta privo di concentrazione nelle cellule beta del pancreas, quelle che secernoeffetti allucinogeni, dice Kreil.
no l’insulina. In esperimenti preliminari recentemente condotti in
Australia nel suo laboratorio, Kuchel ha scoperto in cuori umani e
Un mondo di ombre
di topo enzimi che convertono amminoacidi dalla forma L a quelAnche se si trovano nei veleni di una vasta gamma di organi- la D, simili a quelli del veleno dell’ornitorinco.
Quale preciso ruolo possano avere questi enzimi nella fisiologia
smi, in altri esseri viventi i D-amminoacidi servono a funzioni più
pacifiche. Le aragoste, per esempio, li usano come catalizzatori per umana, dice Kuchel, è un mistero. Se non altro, l’idea che potrebbero avere qualche importante funzione non è più ridicola.
l’accoppiamento e per tenere a posto i propri livelli di sali.
n
I più grandi utilizzatori di D-amminoacidi però sono sempre i
microbi; ma anche qui i ricercatori stanno scoprendo nuove funper approfondire
zioni per questo genere di molecole. La maggior parte dei batteri
costruisce le proprie pareti cellulari a partire da una matrice ap- Emerging Knowledge of Regulatory Roles of D-Amino Acids. Cava F. e altri, in
piccicosa di zuccheri e proteine, i cosiddetti peptidoglicani, mo- «Bacteria in Cellular and Molecular Life Sciences», Vol. 68, n. 5, pp. 817-831, marzo
dificati con D-alanina e altri D-amminoacidi. Nel 2009 Matthew 2011. www.ncbi.nlm.nih.gov/pmc/articles/PMC3037491.
Waldor, che lavora alla Harvard University e allo Howard Hughes D-Amino Acids in Chemistry, Life Sciences, and Biotechnology. Brückner H. e
Fujii N. (a cura), Wiley, 2011.
Medical Institute, ha trovato che i batteri rinforzano i peptidogliHigh Dose D-Serine in the Treatment of Schizophrenia. Kantrowitz J. e altri, in
cani con una sorta di malta contenente D-metionina e D-leucina. «Schizophrenia Research», Vol. 121, n. 1, pp. 125-130, agosto 2010.
Inoltre questi D-amminoacidi possono rimodellare i peptidoglica- http://www.ncbi.nlm.nih.gov/pubmed/20541910.
ni dei batteri vicini, anche quelli di specie diverse. La scoperta, se- The New Ambidextrous Universe: Symmetry and Asymmetry from Mirror
condo Waldor, suggerisce che i microrganismi usino in qualche Reflections to Superstrings. Gardner M., terza edizione rivista, Dover, 2005.
Molecole allo specchio
che in certe soluzioni sperimentali mirate a simulare il brodo primordiale che potrebbe essere esistito sulla Terra 4 miliardi di anni fa il predominio di certi L-amminoacidi semplici tende a favorire, per complesse ragioni chimiche, la formazione di carboidrati
destrogiri, che è poi l’orientamento effettivamente presente in tutto il campo della biologia.
Alle eccezioni alla regola per cui gli amminoacidi naturali sono
levogiri è stata dedicata maggiore attenzione negli anni novanta,
dopo che Snyder ha mostrato che nel cervello umano alcuni composti destrogiri funzionano da neurotrasmettitori. Nel 2002 Philip
Kuchel, chimico dell’Università di Sydney, ha trovato D-amminoacidi nel veleno dell’ornitorinco. Nel 2009 ricercatori della Harvard
Univesity e dell’Howard Hughes Medical Institute hanno scoperto
che parecchi D-amminoacidi svolgevano funzioni nuove e inattese
nelle pareti cellulari batteriche. Nel 2010 gli scienziati hanno osservato che i complessi raggruppamenti di batteri che si espandono a
ricoprire di una sottile pellicola su vari tipi di superfici – dalle sorgenti calde ai dispositivi medici – sembrano usare D-amminoacidi
come indicazione per la dispersione dei biofilm stessi.
Nell’uomo si è osservato che l’acido D-aspartico è un neurotrasmettitore coinvolto nel normale sviluppo cerebrale. La D-serina,
poi, collabora con un L-amminoacido, il glutammato, nell’attivazione nei neuroni di alcune molecole essenziali per la plasticità sinaptica, una proprietà chiave, a sua volta, per l’apprendimento e la
formazione dei ricordi. Inoltre la D-serina sembra essere un fattore
importante in un disturbo complesso e molteplice come la schizofrenia. Le persone che ne soffrono hanno nel cervello minori quantità di questa molecola, e la scoperta ha spinto alcune aziende farmaceutiche a cercare il modo di incrementare i livelli di D-serina
in vista di possibili terapie. In altre circostanze, però, averne troppa può causare problemi. In chi è vittima di ictus, un suo eccesso
può portare a una maggiore gravità dei danni cerebrali. I ricercatori quindi cercano anche di sviluppare farmaci che abbassino i livelli di D-serina per mitigare i danni da ictus.
Le nostre fabbriche cellulari producono solo L-amminoacidi,
quindi i ricercatori si sono chiesti come mai nel nostro corpo ci
sia­no anche D-amminoacidi. Snyder ha trovato che le cellule cerebrali non sintetizzano la D-serina da zero, ma producono un
enzima che inverte la configurazione tridimensionale della serina
dalla forma L alla forma D, approfittando degli alti livelli di L-amminoacido già disponibili.
La stessa strategia è adottata nei casi in cui un D-amminoacido fa parte di un peptide, una breve catena di amminoacidi, come
nel veleno dell’ornitorinco. In questi casi i ribosomi sintetizzano
come al solito il peptide partendo dagli ordinari L-amminoacidi, e
poi un enzima modifica un particolare residuo della catena invertendone la configurazione dalla forma L a quella D. Potendo approfittare del macchinario cellulare con cui produce o accumula
gli L-amminoacidi, non c’è stato bisogno che si evolvesse l’intera
serie di enzimi biosintetici altrimenti necessaria a dare la molecola
destra, spiega Günter Kreil, chimico dell’Accademia delle scienze
di Vienna, che nel 2005 ha trovato un enzima usato da certe rane
arboricole velenose del Sud America per fabbricare i D-amminoacidi identificati nel loro veleno.
539 luglio 2013
Illustrazione di Jen Christiansen; consulenza grafico: Martin Ma, Johns Hopkins University School of Medicine
maggior parte delle piante e degli animali, e quindi non potrebbero lavorare al suo interno. Negli ultimi anni, però, sono spuntati composti destrogiri con attività biologica un po’ dappertutto:
dalle sostanze prodotte dalle aragoste per dare inizio al rapporto sessuale fino a una droga allucinogena usata da certi cacciatori
indigeni del Perù. La cosa più affascinante è che si è visto che alcuni amminoacidi destrogiri svolgono funzioni importanti nella
fisiologia umana, con grandi potenzialità per lo sviluppo di nuovi trattamenti per, tra l’altro, fibrosi cistica, schizofrenia e degenerazione maculare.
Solomon Snyder, neuroscienziato della John Hopkins University che ha effettuato molte delle prime ricerche sulle funzioni degli
amminoacidi destrogiri nel cervello, dice di aver incontrato notevoli resistenze quando si è trattato di pubblicare il suo primo lavoro in materia. Del resto, per Snyder questi composti erano interessanti proprio perché sembravano violare la «prima regola della
biologia dei mammiferi», per riprendere le sue parole. «Come spesso succede nella scienza, quando salta fuori qualcosa di veramente
nuovo o diverso c’è qualcuno che dice: “Ma è ridicolo”».
Nei fatti, invertire un amminoacido levogiro nella sua immagine speculare richiede solo pochi semplici passaggi biochimici. Era
dunque inevitabile, probabilmente, che l’evoluzione facesse qualche esperimento con questi composti. «La natura è sempre stata capace di usarli», dice Richard Losick, biologo cellulare alla Harvard
Medical School. «Siamo noi che lo abbiamo capito tardi».
www.lescienze.it
Le Scienze 71