INTOSSICAZIONI
ALIMENTARI
Vibrioni
Clostridium botulinum
Stafilococcus aureus
VIBRIONI PATOGENI
Le Vibrionaceae
La Famiglia delle Vibrionaceae comprende i generi: Vibro, Aeromonas,
Pseudomonas, e alcuni generi meno noti nell’ambito della microbiologia degli
alimenti come Catenococcus, Listonella, Moritella, Photobacter e
Photobacterium.
Il genere Vibro comprende bacilli:
Gram- di forma ricurva (0,5-0,8 µm di
larghezza e 2-3 µm di lunghezza)
Flagello polare monotrico
Metabolismo sia fermentativo che
respiratorio e non producono spore
Ossidasi+ e glucosio fermentanti
Buona crescita in terreni alcalini (pH 99.6)
Sono parte della flora batterica acquatica
autoctona
Le infezioni sono trasmesse per
contatto diretto con l’ambiente acquatico o
indirettamente attraverso cibo o acqua
contaminata
Vibrioni: sopravvivenza
nell’ambiente marino
Essendo autoctoni ambientali, i vibrioni sono
costretti
a
subire
profonde
e
frequenti
modificazioni
dell’ambiente
circostante
(temperatura,
concentrazione
dei
nutrienti,
salinità, pressione osmotica, pH, ecc…).
I vibrioni contrastano tali cambiamenti mediante
una serie di adattamenti di carattere fisiologico e
biochimico.
L’adattamento più interessante è l’ingresso in una
fase di quiescenza (i vibrioni restano vitali ma non
sono coltivabili, e pur mantenendo la loro
patogenicità, subiscono modificazioni morfologiche e
fisiologiche, quali dimensione, metabolismo e cicli di
divisione)
Sopravvivenza nell’ambiente marino:
fattori interferenti
L’isolamento di pressoché tutte le specie diventa
piuttosto raro quando la temperatura dell’acqua
<10°C (frequente >17°C);
Le specie delle acque estuarie e fluviali (V.
cholerae) tollerano salinità comprese tra 0-3%,
mentre i vibrioni tipici degli ambienti costali
risentono maggiormente delle concentrazioni di Na+
e crescono più rapidamente con salinità ≥3%;
I vibrioni sono molto sensibili alle condizioni acide
(la clorazione è usata come mezzo di prevenzione
per il colera);
L’associazione con zoo e fitoplancton (copecodi,
alghe verdi, cianoficee) e con macrofite (alghe
brune) permette ai vibrioni sopravvivenza più lunga
rispetto alle cellule freeliving.
Vibrionaceae associate con
malattie dell’uomo
Frequenza delle sindromi indotte da
Vibrionaceae
V. cholerae
È l’agente eziologico del colera
Riveste un ruolo fondamentale
per la salute pubblica a causa
della sua rapida diffusione in
aree
con
scarsa
igiene e
improprio
trattamento
delle
acque di scarico, e per le severe
conseguenze quando l’accesso
alle cure sanitarie è limitato
La
storia
moderna
caratterizzata da 7 pandemie
è
V. cholerae - Tassonomia
V. cholerae è diviso in oltre 130 sierogruppi (Ag.
somatico O)
Il sierogruppo O1 include i ceppi responsabili
dell colera epidemico ed è suddiviso in 2 biotipi
(Classico ed El Tor)
I biotipi non hanno significato tassonomico, ma
epidemiologico perché correlano con la severità
clinica dell’infezione (El Tor è meno severo e con un
maggior numero di casi asintomatici rispetto al
Classico)
I ceppi dei sierogruppi diversi da O1 (V. cholerae
non-O1) sono associati con casi sporadici di
gastroenterite e lievi forme simili al colera
Recenti epidemie, in India e Bangladesh, di una
nuova specie (V. cholerae O139 o V. cholerae
Bengala)
V. cholerae – La malattia (I)
È una diarrea secretoria causata dai ceppi tossigenici di V.
cholerae O1 e O139
La trasmissione avviene di solito per ingestione di cibo o
acqua contaminata (nelle persone sane la dose infettiva e alta,
108 batteri)
Dopo un periodo di incubazione di 12-72 ore si hanno i sintomi
clinici (diarrea acquosa profusa, nausea, crampi addominali e
febbre)
In assenza di una adeguata terapia reidratante, la perdita di
fluidi può portare rapidamente ad acidosi metabolica (perdita di
HCO3-), ipocaliemia, shock ipovolemico (perdita di K+), aritmia
cardiaca e morte
Solo una piccola % sviluppa la malattia, nella maggior parte è
asintomatica o si manifesta con sintomi lievi
V. cholerae – La malattia (II)
La modalità primaria di trasmissione è la via orofecale attraverso acqua contaminata
I pazienti nella fase acuta della malattia possono
espellere fino a 1013 batteri al giorno, per cui
possono determinare un sostanziale inquinamento
dell’ambiente. In questi casi il cibo contaminato con
acqua o feci è una importante via di trasmissione
secondaria.
• Paesi endemici
• Paesi non endemici
Il V. cholerae O1 può essere presente in riserve
naturali (autoctono) è causare casi sporadici privi di
contaminazione fecale.
V. cholerae – Patogenesi
La patogenesi è determinata da un insieme di
fattori di virulenza prodotti dai ceppi
tossigenici di V. cholerae O1 e O139:
- Enterotossina colerica (CT): che lega i
recettori gangliosidici GM1
- Pilo coregolato con la tossina (TCP):
tossina connessa al pilo importante fattore
di colonizzazione
Enterotossina colerica (CT)
V. parahaemolyticus
Distribuzione e concentrazione è influenzata da fattori
ambientali (salinità, temperatura) e dall’interazione con
forme di vita superiori dell’ambiente marino.
Vista la scarsa correlazione di questi batteri con
l’inquinamento fecale, la contaminazione dei prodotti della
pesca freschi (crostacei, molluschi, pesce) è strettamente
legata alla presenza naturale nell’ambiente (concentrazione
in genere intorno a 103/gr).
Negli adulti sani la dose infettante è >105 unità;
Epidemie e casi singoli sono associati a consumo di cibo
crudo o parzialmente cotto (crostacei cotti, molluschi crudi,
pesce) in quanto il batterio è molto sensibile al calore.
Fa parte della flora batterica autoctona nell’ambiente
marino costale nelle regioni tropicali e temperate di tutto il
mondo.
V. parahaemolyticus
Causa gastroenterite acuta;
Periodo di incubazione di 4-92 h (media 24 h);
I sintomi clinici comprendono diarrea (talora
sanguinolenta), dolore addominale, nausea, vomito,
possono essere intensi ma le morti sono rare;
I ceppi di V. parahaemolyticus sono classificati
come Kanagawa-positivi o Kanagawa-negativi in
base alla capacità di produrre TDH, una emolisina
termostabile diretta;
Producono varie sostanze emolitiche (emolisine,
citotossine, fattori di adesione).
V. vulnificus
A differenza di V. parahaemolyticus,
è in grado di dimorare anche in acque
fredde;
Le infezioni da V. vulnificus sono
sporadiche ed associate con il consumo
di ostriche;
La dose infettante è molto bassa in
alcuni gruppi con patologie predisponenti
(malattie
epatiche,
diabete,
immunodepressione)
o
con
comportamenti a rischio (abuso di
alcool)
Fa parte della flora batterica
autoctona nell’ambiente marino ed è
comunemente isolato dai molluschi;
Presente in concentrazione inferiore
rispetto a V. parahaemolyticus, anche
se può raggiungere concentrazioni di
105 cellule/gr in acque molto calde.
V. vulnificus
I sintomi delle infezioni alimentari si manifestano
principalmente al di fuori dell’intestino (febbre,
brividi e nausea, setticemia, lesioni cutanee alle
estremità del corpo);
Il periodo di incubazione (in media di 38 h) è
seguito da un rapido deterioramento delle
condizioni del paziente fino eventualmente alla
morte;
La grande invasività è legata a una notevole
varietà di fattori di virulenza che gli permettono di
evadere le difese dell’ospite:
- strato superficiale simile alla capsula (resistenza
alla fagocitosi)
- siderofori, in grado di strappare il Fe alle
sieroproteine (transferrina e lattoferrina)
- citolisina
V. vulnificus
A causa della grande invasività nei soggetti ad alto rischio
e della gravità dell’infezione che ne consegue è difficile
stabilire dei livelli di contaminazione accettabili;
Pertanto
piccole
concentrazioni
sono
già
considerate rischiose e alcune autorità alimentari
richiedono che ristoratori e rivenditori di ostriche crude
provenienti da zone note per essere naturalmente contaminate
con V. vulnificus pongano sul prodotto un avviso sanitario che
notifichi il rischio per certi individui;
Misure addizionali mirano a limitarne la concentrazione nelle
ostriche dopo la raccolta;
In alcuni stati le ostriche devono essere refrigerate entro
uno specifico tempo dalla raccolta, che è in funzione della
temperatura mensile media delle acque di crescita delle
ostriche (14h con T° H2O 18-23°C, 12h 23-28°C e 6 h
>28°C)
Trasmissione attraverso gli alimenti
La trasmissione è nota solo per il V. cholerae, perchè
soggetta a notifica obbligatoria (Classe I), e può
avvenire attraverso:
Acqua potabile contaminata;
Vegetali provenienti da coltivazioni irrigate con
acque reflue contaminate;
Piatti di carne, pesce e cereali cotti e poi
consumati
freddi
(dovuta
a
contaminazione
secondaria dei cibi, ovvero al trasporto dei
microrganismi attraverso la manipolazione dei cibi
dopo la cottura);
Bevande analcoliche non gassate (succhi di frutta,
latte di cocco) dovuta a contaminazione al momento
della preparazione per uso di acqua contaminata o
per scorretta manipolazione del prodotto.
Trasmissione attraverso gli alimenti
Escludendo le modalità di trasmissione del V.
cholerae, tutti i vibrioni indistintamente hanno
mostrato di avere un veicolo primario di
trasmissione nei prodotti della pesca (pesce,
granchi,
gamberi,
ecc…)
e
nei
molluschi
(soprattutto ostriche e cozze);
La normativa che regola la commercializzazione
dei molluschi (D. Lgs. 530/92) basa il giudizio di
idoneità solo sulla presenza di E. coli e Salmonelle,
rappresentativi di contaminazione fecale;
I vibrioni sono batteri autoctoni dell’ambiente
per cui non vi è corrispondenza tra le
concentrazioni di tali batteri e quelli degli
indicatori di contaminazione fecale.
Epidemiologia delle tossinfezioni da
vibrioni
Infezioni da V. cholerae
È al 3° posto come responsabile per numero di
casi di malattia collegati al consumo di molluschi;
L’ultima epidemia in Italia è stata nel 1973 con
278 casi di cui 28 letali;
A causa delle riserve ambientali all’interno dei
pesci, molluschi e plancton, c’è il potenziale per tali
ceppi patogeni di colonizzare nuove regioni;
Esiste anche il pericolo della mutazione di tali
ceppi.
Epidemiologia delle tossinfezioni da
vibrioni
Infezioni da V. parahaemolyticus
I molluschi notevolmente
consumati crudi;
rischiosi,
spt.
se
È particolarmente pericoloso nel corso dei mesi
estivi, durante i quali l’aumento della temperatura
delle acque di raccolta favorisce la sua
proliferazione;
L’assenza
dell’obbligo
di
denuncia
per
tossinfezioni diverse da quelle coinvolte da V.
cholerae rende difficile appurare il reale impatto
di tali patogeni sulla popolazione.
Epidemiologia delle tossinfezioni
da vibrioni
Infezioni da V. vulnificus
Non provoca di regola epidemie ma solo episodi
sporadici;
Non sono mai stati riportati casi di infezione
collegabili
alla
medesima
sorgente
alimentare
(probabilmente perché risulta particolarmente infettivo
nei confronti di individui con particolare suscettibilità);
L’incidenza totale delle infezioni da non è chiaramente
determinata (nel 1997-1998 negli USA su un totale di
937 casi di infezioni da vibrioni, 141 erano causate da
V. vulnificus, con 41 decessi).
Tossinfezioni in Italia
Gli studi condotti sui molluschi
hanno
evidenziato
un’incidenza
variabile dal 9,6% al 48,4% (con
completa assenza di Salmonelle e
coliformi)
Prevenzione
Cottura a fondo degli alimenti di origine
marina;
Separazione degli ambienti adibiti alla
manipolazione di cibi crudi da quelli
utilizzati per cibi cotti;
Preparazione del personale addetto alla
manipolazione di cibi crudi e cotti;
Rapido consumo dei prodotti ittici cotti.
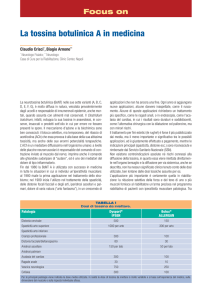
CARATTERISTICHE BIOCHIMICHE DELLE
VIBRIONACEAE
CARATTERISTICHE DI V. PARAHAEMOLYTICUS
E DI V. VULNIFICUS
CARATTERISTICHE DI V. PARAHAEMOLYTICUS E
DI V. VULNIFICUS
Colonie di V. cholerae
(gialle) su TCBS
(tiosolfato-citrato-sali biliari-saccarosio)
V. cholerae
Fig.1. Cellule di V. cholerae 01
(ATCC 14035) colorate con
acridina orange
Fig.2. Cellule di V. cholerae 01
(ATCC 14035) colorate con
acridina orange dopo 6 ore di
incubazione
con
acido
nalidixico
(metodo
di
Kogure’s)
Fig.3. Cellule di V. cholerae 01
(ATCC 14035) colorate con
isotiocianato di fluorosceina
coniugato con Ab fluorescenti
Ricerca mediante metodi molecolari
PCR:
V. cholerae:
-Operone ctx, responsabile della produzione della tossina
colerica,
-gene tcpA, codificante per il pilo coregolatorio con la tossina
-gene sto codificante per una enterotossina termostabile
V. parahaemolyticus
-geni tdh e trh codificanti per le tossine
V. Vulnificus
-gene cth codificante per l’emolisina-citolisina
Uno dei limiti della PCR e che non è in grado di evidenziare la
vitalità di un microrganismo. Poiché solo i batteri vitali sono in grado
di dare tossinfezioni, un alimento contenente microrgnismi non vitali
potrebbe essere erroneamente dichiarato pericoloso dopo analisi con
PCR, tuttavia un campione con una concentrazione (104 cfu/g) è
estremamente improbabile.
I Clostridi
FAMIGLIA: Bacillaceae
Comprende microrganismi sporigeni;
Comprende numerosi “generi”, tra cui 2 importanti
per la patologia umana:
Clostridium
Bacillus
GENERE: Clostridium
BACILLI, GRAM +, SPORIGENI, RELATIVAMENTE GRANDI,
ANAEROBI OBBLIGATI:
i) non producono enzimi in grado di inattivare i prodotti tossici
dell’azoto e dell’ossigeno (catalasi, perossidasi, superossido
dismutasi ecc.);
ii) hanno enzimi che operano bene solo allo stato ridotto.
UBIQUITARI: si moltiplicano nel lume intestinale degli erbivori e le
spore, emesse con le feci, contaminano l’ambiente sopravvivendo
a lungo (possono essere sparse con il vento e sono presenti nella
polvere)
ALCUNE SPECIE ELABORANO POTENTI
ESOTOSSINE
C. tetani: Agente eziologico del TETANO; Tossina tetanica
(tetanospasmina)
C. botulinum: Agente eziologico del BOTULISMO, una grave
intossicazione alimentare; Tossina botulinica
C. perfringens: Agente eziologico della GANGRENA GASSOSA,
una grave patologia che si sviluppa in seguito all'infezione di
ferite con spore. I microrganismi producono gas in seguito ai
processi di fermentazione ed elaborano numerose tossine ad
azione necrotizzante (es. tossina alfa)
C. difficile: Responsabile di una SINDROME DIARROICA
associata all'uso prolungato di antibiotici
I clostridi: batteri sporigeni
Clostridium tetani
Clostridium botulinum
Clostridium perfrigens
Clostridium difficile
anaerobi
Attecchimento e moltiplicazione favorita da:
1.
necrosi del tessuto e quindi diminuito afflusso di sangue e quindi
di O2
2.
presenza contemporanea di batteri aerobi
3.
Acatalasemia (diminuita concentrazione ematica di catalasi,
enzima che converte il perossido di idrogeno in acqua e ossigeno)
I clostridi: batteri sporigeni
bacilli Gram positivi di 3-8 mm di lunghezza
Sono
In gran parte mobili per la presenza di flagelli peritrichi
Raramente capsulati
Producono
terminale
spore
a
localizzazione
somatica
Clostridi
Vivono come saprofiti nel suolo
o nell’intestino di alcuni animali
Le infezioni
introduzione
profondi dei
all’assunzione
nell’uomo sono dovute ad
accidentale nei tessuti
clostridi o delle spore o
con alimenti di tossine
Clostriudium botulinum
Mortale nel 60% dei casi
Intossicazione dovuta ad ingestione di cibi (carni non cotte: la
tossina viene distrutta ad 80°C per 30 min.) contaminati e nei
quali il batterio si moltiplica producendo tossina. Raramente
nelle infezioni da ferite superficiali.
Sono stati identificati otto sierotipi del microrganismo (A, B,
C1, C2, D, E , F, G).I vari sierotipi hanno caratteristiche
diverse di patogenicità per gli uomini e gli animali, ciascuno di
essi elabora una tossina antigeneticamente distinta.
Può trovarsi anche nell’intestino di animali infettati attraverso
soluzioni di continuo della mucosa orale dell’animale a causa
dell’ingestione di foraggio contaminato
Clostriudium botulinum
Gli alimenti epidemiologicamente più importanti
sono le conserve alimentari artigianali, carni
conservate non cotte
Il batterio si moltiplica a livello intestinale e libera la
tossina. Il micro-ambiente intestinale (basso potenziale di
ossidoriduazione) permette il processo germinativo.
Tossina: viene assorbita a livello intestinale (non è
inattivata dagli enzimi proteolitici) e agisce a livello della
giunzione neuromuscolare
Impedisce la
conseguente
trasmissione
dell’impulso
paralisi flaccida
nervoso,
con
(BoNT)
Le neurotossine botuliniche sono i più
potenti veleni noti e sono la causa di
tutti i sintomi di una malattia
neuroparalitica, nota come
botulismo.
Un milligrammo di tossina purificata è sufficiente
per uccidere oltre un milione di cavie !
(BoNT)
La tossina botulinica è rappresentata da una
serie di 8 tossine A-B tra loro correlate.
La produzione di tossina in alcuni ceppi
dipende da geni localizzati su specifici
batteriofagi lisogeni
La tossina principale è una proteina con un
peso molecolare di circa 150 000 che forma
complessi con proteine botuliniche non
tossiche per dare una tossina bioattiva di
peso molecolare di circa 106
(BoNT)
• Viene sintetizzata sottoforma di un
polipeptide monocatenario
• Viene intaccata dalle proteasi endogene
(o dalla tripsina nell’intestino) e
convertita in un polipeptide a doppia
catena
(H=pesante
ed
L=leggera)
diventando attiva
Sito di legame: porzione carbossi-terminale catena H
Dominio formante canale: porzione amino-terminale catena H
Dominio tossico: catena L
Vescicole contenenti acetil-colina
B
A
A
Fibra muscolare
La tossina impedisce il rilascio
dell’acetilcolina dalle vescicole
Stimolazione muscolare BLOCCATA
PARALISI FLACCIDA
Morte per paralisi della muscolatura respiratoria
Clostriudium botulinum
Botulismo del lattante: morte improvvisa del
neonato (a causa della peculiare popolazione
batterica nei primi giorni dopo la nascita)
Botulismo da ferita
Negli Stati Uniti si osservano 110 casi di botulismo
per anno (dei quali il 25% sono dovuti ad
ingestione di cibo, 72% sono infezioni del neonato
(miele, polvere, sporcizia) e il rimanente sono
dovute a ferite)
Clostriudium botulinum
Sintomi:
da 6 ore a 2 settimane (in media 12- 36 ore)
dopo l ‘ ingestione del cibo.
Diplopia, difficoltà di linguaggio e di deglutizione, debolezza
muscolare dalle spalle, al tronco fino agli arti inferiori.
Paralisi respiratoria
Le alterazioni a livello respiratorio e la successiva paralisi
possono richiedere la necessità della terapia intensiva per
settimane
Diagnosi: Ricerca della tossina nell’alimento (inoculazione in
topi)
Terapia: Sieroprofilassi
Se
diagnosticata presto, i casi vengono trattati con
anatossina in grado di bloccare la tossina circolante
Possono essere usati anche degli emetici per l’eliminazione
meccanica del cibo.
Clostridium perfrigens
• Gangrena gassosa
• Intossicazioni alimentari
Clostridium perfrigens
Intossicazioni alimentari
Ingestione di cibi in cui sia presente la tossina
(p.i. 8 a 24 ore, mediamente 12 ore)
Sintomatologia: diarrea e vomito
Alcuni stipiti di C. perfrigens sono in grado di
elaborare una tossina enterotossica che si produce
solo in condizioni in cui sia possibile la sporulazione.
Questa tossina è infatti associata alla tunica
sporale con caratteristica di superantigene.
Intossicazioni alimentari da C. perfrigens
Ceppi enterotossici di C.perfrigens
con tossina enterotossica associata alla tunica sporale
Ingestione cibi contaminati (carni) dalle forme vegetative o dalle spore
Sporulazione e localizzazione all’intestino tenue e produzione tossina
Aumento permeabilità capillari con diarrea, dolore e vomito
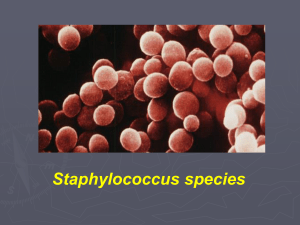
Lo stafilococco patogeno
Staphylococcus aureus. Electron micrograph from Visuals Unlimited, with permission.
Nomenclatura
Esistono oltre 20 specie diStaphylococcus
Staphylococcus aureus
PATOGENI
Staphylococcus epidermidis
Colorazione di Gram
di Staphylococcus aureus in essudato
E’un batterio Gram+, asporigeno,
della famiglia delle Staphylococcaceae,
compreso nel Genere Staphylococcus.
fermenta glucosio e mannitolo
catalasi positivo
coagulasi positivo
colonie giallo oro su agar
Staphylococcus aureus
• Crescono bene in comuni terreni di coltura.
• Sono aerobi-anaerobi facoltativi, con la possibilità
d'utilizzo del sistema dei citocromi in presenza di
ossigeno e della fermentazione in anaerobiosi.
• Presentano una notevole alofilia sviluppo anche in
ambienti che vedono un'elevata concentrazione (7,5%)
di NaCl
Determinanti di virulenza
Gli strumenti dell'azione patogena di S. aureus sono vari
• (1) proteine di superficie che promuovono la colonizzazione dei
tessuti dell’ospite (proteine leganti la laminina e la
fibronectina)
• (2) invasine che promuovono la diffusione dei batteri (leukocidin,
kinases, hyaluronidase);
• (3) fattori di superficie che inibiscono la fagocitosi (capsule,
Protein A);
• (4) proprietà biochimiche che favoriscono la sopravvivenza nei
fagociti (carotenoids, catalase);
• (5) fattori che determinano alterazioni immunologiche (Protein
A, coagulase, clumping factor);
• (6) esotossine capaci di danneggiare le cellule eucariotiche
favorendo la diffusione ai tessuti limitrofi (ma anche distanti) al
luogo dell'infezione primaria. (hemolysins, leukotoxin, leukocidin,
SEA-G, TSST, ET)
• (7) resistenza agli agenti antimicrobici (MRSA Methicillin
resistant Staphylococcus aureus).
Virulence determinants of
Staphylococcus aureus
La capsula
La
capsula
polisaccaridica
è
fondamentalmente composta da un
polimero di acidi uronici.
Il suo potere antifagocitario protegge i
batteri dall'azione dei neutrofili.
Sono almeno 13 i polisaccaridi distinguibili, dei
quali i tipi capsulari 5 e 8 sono posseduti dalla
maggioranza (85%) dei batteri isolati
nell'uomo.
clumping factor
Alla superficie della cellula batterica sono presenti
diverse proteine. Esse possiedono la capacità di
interagire
con
altre
strutture
proteiche
dell'organismo umano (per esempio il fibrinogeno, il
plasminogeno, la laminina ecc.). Queste proteine,
proprio per la capacità posseduta, fungono da adesine.
Tra queste va ricordata una proteina denominata
clumping factor che interagisce con il fibrinogeno,
legandolo e inducendone la precipitazione sulla
superficie della cellula batterica. Sul vetrino, in
conseguenza di ciò è possibile notare ammassi di
cellule batteriche (da cui deriva il termine clump ). Per
osservarli si deve mescolare su un apposito vetrino
una goccia di plasma con un'altra goccia di una
sospensione densa di stafilococchi.
La proteina A
Situata nella parete cellulare, può legare la
porzione (Fc) di alcune immunoglobuline
provocando diverse conseguenze:
1. Inibizione della fagocitosi del batterio,
2. Attivazione
del
sistema
del
complemento
3. Reazioni
di
stimolazione
della
moltiplicazione linfocitaria.
Patogenesi
S. aureus è responsabile di infezioni suppurative acute
che possono essere dislocate in diversi distretti
dell'organismo.
cute
apparato scheletrico
apparato respiratorio
apparato urinario
sistema nervoso centrale
Alcuni stipiti batterici possono provocare inoltre
intossicazioni e manifestazioni morbose di vario tipo
a causa di alcune caratteristiche esotossine che sono
in grado di produrre.
Siti di infezione e malattie causate da
Staphylococcus aureus
Le tossine di S. aureus
Le citolisine o emolisine α (la più diffusamente prodotta), β, γ e δ e la
leucocidina-PV: prodotte nelle infezioni suppurative
La tossina epidermolitica (ET detta anche esfoliatina stafilococcica A o
B). Essa provoca la <<sindrome della cute ustionata da stafilococco>>
o malattia di Lyell (prima infanzia) o malattia di Ritter (neonato).
L'enterotossina, che provoca delle gastroenteriti in seguito
ad una intossicazione di tipo alimentare causata da
assunzione di cibi, ricchi di lipidi (come crema o panna,
favorenti la crescita dei batteri) nei quali sia stata
prodotta una certa quantità di enterotossina.
La tossina dello shock tossico, causa del cosiddetto shock tossico da
stafilococco che vede la comparsa di sintomi gravi generalizzati,
manifestazioni eritematose e sintomi da shock emodinamico. La
mortalità è molto elevata.
Superantigeni: enterotossina e tossina
della sindrome da shock tossico
• enterotossina, di cui esistono 6 tipi antigenici
(SE-A, B, C, D, E e G): sono termostabili
• toxic shock syndrome toxin (TSST-1).
Stimolazione non specifica delle cellule T
da parte dei Superantigeni
Superantigens bind directly to class II major histocompatibility
complexes (MHC II) of antigen-presenting cells. The T cells may
be activated. Cytokines are released in large amounts, causing the
symptoms of toxic shock.
Gli enzimi di S. aureus
la coagulasi stafilococcica che agisce sul fibrinogeno
trasformandolo in fibrina (senza calcio). Significato
ancora incerto, ma prodotta praticamente sempre
nelle infezioni in atto.
la stafilochinasi che trasforma plasminogeno in
plasmina. Il significato è di aumentare la capacità
invasiva (superamento di ostruzioni meccaniche come
coaguli nei capillari).
le lipasi che consentono l'utilizzo di lipidi e le nucleasi
per l'idrolisi di acidi nucleici.
la jaluronato-liasi (aumenta l'invasività del batterio).
Abbatte, infatti, le barriere di jaluronati del tessuto
connettivo.
ureasi e serino-proteasi.
Metodi di identificazione
Esame colturale. 24-48 ore alla temperatura di 37 °C.
Cresce bene nei normali terreni. Tuttavia è meglio
utilizzare piastre di agar-sangue di coniglio che
evidenziano aloni di emolisi intorno alle colonie di
stafilococco.
In alternativa, sfruttando l'alofilia del batterio, si
utilizzano piastre di agar in cui NaCl sia concentrato al
7.5% in modo da inibire la maggioranza degli altri
batteri. Si può poi aggiungere uno zucchero e un
indicatore di pH ottenendo così il viraggio
dell'indicatore in seguito alla produzione di acidi a
causa della fermentazione dello zucchero operata
dallo stafilococco.
Con la colorazione di Gram si potrà osservare, in caso di
colonie di S. aureus, la classica disposizione a
grappolo e la colorazione Gram positiva.
AGAR MS (salato al mannitolo)
Utilizzato per isolare Stafilococchi patogeni.
E’ selettivo perché presenta una elevata concentrazione di NaCl che
inibisce la maggior parte dei batteri tranne quelli sale-tolleranti come gli
Stafilococchi.
Il mannitolo rende il terreno differenziale: questo zucchero infatti viene
fermentato dagli Stafilococchi che daranno origine a colonie giallastre
L’acido prodotto dalla fermentazione del mannitolo determina il viraggio
dell’indicatore di pH (rosso fenolo ) da rosso (alcalino ) a giallo (acido).
Gli stafilococchi non patogeni sono capaci di crescere sul mezzo ma non
producono acido.
Stafilococchi su AGAR SALE MANNITE
terreno utilizzato per l’isolamento di Stafilococchi patogeni
CONTIENE: 7.5% NaCl che inibisce la crescita della maggior
parte degli altri microrganismi e LA MANNITE COME UNICA
FONTE DI CARBONIO
TOLLERANO ELEVATE CONCENTRAZIONI DI NaCl (germi ALOFILI)
LA MAGGIOR PARTE DEI CEPPI PATOGENI FERMENTA LA MANNITE
S. epidermidis:
colonie alcaline
(rosa)
non fermentanti la
mannite
S. aureus:
colonie acidificanti per
fermentazione della
mannite e viraggio al
giallo dell’indicatore
rosso fenolo
Metodi di identificazione
La differenziazione è richiesta rispetto agli stafilococchi non
patogeni, agli streptococchi ed ai micrococchi.
S. aureus si differenza delle altre specie non patogene
(S. epidermidis) in quanto positivo al test per la
coaugulasi, e per l’emolisi su blood agar
S. aureus si distingue dagli streptococchi per la
produzione di catalasi.
Si distingue dai micrococchi, poiché questi ultimi non
sono in grado di fermentare zuccheri, essendo aerobi
obbligati.
Metodi di identificazione
Altre prove utilizzabili sono quelle di agglutinazione
passiva mirate verso la proteina A e il clumping factor.
Infine è possibile anche l'identificazione precisa degli
stipiti produttori di una determinata tossina,
ricercando appunto la stessa nel liquido di coltura del
campione in esame. Per fare ciò si utilizzano tecniche
di agglutinazione passiva (con l'impiego di piccole
particelle di lattice la cui superficie viene ricoperta
previamente di anticorpi anti-tossina) ma anche
attraverso l'impiego di tecniche immunoenzimatiche.
Terapia
L'antibiotico-resistenza è una caratteristica
spesso frequente di questi batteri, specie
nelle
cosiddette
infezioni
nosocomiali,
costituendo un problema da non sottovalutare.
Il fenomeno della resistenza è sempre più
diffuso e in rapida ascesa.
Cefalosporine e penicilline non sono più efficaci.
Ceppi resistenti a Vancomicina e Meticillinoresistenti sono frequenti.
La determinazione della corretta scelta
terapeutica deve basarsi necessariamente
sull'antibiogramma.