Review
GLI OPPIOIDI
E I LORO RECETTORI PERIFERICI
OPIOIDS AND THEIR PERIPHERAL RECEPTORS
Francesco Amato
Direttore Unità Anestesia e Terapia del Dolore
AO Cosenza
RIASSUNTO
La flogosi dei tessuti periferici induce
nei neuroni afferenti primari,
in particolare a livello corpi cellulari
situati nei DRG (gangli della radice
dorsale) un aumento della sintesi
di recettori oppioidi determinandone
un “up-regulation”.
Dopo che i recettori oppioidi vengono
trasportati a livello delle terminazioni
nocicettive essi vengono incorporati
nella membrana neuronale diventando
recettori funzionali.
Le suddette proteine recettoriali vanno
a legarsi agli oppioidi prodotti
dalle cellule immunitarie o a quelli
esogeni. Questi legami portano
a una diretta o indiretta soppressione
delle correnti di Ca2+ indotte
da TRPV1 o di correnti del Na+,
con conseguente ridotta eccitabilità
del neurone e diminuzione
dei segnali trasmessi.
L’osservazione che il sistema
immunitario sia in grado di modulare
il dolore mediante ligandi che
interagiscono con i recettori oppioidi
localizzati sui neuroni sensoriali,
può avere ampie implicazioni
per lo sviluppo di farmaci antidolorifici
innovativi e più sicuri.
Parole chiave
Recettori oppioidi, recettori transienti,
beta arrestin, farmaci antidolorifici
innovativi
SUMMARY
The inflammation of peripheral tissues
leads the primary afferent neurons,
in particular at the cell bodies level
located in the DRG (dorsal root
ganglia), to an increased synthesis
of opioid receptors: determining
an “up-regulation”.
After that opioid receptors
are transported at the level
of the nociceptive terminals,
they are incorporated into
the neuronal membrane
becoming functional receptors.
The above receptor proteins bind
to opioid produced by immune cells
or the exogenous ones. This leads
to a direct or indirect suppression
of the Ca2+ currents induced by
TRPV1 or the currents of the Na+,
resulting in neuronal reduced
excitability and in transmitted
signals decrease.
The observation that the immune
system is able to modulate the pain
by ligands that interact with the
opioid receptors located on sensory
neurons, may have broad implications
for the development of innovative
and safer pain drugs.
Key words
Opioid receptors, transient receptors,
beta arrestin, innovative analgesic drugs
Volume 19 Pathos Nro 4, 2012
9
Nel sistema nervoso periferico i neuroni sensoriali primari possono essere
attivati da segnali nocicettivi di tipo
termico, meccanico o chimico attraverso l’apertura di molti canali ionici
che creano un cancello non voltaggio
dipendente. I canali ionici coinvolti
in questo processo sono:
1 - canali sodio Toxin - tetratoxin resistant (TTX, Nav 1.7, Nav 1.8, Nav
1.9), degenerin-epithelial (MDEG),
acid-sensing ion channels (ASIC).1
2 - ATP - sensitive purine receptors
(P2X3).2
3 - Canali calcio: transient receptor
potential vanilloid ion channels: TRIPV1, TRIPV2, TRIPV3, TRPM8,
TRIPA1.3
I recettori “Transient” rispondono oltre che ai diversi livelli termici anche
ad altre modalità di stimoli, agendo
da “sensori del dolore”.4
Il terminale della fibra C presenta una
grande complessità, infatti, per ogni
livello di sensazione è presente uno
specifico sistema di trasduzione.5-8
L’attivazione dei recettori attiva poi la
scarica dei potenziali di azione (Pd’A)
condotti dagli assoni che trasmettono
l’informazione lungo il sistema sensoriale.
In presenza di un dolore acuto così
detto “fisiologico”, solo il 20 per cento della popolazione dei nocicettori
viene attivata; mentre solo durante
un’infiammazione cronica o una lesione tessutale molto forte, che dura
a lungo, si ha un’attivazione del 100
per cento. In particolare durante una
flogosi o una lesione nervosa, la liberazione di sostanze lungo i terminali
periferici provoca evidenti modificazioni, strutturali e/o funzionali.
Queste modificazioni sono dovute al
rilascio di idrogenioni che realizzano
10
uno stato di acidosi locale con riduzione del pH dei tessuti circostanti. A
questo accumulo di H+ si accompagna quello delle sostanze provenienti
dalle cellule danneggiate (K+, ATP,
metaboliti dell’acido arachidonico,
così come delle COX2, PGE2), di
neurotrasmettitori delle fibre C (SP,
CGRP), di sostanze modulatrici delle cellule della GLIA (NGF; GDNF)
o di sostanze, come la bradichinina
(BK) proveniente da cellule vascolari danneggiate. Una miriade di mediatori, dunque, presenti nel tessuto
danneggiato sono coinvolti nei processi infiammatori, che si associano
ad una lesione tissutale e/o alla lesione di un nervo o a un’abnorme reattività immunitaria.
L’attivazione dei nocicettori e la trasduzione dei segnali nocicettivi, che
avviene in recettori come il TRPV1,
o il recettore Purinico P2X3, o il
meccanorecettore DEG, ha come risultato finale una depolarizzazione
della membrana cellulare, che genera
veloci potenziali di azione che lungo
l’assone dell’afferente primario, rag-
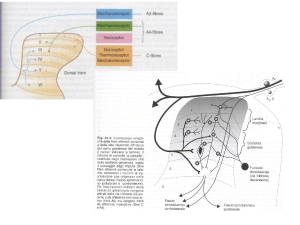
Figura 1
Dopo una noxa patogena e la sensibilizzazione degli afferenti primari nel ganglio
della radice dorsale vengono sintetizzati i recettori oppioidi e i neuropeptidi
(come la sostanza P). Tutti vengono poi trasportati lungo i microtubuli intra-assonali
fino alla periferia del neurone afferente primario. A questo livello i recettori oppioidi
vengono incorporati nella membrana neuronale resa più impermeabile e diventano
recettori funzionali. Dopo l’attivazione con oppioidi esogeni o endogeni, si ha
l’inibizione della G-proteina. Questo porta alla diretta o indiretta (tramite la riduzione
dell’adenosina monofosfato ciclico) soppressione delle correnti del Ca2+ o Na+
e conseguente attenuazione del rilascio della sostanza P.
Ganglio della radice dorsale
Midollo spinale
Assone
Sostanza P
Recettori
degli oppioidi
Canali del sodio
cAMP
Microtubuli
Proteina G
Oppioidi
Canali del calcio
Volume 19 PATHOS Nro 4, 2012
giungono i neuroni del corno posteriore del midollo spinale.9-10
Per quanto riguarda il processo di
sensibilizzazione periferica esso molto
verosimilmente è sostenuto dall’attività di diverse sostanze:
- dalla bradichinina che è un mediatore coinvolto in una serie di processi fisiopatologici compreso il dolore
cronico;11
- dal Nerve Growth Factor (NGF)
che va a legarsi al recettore TrKA (tirosin chinasi A). Dopo una lesione
(noxa) sono necessari i fattori di crescita come il nerve growth factor per
riparare il danno, ma in molti casi le
neurotrofine hanno solo scopo puramente flogistico, ovvero di irritazione
locale, che agirà nel tempo come richiamo di leucociti e citochine antiinfiammatorie;12
- da alcuni impulsi che possono viaggiare in senso anterogrado lungo l’assone periferico del neurone sensoriale
periferico, verso i terminali nervosi
distali, con il risultato di rilasciare
neuropeptidi nella zona lesa. Questo rilascio di neuropeptidi provoca
vasodilatazione, permeabilità vasale
venosa, stravaso di plasma, edema e
arrivo di leucociti :“infiammazione
neurogenica”.13
- dalle sostanze prodotte dal sistema
immunitario come l’istamina.14
Elettrofisiologicamente, questa sensibilizzazione è caratterizzata da aumento dell’eccitabilità neuronale (aumento della frequenza di scarica), aumento di risposte agli stimoli nocicettivi e diminuita soglia per gli stimoli
termici e meccanici. Mentre i segnali
nocicettivi si propagano dal neurone
sensoriale primario al midollo spinale
prima ed al cervello poi, dove sono
percepiti come dolore, contempo-
raneamente si attivano meccanismi
endogeni per neutralizzare il dolore
e controllare la situazione infiammatoria.
La flogosi dei tessuti periferici, infatti, porta a livello dei neuroni afferenti primari, in particolare nei corpi
cellulari collocati nei DRG (dorsal
root ganglion), a un incremento della
sintesi di recettori oppioidi: determinando un “up-regulation” dei suddetti recettori .
I recettori degli oppioidi, ma anche
i neuropeptidi (come la sostanza P)
pro-nocicettivi e pro-infiammatori,
dopo essere stati sintetizzati dal ganglio della radice dorsale vengono trasportati lungo microtubuli intra-assonali nei processi centrali e periferici
del neurone primario afferente.
Nel tessuto infiammato la permeabilità del perinevrio aumenta permettendo l’accessibilità dei recettori
oppioidi nella membrana cellulare a
livello distale (Figura 1).15-17
Dunque i neuroni sensoriali periferici
esprimono recettori per i peptidi oppioidi, che possono essere modulati
dagli oppioidi endogeni o dai farmaci
oppiacei. In seguito agli stimoli stressogeni o in risposta ad agenti che rilasciano sostanze come il CRF (Corticotropin Releasing Factor), citochinine, chemochine e catecolamine, i
leucociti secernono oppioidi.
Il legame di peptidi oppioidi, derivati
da cellule immunitarie o di oppiacei
esogeni, rispettivamente con i recettori periferici determina il loro accoppiamento con una proteina G trimerica, che si dissocia nelle seguenti
subunità :
- Complesso G-α
- Complesso G-βγ
Queste subunità inibiscono le adenil-
Volume 19 Pathos Nro 4, 2012
ciclasi e di conseguenza inibiscono la
produzione di c-AMP o interagiscono
direttamente con differenti canali ionici della membrana.18 Questo porta
a una diretta o indiretta (tramite diminuzione di adenosina monofosfato
ciclico) soppressione delle correnti di
Ca2+ indotte da parte dei TRPV1 o
di correnti del Na+, con conseguente ridotta eccitabilità del neurone e
diminuzione dei segnali trasmessi.
Successivamente, il rilascio di SP è
attenuato.
In particolare, all’interno del tessuto leso, questi eventi realizzano un
effetto antinocicettivo e antiinfiammatorio. Così il controllo autogeno
del dolore è realizzato dal legame di
peptidi oppioidi, derivati da cellule
immunitarie, con i recettori degli oppioidi presenti sui neuroni sensoriali
periferici. Il concetto che il sistema
immunitario sia in grado di modulare
il dolore mediante ligandi che interagiscono con i recettori oppioidi presenti sui neuroni sensoriali, può avere
ampie implicazioni per lo sviluppo di
farmaci antidolorifici più sicuri.19
L’osservazione che l’infiammazione
dei tessuti periferici porta ad una
maggiore funzionalità dei recettori
oppioidi sulla superficie dei neuroni
sensoriali distali e alla produzione
locale di peptidi oppioidi endogeni
indica nuove applicazioni. A questo
punto bisogna prendere in considerazione il perché si verifichino fenomeni di tolleranza legati agli oppioidi. Secondo gli studi condotti da
Laura Bohn20, l’attenzione si focalizza
su un particolare processo a cui si associano direttamente gli effetti collaterali (side effects). È stato osservato
come una proteina denominata ‘beta
arrestin’20 determini la invaginazione
11
del bilayer fosfolipidico della membrana dove è posizionato il recettore
oppioideo, dopo essere stato attivato
dal proprio ligando.
Esso poi viene riciclato o degradato
nei lisosomi. Quali obiettivi si possono perseguire in futuro?
Da quanto esposto finora, si evince
che gli obiettivi da raggiungere potranno riguardare le seguenti finalità:
1 - lo sviluppo e l’applicazione periferica di agonisti oppiacei;
2 - il targeting selettivo delle cellule
immunitarie contenenti oppiacei sui
siti di lesione dolorosa;
3 - l’ottimizzazione della selettività
delle cellule contenenti oppioidi a livello della ferita e l’incremento della
sintesi dell’oppioide periferico attraverso la genetica (ad esempio con la
terapia genica);
4 - un intervento mirato sulla beta
arrestin;
5 - la diminuzione dell’attività dei
recettori TRPV1 in fase di sensibilizzazione.
La ricerca futura si soffermerà sulla
farmacologia e biologia molecolare
per lo sviluppo di nuovi farmaci selettivi, allo scopo di ottenere una scelta
razionale dei trattamenti individuali
dei singoli i pazienti, per realizzare,
infine, una combinazione di farmaci
innovativi che consentano di ottimizzare i benefici e minimizzare i rischi
associati alla terapia con oppioidi.
L’obiettivo finale è quello di evitare gli effetti collaterali negativi degli
analgesici attualmente disponibili,
quali depressione respiratoria, deficit
cognitivo, dipendenza, sanguinamento gastrointestinale e complicanze
tromboemboliche.
12
BIBLIOGRAFIA
1) Schuelert N, McDougal JJ. Involvement of
Nav 1.8 sodium ion channels in the transduction of mechanical pain in a rodent model of
osteoarthritis. Arthritis Research & Therapy
2012, 14:R5 doi:10.1186/ar3553. Published: 7
January 2012.
2) Gum R, Wakefield B, Jarvis M. P2X receptor
antagonists for pain management: examination
of binding and physicochemical properties. Purinergic Signalling (16 November 2011), pp. 1-16.
3) Nilius B, Owsianik G. The transient receptor
potential family of ion channels. Genome Biol.
2011; 12 (3): 218. Epub 2011 Mar 17. Review.
4) Bang S, Yoo S, Yang TJ, Cho H, Hwang SW.
Nociceptive and proinflammatory effects of dimethylallyl pyrophosphate via TRPV4 activation. DOI: 10.1111/j.1476-5381.2012.01884.x
5) Merck Manual Home Health Handbook.
Overview of pain (updated Aug 2007). http://
www.merckmanuals.com/home/brain_spinal_
cord_and_nerve_disorders/pain/overview_of_
pain.html (accessed Mar 2012).
6) Merck Manual Home Health Handbook.
Types of pain (updated Aug 2007). http://www.
merckmanuals.com/home/brain_spinal_cord_
and_nerve_disorders/pain/types_of_pain.html
(accessed Mar 2012).
7) Physiology and pathophysiology of pain (revised September 2007). In: eTG complete. Melbourne: Therapeutic Guidelines Limited; 2011
Nov. http://online.tg.org.au/complete/ (accessed
Mar 2012).
8) Types of pain (revised February 2010). In:
eTG complete. Melbourne: Therapeutic Guidelines Limited; 2011 Nov. http://online.tg.org.
au/complete/ (accessed Mar 2012).
9) Levine JD, Alessandri-Haber N. TRP channels: targets for the relief of pain. Biochim Biophys Acta. 2007 Aug; 1772 (8): 989-1003. Epub
2007 Jan 23.
10) Rech JC, Eckert WA, Maher MP, Banke T,
Bhattacharya A, Wickenden AD. I Recent advances in the biology and medicinal chemistry of
TRPA 1. Future Med Chem. 2010 May; 2 (5):
843-58.
11) Zhang X, Huang J, McNaughton PA.
NGF rapidly increases membrane expression of
TRPV1 heat-gated ion channels. The EMBO
Journal (2005) 24, 4211 – 4223. doi:10.1038/
sj.emboj.7600893. Published online: 1 December 2005.
12) Clifford J, Woolf M, Qiufu M. NociceptorsNoxious Stimulus Detectors Neuron, Volume
55, Issue 3, 353-364, 2 August 2007.
13) Park CK, Lü N, Xu ZZ, Liu T, Serhan CN,
Volume 19 Pathos Nro 4, 2012
Ji RR. Resolving TRPV1 and TNF-α Mediated
Spinal Cord Synaptic Plasticity and Inflammatory Pain with neuroprotectin D1. J Neurosci.
2011 October 19; 31 (42): 15072–15085.
14) Marchand F, Perretti M, McMahon SB. Role
of the Immune system in chronic pain. Nature
Reviews Neuroscience 6, 521-532 (July 2005).
doi:10.1038/nrn1700
15) Stein C, Clark JD, Oh U, Vasko MR, Wilcox GL, Overland AC et al. Peripheral mechanisms of pain and analgesia. Brain Res Rev 2009,
60: 90-113.
16) Busch-Dienstfertig M, Stein C. Opioid receptors and opioid peptide-producing leukocytes
in inflammatory pain. Basic and therapeutic
aspects. Brain Behav Immun. 2010 Jul; 24 (5):
683-94. Epub 2009 Oct 29. Review. PMID:
19879349 [PubMed - indexed for MEDLINE).
17) Hua S, Cabot PJ. Mechanisms of peripheral
immune-cell-mediated analgesia in inflammation: clinical and therapeutic implications. Trends Pharmacol Sci. 2010 Sep; 31 (9): 427-433.
Epub 2010 Jun 28.
18) Cunha TM et al. Morphine peripheral analgesia depends on activation of the PI3Kgamma/
AKT/nNOS/NO/KATP signaling pathway.
Proc Natl Acad Sci USA. 2010 Mar 2; 107 (9):
4442-4447. Epub 2010 Feb 10.
19) Stein C, Machelska H. Modulation of Peripheral Sensory Neurons by the Immune System:
Implications for Pain Therapy. Pharmacol Rev
December 2011 63:860-881.
20) Nguyen PT, Schmid CL, Raehal KM, Selley
DE, Bohn LM, Sim-Selley LJ. β-arrestin2 regulates cannabinoid CB1 receptor signaling and
adaptation in a central nervous system regiondependent manner. Biol Psychiatry. 2012 Apr
15; 71 (8): 714-724. Epub 2012 Jan 20.