• Nelle cellule, le singole reazioni enzimatiche fanno
parte di sequenze a più tappe chiamate vie
metaboliche.
• In una via metabolica, il prodotto di una reazione
f
funge
d
da substrato
b
nella
ll reazione
i
successiva.
i
• Si definisce metabolismo l’insieme di queste vie
metaboliche.
metaboliche
• Le vie metaboliche vengono classificate in:
(
)
- cataboliche (demolitive)
- anaboliche (sintetiche).
principali costituenti chimici della cellula
Trigliceridi: Acidi grassi
eg
glicerolo. Colesterolo
Glucosio, fruttosio e glicogeno
carboidrati
lipidi
p
amminoacidi
pproteine
Ioni, vit,
micronutrienti
Sintesi
Si
t i e catabolismo
t b li
d
delle
ll b
basii
azotate
acidi
idi nucleici
l i i
Alimenti
Cereali: tutte le «piante erbacee che producono frutti i
quali, macinati, danno farina da farne pane e altri cibi».
L’indice glicemico o IG (dall'inglese Glycemic index, abbreviato in GI) di un alimento indica la velocità con cui aumenta la glicemia in seguito all'assunzione di un quantitativo dell'alimento contenente 50 g di carboidrati: viene ottenuto misurando l'andamento della curva a campana dal momento dell'ingestione a due ore dopo. Questo parametro è espresso in percentuale, e si rapporta comunemente alla velocità di è
l
ll
l
àd
aumento della glicemia con la stessa quantità di glucosio o di pane bianco. A seconda se l’IG fa riferimento a glucosio o pane bianco, viene loro assegnato il valore di 100. Per convertire l‘IG da glucosio a pane bianco, basta moltiplicare per 1,37, viceversa dividere per 1,37da pane bianco a glucosio.
glucosio a pane bianco, basta moltiplicare per 1,37, viceversa dividere per 1,37da pane bianco a glucosio.
coinvolti nel metabolismo energetico
sono:
da tavola
tavola, latte
Dopo la digestione:
I monosaccaridi ottenuti vengono assorbiti dall'intestino con un
meccanismo di trasporlo attivo, che permette di trasferire gli zuccheri
nel sangue
g
anche q
quando la loro concentrazione nel sangue
g
èp
più alta di
quella nel lume intestinale.
I monosaccaridi passano dalle venule dell'intestino alla vena porta,
attraverso la quale vengono trasportati al fegato e quindi al resto
dell organismo
dell'organismo
DEFICIT DI
DISACCARIDASI
Il deficit più comune di disaccaridasi è quello della
lattasi che provoca intolleranza al latte.
latte.
Il deficit
d fi it di llattasi
tt i è comune nell'adulto,
ll' d lt nella
ll
maggioranza della popolazione africana di colore e
nella quasi totalità delle popolazioni asiatiche
asiatiche.
Una curiosità è rappresentata
pp
dal deficit di trealasi
una glicoproteina dell’orletto a spazzola che idrolizza
il trealosio (nei funghi). Un incidenza rara nella
popolazione,
l i
con l’l’eccezione
i
d
della
ll G
Groenlandia
l di d
dove
l’incidenza è di 1/13.
La glicemia
• L
La glicemia
li
i può
ò essere d
definita
fi it b
banalmente
l
t
come la concentrazione di glucosio nel sangue.
• Valori
V l i normali:
li sono iindicati
di ti d
da un iintervallo
t
ll di
circa 60-100mg/100ml (dl) che varia a seconda
della metodologia utilizzata per determinarla.
determinarla
• Questo valore deve essere mantenuto.
• Per
P il mantenimento
t i
t cii sono una serie
i di
meccanismi che presiedono a quella che viene
definita come:
l’omeostasi del glucosio.
Insulina
Intake
Glicemia
Utilizzo del
glucosio
alimentare
Glucagone
Durante il digiuno: glucagone,
adrenalina, cortisolo, ormone
della crescita
crescita.
Il pancreas esocrino produce
insulina e glucagone, che dirigono
il metabolismo direttamente.
L’omeostasi del g
glucosio è il risultato di:
Glicogenolisi
Glicogeno
Glicogenosintesi
Gl
Glucosio
i
Glicolisi
pool di glucosio
Lattato-Piruvato
Gluconeogenesi
14 membri
(1- 14)
14
14)
Il GLUT (qualsiasi tipo) ha due diverse
conformazioni: una con il sito di legame per il
glucosio sul versante interno ed una con il sito sul
versante esterno della membrana cellulare. Il
trasporto avviene in quattro tappe:
1. Il glucosio extracellulare si lega al suo sito di
l
legame,esposto
t sulla
ll faccia
f
i esterna.
t
2. Il trasportatore cambia di conformazione: il sito
di legame è ora intracellulare.
3. Il glucosio è rilasciato internamente.
4. Il trasportatore ritorna alla prima conformazione,
con il sito di legame
g
esposto
p
esternamente.
Concentrazione glucosio ematico: 5mM =
90mg/100ml
Intervallo g
glicemico normale:
60-120mg/100ml
g
KT dei Glut per il glucosio: 1 mM(Glut1,3); 5mM
(Glut4); 15-20mM
15 20mM (Glut2)
(Glut2).
Per KT si intende la concentrazione di sub. a cui si raggiunge la metà
della Vmax di trasporto (maggiore è la KT minore è l’affinità del
trasportatore per il substrato)
G
L
I
C
O
L
I
S
I
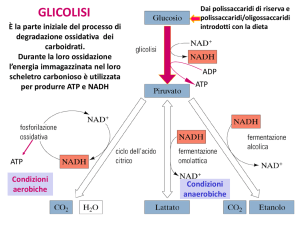
INTRODUZIONE ALLA GLICOLISI
• Il glucosio: combustibile universale per le cellule
che lo utilizzano per produrre ATP mediante la
glicolisi.
glicolitica p
può p
produrre ATP
• La via g
indipendentemente dalla presenza di O2.
• Il Glucosio è il glucide più rappresentato nella
dieta, con una funzione prevalentemente
energetica per le cellule, in particolare quelle
nervose, come il cervello e il gl. rosso.
La glicolisi inizia con la fosforilazione del glucosio (G-6P) ad opera della
esochinasi. Il G-6P viene ossidato e scisso in 2 molecole di p
piruvato con
produzione di 2 molecole di NADH e 2 molecole di ATP (fosforilazione a livello
del substrato)
C6H12O6 + H2O
6CO2 + 6H2O + Calore
Reazione chimica che può avvenire in
provetta in un’unica tappa
distinte in 3 fasi
L’
L’esochinasi
hi
i iinnesca lla glicolisi
li li i
Almeno IV isoforme di esochinasi
I, II, III funziona su + substrati anche
a basse concentrazioni di
glucosio a velocità ridotta,
glucosio,
ridotta
sequestra solo gli zuccheri realmente utilizzabili.
E’ inibita dal glucosio6P
o Esochinasi IV
parenchima epatico e cellule β pancreas:
Km molto alta, ([glucosio] post prandiale)
Vmax molto elevata, in realtà presenta una curva
di saturazione sigmoidale (cooperatività), infatti è
regolata
g
dal fruttosio-6P e non da g
glucosio-6P))
(il fegato può captare il glucosio
dal sangue portale) (glut2), efficacemente.
_
La glucochinasi è una proteina inducibile
glicolisi
Ossidazione a lattone
e conversione in pentoso fosfati
Isomerizzazione a glucosio-1P e formazione di glicogeno
La seconda tappa
pp della glicolisi
g
è una isomerizzazione: una reazione
che cambia la forma di una molecola, senza aggiungere o rimuovere
atomi.
Regolazione secondo economia
metabolica
Perchè AMP e non ADP?
2ADP
ATP+AMP
-
Siti allosterici distinti e quindi additivi
Questa tappa è fondamentale per la regolazione della glicolisi, il glucosio è immesso in maniera
irreversibile nella via glicolitica. L’enzima è attivato allostericamente da alte concentrazioni di
AMP, e inibito da alte concentrazioni di citrato e di ATP.
Q i di se i lilivelli
Quindi
lli di energia
i iintracellulare
t
ll l
sono elevati
l
ti lla glicolisi
li li i rallenta,
ll t mentre
t accelera
l
se sono
bassi.
• Il più potente attivatore della
,
,
fosfofruttochinasi è il fruttosio-2,6-bisfosfato,
si forma dal fruttosio-6P per azione della
fosfofruttochinasi-2
fosfofruttochinasi
2 e viene defosforilato dalla
fruttosio-2,6 bisfosfatasi-2.
L’enzima aldolasi catalizza sia la formazione dell’1,6 fruttosio-bisP che la scissione in due triosi.
All’equilibrio prevale l’esoso (89% vs 11%) perchè la reazione possa procedere nel senso glicolitico uno dei 2 triosi
deve essere rimosso
rimosso.
DAP e GAP sono interconvertibili (triosoP-isomerasi), la reazione implica la
formazione di un composto intermedio (l’endiolo). La GAP viene consumata nelle
reazioni successive e il DAP convertito in GAP.
Il DAP può essere anche trasformato in glicerolo-3P e seguire un’altra via.
La trioso fosfato isomerasi è stata descritta come un enzima perfetto. Compie il suo lavoro miliardi
di volte più velocemente rispetto alla reazione non catalizzata.
catalizzata È così veloce che la velocità di
reazione è determinata da quanto velocemente possono arrivare all'enzima le molecole.
L’ac. 1,3bisP-glicerico è un composto ad alta energia. La variazione di energia libera
Generata dal distacco del Pi in posizione 1 è di 12Kcal/mole (∆G° = -12kcal/mole)
(notare il simbolo di legame ad alta energia)
La reazione richiede quantità catalitiche di 2,3-bisfosfoglicerato.
Il 2,3-bis-Pglicerato cede il Pi 3 diventando 2-fosfoglicerato, il Pi ceduto viene
legato al substrato della reazione (3fosfoglicerato) che diventa 2,3 bis...e
così via.
Estere fosforico
ad alto contenuto di E
Estere fosforico
a basso contenuto di E
INTRODUZIONE ALLA GLICOLISI
• Il glucosio: combustibile universale per le cellule
che lo utilizzano per produrre ATP mediante la
glicolisi.
glicolitica p
può p
produrre ATP
• La via g
indipendentemente dalla presenza di O2.
• Il Glucosio è il glucide più rappresentato nella
dieta, con una funzione prevalentemente
energetica per le cellule, in particolare quelle
nervose, come il cervello e il gl. rosso.
distinte in 3 fasi
Intrappola il glucosio nella cellula,
fa procedere la reazione
Almeno IV isoforme di esochinasi
I, II, III funziona su + substrati anche a basse concentrazioni di
glucosio, a velocità ridotta, sequestra solo gli zuccheri realmente utilizzabili.
E’ inibita dal glucosio6P
o Esochinasi IV parenchima epatico e cellule β pancreas:
Km molto alta,, ([g
([glucosio]] post
p
prandiale)
p
) Vmax molto elevata,, in realtà presenta
p
una curva
di saturazione sigmoidale (cooperatività), infatti è regolata dal fruttosio-6P e non da glucosio-6P)
(il fegato può captare il glucosio dal sangue portale) (glut2), efficacemente.
-
-
2 molecole di ATP investite rendono impossibile tornare indietro,
la glicolisi ora è definitivamente commissionata.
Perchè AMP e non ADP?
2ADP
ATP+AMP
H
O--P
fruttosio-2,6-bisfosfato
Se c’è molto glucosio 6P,
6P, quindi, molto fruttosio 6P
la fosfofruttochinasi è regolata allostericamente da
fruttosio 2,62,6-bisbis-P (prodotto da PP--fruttoKinasi2, PFK2 e
d f f il t da
defosforilato
d ffruttosio
tt i 2
2,6
2,66-bisP
bi P asi2,
i2 FBP asi2),
i2) sii
produce un intermedio che non può procedere, che
sottrae substrato e che inibisce l’enzima PFK1: risultato
la g
glicolisi rallenta.
rallenta
n .
Quarta reazione
L’enzima aldolasi catalizza sia la formazione dell’1,6 fruttosio-bisP che la scissione in due triosi.
All’equilibrio
q
p
prevale l’esoso (89% vs 11%) perchè
p
la reazione possa
p
procedere
p
uno dei 2 triosi deve essere rimosso.
L’ac. 1,3bisP-glicerico è un composto ad alta energia. La variazione di energia libera
Generata dal distacco
d stacco del Pi in
n posizione
pos z one 1 è di
d 12Kcal/mole
Kcal/mole (ΔG°
(ΔG = -12kcal/mole)
kcal/mole)
Lo stesso Enzima trasferisce il Pi sull’ADP
La reazione richiede quantità catalitiche di 2,3bisfosfoglicerato.
Il 2,3-bis-Pglicerato
2 3 bis Pglicerato cede il Pi 3 diventando 22
fosfoglicerato, il Pi ceduto viene
legato al substrato della reazione (3fosfoglicerato) che
diventa 2,3 bis...e
così via.
Da basso ad alto contenuto di Energia Δg -15Kcal/mole
10 reazioni in successione lineare
costituiscono il pathway della
glicolisi.
Il glucosio viene ossidato
per p
produrre due
lentamente p
tronconi da 3 atomi di carbonio:
piruvato
La fermentazione alcolica è una forma di metabolismo energetico che avviene in alcuni lieviti in
assenza di ossigeno:
•
E’ responsabile
bil di diversi
di
i fenomeni
f
i che
h vediamo
di
ognii giorno,
i
quali
li la
l lievitazione
li i i
d l pane o
del
la trasformazione del mosto in vino.
•
E’ operata da una particolare classe di microrganismi, i Saccaromices dei quali il più comune
è senz'altro
' lt il S.
S cerevisiae,
i i
presente
t sulla
ll buccia
b
i dell‘uva
d ll‘
come nell lievito
li it di bi
birra.
•
Fu il primo processo metabolico realizzato in vitro, grazie all'isolamento degli enzimi, così
chiamati proprio perché isolati nel lievito (zimé). Ciò apportò un duro colpo al vitalismo
Tiamina PPi (vit B1)
La fermentazione lattica è una forma di metabolismo energetico che avviene in alcuni batteri e nella
cellula animale in assenza di ossigeno.
• Consiste nella trasformazione di una molecola di glucosio (o di un altro zucchero fermentabile) in due
molecole di acido piruvico che vengono successivamente ridotte ad acido lattico con una bassa resa
energetica.
• Questa via metabolica prende il nome dal principale prodotto finale ma viene detta anche omolattica
per distinguerla da quella eterolattica che utilizza un meccanismo diverso.
La fermentazione
L
f
t i
lattica
l tti sii incontra
i
t principalmente
i i l
t neii lattobacilli
l tt b illi e nell metabolismo
t b li
anaerobico
bi di
alcuni tessuti (muscolo, eritrociti) degli organismi pluricellulari.
• La fermentazione lattica svolta dai lattobacilli è presente nel tratto gastrointestinale umano in cui
assume un ruolo
l tanto
t t importante
i
t t da
d spingere
i
alcuni
l
i a considerare
id
i lattobacilli
l tt b illi dei
d i probiotici.
bi ti i
• La fermentazione lattica è coinvolta nella preparazione di numerosi alimenti tra cui ricordiamo lo
yogurt, il kefir, i capperi ed i crauti.
P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright © 2006
Quando nel muscolo scheletrico la produzione di NADH eccede la capacità riossidativa
(catena respiratoria), allora il rapporto NADH/NAD diventa elevato e questo favorisce la
trasformazione del p
piruvato in lattato.
Nel fegato e nel cuore questo rapporto (NADH/NAD) è basso. quindi il lattato è ossidato a
piruvato. Nel fegato il piruvato è poi convertito in glucosio oppure è decarbossilato a
AcetilCoA
Acidosi lattica. Elevata
concentrazione nel plasma di ac
ac.
Lattico. Si verifica per un collasso
del sistema circolatorio
(infarto,embolia polmonare,
emorragie massive).
Tutte hanno in comune il deficit di
O2 a carico dei tessuti con
conseguente rallentamento della
catena respiratoria e riduzione di
ATP . Per sopravvivere le cellule
usano la glicolisi anaerobia
anaerobia.
Quando il danno viene risolto le
cellule recuperano una normale
attività, utilizzando un surplus di
ossigeno. Debito di ossigeno
P. Champe, R. Harvey, D. R. Ferrier, LE BASI DELLA BIOCHIMICA, Zanichelli Editore S.p.A. Copyright © 2006
In sintesi la regolazione della
glicolisi avviene:
• A lilivello
ll d
della
ll ffosforilazione
f il i
d
dell Gl
Glucosio
i
isoenzimi della famiglia delle esochinasi
inibizione allosterica da F-6P compartimentalizzazione
nel nucleo dell’enzima epatico (GKRP)
• A livello della fosfofruttochinasi-1
ATP Citrato
ATP,
Cit t
AMP e ffruttosio
tt i 2,6
2 6 bi
bisP
P
P. Champe, R. Harvey, D. R.
Ferrier, LE BASI DELLA
BIOCHIMICA Zanichelli Editore
La via del glucagone promuove la sintesi di
cAMP e l’attivazione della PKA che fosforila
gli E
E.
La forma fosforilata dell’E. è sempre
inattivata mentre quella defosforilata (via
dell’insulina) è attiva.
P. Champe, R. Harvey, D. R.
Ferrier, LE BASI DELLA
BIOCHIMICA Zanichelli Editore
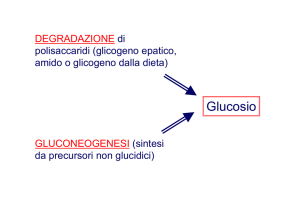
Il glucosio può essere sintetizzato a
partire da precursori non glicidici
• 120g di glucosio servono al cervello (120/160 totali per l’organismo intero).
• 20g
20 sono neii li
liquidi
idi organici.
i i
• 190g rappresentano la riserva sotto forma di glicogeno
La gluconeogenesi converte:
piruvato
glucosio
Decima reazione nella via glicolitica
Prima nella neoglucogenesi
Fosfenolpiruvato
2-fosfoglicerato
3-fosfoglicerato
1,3bisfosfoglicerato
gliceraldeide3-P
Diidrossiaceton-P
Fruttosio 1,6bP
fosfofrottochinasi: AMP
ATP e citrato
Fruttosio 1,6 bis fosfatasi:AMP
ATP e citrato
_
fosfatasi
+
+
Fruttosio 6-P
Glucosio 6-P
1
10
9
2
3
8
4
5
7
6
5
7
8
9
10
6
4
3
2
1
Ciclo di Cori
Ciclo dell’Alanina
dell Alanina