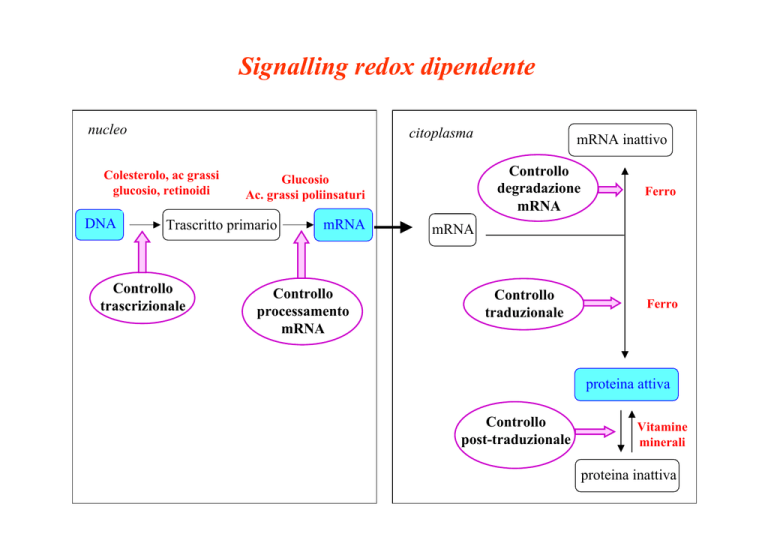
Signalling redox dipendente
nucleo
citoplasma
Colesterolo, ac grassi
glucosio, retinoidi
DNA
Controllo
trascrizionale
Controllo
degradazione
mRNA
Glucosio
Ac. grassi poliinsaturi
Trascritto primario
mRNA
Controllo
processamento
mRNA
mRNA inattivo
Ferro
mRNA
Controllo
traduzionale
Ferro
proteina attiva
Controllo
post-traduzionale
Vitamine
minerali
proteina inattiva
DNA Frequenza
ATG
5’
TAA
TAG
TGA
Punto preciso di inizio
CAT TATA
Introne
Esone
Promotore
Esone
Introne
Terminazione
3’
AATAA
Esone
5’ NT
Trascritto primario
5’
3’ NT
UAA
UAG
UGA
AUG
3’
AAAAA
CAP
5’ NT
mRNA
5’
3’ NT
UAA
UAG
UGA
AUG
CAP
poli-A
5’ NT
3’
AAAAA
3’ NT
COO-
Proteina
NH3+
CHO-RE = Carbohydrate Response Element
DR-1 = Direct Repeat-1
IRE = Insulin Response Element
GLU-RE = Glucose Regulatory Element
E = Exon
I = Intron
CHO-TF = Carbohydrate Transcription Factor
HNF-4 = Hepatic Nuclear Factor-4
PPARγ = Peroxisone Proliferator Activator Receptor γ
USF-1 = Upstream Stimulatory Factor-1
SREBP-1 = Sterol Regulatory Element Binding Protein-1
Promotore
CHO
TF
5’
CHO-TF
HNF4
PPARγ
SpI
CHO-RE
DR-1
SpIRR
ACIDO GRASSO SINTETASI
NFY
SpI
NFY/SpI
USF-1
SREBP-1
POL II
IRE
CAT TATA
GLU
RE
E
I
E
3’
I
IL CONTROLLO DELLA TRASCRIZIONE E’ MEDIATO DA
FATTORI TRASCRIZIONALI
diversi domini funzionali
Dominio di legame al DNA
riconosce una specifica sequenza di 8-12 basi del DNA
comuni tipi di legame
Zinc finger
Leucine zipper
Dominio di transattivazione
regola attività della RNA polimerasi II
Dominio di regolazione
dipende da una specifica via di segnale cellulare
regolazione da ligando (allosterica)
modificazione covalente (fosforilazione , proteolisi)
interazione con altre subunità regolatorie
modificazione redox
2SH
-S
S-
REGOLAZIONE DA LIGANDO (mediante fattori lipofilici)
Peroxisome proliferator-activated receptors (PPARα, γ e δ) acidi grassi polinsaturi
Retinoid receptors carotenoidi (licopene),
Vitamin D3 receptors
Estrogen receptors: isoflavoni (genisteina), lignani
ABBONDANZA
SREBP-2 (Sterol Regulatory Element-Binding Protein-2): regolazione del colesterolo
SREBP-1: regolazione degli acidi grassi polinsaturi
FOSFORILAZIONE e DEFOSFORILAZIONE
mediante chinasi o fosfatasi (Mitogen Activated Kinases)
glucosio, polifenoli (resveratrolo), catechine, isotiocianati
STATO REDOX
AP-1 (Activating Protein-1) e NF-kB (Nuclear Factor-kB)
vitamine antiossidanti, polifenoli, composti solforosi
Specie reattive dell’ossigeno (ROS)
Radicali endogeni
1)
catena di trasporto degli elettroni
2)
difesa immunitaria aspecifica
(NADPH ossidasi)
3)
sistema della xantina ossidasi
(forma superossido)
Superossido
Perossido d’idrogeno
Radicale idrossile
Acido ipocloroso
Ossido nitrico
Perossinitrito
eO2
e.
O2-
eH2O2
e.
OH -+ OH
2H+
O 2-.
H2O 2
OH .
HOCl
NO.
(neutrofili, mieloperossidasi)
.
.
OONO - (NO + O2 OONO )
Radicali esogeni
Fumo di sigaretta, radiazioni, ozono e farmaci
2H+
H2O
Difese antiossidanti
Difese enzimatiche:
Superossido dismutasi (2O2-. + 2H+
H2O2 + O2)
Catalasi (H2O2 in H2O)
Glutatione perossidasi (perossidi nei rispettivi alcooli)
Difese non enzimatiche: (molecole a basso PM)
Tocoferoli e carotenoidi (perossidazione lipidica)
Vitamina C, glutatione, acido urico, tioli (idrosolubili)
Sequestratori di metalli:
Transferrina, ferritina e lattoferrina (Fe)
Ceruloplasmina (Cu)
Albumina (Fe e Cu)
Equilibrio Redox
Ossidanti eccedono i sistemi di difesa :
Danno cellulare e morte
irreversibile
Ossidanti
reversibile
Antiossidanti
Piccole variazioni nei livelli di ROS :
Signalling cellulare
Espressione genica
Cambiamenti nel metabolismo
Patologie correlate allo stato redox
MALATTIE DEGENERATIVE
MALATTIE AUTOIMMUNI E INFIAMMATORIE
MALATTIE CARDIOVASCOLARI
CANCRO
INVECCHIAMENTO
Sangue
Sistema nervoso
Occhio
Tratto gastrointestinale
Sistema cardiocircolatorio
Sistema immunitario
Rene
Polmone
Epidermide
Sistema riproduttivo
Talassemia, anemie croniche, favismo
Parkinson’s, insulto ipertensivo cerebro-vascolare,
encefalomielite allergica, distrofia muscolare, Alzheimer
Cataratta, retinopatie
Danni epatici, pancreatite, epatomegalia, epatoma
Cardiomiopatia da alcool, aterosclerosi, infarto, aritmia
Sindromi autoimmuni, artrite reumatoide, AIDS
Sindromi nefrotiche autoimmuni, nefrotossicità
Enfisema, displasia broncopolmomare
Porfiria, dermatite da contatto, psoriasi, radiazioni solari,
vitiligine
Atrofia testicolare
Tioli sono i sensori dello stato redox cellulare
SNO
SH
Chinasi
Fosfatasi
TF
SSG
S
S
SOH
SO2H (SO3H)
Conseguenze:
Alterazione della struttura tridimensionale
Incapacità di legare lo zinco (Zn-finger chinasi e fattori di trascrizione)
Incapacità di legare il DNA (cisteine nel dominio di legame al DNA)
glutatione e tioredossina
sono i maggiori sistemi riducenti
ditiolo / disolfuro
GSH = γGlu-Cys-Gly
GSSG
NADPH
Vit C
NADP+
Tioredossina reduttasi
DHA
99%
GSH
NADP+
Trx
(ox)
Trx
(rid)
Glutatione reduttasi
Nucleo
GSSG
NADPH
tioredossina
(rid)
Ref1 (Redox Factor 1)
Cistina
GSSG
(OSSIDANTE)
Cisteina
(RIDUCENTE)
GSH/GSSG
Squilibrio
* NADPH
* Tioredossina
* Glutatione
Scambio
tiolo/disolfuro
Apoptosi
Riduzione
di ponti
disolfuro
Proliferazione
Sistema TrxR/Trx
•Riduzione ROS
•Regolazione ormonale (stato rid. recettore
glucorticoidi, estrogeni, 5’deiodinasi)
•Ribonucleotide reduttasi
•Refolding proteine ossidate
•Induzione fattori di crescita e citochine
Fattore di
crescita
Cofattore
Trx
Regolatore di
fattori
trascrizionali
Chaperone
Legame
a
proteine
Diversi componenti della dieta possono influenzare
l’equilibrio ditiolo/disolfuro
amminoacidi solforati
metionina + cisteina
glutammina
flavina
GSH
GSSG
selenio
vitamina C
vitamina E
Composti bioattivi
(polifenoli)
induttori enzimi fase II
Enzimi sintetici
I meccanismi di segnale differiscono tra ROS endogeni ed esogeni
H 2O 2
O2
-.
ROS
esogeni
NADPH ossidasi
Membrana
cellulare
ROS endogeni
(H2O2)
Aumento del
potenziale di disulfide
Stato redox
Attività
enzimatica
Fosfatasi
Chinasi
(MAP, JAK/STATs)
Canali ionici
Ponti disolfuro
proteina/proteina
Glutatione-S-tiolazione di
cisteine reattive
Guanilato ciclasi
Attivazione
di fattori trascrizionali
Fosfolipasi
(A2, C, D)
Cascata di
fosforilazione
Attivazione
di fattori trascrizionali
ATTIVAZIONE IMMUNE
citochine
STRESS
STIMOLI MITOTICI
Fattori di crescita
ROS, UV, corpi chetonici, iperglicemia
Ras
MAPKKK
MAPKK
Ser/Thr
TAK1
ASK1
Raf
MEKK1
MKK3/6
MEK5
MEK1/2
MEK4/7
p38
ERK5
ERK1/2
JNK
MAPK
IRS
¾IRS1
P
TF
MAPK= Mitogen Activated Protein Kinase
ERK= Extracellular-Regulated Kinases
IRS-1 = insulin receptor substrate-1
TF
Geni bersaglio
Shock termico
OSSIDANTE
Tioli
Esteri del forbolo
Tioli
Ossidazione dei tioli, ROS
Denaturazione proteica
HSF1
Tioli
Espressione
di Fos, Jun
Stress ossidativo
ROS
trimero
HSF1
Traduzione del
messaggero p53
Fos/Jun
p53
Trx
Ref-1
IkB
Tioli
p50
p65
Trx
Trx
Ub P P
DNA
HSE
AP-1 sito
p53
RIDUCENTE
kB
Tioli
gene
Degradazione di IkB
N-acetilcisteina
GSH
cisteina extracellulare
tioredoxina
Acido lipoico
Vitamin C
FATTORI DI TRASCRIZIONE REDOX SENSIBILI
HIF-1α
p53
Glucocorticoid receptor
Hypoxia-inducible factor 1
arresto del ciclo cellulare ed apoptosi
recettore di ormoni steroidei
TTF
Thyroid transcription factor-1. Geni specifici della tiroide e dei
pneumociti.
proliferazione e differenziamento delle cellule emopoietiche
Nuclear factor-Y. Fattore di trascrizione generico
Nuclear factor-1. Geni ubiquitari o regolati da ormoni, nutrienti e
sviluppo
Early growth response factor-1. E’ inducibile (ormoni, neurotrasmettitori, fattori di crescita e differenziativi, metaboliti citotossici)
Upstream stimulatory factor. Geni del metabolismo (enzimi glicolitici
e lipogenici)
differenziamento della tiroide
omeogene. Embriogenesi
Polyomavirus enhancer-binding protein 2. Osteogenesi ed emopoiesi
GA-binding protein α. Geni specifici della linea mieloide e delle giunzioni
c-Myb
NF-Y/CBF
NF-1/CTF
EGR-1
USF
Pax8
HoxB5 (Hox 2.1)
PEBP2
GABPα
neuromuscolari
HLF
HIF-like factor
Una o più cisteine nel dominio di legame al DNA, di transattivazione,
di localizzazione nucleare e/o di oligomerizzazione
NF-kB/Rel family
RHD
p65 (RelA)
RelB
LZ
TAD
RHD
c-Rel
RHD
p100/p52 (NF-kB2)
RHD
p105/p50(NF-kB1)
RHD
TAD
TAD
Le ripetizioni di anchirina si
legano al dominio di omologia
Rel, sequestrando NF-kB nel
citoplasma. Nel caso di p100 e
p105, il legame può essere
intramolecolare o con l’altra
subunità formante il dimero.
I-kB family
IkBα
IkBβ
IkBε
IkBγ
BCL-3
IKK family
IKKα
Kinase domain
LZ
HLH
IKKβ
Kinase domain
LZ
HLH
NEMO/IKKγ
α
CC1
α
CC1
LZ
Z
A
B
Cytokines, viral infection, stress
Receptor
a
IKKα
IKKγ
IKKβ
cytoplasm
RelA
IKKα
MAP3K
b
IKKα
P P
IKKα
IKKγ
IKKβ
P P
IKKα
P
RelB
p100
IkB
p50
RelA
P
P
IkB Ub Ub Ub Ub Ub Ub
RelB
P P
p100
Ub Ub Ub Ub Ub Ub
p50
P
P
IkB Ub Ub Ub Ub Ub Ub
RelB
p52
RelA
p50
26S proteasome
nucleus
RelA
p50
RelB
p52
NF-kB responsive genes
NF-kB e ROS
TNF-R
IL1-R
IKK’S
ROS
MEKK1
ROS
IkBα
IkBα
p50 p65
P P
p50 p65
P
ROS
Legame al DNA
ROS
degradazione
Inflammatory
mediators
P P
IKKα
IKKγ IKKβ
P P
p65
P P
IKKα
IKKγ IKKβ Cys179-NO
P P
IkB
p50
p65
.
NO
P
P
IkB Ub Ub Ub Ub Ub Ub
.
p50
P
P
IkB Ub Ub Ub Ub Ub Ub
26S proteasome
p65
p50
p65
NO
iNOS
Cys62-NO
p50
p65
iNOS
p50
nucleus
Activating protein 1 (AP-1)
• Fattore di trascrizione dimerico, redox sensibile, composto da
proteine appartenenti a famiglie
- Jun (c-Jun, Jun B, Jun D)
- Fos (c-Fos, Fos B, Fra-1, Fra-2).
• Composizione modulata dalla fosforilazione indotta da
chinasi:
protein-chinasi C (PK-C),
c-Jun N-terminale chinasi (JNK).
• Differenti complessi di AP- 1 modulano differenti geni
bersaglio.
c- Jun: µciclo cellulare (µ ciclina D1, ¶ oncosoppressore p53)
Jun B: ¶ ciclo cellulare
p38
ERK
JNK ERK
p38
TCF SRF SRF
CREBCREB
SRE
CRE
c-fos
TATA
FRK
c-Fos
c-Fos
JNK
p38
c-Jun
JNK
ATF2 c-Jun
c-jun
TRE
c-Jun
TATA
Gene expression
Extracellular stimuli
Ras
Rac, Cdc42Hs
Raf
MEKK
ASK1
MAPKK
MEK
JNKK
MKK3, MKK6
MAPK
ERK
JNK
p38
MAPKKK
VITAMINA C
Donatore monoelettronico → radicale poco reattivo
NADH
CH2OH
H OH
CH2OH
H OH
O
O
-e
H
OH
CH2OH
H OH
O
O
HO
.
O
O
O
+
H
-e -H
H
+e
HO ACIDO
GSH
NADPH
idrolisi dell’anello
+
+e +H
O
O
L-ASCORBICO
RADICALE
ASCORBILE
ACIDO 2,3 DICHETO
GULONICO
ACIDO L-DEIDRO
ASCORBICO
ACIDO OSSALICO
livello urinario
35 –40 mg /die
CONCENTRAZIONE PLASMATICA
< 11 µmol/l (0,2 mg/100 ml) → carenza
11 – 28 µmol/l → rischio di carenza
34-45 µmol /l → norma (RDA = 75-90 mg /die)
60 µmoml/l → saturazione tissutale (introito ~ > 100 mg/die)
CONCENTRAZIONE CELLULARE = mM
Vit C: trasporto attivo Na-dipendente SVCT1 intestino, rene
SVCT2 altri tessuti
Deidroascorbato: trasporto mediato da GLUT
riconvertito a Vit C
FUNZIONI
Mono- e di- ossigenasi Fe o Cu dipendenti (collagene, carnitina e catecolamine)
Inattivazione di specie ossidanti (previene ossidazione LDL)
Rigenerazione della vit E
Assorbimento e metabolismo del ferro
Regolazione fattori redox-sensibili
CHERATINOCITA
Vit C protegge dal danno ossidativo modulando l’attività di AP-1
In particolare, contrasta gli effetti indotti da UV-B tramite:
aumento dell’espressione di Fra-1 (complessi AP-1 inibitori)
inibizione della fosforilazione di JNK (e conseguentemente di c-Jun)
-
+
-
+
+
+
AA-2P
UV-B
Fra-1
fosfo JNK1
fosfo c-jun
Vit C induce il differenziamento epidermico attraverso la cascata PK-C/AP-1
PK-C
8
S
Totale
Citosol
Membrane
S S X
Attività CAT
(volte su controllo)
4
2
0
Calcio
+
TGasi 1
Loricrina
Cheratina 1
1
-
AA-2P
+
0.2
0.1
0
S
H
2
Vitamina C
+ AA-2P
- CaCl2
S
H
3
0
Ctrl
S
H
S
H
AP-1 wt
AP-1 mut
4
-
Dominio catalitico
Zn2+
OD600 nm/mg di proteina
Attività PK-C
cpm (x 1000)
6
Dominio regolatorio
-
+
+
-
AA-2P
CaCl2
Stress ossidativo (UV, H2O2, leptina)
+
+
JNK- P
-
nucleo
c-Jun- P
+
c-Fos
JunB
Fra-1
Fra-2
c-Jun- P
AP-1
Trascrizione genica
AA
CONCLUSIONI
+
L’acido ascorbico regola la cascata PK-C/JNK/AP-1
·
·
+
mediante un controllo trascrizionale
mediante un controllo post-traduzionale
Questa regolazione può:
antagonizzare l’espressione
genica coinvolta nel danno
cellulare indotto dagli UV-B
promuovere il differenziamento
epidermico mantenendo uno
stato redox cellulare bilanciato.
CELLULE MUSCOLARI
• Il differenziamento è accompagnato da un aumento della resistenza allo stress
ossidativo
• La resistenza è legata al cambiamento della composizione di AP-1 (maggior
presenza di subunità inibitorie Fra-1 e Fra-2)
• La vitamina C induce la componente inibitoria di AP-1
• Lo stress ossidativo indotto dalla deplezione di glutatione è contrastato da
un’aumentata espressione ed attività della tioredossina reduttasi, nonché da un
aumentato trasporto di vitamina C (aumento nell’espressione del trasportatore Na- - + + - H2O2
dipendente)
-
Ctrl
H2O2 50 µM
H2O2 100 µM
H2O2 300 µM
H2O2 300 µΜ + vit C
% di nuclei apoptotici
100
80
+
-
+
-
vit C
Miotubi
AP-1
60
40
20
Fra-1
0
Mioblasti
Miotubi
Fra-2
+
+
-
+
+
-
H2O2
vit C
Attività chemopreventiva della vit C
Controllo del
danno al DNA
MLH1(mismatch repair)
+
c-Abl (tirosin chinasi)
Vit C
La vitamina C modula
MLH1 e p73, ma non
p53 e c-Abl
C
p53
p73
+
MLH1
p73
p53
c-Abl
Riparo del danno
Arresto della crescita
Morte cellulare
Vit C
α
β
γ
aumenta la suscettibilità cellulare
all’apoptosi indotta da agenti che
provocano danno al DNA (in
maniera c-Abl dipendente).
Attività anticarcinogenica della vitamina C
Danno al DNA
(cisplatino)
c-Abl
+
Viability (%)
MLH1
105
95
85
Vit C
c-Abl +/+
75
0
p73
10
105
+
Viability (%)
p53
1
cisplatin (µM)
95
85
75
Arresto della crescita
Apoptosi
c-Abl -/65
0
1
cisplatin (µM)
10