Cagliari 23/24 giugno 2005
Innovazioni Terapeutiche in Oncologia Medica
II FARMACI
FARMACI CON
CON INCAPSULAZIONE
INCAPSULAZIONE LIPOSOMIALE
LIPOSOMIALE
IN
IN ONCOLOGIA
ONCOLOGIA
dall’innovazione
dall’innovazione tecnologica
tecnologica all’impiego
all’impiego clinico
clinico
Prof. Luigi Cattel
Dip. di Scienza e Tecnologia del Farmaco
Università di Torino
Catene aciliche
Parte idrofobica
Zona idrofila
Testa Polare
Testa polare
Parte idrofila
O
H 3C
O
H 3C
O
O
CH2
H
C
O
O P R
C
H2
O-
Fosfolipide
1961 – A.D. BANGHAM, Cambridge
SCOPERTA
CASUALE
Catena idrofobica
LIPOSOMI
Mimano la membrana cellulare
Intrappolano i soluti
come
II Liposomi
LIPOSOMI
COME
DRUG
SYSTEM
Drug DELIVERY
Delivery Sistem
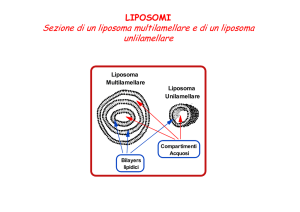
Durante la loro formazione i liposomi hanno la capacità di
incapsulare sostanze biologicamente attive:
• sostanze idrosolubili nei compartimenti acquosi;
• sostanze liposolubili tra le lamelle lipidiche;
• sostanze anfipatiche la cui parte lipofila viene incorporata tra le
lamelle lipidiche e la parte idrofila nei compartimenti acquosi.
Molecole Idrosolubili
Molecole Liposolubili
Molecole anfipatiche
LE CARATTERISTICHE
CHIMICHE INFLUENZANO
LA STRUTTURA
FISICA INFLUENZA
• Fluidità di membrana
• Carica elettrica
• Permeabilità
• Dimensioni
• Forma
MLV (multilaier vesicle)
100 – 1000 nm
≥ 5 lamelle concentriche
< 5 (oligo lamellar vesicle)
SUV (small unilamellar vesicle)
25 nm (lecitina uovo)
50 nm (DPPC)
LUV (large unilamellar vesicle)
1000 nm
IUV (intermediate sized unilamellar vesicle)
REV (reverse phase evaporation vesicle)
DRV (dried reconstituted vesicle)
VET (vesicle extruded tecnique)
100 nm
Schematizzazione morfologico-strutturale
dei vari tipi di liposomi
OLVs
MLVs
MUVs
LUVs
MVVs
SUVs
MUVs
MLV-REVs; SPLV
Stabilità del Sistema Liposomiale
STABILITÀ E STABILIZZAZIONE
Le sospensioni liposomiali pongono problemi di stabilità, intendendo con questo termine sia la
stabilità fisica delle sospensioni, sia la stabilità chimica del principio attivo e dell’involucro
lipidico liposomiale. L’instabilità in vitro dei liposomi può essere dovuta a diversi fattori:
1.
AUTOOSSIDAZIONE DEI FOSOFOLIPIDI – Tale processo avviene per perossidazione lipidica
ed è favorita dalla presenza di ossigeno, di ioni metallici, della luce e pa pH elevati.
L’ossidazione può essere rallentata con l’uso di agenti chelanti, di antiossidanti e tocoferoli.
Anche il colesterolo ha un ruolo predominante nella stabilizzazione delle membrane liposomiali.
2.
AGGREGAZIONE TRA LE VESCICOLELIPOSOMIALI – Tale processo è evitabile facendo
ricorso a vescicole cariche ed a stabilizzanti (viscosizzanti) di varia natura.
3.
PERDITA DEL PRINCIPIO ATTIVO – Tale processo è funzione della percentuale di colesterolo,
della natura dei fosfolipidi, della carica delle vescicole, della dimensione e delle caratteristiche
chimico-fisiche del principio attivo. Per ridurre la perdita del principio attivo, esistono due
soluzioni:
• fisica: la liofilizzazione dei liposomi
• chimica: l’utilizzo di fosfolipidi diacetilenici che, formando tra le varie molecole dei legami
chimici, irrigidiscono il sistema e riescono a trattenere per più tempo il principio attivo.
N.B.: questo tipo di liposomi non può essere somministrato per via parenterale a causa degli
effetti collaterali.
Liposomes extravasation: anatomyc barriers
Schematic representation of the liver sinusoid. The sinusoid connects the portal vein (and the
hepatic artery) with the central vein and facilitates the exchange of nutrients and metabolites
between the blood and the liver parenchyma. The sinusoidal endothelial cells forms a
fenestrates sheath around the sinusoid that regulates the exchange between the lumen and the
space of Disse (the space between the endothelial layer and the hepatocytes). The Ito cells are
located in this space; they embrace the endothelial layer with their extended structures.
Liposomes extravasation: in tumour tissues
Liposome classification based on composition and mode of drug delivery
Type
Characteristics
Conventional Liposomes (CL)
• subjected to RES uptake
• short circulation half- time
• dose dependent
pharmacokinetic
• variable stability: storage as
lyophilised or pro
- liposome
powder
• “pure lipid approach”
• less subjected to RES uptake
than CL
• long circulating half- time
• high stability on storage
• neutral and/or negatively
charged phospholipid plus
cholesterol
• variable size
• Ambisome (Nextar)
• Myocet (Liposome
Inc.)
• DSPC cholesterol
• high transition
temperature/saturated
phospholipid
• small size (< 100 nm)
• Daunoxome (Nextar)
•
•
•
•
not subjected to RES uptake
long circulating half- time
variable size
not stable
• surface modifiers liposomes
• (monosialoganglioside) GM1
liposome
• (palmitylglucuronyl) PG1CUA
liposome
Commercially not
available
•
•
•
•
•
not subjected to RES uptake
Stealth® liposomes
very long circulating half- time
small size (< 100 nm)
high stability on storage
• PEG surface
- modified
liposomes
• high transition temperature
lipids
• Caelyx (Europe)
• Doxil (USA)
1°
Long Circulating Liposomes
(LCL)
2°
Sterically Stabilized
Liposomes (SSL)
3°
Pegylated Liposomal
Doxorubicin (PLD)
4°
Formulation
Product / Company
• AmBisome®
Ambisome
L’AmBisome ® è una formulazione di
liposomi SUV a lunga circolazione
contenenti amfotericina B che ha
dimostrato una maggiore efficacia
comparata al farmaco convenzionale in
studi di candidiasi sistemica su animali
Fig. 3
ANTIMICROBICI
I liposomi contenenti il farmaco arrivano ai macrofagi (o alle altre cellule target dotate di attività
fagocitaria) per endocitosi (1); dopo fusione degli endosomi con i lisosomi (L) si ha la distruzione
del bilayer liposomiale (3) e il rilascio delle molecole di farmaco nell’apparato lisosomiale. Nei
lisosomi e negli altri compartimenti cellulari sono presenti i microorganismi patogeni da colpire
(effetto cavallo di Troia)
MIOCET Doxorubicina Liposomiale
pH 4
DOX–H+
pH 7,8
DOX
citrate
buffer
DOX
DOX–H+
carbonate
buffer
Doxorubicin (DOX) loading by pH transmembrane gradient
Myocet® Preparation
• Supplied as 3-vial system
– Doxorubicin
– Buffer
– Liposomes
• Equilibrate vials to 55° to 60° C
• Reconstitute doxorubicin with sodium chloride for injection
• Adjust pH of liposomes with buffer
• Add pH-adjusted liposomes to reconstituted doxorubicin
• Mix thoroughly
• Allow mixture to cool to room temperature
Myocet® (Elan Corporation)
Quality control assays of pharmaceutical liposomal formulations
Methodology
Characterization assays
pH
pH meter
Osmolarity
Osmometer
Phospholipid concentration
Lipid phosphorus content (Fiske and Subbarow or Bartlett method)
Cholesterol concentration
Cholesterol oxidase assay. HPLC
Drug concentration
Spectrophotometry. HPLC or other chromatografic procedures
Biochemical stability assays
pH
pH meter
Phospholipid peroxidation
Conjugated diens, lipid peroxides, thiobarbituric acid (TBA) test and acid compisition (GC)
Phospholipid hydrolysis
TLC. HPLC
Cholesterol autooxidation
TLC. HPLC
Antioxidant degradation
TLC. HPLC
Drug degradation
TLC. HPLC. Spectroscopy
Physical stability assays
Vesicle size distribution: submicrometer
range
micrometer range
Electrical surface potential and surface pH
Photon correlation spectroscopy. Gel inclusion chromatography and specific turbidity
Coulter counter. Laser diffraction and light microscopy
Zeta potential measurements. Use of electrical field or pH sensitive probes
Percentage of free drug
Gel exclusion chromatography. Ion exchange chromatography and protamine precipitation
Dilution dependent drug release assay
Dilution effect (0 – 10,000-fold) on liposomal drug/PL ratio
Drug phospholipid ratio
Determination of drug and phospholipid content
Biological assays
Sterility
Aerobic and anaerobic bottle culture
Pyrogenicity
Rabbit and/or Limulus amebocyte lysate (LAL) tests
Animal toxicity
Monitor survival
Relevant body fluid-induced leakage
Gel exclusion chromatography. Ion exchange chromatography and protamine precipitation
ANTITUMORALI
• DaunoXome ®
Il DaunoXome ® contiene una
soluzione di Daunorubicina
incapsulata in liposomi
unilamellari composti da DSPC e
CHOL (60-80 nm di diametro) che
incorporano nei tessuti tumorali
una quantità di principio attivo 10
volte maggiore rispetto al farmaco
libero
Fig. 9
Structure of CaelyxTM
PEG
Evades immune system
Prolonged circulation
Drug stays in liposome
until it reaches target
Doxorubicin
Drug concentrates
in tumour
Liposoma
Stealth
Liposoma
Convenzionale
Comparison of Liposomal
Anthracycline Preparations
Agent
Anthracycline
Membrane
Constituents
Size
Mononuclear
Phagocyte
System (MPS)
CAELYX™/ Doxil® Doxorubicin
(PLD)
Cholesterol, saturated
phosphatidylcholine,
polyethylene glycol
85 nm
Avoids
MPS
Myocet®
Doxorubicin
Cholesterol, egg
phosphatidylcholine
150 to
250 nm
Taken up
by MPS
DaunoXome®
Daunorubicin
Cholesterol,
50 nm
distearoylphatidylcholine
Sparano JA. Semin Oncol. 2001;28:32-40.
Avoids
MPS
Human pharmacokinetics of free doxorubicin and doxorubicin entrapped in
conventional liposome (CL) or in long-circulating liposomes such as
pegylated liposomes doxorubicin (PDL)
Formulation
Clearance
l ∗ h−1
Volume of
distribution
Area under the
curve
(l)
µg∗h∗ml-1
Half-life (h)
α
β
Free
doxorubicin
45
1400-3000
1-5
0.08
20
CL
21.8
200
13.6
0.45
13.5
PLD
0.1
5-7
1096
5
50-55
The
number
of
free
doxorubicin
and
PLD
(hydrogenated
soy
phosphatidylcholine:cholesterol:PEG2000-distearoylphosphatidylethanolamine, 2:1:0.1) are
given for a single dose of 50 mg/m2, and the number of CL (egg
phosphatidylcholine:cholesterol, 55:45) are given for a dose of 90 mgm2
Comparison of Liposome
Clearance from Blood
Drug Concentration (mcg/mL)
14
CAELYX™/Doxil® (PLD)
DaunoXome®
12
Myocet®
10
8
6
4
2
0
0
4
DaunoXome® (NeXstar Pharmaceuticals)
Myocet® (Elan Corporation)
8
12
16
Hours After Infusion
20
24
Dose-Dependent Clearance of
CAELYX™
PK Simulations: 10-60 mg/m2
Plasma Concentration Doxorubicin
(µg/mL)
100.000
10.000
1.000
10
20
30
40
50
60
0.100
0.010
0.001
0.000
0
48
Martin F and Amantea M.
96
144 192 240 288 336 384
Time Following Infusion (hours)
432
480
mcg DOX—Equivalents per mL
CAELYX™/ Doxil® (PLD) Remains
Encapsulated in the Liposome
100.00
PLD 50 mg/m2
10.00
1.00
Encapsulated PLD
Total PLD
0.10
0.01
0
24
48
72
96
120
Hours After Injection
Gabizon AN. Cancer Res. 1994;54:987-992.
144
168
b) TESSUTO TUMORALE
a) TESSUTO NORMALE
~
endotelio continuo
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~ ~
~
~
~
~
~
~
endotelio discontinuo
~
~
~
~
~
~ ~
~
~ ~
~ ~ ~ ~
~
~
~ ~ ~ ~~
~ ~
~
~
~
drenaggio
linfatico
~
~
~
~
~
~ ~
~
~
~
~
~
~
~
~ ~
~
~
~
~
~
~ ~
~ ~
~
~
~
~
~ ~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~
~ ~ ~ ~
~
~
~
~
~
~
~
~
~
~ ~
~~ ~
~
~
~
~
drenaggio
~ linfatico
ridotto
~
~
Rappresentazione schematica dell’EPR: nel tessuto tumorale le macromolecole si
accumulano a causa della presenza dell’endotelio discontinuo e dell’ostruzione dei
capillari linfatici.
Stealth® Liposome Localization in
Human Tumors
Gamma Scintigraphy 24 and 48 Hours After Injection of
Radiolabeled Stealth® Liposomes
(Posterior view)
Lung
tumor
Spleen
Liver
Bone
marrow
Harrington, et al.
Clin Cancer Res. 2001.
Symon et al., Cancer 1999
Figure 2. Hematoxylin and eosin staining
of the bone metastasis in Patient 1
demonstrating the presence of a tumor
cell focus in the central part of the
figure surrounded by connective stromal
tissue in the periphery (×600).
Figure 3. (A) Fluorescence microscopic
(fluorescein filter) image of bone
metastasis in Patient 1 demonstrating
cellular and nuclear accumulation of
doxorubicin with predominant distribution
within a tumor cell focus (3750).
Symon et al., Cancer 1999
Comparative Adverse Event Profile
Doxorubicin
CAELYX™
+++
+/–
Infusion reaction
–
+ if premedicated
Nausea/vomiting
++
+/–
Myelosuppression
+++
+ (not gr 4)
Stomatitis/mucositis
++
++
Vesicant effect
Palmar-plantar skin toxicity Only with infusion
+++
Cardiotoxicity
+++
+
Alopecia
+++
+
Hand-Foot Syndrome
(Palmar-Plantar Erythema)
Summary
• Chemotherapy-induced dermopathy
• Characterized by tingling (dysesthesia), erythema, and swelling
followed in severe cases by skin breakdown
• Affecting hands, feet and other skin areas under prolonged
friction or pressure
• Common side-effect of CAELYX™, dose-intensity and scheduledependent
• Always reversible with complete healing
• Unrelated to chemotherapy vesicant effect
PPE in CAELYX™-Treated Patients
Increased Incidence With Repeated Cycles and Short Intervals
100
First cycle
Percentage Incidence
Second cycle
Third+ cycle
75
50
25
0
50 q3wk
60 q3wk
60 q4wk
Dose (mg/m2) / Schedule
70 q4wk
Vesicant Effect of Intra-Cutaneous
Injection of Doxorubicin Prevented
in CAELYX™ Formulation
Doxorubicin
i.d. 50 µg
Rt. flank
CAELYX™
i.d. 50 µg
Lt. flank
CAELYX™: Correlation of Toxicity
With Pharmacokinetic Parameters
• Leukopenia grade is positively correlated with
Cmax and AUC
• Stomatitis grade is positively correlated with Cmax
and AUC
• Hand-foot syndrome (PPE) grade is positively
correlated with T½ (half-life)
• Plasma levels and T½ during 1st cycle can predict
the risk of PPE in subsequent cycles
Cancer. 2000;89:1037-47.
LIPOSOMI STEALTH
CONCLUSIONI
• I
liposomi stealth
(Caelix) rappresentano la
tecnologia liposomiale più avanzata
• La loro composizione lipidica (fosfolipidi saturi
+colesterolo) e la loro dimensione (80nm) li rende
particolarmente adatti per la terapia antitumorale
(effetto EPR)
• L’introduzione del PEG inibisce l’uptake macrofagico
ed aumenta l’emivita plasmatica e l’AUC
• La stabilità del liposoma nel plasma impedisce il
rilascio della doxorubicina nel miocardio (no tossicità
cardiaca)
I LIPOSOMI NEL FUTURO CLINICO
I LIPOSOMI A TARGETING ATTIVO
I LIPOSOMI NELLA TERAPIA GENICA
I LIPOSOMI NELLA DIAGNOSTICA
Targeting of liposomes
Folic acid targeted liposomes
OH
N
H2N
N
N
COOH
CH2 NH
N
Folic acid
CO NH CH
CH2
CH2
COOH
Receptor-mediated endocytosis
I VIRUS SINTETICI
NELLA TERAPIA GENICA
a un involucro stabile
b ligando per conferire una
particolare affinità al vettore
c molecole che facilitano la
fusione tra il vettore e le cellule
target
d proteine che permettono una
diretta integrazione del vettore
DNA
e sequenze per permettere la
ricombinazione omologa
f regioni promoter tessuto.specifiche
g cDNA terapeutico
Fig. 2
• targeting di liposomi cationici: immunogenosoma
Fig. 9
ÉCHOGRAPHIE
AVANTAGES:
¾ Technique simple, portabilité
¾ Peu coûteuse (equipement,
examen)
¾ Sans risque ni pour le patient
ni pour le professionnel
pratiquant l’examen
PROBLÈME
MAUVAISE ÉFINITION DE
L’IMAGE OBTENUE
PARTICULES ÉCHOGÈNES
Nanoparticules à boules
Le alcane reste à
l'intérieur des
particules même si:
/ ON UTILISE UN ALCANE LINÉAIRE
ET ACYCLIQUE POUR RÉDUIRE
L’ENCOMBREMENT STÉRIQUE;
/ ON UTILISE UN PLGA CARACTÉRISÉ
PAR UNE MAJEURE
CONCENTRATION D’ACIDE
LACTIQUE ET DONC PLUS
HYDROPHOBE;
/ ON AJOUTE À LA SUSPENSION
AQUEUSE DES PARTICULES DES
SUBSTANCES CAPABLES
D’AUGMENTER LA SOLUBILITÉ DU
SOLVANT DANS L’EAU (DMSO,
ÉTHANOL);
/ ON UTILISE LA DIALYSE;
/ ON UTILISE LA LYOPHILISATION.
CONCLUSIONI FINALI
I LIPOSOMI SONO STRUMENTI VERSATILI
UTILI NEL DIREZIONAMENTO DEI FARMACI
NELLA TERAPIA GENICA E NELLA DIAGNOSTICA