CAUSE EXTRACARDIACHE DI
SCOMPENSO CARDIACO
NEONATALE
Corrado Cecchetti, Nicola Pirozzi
Dipartimento di Emergenza
Ospedale “Bambino Gesù”
Slide 001
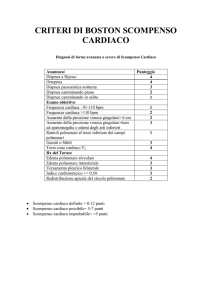
INSUFFICIENZA CARDIACA NEL NEONATO
Sul piano fisiopatologico il cuore del
neonato presenta numerosi fattori
che lo pongono in una condizione di
svantaggio in relazione alle diverse
condizioni patologiche
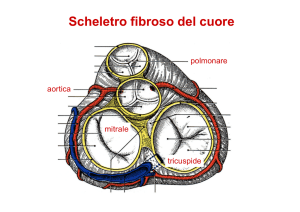
PORTATA CARDIACA
Durante la vita fetale la portata cardiaca è
distribuita ai due ventricoli
• 300 ml (66%) al ventricolo destro
• 150 ml (34%) al ventricolo sinistro.
vita fetale, i ventricoli in parallelo
vita extrauterina, in serie
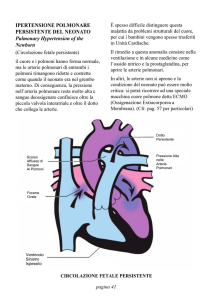
FLUSSO DEL SANGUE NELLA
VITA FETALE
•66 % del flusso sanguigno del VD al tronco
dell’AP
7 % ai rami destro e sin dell’AP
59 % aorta descendente attraverso il DA
•34 % del flusso di sangue del VS
3% arteria coronaria (AC)
21 % vasi epiaortici
10 % all’ istmo aortico si unisce
all’aorta discendente con il flusso
proveniente dal DA.
FASE EXTRAUTERINA
Ogni ventricolo si fa carico tutto il volume che riceve
(circolazione in serie e non in parallelo), con aumento del
lavoro ventricolare sinistro del 200% (da 150 a 450
ml/kg/min).
• Il ventricolo sinistro si trova già, di base, in una condizione
di riserva con difficoltà ad affrontare sia condizioni
– sovraccarichi di volume
– sovraccarichi pressione
– alterazioni non strutturali (anemia, ipoglicemia, ipocalcemia
iperidratazione)
PORTATA CARDIACA NELLA VITA
EXTRAUTERINA
•
prima settimana da 450 ml/Kg/min a 300 ml/kg/min (33
% in meno rispetto alla nascita)
•
6 settimane si riduce fino a 150 ml/kg/min
•
6 mesi 70-80 ml/Kg/min
•
adulto è 70 ml/Kg/min
emodiluizione fisiologica può spiegare in parte la
riduzione dell’effetto dei farmaci inotropi esogeni.
CO
biventricolare
NASCITA
CO
Sinistro
SETTIMANE
MESI
LA RIDUZIONE DELLA
PORTATA
Nei primi giorni di vita il solo meccanismo
di compenso per la ottimizzazione della
portata cardiaca è la frequenza già
mantenuta ad un livello massimale per la
tachicardia fisiologica
DETEMINANTI DELLA FUNZIONE CARDIACA
NEL NEONATO
Contrattilità
La presenza di un ridotto numero di unità
contrattili per mm quadrato di superficie
determina una riduzione della forza contrattile.
•
gli elementi contrattili del neonato non superano
il 30% (vs 70%)
• elevata tendenza a iperplasia mediante fattori di
crescita tessutale.
DETERMINANTI DELLA FUNZIONE CARDIACA
NEL NEONATO
Precarico
Precarico, espresso dalla lunghezza massima della
fibra muscolare a fine diastole dipende da:
a) compliance ventricolare
b) ritorno venoso.
DETERMINANTI DELLA FUNZIONE CARDIACA
NEL NEONATO
Precarico
Il ritorno venoso nel neonato è
aumentato, per:
• incremento della portata cardiaca
• Frank Starling è al livello massimale con ridotto
margine per tollerare carichi aggiuntivi sia per
cardiopatia che per iperidratazione fino ad un
limite massimo dopo il quale si determina un
sovrastiramento.
DETERMINANTI DELLA FUNZIONE CARDIACA NEL
NEONATO
Postcarico
Postcarico è la massima tensione all’inizio della diastole ed è
dipendente in forma direttamente proporzionale alla
pressione intraventricolare e al raggio della cavità
Il raggio della cavità è aumentato per il maggior precarico, per
• incremento del ritorno venoso
• spessore della parete ridotto non consente di compensare un
sovraccarico di pressione.
Eziologia della insufficienza cardiaca
neonatale per
- Cause extracardiache
- Cause cardiache
CAUSE EXTRACARDIACHE DI
SCOMPENSO CARDIACO
• Sovraccarico di volume
•
• Sovraccarico di pressione
• Alterazioni metaboliche del metabolismo
muscolare
•
• Alterazioni del ritorno venoso e del
riempimento ventricolare
CAUSE EXTRACARDIACHE DI
SCOMPENSO CARDIACO
Sovraccarico di volume
• shunt sin-Dx con iperafflusso
polmonare (soprattutto prematuri),
• fistole arterovenose
• insufficienze valvolari
NON CIANOGENE
Con normale flusso polmonare
Con iperafflusso polmonare
coartazione aortica, stenosi
valvolare polmonare
DIV, DIA, pervietà dotto
arterioso, canale
atrioventricolare
CIANOGENE
Con flusso polmonare
Con iperafflusso polmonare
tetralogia di Fallot, atresia
polmonare, atresia della tricuspide con
stenosi polmonare
trasposizione completa dei grossi
vasi, tronco arterioso, ventricolo
unico
Cardiopatie congenite
Iperafflusso polmonare
Calo resistenze polmonari
Shunt sinistro-destro
Quota di sangue in arteria polmonare ed
all’atrio sinistro
Cardiopatie congenite
Iperafflusso polmonare
Direzione ed entità dello
shunt:
• RESISTENZE POLMONARI
• DIMENSIONI DEL DIFETTO
PERVIETA’ DOTTO ARTERIOSO
> prematuri
dismaturi
Pervietà del dotto di Botallo, che mette in comunicazione a.
polmonare ed aorta. Condizione normale nelle prime
settimane di vita
IPERAFFLUSSO POLMONARE
CLINICA
<1500 g
Silente se di piccole dimensioni
R endocardite
Soffio continuo sottoclaveare sx
Scompenso se di grandi dimensioni
Rischio di emorragia endocranica
Rischio di NEC
PERVIETA’ DOTTO ARTERIOSO
TERAPIA
NEONATO A TERMINE
Chiusura chirurgica/percutanea
(6-12 ms)
NEONATO PRETERMINE
Se non impatto clinico follow-up fino ai 6 mesi
probabilità di chiusura spontanea tardiva
alta
Se sintomatico
chiusura farmacologica mediante
indometacina in 3 dosi a intervalli di 12-24 ore
CAUSE EXTRACARDIACHE DI
SCOMPENSO CARDIACO
Sovraccarico di pressione
• patologie ostruttive sinistre (Stenosi
Aortica, CoAo)
• patologie ostruttive destra (stenosi
polmonare valvolare critica).
NON CIANOGENE
Con normale flusso polmonare
Con iperafflusso polmonare
coartazione aortica, stenosi
valvolare polmonare
DIV, DIA, pervietà dotto arterioso,
canale atrioventricolare
CIANOGENE
Con flusso polmonare
Con iperafflusso polmonare
tetralogia di Fallot, atresia
polmonare, atresia della tricuspide con
stenosi polmonare
trasposizione completa dei grossi vasi,
tronco arterioso, ventricolo unico
DEFINIZIONE
• Restringimento tra arco aortico e aorta discendente a
livello del dotto arterioso
• Può essere isolata, associata a DIV e a persistenza del
dotto arterioso
• Si distinguono in
– Esordio neonatale: perfusione del circolo sistemico
distale è assicurata dal PDA; la chiusura del dotto
aumenta l’iperafflusso polmonare, con stasi
polmonare, ipoperfusione e insufficienza renale
progressiva
– Forme infantili: senza dotto-dipendenza, nelle quali
prevale l’aumento della pressione nel ventricolo
sinistro, nell’aorta ascendente e nei vasi epiaortici
FISIOPATOLOGIA
• Sovraccarico pressorio con aumento del
post-carico
– Evolve in scompenso cardiaco nel neonato
• Aumento pressorio ai distretti superiori
• Sviluppo di ipertrofia ventricolare sinistra
• Sviluppo di circolo collaterale arterioso
distretti superiori Æ distretti inferiori
CLINICA
• NEONATALE
– Nella seconda settimana di vita scompenso cardiaco che
precipita dopo la chiusura del dotto arterioso
– I polsi femorali sono assenti
– La saturazione O2 è inferiore negli arti inferiori rispetto ai
superiori
– La pressione arteriosa sugli arti inferiori è ridotta rispetto a
quella dei superiori
– Nel 50% dei casi è presente soffio sistolico, il T2 è unico e forte,
generalmente presente il ritmo di galoppo
CLINICA
INFANTILE
– Improbabile lo scompenso cardiaco e le condizioni generali si
mantengono buone
– Iposfigmia dei polsi femorali
– Pressione arti inferiori è ridotta rispetto a quella degli arti
superiori
– Soffio sistolico eiettivo in parasternale sinistra alta
COSA FARE NEL NEONATO
• Ricovero alla nascita per diagnosi prenatale
• Monitor Sat O2 con sensore arto superiore + arto
inferiore
• Misurare Pressione Arteriosa arto superiore + arto
inferiore per 3 volte al giorno
• Controllare la diuresi
• Su accordo e indicazione dei cardiologi specialisti,
iniziare terapia con ossigeno a flusso libero davanti alla
bocca
DIAGNOSI
• NEONATALE
–
–
–
–
–
Ecografia pre-natale
Rx Torace : cardiomegalia, congestione venosa polmonare
ECG : ipertrofia ventricolare destra
Ecocardiografia : documentazione della coartazione aortica
Cateterismo cardiaco + angiografia
• INFANTILE
– Rx Torace : cuore normale o lievemente ingrandito
– ECG : normale o ipertrofia ventricolare sinistra
– Ecocardiografia con doppler : turbolenza del flusso a livello del
restringimento
– Cateterismo cardiaco + angiografia
TERAPIA
• NEONATALE
• Terapia insufficienza cardiaca
• Infuisione ev continua di Prostaglandine E1 per tentare di riaprire il
dotto e ristabilire un flusso in aorta discendente e reni
• Con paziente stabilizzato: correzione chirurgica della coartazione
aortica
• Nel 30% dei casi a distanza si forma nuovamente coartazione
aortica : correggibile con angioplastica percutanea con palloncino
• INFANTILE
• Correzione chirurgica elettiva
– 2 anni : nel bambino asitnomatico
– al momento della diagnosi (se diagnosi fatta già dopo i 2 anni
di età)
– Prima dei 2 anni se ipertensione severa e cardiomegalia
STENOSI E ATRESIA DELLA POLMONARE
Strozzatura alla via d’uscita del
ventricolo dx in sede valvolare,
sopravalvolare o sottovalvolare
portata polmonare
ipertrofia ventricolare dx
CLINICA
Modesta/nulla nelle forme lievi
Nelle forme gravi: cianosi, facies
tondeggiante, vene giugulari pulsanti
TERAPIA
Follow-up ecocardiografico nei casi lievi
Intervento chirurgico nelle forme gravi (entro i 10 aa)
CAUSE EXTRACARDIACHE DI
SCOMPENSO CARDIACO
Alterazioni metaboliche del metabolismo muscolare
Cause che compromettono la produzione, la riserva
e l’utilizzo di energia con deterioramento primitivo
dell’elemento contrattile e conseguente disfunzione
miocardica.
All’interno di questo gruppo possiamo considerare
ipossia acidosi ipoglicemia., alterazioni elettrolitiche
FATTORI METABOLICI
Glucosio
Il muscolo cardiaco nel neonato:
• Utilizza unicamente come combustibile
glucosio-6-fosfato.
• depositi di glucogeno del neonato
• Solo tardivamente si sviluppano altre vie
metaboliche (acidi grassi) che minimizzano
l’impatto dei rischi cardiologici connessi
all’ipoglicemia.
Incidenza
• 2% nel neonato a termine
• 8% nel neonato LGA (grande per l’età gestazionale)
• 15% nel neonato SGA (piccolo per l’età gestazionale)
ABC dell’omeostasi del glucosio nel feto e
neonato
• In gravidanza, il glucosio passa al feto in maniera continua
attraverso la placenta, per diffusione facilitata. La glicemia
fetale è ~ 70% di quella materna, cioè > 50 mg/dl.
• Le scorte di glicogeno epatico fetale:
– raddoppiano alla 36° settimana di gravidanza diventando il triplo
dell’adulto.
– si esauriscono entro le prime 24 ore di vita
• Alla nascita, la glicemia scende e rimane per qualche ora
intorno ai 30 mg/dl (cioè al 5° percentile dei valori materni)
per poi risalire a livelli >36 mg/dl che si mantengono per 72
ore.
LIVELLI DI GLICEMIA E RISCHIO
Neonati a rischio:
Consigliato lo screening (prima del pasto ed entro 2-3 ore dalla
nascita o se compaiono sintomi)
Se glicemia <45 mg/dl *
• stretta sorveglianza
• trattamento se i livelli non migliorano dopo il pasto
• trattamento se compaiono manifestazioni cliniche
Se glicemia <20-25 mg/dl
• glucosio e.v. per inalzare i livelli
> 45 mg/dl
* < 36 mg/dl (nel lavoro originale)
Terapia dell’ipoglicemia neonatale
Davanzo R, Barth E, Demarini S, “L’ipoglicemia neonatale”, Medico e Bambino 2004;23:699-704
Glicemia < 45 mg/dl (dopo il pasto o in presenza di sintomi)
Crisi convulsive: SG 10% 2 ml/kg ev in bolo B infusione SG 10% 8 mg/Kg/m
In tutti gli alti casi : SG 10% ev in flebo (85-115 ml/Kg/die = 6-8 mg/Kg/m)
Se la glicemia rimane < 45 mg/dl
salire a 8,10,12 e 15 mg/Kg/m (SG 10-12%) in base ai controlli glicemici orari
portare la glicemia > 45 mg/dl
(per SG >12% o fabbisogni di glucosio >10 mg/Kg/m Ö catetere venoso centrale)
Se l’ipoglicemia è ricorrente e il fabbisogno di glucosio ev è >15mg/Kg/m:
Idrocortisone: 10 mg/Kg/die ev in 2-4 dosi
Glucagone: 300 gamma im oppure in infusione continua 20-40 gamma/h
fino a
FATTORI METABOLICI
Calcio
Ipocalcemia per insufficiente scambio
fosforo calcio in età neonatale si
associa ad una ridotta organizzazione
del reticolo sarcoplasmatica per cui la
disponibilità di calcio è inferiore
CALCIO
• E’ presente nel siero in tre forme distinte:
– 30-50% legato a proteine
– 5-15% in complessi con citrato, bicarbonato, fosfato e lattato
– 50% è calcio ionizzato Ca ++ è la sola forma biologicamente attiva
e pertanto clinicamente importante
• Il metabolismo del calcio è strettamente correlato a fosforo
(P) e del megnesio (Mg)
• Normali livelli ematici di calcio ionizzato sono essenziali
per il processo della coagulazione, eccitabilità neuromuscolare, integrità e funzionalità delle membrane
cellulari, attività enzimatica e secretoria cellulare,
osteogenesi e mantenimento dell’integrità ossea
NEONATO E OMEOSTASI CALCICA
Il neonato sano a termine alla nascita presenta elevate
concentrazioni di
• Ca sierico [10-11 mg/dl]
• P [5-6 mg/dl
• Mg sono strettamente correlati a quello materno
Entro le prime 24-48 ore di vita la calcemia diminuisce di
circa 2 mg/dl
IPOCALCEMIA
NEONATALE
Calcemia < 8 mg/dl
Calcio ionizzato < 4 mg/dl
Cause :
•PREMATURITA’
•DIABETE MATERNO
•ASFISSIA FETALE O NEONATALE
•FARMACI ALLA MADRE IN GRAVIDANZA:
•TAGLIO CESAREO IN ASSENZA DI
TRAVAGLIO
• FRATTURA DELLA CLAVICOLA
FATTORI METABOLICI
Hb Fetale
Hb fetale gioca un ruolo negativo per la ridotta
quantita di 2-3 difosfoglicerato che sposta la
curva di dissociazione Hb a sinistra.
Determina maggiore difficoltà a cedere ossigeno
ai tessuti, con una maggiore necessità di flusso
sanguigno che il cuore neonatale non sopporta.
Con età la Hb fetale si riduce e i problemi si
attenuano
IPOSSIA ACIDOSI
Molteplici condizioni inducono ipossia e
acidosi elementi che deteriorano
fortemente la contrattilità miocardica
INNERVAZIONE E
CATECOLAMINE
• Nel neonato la innervazione simpatica è
irregolare e incompleta
• deficit che determina una eccessiva quantità di
catecolamine circolante (> 30 volte dell’adulto).
• ridotto numero e densità di beta recettori è
aggravato da una emodiluizione fisiologica che
riduce l’efficacia delle catecolamine esogene.
• I meccanismi di compenso si sviluppano solo
tardivamente e richiedono un maggior tempo di
sviluppo
CAUSE EXTRACARDIACHE DI
SCOMPENSO CARDIACO
Alterazioni del ritorno venoso e del
riempimento ventricolare
Fibroelastosi endomocardica
Forme ipertrofiche
sepsi
Questi quadri rispondono favorevolmente e
rapidamente al trattamento eziologico
(glucosio, calcio per ipocalcemia , trasfusione)
e al trattamento con farmaci inotropivasodilatatori che sono solo palliativi per il
trattamento eziologico.
Slide 004