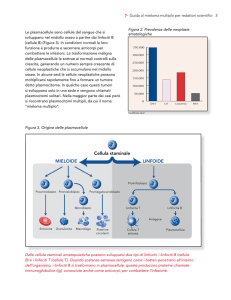
Sviluppo dei Linfociti B
Fase Antigene-indipendente:
n
Midollo
n
Organi Linfoidi Secondari
Fase Antigene-dipendente:
n
Organi Linfoidi Secondari
risposta ad Antigeni T-dipendenti
risposta ad Antigeni T-indipendenti
Alcuni marcatori dei B maturi
n
Attivazione BCR:
n
n
n
Molecole di adesione:
n
n
n
n
CD21: rec C3d
CD35: rec C3b
Differenziamento:
n
n
n
VLA-4: integrina, lega VCAM-1
CD34: lega la L-selettina
Recettori per il Complemento:
n
n
CD19: trasmette segnale
CD45 (B220): tirosin-fosfatasi
CD10: sui B precursori
CD43: su B immaturi
Cooperazione T/B:
n
n
CD80 (B7): lega CD28 e CTLA-4 sui T
CD40: lega CD40L sui T
MATURAZIONE DEI
LINFOCITI B NEL MIDOLLO
i Progenitori dei Linfociti B nel Midollo
Progenitori
marker
HSC
cKit++
MPP
cKit++
Flt3
ELP
cKit+
(precursore
linfoide precoce)
Rag+
CLP
cKit+
(progenitore
linfoide comune)
IL-7R+
Rag+
Potenzialità e attività
Progenitore totipotente
Progenitore multipotente: CMP e ELP
dà origine a T,B,NK
Inizia riarrangiamento D-J catena H
dà origine a T,B,NK
riarrangiamento D-J catena H
Maturazione dei Linfociti B nel midollo
HSC
MPP
ELP
CLP
pro -B
pre-BI
Large
preBII
Small
preBII
Immature B
i Progenitori dei Linfociti B nel Midollo
Progenitori
Pro-B
Attività
marker
B220 (CD45)+
IL-7R+,
B (T)
riarrangiamento D-J catena H
IL-7R+, B220+,
CD19+ , CD10, RAG+,
VpreB, λ5,Iga e Igb
Completa il riarrangiamento DJ e inzia il V-DJ catena H
Pre-B II
grande
IL-7R+, B220+, CD19+,
CD10, Igα, Igβ, µ,
VpreB, µλ5
Esprime il pre-BCR
esclusione allelica - Prolifera
Pre-B II
piccola
IL-7Rlow, B220+,CD19+,
RAG+, Igα, Igβ, µ
Riarrangiamento V-J catena L.
Non prolifera
B
Immaturo
B220+, CD19+, RAGlow,
Igα, Igβ, µ, k/λ
Esprime BCR con IgM
Test di Autoreattività:
Pre-B I
n
n
Revisione del recettore
Selezione Negativa
Pre-BCR
Struttura:
n
Surrogato della catena L invariante:
catena VpreB + catena λ5 con una specificità unica
(regione UR)
n
Catena μ
n
Igα+ Igβ
Struttura differenziale del Pre-BCR
UR
(regione
unica)
Geni e
Struttura
del
Surrogato
della
catena L
Funzioni del pre-BCR
nel Pre-B II grande:
n Induce
il segnale di proliferazione
n Inibisce
n Induce
n Induce
n Induce
l’espressione del surrogato
il riarrangiamento della catena L
l’esclusione allelica
l’eliminazione dei cloni autoreattivi tramite
Selezione Negativa e Revisione del Recettore
Il pre BCR autoreattivo
induce la Prima
Ricombinazione del gene L
(prima Revisione del
Recettore )
il BCR nei B immaturi
autoreattivi induce una
Seconda Ricombinazione del
gene L
(seconda Revisione del
Recettore )
Nello sviluppo
dei B i
recettori
autoreattivi
stimolano la
Proliferazione
e la
Revisione del
Recettore
Revisione del
Recettore
Importanza dell’Autoreattività nei
primi stadi dello sviluppo dei B
Induce l’espansione clonale dei precursori
n E’ necessaria per la generazione della
diversità
n Il pre-BCR, esprimendo un recettore
invariante autoreattivo, assicura la
sopravvivenza dei B che hanno espresso
una catena H produttiva
n
Eliminazione dei Cloni Autoreattivi
= Induzione della Tolleranza
Nella maturazione e nell’attivazione dei Linfociti B si possono formare
cloni che riconoscono il self:
n
Durante il riarrangiamento V(D)J sia primario che secondario
(Revisione del Recettore, centrale e periferica)
n
Durante l’Ipermutazione Somatica nei Centri Germinativi, dopo il
contatto con l’antigene
L’Eliminazione dei cloni autoreattivi avviene:
n sia nel Midollo che in Periferia tramite la Selezione Negativa:
n
n
Delezione Clonale (apoptosi)
n
Anergia (arresto del differenziamento)
nel Midollo tramite la Revisione del Recettore
MATURAZIONE DEI
LINFOCITI B NEGLI ORGANI
LINFOIDI SECONDARI
n
n
I linfociti B immaturi igM+ escono dal midollo e
migrano nella milza dove si differenziano in
Linfociti B Maturi Vergini igM+IgD+
I B maturi vergini (CXCR5+) ricircolano e migrano
nelle aree B-dipendenti degli OLS (CXCL13+),
dove incontrano l’antigene e vengono attivati
Sottopopolazioni di Linfociti B
Periferici Vergini
n
Linfociti B1
n
Linfociti B di Transizione (nella milza)
n
Linfociti B2 :
n Follicolari
n Zona Marginale della milza
Sottopopolazioni dei Linfociti B
Linfociti B1
n
Originano dal fegato fetale
n
Si trovano nelle cavità sierose e nelle mucose
n
B220low e IgDlow
n
n
Producono Plasmacellule secernenti IgM e IgA
poco variabili (Anticorpi Naturali),
spontaneamente o in risposta ad antigeni TI.
Difesa immediata antibatterica
Linfociti B2: Differenziamento in
periferia
B2 cell
B2 cell
Linfociti B2 B220+
B di
Transizione
IgM +++,
IgD+
B2 Matura
Follicolare
IgM +,
IgD+++
n Selezione
Negativa Periferica
n Breve
vita
n Sensib. apoptosi
n Presentano
Ag ai linfociti T
n Proliferano
B2 Matura
Zona
Marginale
IgM +++,
IgD+
n Differenziano
in Plasma cellule
Linfociti B 2
n
B Marginali:
n
n
n
n
n
sono localizzati solo nella Zona Marginale della milza
(nell’uomo anche in altri OLS e circolanti).
Producono anche Anticorpi Naturali
Hanno BCR polireattivi e TLR e hanno funzione di
Linfociti B Innati.
Dopo contatto con l’antigene attivano una rapida
(1-2gg) risposta sia di tipo innato TI che adattativa TD
con anticorpi a bassa affinità
B Follicolari:
n
n
n
sono circolanti o localizzati nelle aree B dipendenti degli
OLS.
Hanno BCR monoreattivi.
Dopo contatto con l’antigene, attivano una lenta (circa 7
gg) risposta immune adattativa TD con anticorpi ad alta
affinità
Linfociti B regolatori (Breg)
n
n
n
n
n
n
Sono una popolazione di B, individuata nel 1970 nei topi, con ruolo
immunosoppressivo: inibisce le altre cellule immuni tramite
produzione di citochine (Il-10 e TGF-β) e presentazione
antigenica.
Non hanno un fenotipo specifico
Sono note come B10, perché regolano la risposta immune tramite
la produzione di IL-10, che è una citochina anti-infiammatoria
L’IL-10 prodotta dai Breg regola la produzione di TNF-αdai
monociti, inibisce la produzione di citochine pro-infiammatorie dai
TCD4+, sopprime la proliferazione cellulare e attiva i Treg
Sono potenti regolatori delle malattie allergiche e autoimmuni, del
cancro, delle infezioni, del rigetto ai trapianti.
La recente scoperta di B10 umane permette alla ricerca clinica di
utilizzare il potenziale regolatore di queste cellule nel trattamento
di malattie immunitarie (SLE e MS) e di risposte immuni aberranti
Mouse B1, B2 and regulatory B cell subsets phenotype .
!
DESTINO DELLE CELLULE B MATURE
n
n
n
La vita delle cellule B mature dipende dalla
selezione con l’antigene
Cellule B non stimolate sopravvivono al
massimo qualche giorno
La reazione con l’antigene porta
all’attivazione e alla diversificazione delle
cellule B2
Ruolo dell’Antigene nel Destino dei
Linfociti B
Antigeni Self:
n Presentati nel midollo a cloni B immaturi
autoreattivi inducono la Selezione Negativa
(anergia, delezione) o la Revisione del Recettore
n Presentati nella milza ai B immaturi autoreattivi
inducono la Selezione Negativa
Antigeni non Self:
n Presentati negli OLS a cloni B maturi inducono
l’attivazione e l’ulteriore differenziamento
ATTIVAZIONE DEI
LINFOCITI B
n
1a fase: Riconoscimento dell’Antigene
n
2a fase:
n
n
a) Cooperazione con i Linfociti T e differenziamento in
Plasmacellule
b) Migrazione nei Centri Germinativi e ulteriore
differenziamento
Cattura dell’antigene da parte dei
Linfociti B nei Linfonodi
Grazie a tecniche di microscopia in vivo si sono evidenziate
due vie che dipendono dalla natura dell’antigene:
n
n
1.Antigeni Piccoli Solubili (<60kD):
trasportati passivamente nei Condotti
Reticolari del follicolo
catturati
direttamente dai linfociti B
2.Antigeni Particellati (virus, Complessi
Immuni…): catturati dai macrofagi del SCS o
dalle FDC nei follicoli
presentati ai linfociti B.
Condotti Reticolari
Sono costituiti da Fibre Reticolari formate da
collagene e rivestite da Fibroblasti Reticolari (FRC)
n
n
Sede:
n Nel linfonodo: nei follicoli associati alle FDC e
nella zona paracorticale
n Nella milza: nelle aree T e B dip
Funzioni:
n Secrezione di chemochine specifiche
migrazione dei linfociti e delle DC
n Trasporto passivo di piccoli antigeni
Sezioni longitudinale e trasversale
di un condotto reticolare
Condotti Reticolari differenti per la
Migrazione dei Linfociti T e B nei
Linfonodi
CXCR5+
CCR7+
Vie di trasporto dell’antigene (Solubile e
Particellato) nel linfonodo
Dinamica della cattura dell’antigene
nel linfonodo (in vivo)
Macrofagi del SCS
Antigeni nel SCS
Macrofagi Midollari
Antigeni nel
follicolo e
nella
midollare
Antigeni nel GC
cattura degli antigeni
particellati nel linfonodo
Gli Antigeni nativi (>60 kDa), entrati tramite i vasi linfatici
afferenti nel seno sottocapsulare (SCS), si legano ad
anticorpi o complemento (CI):
n
n
n
Sono catturati dai Macrofagi Sottocapsulari (in pochi
minuti)
Migrano nella regione midollare per essere catturati e
degradati dai Macrofagi Midollari (in poche ore)
Si infiltrano nei follicoli dove sono trattenuti
sulle FDC (per giorni o settimane)
Ruolo dei B nella cattura dell’ antigene
nativo presente sui macrofagi del SCS
Non cognate B cell
Cognate B cell
Riconoscimento degli antigeni
nativi da parte dei Linfociti B
n
In pochi minuti:
n
n
n
n
I Linfociti B Marginali affini riconoscono i complessi immuni
(CI) presenti sui macrofagi del SCS
Trasportano i CI al bordo dei follicoli dove cooperano con i T e
si differenziano in Plasmacellule precoci secernenti anticorpi a
bassa affinità
Altri B non affini trasportano i CI all’interno del follicolo sulle
FDC
Entro diversi giorni/settimane:
n
I Linfociti B follicolari affini catturano i CI presenti su FDC nei
follicoli
n
cooperano con i T differenziandosi in Plasmacellule secernenti
anticorpi ad alta affinità
ATTIVAZIONE DEI LINFOCITI B2
con antigene T-indipendente:
Antigene T-indipendente
Linfociti B2 MZ
Plasmacellule Extrafollicolari
che producono Ig
a vita breve e a bassa affinità
Attivazione
dei
B2 Marginali
umani con
Antigeni TI
Nat.Rev.Immunol 2013,13
Attivazione TD dei B2 MZ
nella milza
CG
ATTIVAZIONE DEI LINFOCITI B2
con Antigene T-dipendente :
Antigene T-dipendente
Linfociti B2 MZ
Plasmacellule
a breve vita: Ig
a bassa affinità
Attivazione rapida dei B
Linfociti attivati Th
Linfociti B2 FO
Attivazione tardiva dei B
Linfociti T FH
n
n
Plasmacellule a lunga vita: Ig ad alta affinità
cellule della memoria
Cooperazione Primaria T-B
PC
CG
Cooperazione
B/T
primaria :
Attivazione B
Migrazione dei B attivati dall’antigene verso la
zona esterna del follicolo (mediata da CCR7)
Cooperazione 1°dei B con i T attivati (TH )
Via Extrafollicolare :
Proliferazione
Differenziamento in
Plasmacellule a breve vita con
anticorpi a bassa affinità
Via Follicolare:
Nel Centro Germinativo
Zona Scura:
Proliferazione e Diversificazione
Zona Chiara:
Cooperazione 2° B/T
Differenziamento dei Linfociti B2
follicolari nei Centri Germinativi
Proliferazione e Diversificazione nella
Zona Scura dei GC
Migrazione nella zona chiara del GC:
n
2° Riconoscimento dell’antigene, presentato dalle FDC
n
2° Cooperazione con i TFH
Differenziamento in :
n
1.
2.
- Plasmacellule a lunga vita e ad alta affinità
- B memoria
T Helper Follicolari : TFH
"
"
"
"
Sono Th attivati (CXCR5++) che migrano nei Follicoli
(CXCL13+)
Sono specializzati per cooperare con i B nei follicoli
durante il loro differenziamento antigene-specifico
Promuovono l’espansione clonale dei B, lo scambio
isotipico, il differenziamento in plasmacellule e in
cellule di memoria e la formazione dei CG
Sono attivati da Cellule Dendritiche, Linfociti B, IL-12
Legame dei B con
FDC e Tfh nel
Centro
Germinativo
Eventi
maturativi dei
B nel Centro
Germinativo
TFh
Selezione
dei Lnfociti
B nel
Centro
Germinativo
Ann.Rev.Immu. 2012,12
CXCL13 +
CXCL12 +
Eventi maturativi nel Centro Germinativo
ZONA SCURA:
Espansione clonale dei B attivati
Diversificazione del BCR:
Ipermutazione somatica e Revisione del recettore
Maturazione dell'affinità
Apoptosi
ZONA CHIARA:
Riconoscimento con l’antigene presentato dalle FDC
Apoptosi
Selezione Positiva dei cloni con alta affinità
Cooperazione con i TFH
B memoria (Ricircolo) e PC a lunga vita
Apoptosi
Linfociti B di Memoria
Cellule a lunga vita con elevata affinità specifica verso gli
antigeni:
n cellule secernenti anticorpi (Plasmacellule a lunga vita)
n cellule non-secernenti
Attivazione delle cellule di memoria non- secernenti, dopo
riesposizione all'antigene:
n
n
n
Rapida espansione clonale
Rapida attivazione dei CG.
Elevati livelli di anticorpi circolanti ad alta affinità
Schema Risposte TD
dei B2 nella milza
Nat.Rev.Immunol 2013,13
Meccanismi dell’Attivazione
dei Linfociti B
n
n
n
n
n
n
n
n
n
Legame del BCR con l’Ag
Attivazione del Recettore
Trasduzione del segnale
Attivazione del Citoscheletro
Internalizzazione Ag
Processazione Ag
Presentazione Ag ai Th
Cooperazione B/T
Attivazione dei B e dei T
Attivazione
dei B
Legame con
l’antigene
tramite
BCR, Cd21 e
TLR
CD8
1
o CD21
primi segnali
di attivazione
di BCR e CD21
modello dell’inizio
dell’attivazione dei
B in risposta al legame con
l’antigene
legato su APC
• Legame del BCR con l’ antigene
• Cambiamento conformazionale del
recettore
• Reclutamento delle kinasi Lyn
• Fosforilazione delle ITAM di Igα/β
• Formazione dei “Microcluster”
Sinapsi Immunologiche nei Linfociti B
Funzioni dei microcluster: Trasduzione del segnale e Polimerizzazione dell’Actina
Nat.Rev.Immunol. 2013,13,475
Attivazione dei Linfociti :
Formazione delle Sinapsi
n
n
n
Gli antigeni nativi, legati sulla membrana delle APC specializzate
(Macrofagi, FDC, DC), vengono riconosciuti dai BCR delle cellule B
Si forma una piccola piattaforma di segnale o "Microcluster”:
. Attivazione di Igα/Igβe di CD19,
. Attivazione di prime molecole di segnale (Src),
. Attivazione delle Integrine (LFA1, VLA4) che
promuove l’adesione dei B con le APC
. Polimerizzazione rapida dell’actina che porta alla
riorganizzazione del citoscheletro: allargamento e
contrazione della piattaforma
La concentrazione di molti "Microclusters” e la polarizzazione
dei microtubuli formano la Sinapsi
Immunologica
Sinapsi Immunologiche nei Linfociti B
Nat.Rev.Immunol. 2013,13,475
Sinapsi Immunologica dei Linfociti B:
Struttura
Area della membrana specializzata ricca di colesterolo,
glicosfingolipidi, molte proteine del segnale e Molecole
Adattatorie.
E’ associata a proteine del citoscheletro
Una Sinapsi matura è formata da tre zone concentriche:
1. centrale: con BCR + ag
2. mediana: con molecole di adesione e Lisosomi
3. periferica: con actina
Sinapsi Immunologica dei
Linfociti B: Funzioni
n
n
n
n
Trasporto di lisosomi al sito dell’incontro con
Ag
Esocitosi di proteasi lisosomiali in situ
Estrazione dell’Antigene dalle APC
Internalizzazione del complesso BCR/Ag
Processazione Ag e Presentazione ai Linfociti T
Membrane
trafficking
events
required for
antigen
processing
in B cells
APC
Synapse I
1° Cooperazione T/B
In tutte le
Cooperazioni si
formano Sinapsi
Immunologiche
2° Cooperazione T/B
La Maturazione dei B è controllata a
livello trascrizionale da diversi fattori
Durante lo sviluppo nel midollo osseo :
n
Recettori Transmembranari:
n
c-kit, Flt3, IL-7R: controllano i progenitori
e non sono specifici
Fattori di Trascrizione:
non specifici:
NFkB, PU.1, Ikaros, IRF
specifici:
E2A, EBF: controllano il riarrangiamento V(D)J
Pax5: attiva la trascrizione di geni specifici dei B
n
reprime geni della linea non-B
Azione dei Fattori di Trascrizione nello
sviluppo dei B nel midollo
Specifici dei B
Controllo trascrizionale nei B durante il
differenziamento in periferia :
n
Recettori Transmembranari :
n
n
BCR, BAFF-R (specifici per i B)
Fattori di Trascrizione :
n
n
NFkB, Notch2, Aiolos (non specifici)
OCT2, OBF1, Pax5 (specifici per i B)
Controllo Trascrizionale del Differenziamento
dei Linfociti B in periferia
(B2)