Scuola di Scienze mediche e Farmaceutiche
VIRUS di EPSTEIN BAR
www.microbiologia.unige.it
Prof. Oliviero E. Varnier
2014
Microbiologia – DISC
EBV
2
di
29
CENNI STORICI
!
Nel 1961 un chirurgo che lavorava in
Uganda, Denis Burkitt, presentò i risultati
delle sue ricerche allo staff della Middlesex
Hospital Medical School in Inghilterra.
!
Riferì che l’incidenza di un particolare tipo di
tumore in bambini africani presentava una
distribuzione geografica in rapporto alle
piogge e alla temperatura.
3
di
29
CENNI STORICI
!
Tale malattia, che colpisce circa 8 bambini su 100,000 in
alcune zone dell’Africa e della Nuova Guinea, presto fu
conosciuta come linfoma di Burkitt.
!
L’influenza del clima sull’incidenza del tumore suggeriva che un
fattore biologico ancora sconosciuto doveva essere coinvolto.
4
di
29
CENNI STORICI
!
Tre ricercatori, M.A. Epstein, Y.M. Barr and B.G. Achong, tentarono di
individuare i possibili virus oncogeni in campioni di tessuto neoplastico inviati
dall’Uganda in Inghilterra.
!
Nel 1964 riuscirono ad individuare l’agente eziologico utilizzando il
microscopio elettronico: si trattava di un nuovo virus appartenente alla
famiglia ‘herpesviridae’.
5
di
29
CRONOLOGIA
! 1958 prima descrizione del linfoma di Burkitt nella zona
malarica dell’Africa.
! 1964 Epstein e Barr ottengono linee cellulari di linfoma di
Burkitt; prima descrizione di un herpes virus infettante
tali cellule.
! 1968 EBV viene riconosciuto come agente eziologico
della mononucleosi infettiva.
! 1969 dimostrazione della capacità di EBV di trasformare
linfociti in coltura; EBV può immortalizzare cellule in
coltura e causare tumori in primati non umani.
6
di
29
INTRODUZIONE
B-91
! Il virus EB (da Epstein e Barr, che per primi l’hanno
isolato) è un herpesvirus ubiquitario responsabile
della mononucleosi infettiva e, in tempi recenti,
ritenuto uno dei fattori a rischio dello sviluppo del
linfoma di Burkitt, del carcinoma nasofaringeo e di
altre sindromi linfoproliferaive in soggetti immunocompromessi.
! L’EBV è un potente mitogeno per le cellule B, che
immortalizza in vitro.
7
di
29
Proprietà del virus
B-91
! EBV è un gamma-herpesvirus con una morfologia simile a
quella degli altri herpesvirus umani e un DNA virale di 184 kbp.
! Lo spettro d’ospite e il tropismo di tessuto di EBV sono
determinati dalla limitata distribuzione del recettore cellulare,
che è il recettore per il componente C3d del complemento (CR2
o CD21) e da un corecettore costituito dalle molecole di classe
II del sistema HLA.
! Tali recettori sono espressi sulle cellule B dell’uomo e dei
primati e sulle cellule epiteliali dell’orofaringe e del nasofaringe.
! Dopo 4-6 settimane di incubazione elevati titoli virali sono
osservabili nei lavaggi orofaringei e nella saliva.
! La produzione di elevate quantità di virus è la conseguenza di
attiva replicazione di EBV nei linfociti B (considerati il bersaglio
elettivo), che infiltrano la mucosa orofaringea.
8
di
29
Proprietà del virus
B-91
! L’infezione da EBV presenta due decorsi:
! un’infezione di tipo latente e
! una infezione di tipo replicativo.
! EBV, una volta entrato in un linfocita B quiescente, va incontro a
latenza prima di iniziare un ciclo litico, mantenendosi in forma
episomale circolare con proprietà simili al DNA cromosomale.
! I linfociti B infettati vanno quindi incontro a immortalizzazione,
proliferando continuamente ed esprimono un limitato numero di geni
virali, tra cui:
! 6 proteine nucleari della famiglia EBNA (EBV Nuclear Antigens)
! 3 proteine di membrana LMP (Latent Membrane Protein).
! A seconda del tipo di cellula infettata (linfociti B normali, cellule del
linfoma di Burkitt, cellule del carcinoma nasofaringeo) la fase di
latenza di EBV presenta caratteristiche differenti in relazione al tipo
di proteine che vengono espresse.
9
di
29
Proprietà del virus
B-91
L’attivazione del programma litico in vivo inizia quando,
tramite mecanismi non ancora chiariti, vengono espressi:
! due geni precocissimi E (immediate early) designati
BZLF1 e BRLF1, che codificano per proteine nucleari ad
attività trascrizionale che regolano l’espressione di geni
virali recoci (E, early) e di geni cellulari utili alla sintesi del
DNA virale.
! L’attivazione dei geni precoci è seguita da un’attiva sintesi
del DNA virale, all’espressione dei geni codificanti per le
proteine tardive (L, late) e dall’assemblaggio dei virioni.
10
di
29
Meccanismi patogenetici
B-92
! L’infezione da EBV è molto diffusa ed è trasmessa attraverso la
saliva e le secrezioni faringee, direttamente o tramite lo scambio di
utensili: bicchieri, posate, spazzolini ecc.
! Nei bambini l’infezione presenta un decorso subclinico inapparente,
mentre nei giovani adulti “malattia del bacio” può presentare un
decorso subclinico a diversi livelli di gravità.
! I linfociti B infettati da EBV vanno incontro ad attiva proliferazione
in assenza di apoptosi, che viene inibita da alcune proteine virali.
! La proliferazione policlonale di linfociti B si accompagna a
un’elevata produzione di immunoglobuline, tra cui IgM
! L’ingrossamento dei linfonodi, della milza e del fegato, tipico della
mononucleosi infettiva, è causato dalla proliferazione massiva sia
delle cellule B infette sia delle cellule T attivate.
11
di
29
Meccanismi patogenetici
! La linfocitosi, che si osserva nel sangue periferico a partire
dalla 2° settimana dall’infezione, è dovuta all’attivazione e
alla proliferazione dei linfociti T, che appaiono come linfociti
atipici.
! La risoluzione della malattia si osserva in seguito alla
completa eliminazione delle cellule B infettate produttivamente
da parte dei linfociti T citotossici, che riconoscono i peptidi
virali esposti sui linfociti B.
! Tuttavia, una piccola percentuale di linfociti B memoria
esprimenti gli antigeni EBNA non viene eliminata e
rappresenta la sede di latenza di EBV, che persisterà per tutta
la vita del paziente e darà avvio alla fase di riattivazione in
seguito a stimoli opportuni.
12
di
29
EPIDEMIOLOGIA
! Quasi tutta la popolazione (90-95%) è infettata da EBV e
questi soggetti, sebbene spesso asintomatici, liberano il virus
occasionalmente per tutta la loro vita.
! Il virus viene trasmesso per contatto intimo.
! L’infezione è associata con fattori socioeconomici e nei paesi
in via di sviluppo, la sieropositività si osserva più
precocemente che nei paesi industrializzati.
! Fino all’80% degli studenti che iniziano il college negli USA è
sieropositiva e molti dei studenti negativi diventeranno positivi
durante il college.
! Il virus può essere trasmesso anche con le trasfusioni di
sangue.
13
di
29
Mononucleosi Infettiva
14
di
29
MONONUCLEOSI INFETTIVA
B-93
! Come già osservato per altre infezioni primarie causate da
herpesvirus, anche nel caso di EBV la maggior parte delle
infezioni primarie presenta un decorso asintomatico.
! Le manifestazione cliniche della mononucleosi infettiva, che
compaiono dopo 30-40 giorni dal contagio, sono rappresentate da:
! malessere generale, astenia, rialzo febbrile, faringite
accompagnata da linfoadenopatia cervicale ed epatosplenomegalia.
! Raramente fatale nei soggetti sani, l’infezione può essere
accompagnata da complicanze soprattutto di natura neurologica, che comprendono la sindrome di Guillain-Barré e una
meningoencefalite asettica.
! La malattia dura dalle 2 alle 4 settimane, ma in alcuni
individui possono perdurare per alcuni mesi febbricola e
miastenia.
15 di 29
TUMORI CAUSATI DAL VIRUS di EPSTEIN-BARR
•
Linfoma di Burkitt
- circoscritto all’Africa Centrale
- eziologia multifattoriale
- l’infezione da EBV è necessaria ma
non è sufficiente
•
Carcinoma nasofaringeo
- in alcune regioni della Cina
•
Linfomi B
- in pazienti immunosoppressi
16
di
29
EBV e il Linfoma di Burkitt (BL)
HIV
MALARIA
EBV
B-cell
B-cell
B-cell
B-cell
B-cell
Attivazione policlonale
B-cell
Iniziazione
EVENTO
GENETICO
B-cell B-cell
B-cell
Attivazione
B-cell
policlonale
e immunosoppressione
BL
B-cell
Pool allargato
Traslocazioni
cromosomiche
MALNUTRIZIONE
c-myc da 8 al locus delle catene pesanti in 14
c-myc da 8 al locus delle catene leggere in 2 o 22
RISULTATO: super espressione di c-myc
17
di
29
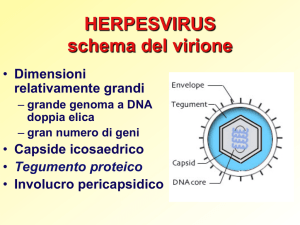
MORFOLOGIA
Il tipico virione erpetico è costituito da
quattro componenti strutturali:
§ NUCLEO (core, Ø 75 nm):
ð contiene una molecola di DNA
lineare a doppia elica (ds)
§ CAPSIDE PROTEICO (Ø 90-110 nm):
ð di forma icosaedrica circonda il core
ð costituito da 162 capsomeri prismatici
§ TEGUMENTO (20-40 nm di spessore):
ð zona amorfa ed asimmetrica di materiale proteico disposta attorno
al capside
§ PERICAPSIDE:
ð membrana esterna di natura fosfolipidica di origine cellulare
arricchita di glicoproteine virus-specifiche che sporgono dalla
superficie (spikes)
di 29
18
EBV: ANTIGENI
!
Antigeni precoci: sono proteine non strutturali, la cui
sintesi non dipende dalla replicazione del DNA virale.
!
Antigeni tardivi: sono i componenti strutturali del
capside virale (antigeni del capside) e dell’involucro virale
(pericapside). Sono prodotti in abbondanza nelle cellule con
infezione virale produttiva.
19
di
29
REPLICAZIONE VIRALE 1
Il processo che conduce alla replicazione
inizia con l’interazione delle glicoproteine virali
gp350/220 con uno specifico recettore
cellulare di membrana: CR2/CD21 recettore
della frazione C3d del complemento
Una penetrazione efficiente richiede la presenza di altre proteine accessorie: gp25, gp 42/38
e gp85, che mediano l’interazione con le molecole MHCII (co-recettori)
Dopo la fusione il nucleocapside si libera del
pericapside e rimane avvolto dal tegumento.
Viene rilasciato all’interno del citoplasma
20
di
29
REPLICAZIONE VIRALE
EBV aderisce alle cellule legando il
recettore del componente C3d del
sistema del complemento (CD21). Il
legame è mediato dalla glicoproteina
virale gp350/220, che è coinvolta
nella penetrazione del virus. Molecole gp350/220 multiple crosslegano CD21 determinando il
patching e in seguito il capping dei
complessi ligando-recettore.
Quindi il virus penetra nella cellula
per fusione dell’involucro con la
membrana plasmatica.
21
di
29
DIAGNOSI
nei casi di mononucleosi infettiva la diagnosi viene effettuata in
base alla caratteristica triade di sintomi (il quadro clinico permane
per un periodo di 1-4 settimane dalla comparsa)
1) Febbre
2) Faringite
e dalla presenza di anticorpi eterofili
!
3) Linfoadenopatia
Test di Paul-Bunnel positivo
(Mono Test, test di emoagglutinazione di emazie ovine o equine)
•
risultati falsi positivi 3% dei casi
•
risultati falsi negativi 10-15% dei casi
In caso di Mono Test negativo si procede con una diagnosi di
conferma/differenziale (per distinguere l’infezione da EBV da
mononucleosi di altra origine)
!
Diagnosi sierologica indiretta
!
Diagnosi diretta
!
isolamento del virus
!
identificazione del DNA virale
22
di
29
DIAGNOSI INDIRETTA 1
RICERCA DI ANTICORPI DIRETTI VERSO:
!
!
!
VCA (Viral Capsid Antigens) antigeni capsidici
!
gp110 e gp350 del pericapside e del nucleocapside
!
IgM: compaiono precocemente e scompaiono dopo 4-6 settimane
!
IgG: compaiono nella fase acuta con un picco dopo 2-4 settimane e declinano
lentamente persistendo per tutta la vita
EA (Early Antigens) antigeni precoci:
!
Precocissimi: BZLF1
!
Precoci: BALF2, BHRF1, BMRF1 e BSMLF1)
!
IgG: prodotte durante le fasi iniziali dell’infezione sia in fase acuta che cronica
EBNA (Epstein Barr Nuclear Antigens) antigeni nucleari
!
IgG: compaiono diverse settimane o mesi dopo l’infezione e persistono
23
di
29
Tabella 38.2 Profi lo sierologico delle infezioni da EBV B-95
24
di
29
DIAGNOSI INDIRETTA 2
VCA
IgM
VCA
IgG
EA
IgG
♦
♦
♦
Infezione cronica
♦
♦
Infezione pregressa
♦
Riattivazione
♦
Infezione acuta
sintomi
EBNA
IgG
♦
♦
⇑
VCA-IgG
EBNA-IgG
EA-IgG
VCA-IgM
1
2
3
4
5
6
mesi
25
di
29
DIAGNOSI DIRETTA
ISOLAMENTO DEL VIRUS
! EBV infetta e immortalizzare linfociti umani in coltura
! Esame indaginoso non utilizzato in diagnostica
IDENTIFICAZIONE DEL DNA VIRALE
! mediante PCR in campioni di saliva, sangue intero, tessuto linfoide
26
di
29
VACCINO
!
!
L’allestimento di un vaccino verso EBV risulterebbe di utilità per diversi
gruppi di persone sieronegative:
!
pazienti che devono essere sottoposti a trapianto di midollo o di
organo solido
!
individui che vivono in aree geografiche a rischio di elevata incidenza
di linfoma di Burkitt o di carcinoma nasofaringeo
Diversi studi sperimentali sono ancora in corso per valutare la sicurezza e
l’efficacia di alcuni vaccini:
!
per prevenire l’infezione primaria
!
!
contro la proteina gp220/350, capace di indurre risposta
immunitaria sia umorale che citotossica (dati preliminari hanno
evidenziato la comparsa di Ab neutralizzanti nei soggetti a cui era
stato somministrato il vaccino)
per generare una risposta immunitaria terapeutica via CTL
!
contro il peptide sintetico parte dell’antigene EBNA 3A
!
contro la proteina LMP 2 (espressa dal virus ricombinante
Ankara)
27
di
29
TERAPIA
! Mononucleosi infettiva
! acicloguanosina a dosi elevate (substrato della deossinucleoside kinasi virale e
inibitore della DNA polimerasi): beneficio marginale
!
!
!
!
inibisce la replicazione virale
riduce l’eliminazione del virus
non ha nessuna efficacia sui sintomi della malattia (causati dalla RI dell’ospite)
corticosteroidi: nei pazienti con complicanze gravi
! Linfoma di Burkitt
! chemioterapia (il linfoma si presenta con localizzazione multifocale)
! resezione chirurgica e radioterapia (riduzione della massa tumorale)
! Carcinoma nasofaringeo
! ablazione chirurgica della
radioterapia
lesione in associazione ad applicazioni di
! PTLD
!
!
!
riduzione della terapia immunosoppressiva
chemioterapia (antracicline, mifepristone e acido retinico)
infusione di linfociti T citotossici EBV-specifici autologhi (prevenzione)
28
di
29
! fine
29
di
29