Lenti a Contatto - Contact lenses
Agosto 2010, volume XII, numero 2
Prevenire la miopia con lenti a contatto morbide.
Attenzione alla retina periferica
Luigi Lupelli
Occhio secco e lenti a contatto
Gonzalo Carracedo OD, Msc
L’acido ialuronico e le sue applicazioni in contattologia
Matteo Fagnola, Marco Paolo Pagani, Silvio Maffioletti,
Silvia Tavazzi, Antonio Papagni
La ricerca di nuovi materiali biocompatibili per la manutenzione
quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
03>
9 7 7 0 0 0 2 0 3 83 7 0
Poste Italiane. Spedizione in a. p. - 70% - DC/DCI/VC nr 2- 2010
Nicola Pescosolido, Chiara Nardella
dodicesimoanno
con il patrocinio di
Lenti a Contatto - Contact lenses
Agosto 2010, volume XII, numero 2
Sommario
Editoriale
Luigi Lupelli
Prevenire la miopia con lenti a contatto morbide.
Attenzione alla retina periferica
pag. 35
Articoli
Gonzalo Carracedo
Occhio secco e lenti a contatto
Matteo Fagnola, Marco Paolo Pagani, Silvio Maffioletti,
Silvia Tavazzi, Antonio Papagni
L’acido ialuronico e le sue applicazioni in contattologia
pag. 37
pag. 45
Nicola Pescosolido, Chiara Nardella
La ricerca di nuovi materiali biocompatibili per la manutenzione
quotidiana delle lenti a contatto in silicone idrogel e per una nuova
frontiera delle lenti a contatto medicali
pag. 53
Rubriche
Luigi Lupelli
Pillole di lac e dintorni
Laura Boccardo
Tips & tricks
Laura Boccardo
INIEZIONE PERICHERATICA IN LUCE DIFFUSA 16x foto di Fabrizio Zeri
In libreria
pag. 61
pag. 63
pag. 64
dodicesimoanno
con il patrocinio di
Lenti a Contatto - Contact lenses
Agosto 2010, volume XII, numero 2
Lenti a contatto
Contact lenses
Codirettori scientifici
L. Lupelli (Roma), N. Pescosolido (Roma)
Comitato scientifico
L. Boccardo (Certaldo), M. Bovey (Palermo),
R. Fletcher (London), A. Fossetti (Firenze),
P. Gheller (Bologna), M. Lava (Roma), S. Lorè (Roma),
A. Madesani (Forte dei Marmi), S. Maffioletti (Bergamo),
L. Mannucci (Padova), U. Merlin (Rovigo),
M. Pastorelli (Novi Ligure), M. Rolando (Genova),
A. Rossetti (Cividale del Friuli), C. Saona (Barcelona),
L. Sorbara (Toronto), M. Zuppardo (Roma)
Ringraziamenti
Si ringraziano A.I.LAC e S.Opt.I.
per la collaborazione scientifica
Comitato editoriale
A. Calossi (Certaldo), O. De Bona (Marcon),
M. Lava (Roma), C. Masci (Roma), F. Zeri (Roma)
Segreteria
O. De Bona
via E. Mattei, 11 - 30020 Marcon (VE)
tel. 041.5939411
e-mail: [email protected]
Nome della rivista
LAC
Direttore responsabile
Marco Perini
Proprietario testata
BieBi Editrice
Editore
BieBi Editrice di Mauro Lampo
Via Losana, 4 - 13900 Biella
Tiratura
Quadrimestrale, 32 pagine
Tipografia
Arti Grafiche Biellesi
Via Biella, 58 - 13878 Candelo (BI)
Registrazione Tribunale
Biella, in data 6/5/99 al n. 487
Sped. gratuita
Numeri arretrati
Presso la segreteria
34
E D ITO R IAL E
Prevenire la miopia con lenti a contatto morbide
Attenzione alla retina periferica
Luigi Lupelli
Università degli Studi Roma Tre
Circa un quarto della popolazione del mondo occidentale è miope. Tale percentuale appare crescere in questi
ultimi anni1, in particolare in Cina.2-3, tanto che è stato
prospettato che nel 2020 circa un terzo della popolazione mondiale sarà miope.
Talvolta la miopia può essere congenita o insorgere
nell’età adulta ma questi due tipi di miopia sono piuttosto infrequenti. La miopia più comune è quella che si
manifesta nell’età scolare e che si caratterizza, tra l’altro, per aumentare di valore negli anni successivi.
Diversi approcci sono stati proposti e posti in atto con
lo scopo di poter controllare la progressione miopica
propria della tarda infanzia e dell’adolescenza. Quelli
farmacologici e ottici hanno ottenuto più credito. I farmaci più usati sono gli antimuscarinici4-8 e, tra questi,
l’atropina5-6 ha dimostrato di essere la sostanza più efficace. La presenza di rilevanti effetti collaterali rende
però estremamente marginale il loro uso. Gli approcci ottici sono stati utilizzati in maniera più estesa. Tra
questi l’ipocorrezione, a dispetto del massiccio utilizzo
anche nel tempo, si è mostrata un metodo totalmente
inefficace9. Gli occhiali sono stati prescritti anche con
lenti bifocali o progressive con lo stesso scopo. Nonostante tale metodo risultati certamente più efficace
della semplice ipocorrezione, gli effetti nell’ostacolare
lo sviluppo della miopia sono così limitati che, in particolare nei miopi non esoforici, non pare giustificata
la prescrizione10-14.
L’applicazione convenzionale (allineamento apicale)
di lac RGP è stata spesso considerata la procedura più
efficace per il controllo della miopia, ma recentemente
è stato confermato che l’effetto è di semplice modellamento corneale piuttosto che d’inibizione dell’allungamento della camera vitrea15.
Nuova linfa nel controllo della progressione miopica è
stata apportata dallo spostamento dell’interesse della
ricerca dal defocus foveale a quello periferico. E così,
in prima analisi, si è trovato che se da un lato la maggior parte degli ipermetropi, e anche degli emmetropi,
si caratterizza per la presenza di un defocus miopico
nella retina periferica, dall’altro i miopi mostrano un
defocus periferico ipermetropico16-18. Allora il mondo
della ricerca si è domandato se non fosse proprio questa peculiare ipercorrezione periferica a indurre nei
miopi il progressivo allungamento della camera vitrea
e quindi essere la causa dell’incremento della miopia.
In particolare Earl Smith III (2005, 2007, 2009) nel dipartimento di optometria dell’Università di Huston,
già crogiolo di ricerche sulla progressione miopica con
Grosvenor, i Perrigin e Goss.
Smith e collaboratori19-21, hanno mostrato, con esperimenti su animali, che l’informazione visiva proveniente dalla fovea non è essenziale nel regolare la normale
crescita oculare, né elimina il processo di emmetropizzazione. Da qui lo stesso gruppo di ricerca è arrivato a
suggerire il possibile intervento ottico per controllare
la progressione miopica attraverso la manipolazione
del fronte d’onda periferico che può essere portato davanti alla retina.
Dal versante clinico alcuni gruppi di ricerca coordinati
da Cho22-23 e da Walline24 hanno mostrato che è possibile, nei miopi, ridurre l’allungamento della camera
vitrea, e quindi la progressione miopica, se vengono
applicate lenti a contatto RGP in modalità ortocheratologica notturna. Anche in questo caso è stato ipotizzato che l’effetto sia dovuto al decremento o alla
neutralizzazione del defocus ipermetropico periferico
indotto dall’aumento di curvatura della superficie corneale paracentrale, che s’induce con le lac a geometria
inversa22.
Gli effetti di rallentamento della progressione miopica
che si ottengono, in maniera parziale, con l’ortocheratologia notturna, possono essere ottenuti con l’applicazione, più semplice e, possibilmente, dagli effetti più
prevedibili, di lenti a contatto morbide?
Tale interrogativo, oltre che a Huston, con il gruppo coordinato da Smith, se lo sono posto in Australia (Brian
Holden Vision Institute) e in Nuova Zelanda (Philips
nell’Università di Auckland). L’effetto di ciò è stato lo
sviluppo di due brevetti, già acquisiti dalle aziende, di
altrettante lenti a contatto morbide con geometrie tali
da poter gestire non soltanto la visione centrale, per
ottimizzare la percezione del dettaglio, ma anche la visione periferica, per ottimizzare la prevenzione della
progressione miopica.
Certamente è indispensabile analizzare i risultati delle
ricerche nel tempo ed è necessaria poi la verifica sul
campo, ma se ci viene data la possibilità di dire stop
alla miopia con il comfort e la semplicità di una lente
a contatto morbida è naturale pensare che il futuro dei
miopi, a rischio potenziale di incremento del difetto, è
decisamente più luminoso.
35
Prevenire la miopia con lenti a contatto morbide attenzione alla retina periferica
Bibliografia
1. Vitale S, Sperduto RD, Ferris FL III. (2009) Increased prevalence
of myopia in the United States between 1971-1972 and 19992004. Arch Ophthalmol. 2009; 127: 1632-9
2. Lin LL, Shih YF, Hsiao CK et al. Epidemiologic study of the
prevalence and severity of myopia among schoolchildren in
Taiwan in 2000. J Formos Med Assoc 2001; 100: 684–91.
3. Saw SM, Chua WH, Gazzard G, Koh D, Tan DT, Stone RA. Eye
growth changes in myopic children in Singapore. Br J Ophthalmol. 2005;89:1489-94
4. Ehrlich DL, Atkinson J, Braddick O et al. Reduction of infant myopia: A longitudinal cycloplegic study. Vision Res
1995;35:1313–24.
5. Shih YF, Hsiao CK, Chen CJ, Chang CW, Hung PT, Lin LL. An
intervention trial on efficacy of atropine and multi-focal glasses in controlling myopic progression. Acta Ophthalmol Scand
2001;79: 233–6.
6. Chua WH, Balakrishnan V, Chan YH et al. Atropine for the treatment of childhood myopia. Ophthalmology 2006; 113: 2285–91.
7. Tan DT, Lam DS, Chua WH, Shu-Ping DF, Crockett RS. Oneyear multicenter, double-masked, placebo-controlled, parallel
safety and efficacy study of 2% pirenzepine Ophtal gel in children with myopia. Ophthalmology 2005; 112: 84–91.
8. Siatkowski RM, Cotter SA, Crockett RS, Miller JM, Novack GD,
Zadnik K. Two-year multicenter, randomized, double-masked,
placebo- controlled, parallel safety and efficacy study of 2%
pirenzepine ophthalmic gel in children with myopia. JAAPOS
2008; 12: 332–9.
9. Chung K, Mohidin N, O’Leary DJ. Undercorrection of myopia
enhances rather than inhibits myopia progression. Vision Res
2002; 42: 2555–9.
10. Yang Z, Lan W, Ge J, Liu W, Chen X, Chen L, Yu M. The effectiveness of progressive addition lenses on the progression of myopia
in Chinese children. Ophthalmic Physiol Opt 2009; 29: 41–8.
11. Edwards MH, Li RW, Lam CS, Lew JK, Yu BS. The Hong Kong
progressive lens myopia control study: study design and main
findings. Invest Ophthalmol Vis Sci 2002; 43: 2852–8.
12. Leung JT, Brown B. Progression of myopia in Hong Kong Chinese schoolchildren is slowed by wearing progressive lenses.
Optom Vis Sci 1999; 76: 346–54.
13. Gwiazda J, Hyman L, Hussein M et al. A randomized clinical
trial of progressive addition lenses versus single vision lenses
on the progression of myopia in children. Invest Ophthalmol
Vis Sci 2003; 44: 1492–500.
14. Hasebe S, Ohtsuki H, Nonaka T et al. Effect of progressive addition lenses on myopia progression in Japanese children: a
prospective, randomized, double-masked, crossover trial. Invest Ophthalmol Vis Sci 2008; 49: 2781–9.
15. Walline JJ, Jones LA, Mutti DO, Zadnik K. A randomized trial
of the effects of rigid contact lenses on myopia progression.
Arch Ophthalmol 2004; 122: 1760–6.
16. Atchinson DA, Pritchard N, Schmid KL et al. Shape of the retinal surface in emmetropia and myopia. Invest Ophthalmol Vis
Sci 2005; 46: 2698-707
17. Charman WN, Jennings JA. Longitudinal changes in peripheral
refraction with age. Ophthal Physiol Opt 2006; 26: 447-55
18. Chen X, Sankaridurk P, Donovan L et al. Characteristics of peripheral refractive errors of myopic and non-myopic Chinese
eyes. Vis Res 2010, 50: 31-5
19. Smith EL III, Kee CS, Ramamirtham R, Qiao-Grider Y, Hung LF.
Peripheral vision can influence eye growth and refractive development in infant monkeys. Invest Ophthalmol Vis Sci 2005; 46:
3965–72.
20. Smith EL III, Ramamirtham R, Qiao-Grider Y, Hung LF, Huang
J, Kee CS, Coats D, Paysse E. Effects of foveal ablation on emmetropization and form-deprivation myopia. Invest Ophthalmol Vis Sci 2007; 48: 3914–22.
21. Smith EL III, Hung LF, Huang J. Relative peripheral hyperopic
defocus alters central refractive development in infant monkeys. Vision Res 2009; 49: 2386–92.
22. Cho P, Cheung SW, Edwards M. The longitudinal orthokeratology research in children (LORIC) in Hong Kong: a pilot study
on refractive changes and myopic control. Curr Eye Res. 2005;
30:71-80
23. Cho P, Cheung SW. Retardation of myopia in orthokeratology
(ROMIO) study: 6-month results. 34th BCLA Clinical Conference. Birmingham (UK), May 27-30, 2010
24. Walline JJ, Jones LA, Sinnott LT. Corneal reshaping and myopia
progression. Br J Ophthalmol. 2009; 93: 1181-5
L.Lupelli / Lac Lenti a contatto 2010; 12 (2): 35-36
36
ARTICO L O
Occhio secco
e lenti a contatto
Gonzalo Carracedo
Departamento de Óptica II (Optometría y Visión), Escuela Universitaria de Óptica,
Universidad Complutense de Madrid, Spagna
danno alla superficie oculare. È accompagnata da un aumento dell’osmolarità del film lacrimale e dall’infiammazione della superficie oculare”1.
Se analizziamo in dettaglio la definizione di occhio secco,
vediamo che si tratta non solo di un disturbo del film lacrimale, ma piuttosto di un problema che coinvolge tutta l’unità funzionale lacrimale (Lacrimal Functional Unit - LFU),2-3
un sistema integrato che comprende la superficie oculare
(cornea e congiuntiva), le ghiandole lacrimali, le ghiandole
Meibomio, le palpebre e l’innervazione sia sensoriale, sia
motoria. La LFU controlla e regola la lacrimazione in risposta a eventuali influenze ambientali o endocrine. Un danno
a qualsiasi componente della unità funzionale lacrimale
può destabilizzare il film lacrimale e causare una patologia
oculare di superficie, che si presenta come occhio secco2-4.
Attualmente vengono inclusi intenzionalmente nella definizione di occhio secco i segni oculari più rilevanti. I pazienti con occhio secco presentano abitualmente sintomi
di fastidio, secchezza, sensazione di sabbia negli occhi,
irritazione, sensazione di corpo estraneo, bruciore o sensibilità alla luce4-7. In funzione del tipo di occhio secco, i
segni che si possono presentare più comunemente sono:
iposecrezione lacrimale8, instabilità del film lacrimale,9
iperosmolarità lacrimale,10-11 colorazione corneale o congiuntivale,12 calo di acuità visiva,13 aumento delle aberrazioni oculari14 e infiammazione oculare15.
L’occhio secco si divide in due tipi principali, l’occhio
secco da ipoproduzione lacrimale e occhio secco da iperevaporazione lacrimale. Queste due forme non sono indipendenti, ma i pazienti presentano eventi riconducibili
ad entrambi i tipi (vedi figura 1).
PAROLE CHIAVE
Occhio secco, lenti a contatto, film lacrimale.
Ricevuto il 25 agosto, 2010; accettato il 14 settembre, 2010.
Sommario
L’occhio secco è considerato la principale causa di abbandono dell’uso delle lenti a contatto. Le alterazioni del
film lacrimale dovute a secchezza oculare nei portatori
di lenti a contatto sono associate a riduzione del comfort,
peggioramento dell’acuità visiva, riduzione dei tempi di
utilizzo e maggior rischio di staining corneale. Si suppone che, durante l’uso delle lenti a contatto, si instauri una
serie di meccanismi che portano all’occhio secco: aumento dell’evaporazione del film lacrimale, infiammazione,
riduzione della produzione di lacrime con conseguente
aumento dell’osmolarità, diminuzione della sensibilità
corneale, sofferenza delle cellule caliciformi e possibile
variazione della concentrazione di diadenosina trifosfato, o qualsiasi combinazione di questi fattori. In questa
rassegna descriveremo le alterazioni del film lacrimale e
della superficie oculare che sono associate con l’occhio
secco negli utilizzatori di lenti a contatto.
L'occhio secco
Nel 2007, il Dry Eye WorkShop (DEWS) ha proposto la
seguente definizione di occhio secco: “L’occhio secco è
una malattia multifattoriale del film lacrimale e della superficie oculare che provoca sintomi di discomfort, disturbi visivi e instabilità del film lacrimale con potenziale
OCCHIO SECCO
Ipo-produzione
Sindrome Sjögren
Primario
Secondario
Figura 1
Classificazione
dell’occhio secco.1
Iper-evaporazione
Ambiente interno:
No-Sindrome Sjögren
Intrinseco
Estrinseco
Insufficiente secrezione
lacrimale
Lipidi Meibomio
Vit. A
Ostruzione dotto
ghiandola lacrimale
Apertura palpebre
Conservanti dei farmaci
Ambiente Esterno:
Blocco del riflesso motore
Ammiccamento
LAC
• Umidità relativa
• Ambiente di lavoro
• Vento
Farmaci sistemici
Azione farmaci
Allergie
• Uso di computer
• Farmaci sistemici
• Invecchiamento
• Donne
37
Occhio secco e lenti a contatto
L’occhio secco da ipo-produzione implica principalmente la diminuzione della secrezione lacrimale,16-17 che causa iperosmolarità e quindi innesca il resto degli eventi
nella patogenesi dell’occhio secco18. L’occhio secco da
ipoproduzione si divide a sua volta in due sottotipi: l’occhio secco associato alla sindrome di Sjögren e l’occhio
secco non associato alla sindrome di Sjögren.
L’altro tipo principale di occhio secco è quello evaporativo, in cui si ha un’eccessiva perdita di liquido lacrimale, che lascia esposta la superficie oculare, malgrado una
normale produzione di lacrime. Questo tipo di occhio
secco si divide a sua volta in intrinseco, quando la causa
è una patologia o una disfunzione propria del paziente, e
in estrinseco, quando l’eccessiva evaporazione è causata
da un fattore esterno.
Fra le cause intrinseche di occhio secco evaporativo troviamo le disfunzioni delle ghiandole di Meibomio,19-20
o patologie come l’ipertiroidismo o il morbo di Parkinson21-22. La causa estrinseca più rilevante è l’uso di lenti a
contatto, e a sua volta l’occhio secco è la principale causa
di abbandono delle lenti a contatto23.
Diagnosi
La diagnosi di occhio secco è difficile perché questa patologia presenta una grande varietà di segni e sintomi e
inoltre non esiste una correlazione tra gli uni e gli altri.
Si possono osservare casi di occhio secco con sintomatologia, ma senza presenza di segni oculari e viceversa24-25. Non esistendo un test gold standard per la diagnosi
dell’occhio secco, il sottocomitato di metodologia per la
diagnosi del DEWS raccomanda la combinazione di alcuni dei seguenti test:26
3- Stabilità del film lacrimale - Per la valutazione dell’instabilità lacrimale, il test più utilizzato è il tempo di rottura
del film lacrimale (Tear Film Break-up Time: TFBUT). Per
eseguire questo test, si deve instillare fluoresceina sodica
sulla superficie oculare. Il tempo normale minimo di rottura è considerato 10 secondi35. Inoltre esistono test non
invasivi, come l’osservazione delle ghiandole di Meibomio e il BUT non invasivo (NIBUT)36.
4- Test per valutare il volume lacrimale - Con questo tipo di
test si misura la secrezione lacrimale, sia riflessa, sia basale. Il più comune è il test di Shirmer, che si esegue con
una cartina Wathman no. 1. Il valore normale per questo
test è di almeno 5,5 mm in 5 minuti30. Altri test meno invasivi sono il filo rosso fenolo, il Tear Turnover rate (TTR)
e la quantificazione del menisco lacrimale marginale37.
5- Test per valutare l’osmolarità - Fino ad oggi questo era
un test di laboratorio con un accesso molto limitato per
i professionisti clinici10. Attualmente è disponibile un
osmometro compatto, che necessita di una minima quantità di lacrime per misurare istantaneamente l’osmolarità.
Questo strumento, chiamato Tearlab Osmolarity (Tearlab
Corporation), ha reso disponibile il primo test di uso clinico per misurare l’osmolarità lacrimale38.
Oltre a questi test diagnostici ampiamente noti, è stata
scoperta una molecola, chiamata diadenosina tetrafosfato,
Ap4A, presente nel liquido lacrimale umano, che aumenta
di concentrazione in caso di occhio secco ed è quindi uno
strumento di diagnosi oggettiva39-40 (vedi figura 2).
1- Questionari soggettivi - Esistono vari tipi di questiona-
ri per valutare i sintomi di occhio secco. I più utilizzati
sono: il questionario di McMonnies,27 il Dry Eye Questionnaire (DEQ) con la sua versione per le lenti a contatto (CLDEQ),4, 28 l’Ocular Surface Desease Index (OSDI),29
e il questionario di Schein25.
2- Test per valutare la superficie corneale - Per evidenziare difetti o erosioni nella superficie oculare si utilizzano coloranti come la fluoresceina per la cornea, che si osserva
meglio con il filtro giallo, o il verde di lissamina e il rosa
bengala per valutare la congiuntiva. I sistemi più usati
per quantificare la colorazione (staining) della superficie
corneale sono il sistema di Van Bijsterveld,30 il sistema
Oxford31 e il sistema CLEK32. Esistono altri test specifici
per gli utilizzatori di lenti a contatto, nei quali si valuta lo
staining corneale come una complicazione dell’uso delle
lenti. I più utilizzati sono le scale di gradazione di Efron33
e del CCLRU34.
Figura 2
Concentrazione di Ap4A e Ap5A nella lacrima di pazienti con
e senza sintomatologia di occhio secco. Si può osservare un
aumento delle concentrazioni di queste molecole nella lacrima
dei pazienti con sintomi di secchezza oculare, tanto più se hanno
anche un volume lacrimale ridotto (> 5 mm Schirmer test).
G. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
38
ARTICO L O
Occhio secco e lenti a contatto
Per ora, uno strumento di misura di questa molecola per
uso clinico è ancora in fase di sviluppo.
Trattamento
Il trattamento dell’occhio secco è difficile e spesso frustrante, poiché le cause che lo determinano, nella maggior parte dei casi, non hanno un trattamento efficace, né
specifico. La prima opzione di fronte ad un occhio secco
lieve o moderato sono i lubrificanti, conosciuti come lacrime artificiali, anche se non imitano la composizione
della lacrima umana. Considerando che l’infiammazione
della superficie oculare è un meccanismo chiave della patogenesi dell’occhio secco, sono stati sviluppati farmaci
antinfiammatori per questa patologia. Le tre famiglie di
antinfiammatori utilizzati sono: la ciclosporina, i corticoidi e le tetracicline.
L’applicazione topica di sieri biologici, come il siero sanguigno o il siero amniotico, può migliorare i segni clinici di occhio secco. Questi fluidi hanno una composizione in qualche modo simile alla lacrima naturale e inoltre sono ricchi
di fattori di crescita, vitamine, immunoglobine e altre proteine necessarie per mantenere sana la superficie oculare.
Recentemente è stata prospettata come possibile terapia
per l’occhio secco l’assunzione di acidi grassi essenziali
come l’Omega-341. È stato dimostrato che l’acido linoleico e l’acido - linoleico somministrati oralmente due volte
al dì, porta ad un significativo miglioramento dei sintomi
di irritazione oculare42.
Un nuovo farmaco, approvato di recente per la commercializzazione, è il DIQUAS che verrà distribuito da
Santen Pharmaceuticals in Giappone. È un segretagogo
(agente chimico che stimola la secrezione) analogo al
Ap4A, che ha la caratteristica di stimolare la secrezione
delle tre componenti principali del liquido lacrimale: acquosa, mucosa e lipidica. Test clinici hanno dimostrato
che riduce significativamente la colorazione corneale43.
Oltre i trattamenti farmacologici per l’occhio secco, esistono altre terapie come l’occlusione dei puntini lacrimali, gli occhiali a camera umida e le lenti a contatto ad uso
terapeutico.
Prevalenza dell’occhio secco negli utilizzatori di
lenti a contatto
I sintomi di occhio secco sono più frequenti negli utilizzatori di lenti a contatto che nel resto della popolazione
e ciò significa che la lente a contatto può produrre alterazioni della superficie oculare. Valutando la differenza
nello stesso soggetto, vari studi hanno dimostrato che la
frequenza e la severità dei sintomi di occhio secco sono
maggiori quando si utilizzano le lenti a contatto44-45. Si
ritiene che la sintomatologia di occhio secco sia la principale causa di intolleranza e abbandono delle lenti a contatto46. Il 51% degli abbandoni si deve all’occhio secco e
una percentuale compresa fra il 12% e il 21% degli utilizzatori riduce le ore di uso delle lenti a causa dei sintomi
di secchezza oculare23.
La prevalenza di occhio secco negli utilizzatori di lenti a
contatto è molto variabile, secondo le condizioni in cui è
stato realizzato lo studio. Fattori come il clima e l’area geografica, l’assunzione di farmaci sistemici o l’età dei soggetti inclusi nello studio possono causare grandi differenze di
prevalenza1. Per questo motivo la percentuale di prevalenza dell’occhio secco negli utilizzatori di lenti a contatto
può variare dal 20% al 74%1, 28, 47. Consideriamo inoltre che
il 38% degli utilizzatori che sono soddisfatti delle loro lenti a contatto, riferisce sintomi di occhio secco48.
Variazioni nel film lacrimale e nella superficie
oculare indotte dalle lenti a contatto
Quando si applica una lente a contatto sull’occhio, questa
interrompe la struttura del film lacrimale, dividendolo in
una porzione pre-lente e una porzione post-lente. La porzione pre-lente è composta da uno strato lipidico molto
sottile e una base acquoso-mucinica. Il suo effetto è migliorare il comfort mediante la lubrificazione e idratazione della lente. La porzione post-lente è formata da uno
strato acquoso-mucinico e da uno strato di mucine che
permettono al film lacrimale di aderire all’epitelio corneale. Il suo effetto è migliorare il comfort dell’uso della
lente a contatto, oltre ad assicurare l’idratazione dell’epitelio corneale ed eliminare i detriti dalla superficie oculare49. La forma e il volume di questa porzione dipendono
dai parametri della lente a contatto, come il raggio di curvatura, il modulo di elasticità e il diametro49.
Strato lipidico
Film lacrimale pre-lente
Strato acquoso
Film lacrimale post-lente
Lente a contatto
Alterazione menisco lacrimale
Staining corneale
Strato acquoso-mucinico
Metaplasia squamosa
Densità cellule caliciformi
Figura 3
Alterazioni prodotte dalla lente a contatto nella lacrima e sulla
superficie oculare.
G. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
39
Occhio secco e lenti a contatto
La divisione del film lacrimale prodotta dalla lente a contatto provoca a sua volta una serie di squilibri che, in conclusione, portano ai tipici sintomi di secchezza oculare.
Come già abbiamo detto, la porzione pre-lente del film
lacrimale è molto instabile, poiché la componente lipidica è molto sottile, tanto da essere assente il alcune zone,
dove quindi il tasso di evaporazione delle lacrime sarà
maggiore del normale. L’aumento dell’evaporazione,
come vedremo nella patogenesi, aumenta l’osmolarità
del liquido lacrimale, causando la comparsa dei sintomi
di secchezza oculare50. Nel caso di lenti a contatto morbide, l’aumento dell’evaporazione lacrimale induce una
maggiore disidratazione della lente, che per reidratarsi assorbe parte dello strato lacrimale post-lente, provocando
secchezza nella superficie corneale49. Inoltre, nel caso della porzione post-lente, il ricambio lacrimale viene ridotto
dalla lente in idrogel e quindi aumenta il tempo di esposizione dell’epitelio corneale agli agenti infiammatori51.
Un’altra variazione che si osserva nel film lacrimale è un
incremento della temperatura, che aumenta fino ad 1°C
con l’uso delle lenti a contatto, le quali provocano un effetto serra52. Si osservano variazioni anche nella morfologia del prisma lacrimale, che si assottiglia nella zona
di contatto con il bordo della lente, con conseguente disidratazione.
Sulla superficie oculare si potrà osservare dello staining,
sia corneale, sia congiuntivale, e variazioni istopatologiche. Di solito in caso di lenti a contatto RGP si potrà vedere una colorazione a ore 3-9, provocata fondamental-
mente da un assottigliamento del film lacrimale in questa
zona, accompagnato a uno scarso movimento della lente.
Nel caso di lente in idrogel, lo staining è di solito centrale o arcuato inferiore. Nel caso dello staining centrale,
la causa è principalmente un insufficiente ricambio lacrimale sotto la lente, mentre lo staining arcuato inferiore è
dovuto per lo più ad un ammiccamento incompleto, che
aumenta la disidratazione della lente 51. Si possono osservare colorazioni anche nella congiuntiva bulbare, che è
correlata con un aumento della sintomatologia di occhio
secco negli utilizzatori di lenti a contatto53. In letteratura
sono riportate variazioni istopatologiche della congiuntiva, che si verificano con differenti materiali per lenti a
contatto. Le variazioni riportate più di frequente sono la
metaplasia squamosa e una diminuzione della densità
delle cellule caliciformi54-55. Queste alterazioni aumentano l’instabilità lacrimale che, come vedremo, è un’alterazione importante nella patogenesi dell’occhio secco.
Patogenesi
In figura 4 è schematizzato il possibile meccanismo di occhio secco indotto dalle lenti a contatto. I fattori scatenanti sono principalmente tre: l’aumento dell’evaporazione
lacrimale, la diminuzione del ricambio lacrimale e il
trauma meccanico sulla superficie oculare. Questi eventi producono variazioni nelle lacrime e nella superficie
oculare, creando un circolo vizioso che si autoalimenta e
provoca un aumento della sintomatologia di occhio secco. Il fulcro del meccanismo sembra che siano i media-
Evaporazione
Produzione lacrimale
Osmolarità
Instabilità lacrimale
Alterazione omeostasi
Mediatori infiammatori
Danno epitelio mucine
Ricambio lacrimale
Sensibilità corneale
Eliminazione detriti
Danno nervi
corneali
Danno superficie
oculare
Frequenza ammiccamento
Figura 4
Schema del meccanismo della patogenesi dell’occhio secco indotto da lenti a contatto.
G. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
40
ARTICO L O
Occhio secco e lenti a contatto
Figura 5
Disidratazione della superficie anteriore di una lente a contatto
RGP.
tori infiammatori, come le citochine o interleuchine, che
aumentano la loro concentrazione a causa dell’evaporazione lacrimale e permangono più tempo sulla superficie
oculare per via dell’insufficiente ricambio lacrimale56-57.
La presenza dei mediatori infiammatori provoca danni
ai nervi corneali diminuendo la sensibilità della cornea.
La perdita di sensibilità altera l’omeostasi naturale della
superficie oculare, facendo sì che diminuisca il volume
lacrimale. Inoltre la presenza di cellule infiammatorie
provoca la diminuzione della produzione di mucina da
parte delle cellule caliciformi e quindi un danno all’epitelio della superficie oculare, rendendo la lacrima più
instabile e aumentando la sua evaporazione. Entrambi i
processi contribuiscono ad aumentare l’osmolarità lacrimale e ciò favorisce la presenza di citochine e inteleuchine nelle lacrime.
All’inizio dell’uso delle lenti a contatto, nel tentativo di
stabilizzare il film lacrimale, aumenta la frequenza di
ammiccamento, ma quando diminuisce la sensibilità, diminuisce anche la frequenza dell’ammiccamento e così
aumenta l’evaporazione del liquido lacrimale51.
Applicazione e riapplicazione delle lenti a contatto
Per molto tempo l’occhio secco è stato considerato una
controindicazione all’uso di lenti a contatto. Inoltre quando un paziente presentava una sintomatologia di occhio
secco dovuto all’uso di lenti a contatto, l’unica soluzione
era quasi sempre interrompere l’uso delle lenti. Ora esistono materiali per lenti a contatto, umettanti e liquidi di
manutenzione che permettono l’uso delle lenti nonostante l’occhio secco.
Ogni volta che si inizia un’applicazione di lenti a contatto
è molto importante condurre un’anamnesi completa, durante la quale vanno acquisite informazioni su patologie,
farmaci o fattori ambientali (uso di computer, ambienti
fumosi, o aria condizionata) che siano correlati con la sintomatologia di occhio secco. Patologie come il diabete, le
allergie o le malattie del tessuto connettivo sono fattori
di rischio per l’occhio secco58-59. Farmaci come gli antistaminici o anche gli antidepressivi aumentano la sintomatologia di secchezza oculare60. Infine, si deve domandare
espressamente se sono presenti sintomi di occhio secco.
Quindi, va eseguito un esame completo in lampada a
fessura, prestando particolare attenzione alle palpebre,
le ghiandole di Meibomio, il BUT e il menisco lacrimale
marginale. Inoltre bisogna guardare se è presente staining corneale, soprattutto di tipo arcuato inferiore, tipico
di un ammiccamento incompleto. Tutti questi esami ci
aiutano a determinare quali pazienti hanno potenziali rischi di sviluppare una sintomatologia di occhio secco con
l’uso delle lenti a contatto e anche a scegliere i materiali
e i sistemi di manutenzione migliori per minimizzare il
discomfort e la secchezza. Nel caso di pazienti già adattati, bisognerà programmare controlli periodici per identificare in modo tempestivo i segni e i sintomi di occhio
secco e prendere le misure opportune.
Al momento di scegliere le lenti a contatto si dovrà tenere conto delle proprietà del materiale. Sarà opportuno
scegliere materiali con un’alta trasmissibilità all’ossigeno (Dk/t) per mantenere l’integrità epiteliale ed evitare
l’iposssia61. È dimostrato che le lenti con un basso tasso
di disidratazione provocano minore secchezza oculare e disconfort, rispetto a quelle che si disidratano più
rapidamente62. Le lenti che si disidratano meno sono le
lenti idrofile a bassa idratazione, non ioniche (Gruppo 1
FDA) e le lenti in silicone idrogel63-64. Altri materiali con
alto contenuto acquoso hanno un tasso di disidratazione
molto basso, che li rende adatti per i pazienti con occhio
secco65-66. Questi materiali sono l’Omafilcon A, che contiene fosoforilcolina, una molecola altamente idrofila che
si trova nella membrana delle cellule degli organismi viventi, e i materiali idrofili con metacrilato di glicerolo,
come lo Hioxifilcon A, sviluppati proprio per risolvere i
problemi di disidratazione dei materiali ad alto contenuto di acqua.
Altre proprietà da considerare sono la bagnabilità della
superficie e la sua affinità con i depositi. Le lenti che hanno buona bagnabilità e poca affinità con i depositi provocano meno sintomi di discomfort67. Le lenti in silicone
idrogel presentano affinità per i depositi lipidici a causa
dell’idrofobia del silicone e quindi, nei pazienti con lacrime grasse, queste lenti a basso contenuto acquoso possono provocare discomfort e ridotta acuità visiva.
Oltre le lenti idrogel che abbiamo già descritto e le lenti silicone idrogel, vale la pena di considerare l’opzione
delle lenti RGP. Queste lenti, quando sono ben applicate,
garantiscono un maggior ricambio lacrimale sotto la len-
G. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
41
Occhio secco e lenti a contatto
te e quindi un minor tempo di permanenza dei mediatori
infiammatori sulla superficie oculare68.
Infine, dobbiamo scegliere le soluzioni per la manutenzione e gli umettanti più adeguati, che siano meno tossici
possibile per la superficie oculare. Fra i conservanti che si
trovano nelle soluzioni per lenti RPG, è stato dimostrato
che il più tossico è il cloruro di benzalconio (BAC), mentre la Clorexidina presenta la minore tossicità69. Inoltre è
ampiamente documentato che anche il thimerosal è tossico per la superficie oculare70. Nelle soluzioni uniche per
lenti morbide si utilizzano conservanti come il Polyquad
o il PHMB, che sono meno tossici per l’epitelio corneale
rispetto ai conservanti precedenti71-72.
Se compaiono sintomi di secchezza oculare, sarà necessario cambiare il sistema di manutenzione, passando a
soluzioni che non contengano BAC o thimerosal e a soluzioni saline e lubrificanti monodose privi di conservanti.
Conclusione
Attualmente l’occhio secco non deve essere considerato
una controindicazione all’uso di lenti a contatto e, quando un paziente presenta una sintomatologia di secchezza
oculare, la soluzione non è quella di interrompere l’uso
delle lenti, poiché esistono materiali, umettanti e liquidi
di manutenzione che permettono un uso sicuro e confortevole delle lenti a contatto nonostante l’occhio secco.
Abstract
Between a 5% and a 20% of developed world population wears
contact lenses. Still a significant number of them will give up
wearing due to intolerance, being dry eyes one of the main
reasons. Dry eye and alterations of the tear film in contact lens
wearers are associated with reductions in functional visual
acuity, reductions in wearing time, and an increased risk of
ocular surface desiccation. It has been speculated that potential mechanisms of dry eye, during contact lens wear include
increased evaporation of the tear film, inflammation, reduced
ability to produce adequate tears with concurrent increased
osmolarity, decrease of corneal sensitivity, damage in goblet
cells and possible changes in diadenosine polyphosphates
concentrations or any combination of these. In this review we
describe the different changes in tear film and ocular surface
that are associated with dry eye in contact lens wearers.
Key words
Dry eye, contact lens, tear film.
Bibliografia
1. The definition and classification of dry eye disease: report of
the Definition and Classification Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf. 2007;5:75-92.
2. Stern ME, Beuerman RW, Fox RI, Gao J, Mircheff AK, Pflugfelder SC. The pathology of dry eye: the interaction between the
ocular surface and lacrimal glands. Cornea. 1998;17:584-589.
3. Stern ME, Beuerman RW, Fox RI, Gao J, Mircheff AK, Pflugfelder SC. A unified theory of the role of the ocular surface in
dry eye. Adv Exp Med Biol. 1998; 438:643-651.
4. Begley CG, Caffery B, Chalmers RL, Mitchell GL. Use of the
dry eye questionnaire to measure symptoms of ocular irritation in patients with aqueous tear deficient dry eye. Cornea.
2002;21:664-670.
5. Nichols KK, Begley CG, Caffery B, Jones LA. Symptoms of ocular irritation in patients diagnosed with dry eye. Optom Vis Sci.
1999;76:838-844.
6. Simpson TL, Situ P, Jones LW, Fonn D. Dry eye symptoms assessed by four questionnaires. Optom Vis Sci. 2008;85:692-699.
7. McMonnies CW. Key questions in a dry eye history. J Am Optom
Assoc. 1986;57:512-517.
8. Nichols KK, Nichols JJ, Lynn Mitchell G. The relation between
tear film tests in patients with dry eye disease. Ophthalmic Physiol Opt. 2003;23:553-560.
9. Goto T, Zheng X, Klyce SD, et al. A new method for tear film
stability analysis using videokeratography. Am J Ophthalmol.
2003;135:607-612.
10. Tomlinson A, Khanal S, Ramaesh K, Diaper C, McFadyen A.
Tear film osmolarity: determination of a referent for dry eye
diagnosis. Invest Ophthalmol Vis Sci. 2006;47:4309-4315.
11. Farris RL, Stuchell RN, Mandel ID. Tear osmolarity variation in
the dry eye. Trans Am Ophthalmol Soc. 1986;84:250-268.
12. Chen JJ, Rao K, Pflugfelder SC. Corneal epithelial opacity in dysfunctional tear syndrome. Am J Ophthalmol. 2009;148:376-382.
13. Rieger G. The importance of the precorneal tear film for the
quality of optical imaging. Br J Ophthalmol. 1992;76:157-158.
14. Montes-Mico R, Caliz A, Alio JL. Wavefront analysis of higher
order aberrations in dry eye patients. J Refract Surg. 2004;20:243247.
15. Massingale ML, Li X, Vallabhajosyula M, Chen D, Wei Y, Asbell
PA. Analysis of Inflammatory Cytokines in the Tears of Dry Eye
Patients. Cornea. 2009; 28: 1023-1027.
16. Khanal S, Tomlinson A, Diaper CJ. Tear physiology of aqueous
deficiency and evaporative dry eye. Optom Vis Sci. 2009;86:12351240.
17. Mathers WD, Daley TE. Tear flow and evaporation in patients
with and without dry eye. Ophthalmology. 1996;103:664-669.
18. Li DQ, Chen Z, Song XJ, Luo L, Pflugfelder SC. Stimulation of
matrix metalloproteinases by hyperosmolarity via a JNK pathway in human corneal epithelial cells. Invest Ophthalmol Vis Sci.
2004;45:4302-4311.
19. Bron AJ, Tiffany JM. The contribution of meibomian disease to
dry eye. Ocul Surf. 2004;2:149-165.
20. Mathers WD. Ocular evaporation in meibomian gland dysfunction and dry eye. Ophthalmology. 1993;100:347-351.
21. Tamer C, Melek IM, Duman T, Oksuz H. Tear film tests in Parkinson’s disease patients. Ophthalmology. 2005;112:1795.
22. Gilbard JP, Farris RL. Ocular surface drying and tear film osG. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
42
ARTICO L O
Occhio secco e lenti a contatto
molarity in thyroid eye disease. Acta Ophthalmol (Copenh).
1983;61:108-116.
23. Young G, Veys J, Pritchard N, Coleman S. A multi-centre
study of lapsed contact lens wearers. Ophthalmic Physiol Opt.
2002;22:516-527.
24. Nichols KK, Nichols JJ, Mitchell GL. The lack of association between signs and symptoms in patients with dry eye disease.
Cornea. 2004;23:762-770.
25. Schein OD, Tielsch JM, Munoz B, Bandeen-Roche K, West S. Relation between signs and symptoms of dry eye in the elderly. A
population-based perspective. Ophthalmology. 1997;104:1395-1401.
26. Methodologies to diagnose and monitor dry eye disease: report
of the Diagnostic Methodology Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf. 2007;5:108-152.
27. McMonnies CW, Ho A. Patient history in screening for dry eye
conditions. J Am Optom Assoc. 1987;58:296-301.
28. Nichols JJ, Mitchell GL, Nichols KK, Chalmers R, Begley C.
The performance of the contact lens dry eye questionnaire as
a screening survey for contact lens-related dry eye. Cornea.
2002;21:469-475.
29. Schiffman RM, Christianson MD, Jacobsen G, Hirsch JD, Reis
BL. Reliability and validity of the Ocular Surface Disease Index.
Arch Ophthalmol. 2000;118:615-621.
30. van Bijsterveld OP. Diagnostic tests in the Sicca syndrome. Arch
Ophthalmol. 1969;82:10-14.
31. Bron AJ, Evans VE, Smith JA. Grading of corneal and conjunctival staining in the context of other dry eye tests. Cornea.
2003;22:640-650.
32. Lemp MA. Report of the National Eye Institute/Industry workshop on Clinical Trials in Dry Eyes. CLAO J. 1995;21:221-232.
33. Efron N. Contact lens complications. First edition ed. Oxford:
Butterworth-Heinemann; 1999.
34. Phillips AJ, Speedwell L. Contact lenses. Fourth edition ed. Oxford: Butterworth-Heinemann; 1997.
35. Vitali C, Moutsopoulos HM, Bombardieri S. The European
Community Study Group on diagnostic criteria for Sjogren’s
syndrome. Sensitivity and specificity of tests for ocular and
oral involvement in Sjogren’s syndrome. Ann Rheum Dis.
1994;53:637-647.
36. Madden RK, Paugh JR, Wang C. Comparative study of two
non-invasive tear film stability techniques. Curr Eye Res.
1994;13:263-269.
37. Occhipinti JR, Mosier MA, LaMotte J, Monji GT. Fluorophotometric measurement of human tear turnover rate. Curr Eye Res.
1988;7:995-1000.
38. Benelli U, Nardi M, Posarelli C, Albert TG. Tear osmolarity
measurement using the TearLab Osmolarity System in the assessment of dry eye treatment effectiveness. Cont Lens Anterior
Eye. 2010;33:61-67.
39. Peral A, Carracedo G, Acosta MC, Gallar J, Pintor J. Increased
levels of diadenosine polyphosphates in dry eye. Invest Ophthalmol Vis Sci. 2006;47:4053-4058.
40. Carracedo G, Peral A, Pintor J. Diadenosine Polyphosphates in
Tears of Sjogren Syndrome Patients. Invest Ophthalmol Vis Sci. 2010.
41. Peral A, Dominguez-Godinez CO, Carracedo G, Pintor J.
Therapeutic targets in dry eye syndrome. Drug News Perspect.
2008;21:166-176.
42. Barabino S, Rolando M, Camicione P, et al. Systemic linoleic
and gamma-linolenic acid therapy in dry eye syndrome with
an inflammatory component. Cornea. 2003;22:97-101.
43. Tauber J, Davitt WF, Bokosky JE, et al. Double-masked, placebo-controlled safety and efficacy trial of diquafosol tetrasodium (INS365) ophthalmic solution for the treatment of dry eye.
Cornea. 2004;23:784-792.
44. Vajdic C, Holden BA, Sweeney DF, Cornish RM. The frequency
of ocular symptoms during spectacle and daily soft and rigid
contact lens wear. Optom Vis Sci. 1999;76:705-711.
45. Guillon M, Cooper P, Maissa C, Girard-Claudon K. Dry eye
symptomatology of contact lens wearers and nonwearers. Adv
Exp Med Biol. 2002;506:945-949.
46. Doughty MJ, Fonn D, Richter D, Simpson T, Caffery B, Gordon
K. A patient questionnaire approach to estimating the prevalence of dry eye symptoms in patients presenting to optometric
practices across Canada. Optom Vis Sci. 1997;74:624-631.
47. Begley CG, Chalmers RL, Mitchell GL, et al. Characterization
of ocular surface symptoms from optometric practices in North
America. Cornea. 2001;20:610-618.
48. Begley CG, Caffery B, Nichols KK, Chalmers R. Responses
of contact lens wearers to a dry eye survey. Optom Vis Sci.
2000;77:40-46.
49. Nichols JJ, King-Smith PE. The effect of eye closure on the postlens tear film thickness during silicone hydrogel contact lens
wear. Cornea. 2003;22:539-544.
50. Gilbard JP, Gray KL, Rossi SR. A proposed mechanism for increased tear-film osmolarity in contact lens wearers. Am J Ophthalmol. 1986;102:505-507.
51. Korb DR. Tear film-contact lens interactions. Adv Exp Med Biol.
1994;350:403-410.
52. Bruce AS, Brennan NA. Corneal pathophysiology with contact
lens wear. Surv Ophthalmol. 1990;35:25-58.
53. Guillon M, Girard-Claudon K, Maissa C, Cooper P. Conjunctival characteristics of contact lens wearers and nonwearers
and their association with symptomatology. Adv Exp Med Biol.
2002;506:939-943.
54. Knop E, Brewitt H. Conjunctival cytology in asymptomatic
wearers of soft contact lenses. Graefes Arch Clin Exp Ophthalmol.
1992;230:340-347.
55. Saini JS, Rajwanshi A, Dhar S. Clinicopathological correlation
of hard contact lens related changes in tarsal conjunctiva by impression cytology. Acta Ophthalmol (Copenh). 1990;68:65-70.
56. Schultz CL, Kunert KS. Interleukin-6 levels in tears of contact
lens wearers. J Interferon Cytokine Res. 2000;20:309-310.
57. Thakur A, Willcox MD. Cytokine and lipid inflammatory mediator profile of human tears during contact lens associated inflammatory diseases. Exp Eye Res. 1998;67:9-19.
58. Wolfe F, Michaud K. Prevalence, risk, and risk factors for oral
and ocular dryness with particular emphasis on rheumatoid
arthritis. J Rheumatol. 2008;35:1023-1030.
59. Alves Mde C, Carvalheira JB, Modulo CM, Rocha EM. Tear film
and ocular surface changes in diabetes mellitus. Arq Bras Oftalmol. 2008;71:96-103.
60. Moss SE, Klein R, Klein BE. Prevalence of and risk factors for
dry eye syndrome. Arch Ophthalmol. 2000;118:1264-1268.
61. Gonzalez-Meijome JM, Jorge J, Almeida JB, Parafita MA. Contact lens fitting profile in Portugal in 2005: strategies for first fits
and refits. Eye Contact Lens. 2007;33:81-88.
G. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
43
Occhio secco e lenti a contatto
62. Pritchard N, Fonn D. Dehydration, lens movement and dryness ratings of hydrogel contact lenses. Ophthalmic Physiol Opt.
1995;15:281-286.
63. Fonn D, Situ P, Simpson T. Hydrogel lens dehydration and subjective comfort and dryness ratings in symptomatic and asymptomatic contact lens wearers. Optom Vis Sci. 1999;76:700-704.
64. Jalbert I, Sweeney DF, Holden BA. Epithelial split associated with wear of a silicone hydrogel contact lens. CLAO J.
2001;27:231-233.
65. Hall B, Jones S, Young G, Coleman S. The on-eye dehydration
of proclear compatibles lenses. CLAO J. 1999;25:233-237.
66. Riley C, Chalmers RL, Pence N. The impact of lens choice in
the relief of contact lens related symptoms and ocular surface
findings. Cont Lens Anterior Eye. 2005;28:13-19.
67. Sindt CW, Longmuir RA. Contact lens strategies for the patient
with dry eye. Ocul Surf. 2007;5:294-307.
68. Nichols JJ, Sinnott LT. Tear film, contact lens, and patient-relat-
ed factors associated with contact lens-related dry eye. Invest
Ophthalmol Vis Sci. 2006;47:1319-1328.
69. Imayasu M, Moriyama T, Ichijima H, et al. The effects of daily
wear of rigid gas permeable contact lenses treated with contact
lens care solutions containing preservatives on the rabbit cornea. CLAO J. 1994;20:183-188.
70. Mondino BJ, Salamon SM, Zaidman GW. Allergic and toxic reactions of soft contact lens wearers. Surv Ophthalmol. 1982;26:337344.
71. Labbe A, Pauly A, Liang H, et al. Comparison of toxicological
profiles of benzalkonium chloride and polyquaternium-1: an
experimental study. J Ocul Pharmacol Ther. 2006;22:267-278.
72. Cavet ME, Harrington KL, VanDerMeid KR, Ward KW, Zhang
JZ. Comparison of the effect of multipurpose contact lens solutions on the viability of cultured corneal epithelial cells. Cont
Lens Anterior Eye. 2009;32:171-175.
G. Carracedo / Lac Lenti a contatto 2010; 12 (2): 37-44
44
ARTICO L O
L’ACIDO IALURONICO
E LE SUE APPLICAZIONI IN CONTATTOLOGIA
Matteo Fagnola, Marco Paolo Pagani, Silvio Maffioletti, Silvia Tavazzi*, Antonio Papagni*
*Dipartimento di Scienza dei Materiali, Università degli Studi di Milano Bicocca
PAROLE CHIAVE
Acido ialuronico, occhio secco marginale
Ricevuto il 16 luglio, 2009; accettato il 3 settembre, 2009.
Sommario
L'acido ialuronico (HA) è una delle molecole più igroscopiche presenti in natura e, idratato, può contenere una
quantità di acqua mille volte superiore al proprio peso.
In contattologia, questa eccezionale capacità di ritenzione idrica viene sfruttata per migliorare l'idratazione
dell'area pre-corneale. L’acido ialuronico è infatti uno dei
principi attivi più impiegati nei numerosi sostituti lacrimali in commercio e nel trattamento delle varie forme di
occhio secco (da quelle più gravi a quelle marginali).
In questo articolo illustriamo le principali caratteristiche
e applicazioni dell’HA.
L'occhio secco
Lo stile di vita del portatore di lenti a contatto (lac) è radicalmente cambiato negli ultimi due decenni. Il computer è divenuto un indispensabile strumento di lavoro per
quasi tutte le professioni, la maggioranza degli uffici e
dei locali commerciali è dotata di aria condizionata, la
giornata lavorativa implica, generalmente, la necessità di
rimanere fuori casa più di 10 ore. Tutto ciò incide negativamente sul comfort delle lac.
Oggi la priorità dell'applicatore è quella di permettere al
portatore un uso confortevole delle lac per l'intera giornata.
Il tasso complessivo di drop out dei portatori di lac si colloca oggi tra il 26% ed il 40%. Tra coloro che rinunciano a
utilizzare le proprie lac, il 51% lo fa perché le ritiene poco
confortevoli e lamenta una sintomatologia riconducibile
alla condizione di occhio secco marginale1.
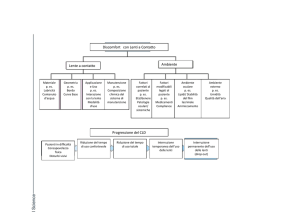
La Figura 1 presenta la classificazione delle sindromi da
occhio secco secondo la Commissione Internazionale del
National Eye Institute (Study Group on Dry Eye). È una
classificazione che prevede due sottocategorie: la cheratocongiuntivite secca derivante da ipolacrimie e quella
derivante da iperevaporazione.
La tipologia di occhio secco “marginale” è la più comune e consegue a specifiche condizioni organiche e/o ambientali; la tipologia di occhio secco “patologico” è meno
diffusa ed è associata a patologie sistemiche che coinvolgono, secondariamente, la salute oculare.
OCCHIO SECCO
cheratocongiuntivite secca
DA IPOLACRIMIE
DA IPEREVAPORAZIONE
Sindrome di Sjögren
Primaria
Ipolacrimie non Sjögren
Malattia della
gh. lacrimale
Distruzione dei
dotti lacrimale
Iposecrezione
riflessa
Da alterazioni della
componente lipidica
Da alterazioni
palpebrali
Da lenti Da alterazioni della
a contatto superficie oculare
Secondaria
Primarie
- Artrite
reumatoide
- Lupus
eritomatoso
sistemico
- Granulomatosi
di Wegener
- Sclerosi sistemica
- Cirrosi biliare
primitiva
- Altre malattie
utoimmuni
- Alacrimia
congenita
- Ipolacrimie
acquisite
Secondarie
- Sarcoidosi
- HIV
- "Graft vs
host disease"
- Xeroftalmia
- Asportazione
della
ghiandola
lacrimale
Primarie
- Tracoma
- Pemfigoide
cicatriziale
- Eritema
multiforme
- Ustioni
- Cheratite
neuroparalitica
- Lac
- Paralisi del
7° n.c.
Secondarie
- Aplasia
- Blefariti
delle gh. di anteriori
Meibomio
- Distichiasi
- Blefariti - Da alterazioni
posteriori dell'ammicca- Malattie mento
ostruttive
delle gh. di
Meibomio
- Xeroftalmia
- Da
alterazioni
dell'apertura
palpebrale
- Da
incongruità
palpebra
bulbo
oculare
Figura 1
Classificazione completa delle sindromi da occhio secco secondo la Commissione Internazionale del National Eye Institute
(Study Group on Dry Eye).
45
L’acido ialuronico e le sue applicazioni in contattologia
Le cause dell'occhio secco marginale sono da ricercare in
uno squilibrio dell'intero sistema lacrimale che, oltre alle
ghiandole lacrimali, comprende anche la superficie corneale, la congiuntiva bulbare, le palpebre e l'ammiccamento. In presenza di occhio secco marginale si osserva
sempre un aumento dell'osmolarità lacrimale, che può
portare a una perdita dell'integrità epiteliale e a una riduzione delle cellule mucipare caliciformi, avviando così
il circolo vizioso che costituisce l’essenza del problema2.
Qualunque lac interferisce con la stabilità del film lacrimale; pertanto persone in una condizione “borderline”
ma normalmente asintomatiche, possono sviluppare la
specifica sintomatologia da occhio secco durante il porto
di lac. Esse infatti interagiscono sia con il film lacrimale (destabilizzandolo) che con la superficie dell'epitelio
corneale (causando perdita di integrità e riduzione dei
microvilli).
Oltre che dalle lac, la manifestazione di una sintomatologia riconducibile ad una condizione di occhio secco marginale può essere indotta da numerosi fattori ambientali;
i più comuni sono la ridotta umidità ambientale, l'uso di
aria condizionata o di termoconvettori per la regolazione
della temperatura, il fumo, la polvere, il vento, l'uso del
computer (che causa riduzione della frequenza degli ammiccamenti). Ognuno di questi elementi, singolarmente
oppure combinati, può rappresentare il meccanismo di
innesco per lo sviluppo di una condizione di occhio secco
marginale.
Un ruolo chiave è relativo alla riduzione della frequenza
degli ammiccamenti e all'aumento della velocità di evaporazione del film lacrimale: esiste un valore predittivo,
definito “indice di protezione oculare” (IPA), che esprime normalità oppure problematicità. L’IPA viene calcolato mediante il rapporto tra il tempo di rottura del film lacrimale (BUT) e l’intervallo di tempo che trascorre tra un
ammiccamento e l’altro (IBI); quando il rapporto BUT/
IBI è minore di 1 è probabile che il portatore sviluppi i
sintomi tipici ed evidenzi i segni caratteristici della condizione di occhio secco marginale3. Altre caratteristiche
che influiscono sul comfort del portatore di lac sono la
bagnabilità, il modulo di elasticità e la levigatezza delle superfici delle lac. Ai portatori di lac che manifestano
condizioni di occhio secco marginale è opportuno applicare lac con un elevato bilanciamento idrico, oppure
utilizzare materiali capaci di rilasciare molecole bioattive
che contrastino la condizione di secchezza.
La terapia della sindrome da occhio secco marginale prevede l’utilizzo di sostituti lacrimali e di prodotti lubrificanti. I sostituti lacrimali contengono acqua, sali, sistema
tampone, conservanti, addensanti e altri ingredienti che
sono finalizzati a integrare la componente mucinica o la
componente lipidica del film lacrimale, a rendere la superficie oculare idrofila, a ridurre la tensione superficiale
e a garantire al film lacrimale una densità che gli permetta
di rimanere disteso sulla superficie corneale per un intervallo di tempo adeguato4. I principali polimeri utilizzati
per i sostituti lacrimali includono derivati della cellulosa
(hydroxypropylmethyl cellulose, carboxymethyl cellulose, hydroxyethyl cellulose), polyvinyl alcohol (PVA),
carbomer, polyvinyl pyrrolidone, polyethylene glycol e
destrano. Sono prodotti generalmente ben tollerati nelle
concentrazioni in uso, ma talvolta le formulazioni maggiormente viscose divengono poco confortevoli e causano visione sfuocata, adesività e formazione di residui.
Alcuni di questi polimeri, che sono definiti Newtoniani,
non riducono la propria densità al momento dell'ammiccamento limitando così la possibilità di distribuirsi sulla
superficie oculare e riducendo quindi la propria efficacia5. Per alleviare il discomfort e superare tali limitazioni,
è recentemente cresciuta l'attenzione verso gli integratori
lacrimali che esibiscono un comportamento non Newtoniano, in particolare verso i polimeri pseudoplastici
come l'acido ialuronico6.
L’acido ialuronico
L'acido ialuronico (HA) è un polisaccaride lineare formato da unità di disaccaridi contenenti N-acetyl-d-glucossamine e acido glucuronico (Figura 2). Possiede una massa
molecolare nell'ordine dei milioni di Dalton ed è dotato
di interessanti proprietà viscoelastiche e reologiche, che
sono l’espressione delle sue caratteristiche polimeriche
e di polielettrolita. L'HA è presente in numerosi fluidi e
tessuti biologici, nei quali gioca un ruolo fondamentale.
In clinica medica è utilizzato come marker diagnostico
per varie patologie tra cui il cancro, l'artrite reumatoide e
alcune malattie epatiche. È utilizzato anche come principio attivo, ad esempio per sopperire alle insufficienze di
CO2OH
O
H
H
H
O
CO2¯
H
HO
O
H
O
H
OH
H
H
OH
H
H
NHCCH3
O
n
Figura 2
Struttura dell'unità di disaccaride che si ripete nell'acido ialuronico.
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
46
ARTICO L O
L’acido ialuronico e le sue applicazioni in contattologia
liquido sinoviale nei pazienti artrosici mediante iniezioni
intra-articolari. Inoltre viene utilizzato nella chirurgia oftalmica, nella chirurgia otorinica e nella chirurgia estetica
per rigenerare e ricostruire i tessuti molli.
Dal 1980 numerosi studi scientifici e industriali hanno
permesso una miglior comprensione delle proprietà e
delle funzioni dell'HA, che ormai è utilizzato in molteplici applicazioni di svariate aree biomediche anche se,
ancor oggi, è considerato un principio attivo di nuova
generazione7-11.
L'HA appartiene ad un gruppo di sostanze conosciute
come glicosaminoglicani (GAGs) e, tra queste, è il polimero strutturalmente più semplice perché è l'unico che
non si presenta associato o legato a proteine, che non è
sintetizzato nell'apparato di Golgi e che non ha gruppi
solfato. L'HA è largamente diffuso nel corpo umano e
in quello degli altri vertebrati, ma la sua maggiore presenza si riscontra nella matrice extracellulare dei tessuti
connettivi lassi12. Si stima che in un essere umano adulto
del peso di circa 70 Kg vi siano 15 g di HA; di questi, più
della metà (56%) è contenuta nella pelle13.
Nella cresta del gallo si trova un’elevata quantità di HA il
quale, oltre che nei vertebrati, è presente in alcune specie
batteriche e in vari tipi di streptococchi mentre è totalmente assente in funghi, piante e insetti. Recentemente è stato
pubblicato un ampio studio sulle fonti da cui può essere
isolato l'HA e sull'eventuale presenza di potenziali impurità 14. Un breve elenco della quantità di HA reperibile nei
differenti tessuti animali è riportato nella Figura 315.
L’acido ialuronico negli organismi viventi
Negli organismi viventi l’HA si concentra principalmente nella matrice extracellulare e nella matrice pericellulare, ma è stato recentemente dimostrato che è presente
anche nello spazio intracellulare16. Nel corpo umano, la
maggior concentrazione di HA è nel fluido sinoviale, nel
cordone ombelicale e nell'umore vitreo. Quasi la metà
dell'HA presente nel corpo umano si trova a livello dermico, localizzato nello spazio intracellulare dove può
raggiungere una concentrazione di 2.5 g/l. Il contenuto
di HA è relativamente scarso nella cartilagine, anche se
ne rappresenta un importante elemento strutturale.
L'HA svolge la funzione di matrice in cui le cellule sono
alloggiate, oltre a giocare un importante ruolo in svariati
processi a livello dermico. È in grado di trattenere acqua
nei tessuti e, di conseguenza, può variare il volume e la
compressibilità della pelle. Può influenzare la proliferazione cellulare, la differenziazione cellulare e i processi di
riparazione del tessuto. Inoltre l’HA si occupa di smaltire
i radicali liberi generati dall'azione dei raggi ultravioletti
solari della pelle (ovvero il più grande organo del corpo
umano e la prima barriera protettiva tra tessuti sottostanti e ambiente esterno): la componente ultravioletta della
luce esercita infatti un forte stress ossidativo sulle cellule,
rischiando di danneggiarne il materiale genetico e causarne degenerazione e morte.
Cambiamenti nell'HA si osservano con l'invecchiamento,
nel corso di processi cicatriziali e nelle malattie degenerative, soprattutto se coinvolgono la pelle17.
Nel fluido sinoviale, l'alta concentrazione di HA a elevata massa molare provvede alla necessaria lubrifica-
TESSUTO O FLUIDO
CONCENTRAZIONE µg/ml NOTE
Cresta di gallo
7500
Il tessuto animale col maggior contenuto di HA
Cordone ombelicale umano
4100
Contiene principalmente HA con peso molecolare relativamente elevato
Articolazione umana
(fluido sinoviale)
Cartilagine nasale bovina
1400-3600
1200
Il volume del liquido sinoviale aumenta in condizione di infiammazione; ciò determina una riduzione della concentrazione di HA
Spesso usato come modello per gli studi sperimentali sulla cartilagine
Corpo vitreo umano
140-340
La concentrazione di HA aumenta con la maturazione del tessuto
Derma umano
200-500
Proposto come agente di "ringiovanimento" in dermatologia cosmetica
Epidermide umana
100
La concentrazione di HA è maggiore in prossimità delle cellule che lo producono
Cervello di coniglio
65
Si suppone che l'HA riduca la probabilità di tumore al cervello
Cuore di coniglio
27
Linfa toracica umana
0.2-50
Urina umana
0.1-0.3
L'HA è il maggior costituente della matrice patologica causa di occlusione dell'arteria in caso di restenosi coronarica
Il basso peso molecolare di questo HA è spiegato dall'assorbimento preferenziale, da
parte delle cellule endoteliali epatiche, per le grandi molecole
L'urina è anche un importante fonte di ialuronidasi
Siero umano
0.01-0.1
La concentrazione di HA aumenta nel siero dei soggetti anziani così come nei
pazienti con artrite reumatoide o cirrosi epatica
Figura 3
Presenza e concentrazione di HA in vari tessuti animali28.
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
47
L’acido ialuronico e le sue applicazioni in contattologia
zione dell'articolazione, assorbe efficacemente gli shock
meccanici, riduce la frizione tra le ossa in movimento e
previene l'usura delle articolazioni. Durante i processi
infiammatori causati dalle patologie artritiche (osteoartriti o artriti reumatoidi), l'alta massa molare dell'HA
viene degradata ad opera di forme reattive di ossigeno,
che riducono la sua viscosità e deteriorano le sue caratteristiche lubrificanti provocando così dolore articolare e
difficoltà di movimento18.
Sebbene in passato si fosse attribuito all’HA semplicemente il ruolo di molecola inerte con funzioni di riempimento del tessuto connettivo, studi successivi hanno
identificato siti di legami proteici e specifici recettori che
evidenziano il ruolo di attiva mediazione dell'HA in numerose attività fisiologiche19. Recentemente è stato infatti
attribuito all'HA un importante ruolo nell'embriogenesi, nella trasduzione dei segnali, nella motilità cellulare,
nell'invasività delle cellule cancerogene e nella formazione delle metastasi20.
Pur presentando una semplice e uniforme struttura primaria, il polimero di HA può raggiungere grandi dimensioni e, proprio in funzione della dimensione raggiunta,
può svolgere un ruolo biologico diversificato. I polimeri
di grandi dimensioni, oltre che svolgere funzioni di riempimento, hanno una funzione anti-angiogenica e immunosoppressiva. I polimeri di medie dimensione (20-50
disaccaridi) si caratterizzano come agenti infiammatori,
immunostimolatori e altamente angiogenici. I polimeri
di piccole dimensioni si comportano come antiapoptotici e stimolano la produzione di proteine implicate nello shock termico21. Una recente pubblicazione22 fornisce
un accurato studio sull'ampio range di dimensioni che
il polimero di HA può assumere e sulle sue specifiche
funzioni.
L'HA presente nel corpo umano è sintetizzato per mezzo
di enzimi chiamati Hyaluronic-Acid-Synthase (HAS); la
sua sintesi è normalmente bilanciata dal contemporaneo
catabolismo, pertanto la sua concentrazione nei tessuti
rimane costante. I cheratinociti dell'epidermide sono un
esempio di cellule che attivamente sintetizzano e catabolizzano ialuronati; in questo caso l'emivita delle molecole
di ialuronato è incredibilmente breve ovvero meno di un
giorno. Esistono però anche cellule che sintetizzano più
HA di quello che catabolizzano, così come esistono cellule che catabolizzano più HA di quello che sintetizzano13.
Le applicazioni dell’acido ialuronico in farmacologia
Le aree di applicazione clinica dell'HA e dei suoi derivati
sono state classificate da Balazs23 nel seguente modo, in
relazione alle loro finalità:
(1)Protezione di tessuti delicati e fornitura di spazio durante interventi chirurgici
(2) Aumento della viscosità, riempimento e aumento di
volume di un tessuto (come la pelle), di un muscolo
sfintere o di un tessuto della faringe
(3) Separazione di tessuti connettivi con superfici traumatizzate a causa di procedure chirurgiche o di traumi al fine di prevenire adesioni o eccessive formazioni cicatriziali
(4) Rimpiazzo o implementazione di fluidi tissutali (ad
esempio rimpiazzo del fluido sinoviale nei soggetti
affetti da artrite per alleviarne la sintomatologia)
(5) Protezione di tessuti sani, feriti o offesi da secchezza o
da agenti nocivi ambientali e promozione della guarigione di determinate superfici.
In farmacologia i gruppi carbossilati di HA sono utilizzati per produrre idrogel cross-linked in grado di intrappolare e poi liberare molecole bioattive. L'HA viene
anche usato per preparare microcapsule che migliorano
la somministrazione di alcuni farmaci24 e per migliorare la biocompatibilità delle microsfere di chitosan usate
come vettori di farmaci25. Microsfere di HA sono inoltre
utilizzate per trasportare plasmidi di DNA e anticorpi
monoclonali nel trasferimento genico e verso specifici
siti bersaglio26.
Le applicazioni dell’acido ialuronico in oftalmologia
Sono ampie le possibili applicazioni dell'HA in Ortopedia, Reumatologia, Otorinolaringoiatria, Dermatologia
e Chirurgia Plastica. Nella terapia delle ferite, l’elevato
peso molecolare dei preparati a base di HA (applicati a
livello topico) promuove e favorisce la guarigione delle
ferite a livello cutaneo, la guarigione delle ulcere venose (specie a livello delle gambe) e la terapia delle lesioni
croniche27. L’HA, grazie alle sue proprietà antiossidanti,
è utile anche come componente antinfiammatorio nelle
ferite profonde con perdita di materiale.
L’HA è il maggior componente del corpo vitreo ed è una
macromolecola assai importante anche in oftalmologia.
Grazie alle sue proprietà viscoelastiche è utilizzato in
numerosi interventi chirurgici in campo oftalmologico,
sia per proteggere i tessuti oculari più delicati che per
procurare spazi durante la manipolazione chirurgica. Il
suo maggior utilizzo consiste però nella sostituzione o
nell’integrazione del corpo vitreo che è stato perso durante varie manovre chirurgiche, la più frequente delle
quali è l’impianto di IOL.
Le soluzioni a base di HA sono anche utilizzate come
protettori viscoelastici dell’endotelio corneale durante gli
interventi di trapianto corneale. Attualmente in oftalmologia sono disponibili numerosi preparati caratterizzati
dalla presenza di catene di HA (di diverse dimensioni
molecolari)28.
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
48
ARTICO L O
L’acido ialuronico e le sue applicazioni in contattologia
Le applicazioni dell’acido ialuronico in contattologia
L'HA è una delle molecole più igroscopiche presenti in
natura e, idratato, può contenere una quantità di acqua
mille volte superiore al proprio peso29. In contattologia,
questa eccezionale capacità di ritenzione idrica viene
sfruttata per migliorare l'idratazione dell'area precorneale30; l’HA è infatti uno dei principi attivi più impiegati
nei numerosi sostituti lacrimali in commercio e nel trattamento delle varie forme di occhio secco (da quelle più
gravi a quelle marginali)31,32.
L'HA, grazie alla sua alta viscosità e alla sua elevata capacità di legare acqua33, viene impiegato come principio
attivo in numerosi colliri in quanto protegge e lubrifica la
superficie oculare e migliora la sintomatologia correlata
alle sindromi da occhio secco34,35. Viene spesso anche inserito nelle formulazioni delle soluzioni per la manutenzione delle lac, in quanto provvede a migliorare e prolungare
il comfort dei portatori aumentando la bagnabilità della
lente e inducendo così una riduzione della frequenza degli
ammiccamenti36,37. L’HA può anche fungere da eccipiente
quando viene utilizzato insieme ai farmaci, aumentando il
loro tempo di permanenza nell'area precorneale e quindi
migliorando la biodisponibilità dei farmaci stessi38,39.
È stato dimostrato che l'applicazione topica di HA (0.1%
W/V) riduce la sintomatologia soggettiva e i segni clinici nei
soggetti con sindrome da occhio secco40,41. Altre ricerche hanno dimostrato che l'HA può efficacemente proteggere l'epitelio corneale42 e migliorare la stabilità del film precorneale43.
L'utilizzo di HA è in grado di ripristinare la secrezione di
lattoferrina e difensine B, grazie alla sua elevata mucoadesività e alla sua capacità di ritenzione idrica nell'area
precorneale; ciò velocizza e favorisce il ripristino della
condizione fisiologica ottimale, agevolando i meccanismi
di riepitelizzazione corneo-congiuntivali. È stato dimostrato che, quando instillato nell'area pre-corneale, l'HA
promuove e favorisce la guarigione fisiologica, stimolando la migrazione e la proliferazione dei cheratociti44,45.
Le soluzioni a base di HA hanno un comportamento
non Newtoniano ovvero sono soluzioni ad alta viscosità quando sono sottoposte a forze di taglio poco intense
(occhio aperto), a bassa viscosità quando sono sottoposte
a forze di taglio più intense (ammiccamento); tale comportamento permette un'adeguata distribuzione e un’ottimale lubrificazione della superficie oculare46,47. Un'altra
rilevante caratteristica dell’HA è la muco-adesività, che
gli permette di formare un rivestimento duraturo e di fornire una stabile protezione alla superficie corneale48-50.
Le caratteristiche biologiche dell'acido ialuronico determinano una modificazione della popolazione microbica
aerobica ed anaerobica presente nel segmento anteriore
dell’occhio, ripristinando i batteri saprofiti della superficie oculare. Utilizzandolo, si osserva infatti una riduzione dello Pseudomonas e dello Staphylococcus aureus
a favore dello Stafilococco epidermidis; ciò avviene probabilmente grazie al ripristino della secrezione di lattoferrina e di difensine B prodotte dalle cellule epiteliali
congiuntivali, che sono debilitate nei soggetti con occhio
secco marginale. L'HA può infatti evitare una situazione
infiammatoria cheratocongiuntivale da iposecrezione,
può risolvere l'iposecrezione relativa ed inoltre può diminuire l'incidenza delle mucin-balls, talvolta associate
all'uso prolungato di lac in silicone idrogel51.
L'HA presente nell'area pre-corneale funge infine da tampone osmotico, aiutando a mantenere l'idratazione del
tessuto. Nel complesso, in sua presenza si riscontra una
maggior funzionalità dell'attività di barriera dell'epitelio
corneale15,52.
Sempre più produttori di lac inseriscono nella matrice
polimerica e/o nel blister della lac dei polimeri capaci
di migliorare la bagnabilità superficiale o la capacità di
mantenere l'idratazione costante; l'acido ialuronico rappresenta un'alternativa ai più noti agenti umettanti impiegati sino ad ora e si differenzia da questi perché è un
polimero naturale, presente nel corpo umano e a livello
oculare. In questi anni sono state introdotte sul mercato
lac contenenti HA nella loro matrice polimerica e nella
soluzione contenuta nel blister, che sfruttano le proprietà
dell'HA per migliorare il comfort durante le ore di porto.
A conferma delle prospettive di impiego dell'HA in contattologia, che presentano interessanti margini di crescita,
alcuni produttori di lac ed alcuni organi di controllo hanno richiesto la messa a punto di tecniche, relativamente semplici, per quantificare l'HA presente in soluzione,
nelle condizioni e nelle concentrazioni tipiche di questi
prodotti. Da un’analisi della letteratura relativa alle tecniche analitiche riportate, risulta che le bande di assorbimento ottico mostrate a lunghezze d’onda intorno a 200
nm o inferiori sono poco utilizzabili, in quanto coperte
dalle bande di assorbimento della matrice polimerica o
della soluzione nella quale l'acido ialuronico è disperso.
La maggior parte dell'ampio ventaglio di tecniche analitiche riportate oggi in letteratura consente l’analisi di
soluzioni contenenti HA a concentrazioni più elevate di
quelle utilizzate in contattologia, peraltro con tecniche
analitiche realizzate per operare in contesti profondamente differenti o che richiedono minor sensibilità.
Recentemente sono però state sviluppate due nuove tecniche per la determinazione di HA in soluzione. La prima è un metodo indiretto che si basa sullo studio della
variazione del tipico picco di assorbimento del colorante libero Alcian Blu in funzione della concentrazione di
HA. L'intensità di tale picco decresce all'aumentare dei
complessi HA/colorante. La sensibilità della tecnica con
Alcian Blu, che può essere utilizzata sia con soluzioni di
acqua deionizzata che con soluzioni saline, permette di
rilevare la presenza di 2.5 µg/ml di HA; la dipendenza
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
49
L’acido ialuronico e le sue applicazioni in contattologia
Figura 4
Assorbanza di soluzioni contenenti HA e Alcian Blu in soluzione
salina. I pallini indicano l’assorbanza media misurata in diverse
soluzioni preparate con le stesse concentrazioni nominali, la barra
dell’errore indica la corrispondente deviazione standard e la linea
indica il fit lineare dei dati sperimentali tra 2.5 e 20 µg/ml 53.
Figura 5
Assorbanza misurata a 520 nm (rombi vuoti) e a 640 nm (rombi
pieni) di soluzioni contenenti Stain All (0.03 mg/ml) e HA (varie
concentrazioni) in acqua deionizzata e metanolo. I rombi indicano
l’assorbanza media misurata in diverse soluzioni con le stesse
concentrazioni nominali e la barra dell’errore indica la relativa
deviazione standard; le linee indicano i fits lineari dei dati
sperimentali nei corrispondenti intervalli di concentrazione 53.
tra il valore di assorbanza misurata a 550 nm la concentrazione di HA risulta lineare nell'intervallo compreso tra
2.5 e 20 µg/ml (Figura 4).
La seconda tecnica, in cui si utilizza il colorante Stain All,
si basa sull'osservazione di due picchi di assorbimento:
uno a 520 nm, che è attribuito al colorante libero e che
decresce all'aumentare della concentrazione di HA; uno
a 640 nm, che è attribuito al complesso HA/colorante e
la cui intensità cresce all'aumentare della concentrazione di HA. Considerando il picco a 520 nm, la sensibilità
della tecnica con Stain All è risultata migliore in quanto
raggiunge 0.25 µg/ml, ma è influenzata dall’eventuale
presenza di altri anioni (come tipicamente accade in soluzione salina). Al contrario, quando si considera il picco
a 640 nm, la sensibilità è la stessa che caratterizza il protocollo basato sull'Alcian Blue (Figura 5)53.
ma, poiché l'HA nei tessuti biologici è generalmente legato anche ad altri biopolimeri, debbono essere adottate
specifiche procedure per renderlo puro. In funzione della
sempre migliore efficienza del processo di “purificazione”, è oggi possibile ottenere preparati di HA di dimensioni comprese tra alcune centinaia di migliaia di Dalton
fino a circa 2.5 MDa così che, attualmente, la domanda di
HA per applicazioni mediche è ampiamente soddisfatta.
In passato l'HA è sempre stato ricavato da tessuti animali
(specialmente dalla cresta di gallo) e l'FDA approva tale
fonte di approvvigionamento per l’uso medico (come, per
esempio, accade con l'Healon in chirurgia oftalmica). Negli ultimi tempi, diverse compagnie hanno però iniziato
a proporre HA prodotto per fermentazione, che viene secreto da microorganismi come lo Streptococcus zooepidemicus e lo Streptococcus equi, utilizzando diversi ceppi
attenuati di streptococchi (s-HA)56,57. Lo s-HA risponde ai
requisiti di massa molare, raggiungendo diversi milioni di
Dalton58. Se l'HA di origine animale ha l’indubbio vantaggio di poter raggiungere pesi molecolari anche superiori
ai 5 MDa, ha però lo svantaggio di poter contenere varie
proteine e di poter causare reazioni allergiche. L'acido ialuronico prodotto per fermentazione non provoca invece
reazioni allergiche e può raggiungere pesi molecolari compresi tra 0.5 e 2.5 MDa; può però contenere endotossine.
Fonti biologiche dell’acido ialuronico
L’indotto economico legato all'HA è enorme e si stima sia
superiore al bilione di dollari54,55; ciò perché l'HA ricopre
un ruolo essenziale dal punto di vista funzionale per numerosi tessuti dei vertebrati. Vari tessuti animali (come la
cresta del gallo, la pelle dello squalo e il globo oculare del
bovino) ne contengono elevate quantità e rappresentano
preziose fonti di approvvigionamento di HA (Figura 3)
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
50
ARTICO L O
L’acido ialuronico e le sue applicazioni in contattologia
Recentemente, per produrre su scala industriale HA (bHA) è stato proposto un nuovo processo di fermentazione
basato sul Bacillus subtilis; questo nuovo tipo di HA non
contiene endotossine, ma non esistono ancora studi clinici
riguardanti il suo utilizzo in forma iniettabile59.
Le prime due tecniche descritte portano alla produzione di HA ad alto peso molecolare (>1 MDa), mentre la
produzione basata sul Bacillus subtilis fornisce HA di
peso molecolare compreso tra 0.6 e 1 MDa. Le soluzioni
preparate con HA ad alto peso molecolare sono viscose
alle concentrazioni utilizzate nei colliri (0.1-0.3% W/V)60.
È importante che siano dotate di una certa viscosità, affinché non vengano immediatamente drenate dalla superficie oculare e possano garantire un lungo tempo di
permanenza nel segmento anteriore dell’occhio, migliorando così la loro efficacia; non devono peraltro essere
eccessivamente viscose in quanto causerebbero visione
sfuocata o fluttuante. Ogni anno sono prodotte e vendute
varie tonnellate di HA prodotto per fermentazione. È presente il rischio che il ceppo batterico subisca mutazioni e
associ la produzione di HA con quella di tossine, pirogeni
o immunogeni; ciò ostacola, nelle applicazioni cliniche,
un'ampia diffusione dell'HA prodotto per fermentazione.
Per questo motivo i campioni di HA derivati dalla cresta
di gallo sono tutt’oggi i preferiti per i trattamenti medici,
specialmente nei casi in cui il prodotto è destinato ad essere iniettato, nonostante che anche questo tipo di HA non
sia esente da difetti: è infatti controindicato nei soggetti
che presentano allergie ai prodotti aviari ed è proprio per
questo motivo che le aziende del settore continuano a ricercare e testare nuove fonti possibili di HA28.
Conclusioni
Le soluzioni oftalmiche ad uso topico contenenti HA sono
sempre più conosciute ed apprezzate grazie alle caratteristiche di questo interessante polimero naturale, che
spesso è utilizzato come agente umettante ed integratore
lacrimale. I recenti sviluppi nel campo delle biotecnologie
consentono oggi di optare per l'HA con il peso molecolare
più adeguato all'uso, scegliendo tra un ampio ventaglio;
vengono proposti HA ad alto peso molecolare (>1 MDa) e
a medio peso molecolare (0.6-1.0 MDa) mentre le soluzioni
oftalmiche che fanno uso di HA presentano generalmente
concentrazioni di HA comprese tra 0.1 e 0.3% W/V.
Numerosi studi stanno analizzando come e quanto il
peso molecolare che caratterizza l'HA possa influenzare
la sua capacità di legare molecole d'acqua, il suo profilo
reologico, il tempo di permanenza nell'area pre-corneale
e la tollerabilità della soluzione oftalmica. Tali studi potranno chiarire se esiste un HA con un peso molecolare
ottimale, da preferire quindi a tutti gli altri, oppure se è
necessario variare il suo peso molecolare in relazione alle
diverse problematiche.
Bibliografia
1 Young G, Veys J, Pritchard N, Coleman S. A multi-centre study
of lapsed contact lens wearers. Ophthal Physiol Opt, 2002;
22:516-527.
2 Lemp MA, Foulks GN. The definition & classification of dry
eye disease. Guidelines from the 2007 international dry eye
workshop.
3 Ousler GW 3rd, Hagberg KW, Schindelar M, Welch D, Abelson
MB. The ocular protection index. Cornea, 2008; 27: 509-513.
4 Bonci E, Altimari S, Mascaro T, Lorenzatti M, Leopardi S, Missiroli A. The use of a new-generation lacrimal substitute in dry
eye sindrome. Italian Ophthlmological bulletin, 2004; 4:1-11.
5 Snibson GR, Greaves JL, Soper NDW, Tiffany JM, Wilson CG,
Bron AJ. Ocular surface residence times of artificial tear solutions. Cornea, 1992; 11:288-293.
6 Ludwig A, Van Ooteghem M. Evaluation of sodium hyaluronate as viscous vehicle for eye drops. J Pharm Belg, 1989;
44:391-397.
7 Camber O, Edman P, Gurny R. Influence of sodium hyaluronate
on the miotic effect of pilocarpine in rabbits. Curr Eye Res, 1987;
6:779-784.
8 Szczotka-Flynn LB. Chemical properties of contact lens rewetters.
A review on hyaluronic acid as a contemporary ingredient in contact lens rewetters. Contact Lens Spectrum, 2006; april: 40-45.
9 Aragona P, Di Stefano G, Ferreri F, Spinella R, Stilo A. Sodium
hyaluronate eye drops of different osmolarity for the treatment
of dry eye in Sjogren's syndrome patients. Br J Ophthalmol,
2002; 86:879-884.
10 Papa V, Aragona P, Russo S, Di Bella A, Russo P, Milazzo G.
Comparison of hypotonic and isotonic solutions containing
sodium hyaluronate on the symptomatic treatment of dry eye
patients. Ophthalmologica, 2001; 215:124-127.
11 Condon PI, McEwen CG, Wright M, Mackintosh G, Prescott RJ,
McDonald C. Double blind, randomised, placebo controlled,
crossover, multicentre study to determine the efficacy of a 0.1%
(w/v) sodium hyaluronate solution (Fermavisc) in the treatment
of dry eye syndrome. Br J Ophthalmol, 1999; 83:1121-1124.
12 Laurent TC, Robert J, Fraser E. Hyaluronan. FASEB J, 1992;
6:2397-2404.
13 Laeschke K. Everything you wanted to know about hyaluronic
acid. Http://www.cristalfillers.com/docs/Everything_About_
HA.pdf.
14 Juhlin L. Hyaluronan in skin. J Intern Med, 1997; 242:61-66.
15 Shiedlin A, Bighelow R, Christophe W, Arbabi S, Yang L, Maier
RV, Wainwright N, Childs A, Miller RJ. Evaluation of hyaluronan from different sources: Streptococcus zooepidemicus,
rooster comb, bovine vitreous, and human humbilical cord.
Biomacromolecules, 2004; 5:2122-2127.
16 Soltes L, Mendichi R, Kogan G, Schiller J, Stankovska M, Arnhold J. Degradative action of reactive oxygen species on hyaluronan. Biomacromolecules, 2006; 7:659-668.
17 Tammi MI, Day AJ, Turley EA. Hyaluronan and homeostasis: a
balancing act. J Biol Chem, 2002; 277:4581-4784.
18 Chong BF, Blank LM, McLaughlin R, Nielsen L. Microbiol Biotechnol, 2005; 66:341-351.
19 Mendichi R, Schieroni AG. Fractionation and characterization
of ultra-high molar mass hyaluronan: 2. On-line size exclusion
chromatography methods. Polymer, 2002; 43:6115-6121.
20 Mengher LS, Bron AJ, Tonge SR, Gilbert DJ. Non-invasive assessment of tear film stability. In Holly FJ (Ed). The Preocular
Tear Film in Health, Disease and Contact Lens Wear. Lubbock,
TX: Dry Eye Institute, 1986:64-80
21 Xu H, Ito T, Tawada A, Maeda H, Yamanokuchi H, Isahara K,
Yoshida K, Uchiyama Y, Asari A. Effect of hyaluronan oligo-
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
51
L’acido ialuronico e le sue applicazioni in contattologia
22
23
24
25
26
27
28
29
30
31
32
33
34
35
36
37
38
39
40
41
42
43
saccharides on the expression of heat shock protein 72. J Biol
Chem, 2002; 277:17308–17314.
Stern R, Asari AA, Sugahara KN. Hyaluronan fragments: an
information-rich system. Eur J Cell Biol, 2006; 85:699–715.
Edmonds ME, Foster AV. Diabetic foot ulcer. Brit Med J, 2006;
332:407-410.
Ky W, Scherick K, Stenson S. Clinical survey of lens care in contact lens patients. CLAO J, 1998;24:4 216-219.
European Federation of National Associations and International Companies of Contact Lens Manufactures, 2003.
Tomlinson A. Complication of contact lens wear. London, Mosby-Year Book, 1992, 195-218.
Vasiliu S, Popa M, Rinaudo M. Polyelecrtolyte capsules made
of two biocompatibles natural polymers. Eur Polym J, 2005;
41:923-932.
Grigorij Kogan, Ladislav Soltes, Robert Stern, Peter Gemeiner. Hyaluronic acid: a natural biopolymer with a broad range of biomedical and industrial applications. Biotechnol Lett, 2007; 29:17–25
Laurent TC, Fraser JRE. Hyaluronan. FASEB J, 1992; 6:2397-2404.
Nakamura M, Hikida M, Nakano T, Ito S, Hamano T, Kinoshita
S. Characterization of water retentive properties of hyaluronan.
Cornea, 1993; 12:433-436.
Dumbleton K, Jones L, Chalmers R, Williams-Lyn D, Fonn D. Clinical characterization of spherical post-lens debris associated with
lotrafilcon high-DK silicone lenses. CLAO J, 2000; 26:4 186-92.
Mengher LS, Pandher KS, Bron AJ. Effects of sodium hyaluronate (0.1 per cent) on break-up time (nibut) in patients
with dry eyes. Br J Ophthalmol, 1986; 70:422-427.
Felt O, Einmahl S, Furrer P, Baeyens V, Gurny R. Polymeric
System for Ophthalmic Drug Delivery. Polymeric Biomaterials,
2002; 377-421.
Bron AJ, Mangat H, Quinlan M, Foley-Nolan A, Eustace P,
Fsadni M, Sunder Raj P. Polyacrylic acid gel in patients with
dry eyes: a randomised comparison with polyvinyl alcohol.
Eur J Ophthalmol, 1998; 8:81-89.
McDonald CC, Kaye SB, Figueiredo FC, Macintosh G, Lockett C. A randomised, crossover, multicentre study to compare
the performance of 0.1% (w/v) sodium hyaluronate with 1.4%
(w/v) polyvinyl alcohol in the alleviation of symptoms associated with dry eye syndrome. Eye, 2002; 16:601-607.
Acosta MC, Gallar J, Belmonte C. The influence of eye solutions on blinking and ocular comfort at rest and during work at
video display terminals. Exp Eye Res, 1999; 68:663- 669.
Sclafani LA. Lubricant eye drops for contact lens wearers. Rev
Cornea Contact Lens, 2005; march: 1-4.
Bernatchez SF, Tabatabay C, Gurny R. Sodium hyaluronate
0.25% used as a vehicleincreases the bioavailability of topically
administered gentamicin. Graefe’s Arch Clin Exp Ophthalmol,
1993; 231:157-161.
Saettone MF, Giannaccini B, Ravecca S, La Marca P, Tota G.
Polymer effects on ocular bioavailability-the influence of different liquid vehicles on the mydriatic response of tropicamide
in humans and in rabbits. Int J Pharm, 1984; 20:187-202.
DeLuise VP, Peterson WS. The use of topical sodium hyaluronate (Healon) in the management of refractory dry eye
syndrome. Ann Ophthalmol, 1984; 16: 823–824.
Stuart JC, Lim JG. Dilute sodium hyaluronate (Healon) in the
treatment of ocular surface disorders. Ann Ophthalmol, 1985;
17: 190–19.
Wysenbeek WS, Loya N, Sira BL. The effect of Eye sodium hyaluronate on the corneal epithelium. Invest Ophthalmol Vis Sci,
1988; 29: 194–199.
Hamano T, Horimoto K, Lee M, Komemushi S. Sodium hyaluronate eye drops enhance tear film stability. Jpn J Ophthal-
mol, 1996; 40:62-65.
44 Tani E, Katakami C, Negi A. Effects of various eye drops on
corneal wound healing after superficial keratectomy in rabbits.
Jpn J Ophthalmol, 2002; 46:488-495.
45 Nishida T, Nakamura M, Mishima H, Otori T. Hyaluronan
stimulates corneal epithelial migration. Exp Eye Res, 1991;
53:753-758.
46 Ludwig A, Van Ooteghem M. Evaluation of sodium hyaluronate as viscous vehicle for eye drops. J Pharm Belg, 1989;
44:391-397.
47 Berriaud N, Milas M, Rinaudo M. Characterization and properties of hyaluronic acid (hyaluronan). In Dumitriu S. Polysaccharides. Structural diversity and functional versatility. New
York, Marcel Dekker Inc, 1998, 313-334.
48 Saettone MF, Monti D, Torracca MT, Chetoni P. Mucoadhesive
ophthalmic vehicles: evaluation of polymeric low-viscosity formulations. J Ocul Pharmacol, 1994; 10:83-92.
49 Greaves JL, Wilson CG. Treatment of diseases of the eye with
mucoadhesive delivery systems. Adv Drug Delivery Rev, 1993;
11:349-383.
50 Saettone MF, Chetoni P, Torraca MT, Burgalassi S, Giannaccini
B. Evaluation of muco-adhesive properties and in vivo activity
of ophthalmic vehicles based on hyaluronic acid. Int J Pharm,
1989; 51:203-212.
51 Hamano T, Horimoto K, Lee M. Sodium hyaluronate eyedrops
enhance tear film stability. Jpn J Ophthalmol, 1996; 40:60-5.
52 Evanko S, Wight T. Intracellular hyaluronan. In: Hyaluronan:
syntesis, function, catabolism. 2001; www.glycoforum.gr.jp/
science/hyaluronan/HA20/HA20E.html.
53 Fagnola M, Pagani MP, Maffioletti S, Tavazzi S, Papagni A. Hyaluronic acid in hydrophilic contact lenses: Spectroscopic investigation of the content and release in solution. Contact Lens
Anterior Eye, 2009; 32:108-112.
54 Balzas EA. Viscoelastic properties of hyaluronan and its therapeutic use. In Garg HG, Hales CA. Chemistry and biology of
hyaluronan. Amsterdam, Elsevier, 2004, 415.
55 Widner B, Behr R, Von Dollen S. Hyaluronic acid production
in Bacillus subtilis. Applied and environmental microbiology,
2005; 71:3747-3752.
56 Chong BF, Blank LM, Mclaughlin R, Nielsen LK. Microbial
hyaluronic acid production. Appl Microbiol Biotechnol, 2005;
66:341-351.
57 Balazs EA. Ultra pure, high molecular wt. hyaluronic acid - is
non-antigenic and used as synthetic aq. humour and synovial
fluid, as nerve tissue and wound protector and drug carrier.
1979;US patent 4,141,973.
58 Maltese A, Borzacchiello A, Mayol L, Bucolo C, Maugeri F, Nicolais L, Ambrosio L. Novel polysaccharides-based viscoelastic
formulations for ophthalmic surgery: rheological characterization. Biomaterials, 2006; 27:5134-5142.
59 Widner W, Sloma A, Thomas M, Tang M. Producing a hyaluronic acid, by cultivating Bacillus cell comprising a nucleic
acid construct comprising a variant amyL promoter, a consensus promoter, and a cryIIIA promoter, and isolating hyaluronic
acid from the cultivation medium. 2005;WO patent application
2005098016-A2.
59 Esposito E, Menegatti E, Cortesi R. Hyaluronan-based microspheres as tools for drug delivery: a comparative study. Int J
Pharm, 2005; 288:35-49.
60 Bothner H, Waaler T, Wik O. Rheological characterization of
tear substitutes. Drug Dev Ind Pharm, 1990; 16:755-768.
M. Fagnola e altri / Lac Lenti a contatto 2010; 12 (2): 45-52
52
Nicola Pescosolido*, Chiara Nardella**
Sapienza - Università di Roma
*Dipartimento di Scienze dell’Invecchiamento
**Dipartimento di Scienze Oftalmologiche
Gli autori revisionano alcuni lavori di letteratura sulla stretta evidenza esistente tra il tipo
di lente a contatto, la soluzione usata per la sua manutenzione, nonchè la loro combinazione
e la presenza di eventi avversi oculari legati al porto giornaliero delle lenti in silicone idrogel
oggigiorno molto diffuse sul mercato.
Tra le diverse associazioni “lente-soluzione” indagate nei vari studi, il perossido di idrogeno
con ogni tipo di lente ha mostrato la più bassa incidenza di eventi infiltrativi corneali, complicanze direttamente correlate con il discomfort e la tollerabilità all’uso delle lac nei sempre
più numerosi consumatori.
Come per eliminare le complicanze legate all’uso di lac è di fondamentale importanza conoscere il tipo di relazione esistente tra le diverse combinazioni “lente-soluzione”, cosi’ lo è la
ricerca di nuovi materiali biocompatibili e la comprensione dei meccanismi di reazione tra
farmaco e struttura della lente nella produzione delle nuove lenti a contatto medicali.
PAROLE CHIAVE
Lenti a contatto in silicone idrogel, soluzioni per
manutenzione lac, lenti medicali
Ricevuto il 14 maggio, 2010; accettato il 14 settembre, 2010.
Introduzione
Le lenti in silicone idrogel hanno conquistato ad oggi un
ampio settore di mercato grazie al caratteristico elevato valore di permeabilità all’ossigeno (Dk) che si traduce nella
capacità di eliminare o ridurre i segni clinici dell’ipossia offrendo così all’occhio un comfort maggiore.
Originariamente introdotte per il porto prolungato, le lenti
a contatto in silicone idrogel sono diffusamente usate anche per l’uso giornaliero. Questo ha indirizzato l’attenzione
dei professionisti e dell’industria del settore verso la conoscenza delle complicanze associate al loro uso come causa
di ridotta tollerabilità e quindi anche verso i sistemi per la
manutenzione quotidiana1. È infatti necessario comprendere come ogni singola soluzione, usata per la manutenzione giornaliera delle lenti a contatto (lac), interagisca in
maniera diversa e specifica con gli svariati materiali in silicone idrogel presenti sul mercato. Tale specificità si traduce
conseguentemente in diversi gradi, più o meno gravi, di discomfort. Dunque, in relazione a quanto detto, assume una
certa importanza la definizione di adeguate indicazioni in
base alle quali poter scegliere una particolare combinazione
“lente-soluzione” che sia più efficace e meno critica.
Rassegna
Sono stati compiuti numerosi lavori al fine di predire l’esito
clinico delle diverse combinazioni esistenti tra soluzioni per
la manutenzione e lenti in silicone idrogel.
Già nel 2002 Jones et al.2 avevano evidenziato e sollevato l’interesse sull’ evidenza di staining corneale risultante dall’uso
di lenti in silicone idrogel associate a specifiche soluzioni.
Più recentemente Andrasko et al. 3, allo scopo di fornire
uno strumento di riferimento che fornisse informazioni
sul livello di biocompatibilità delle diverse combinazioni, hanno formulato una griglia di staining.
I dati si basano su risultati ottenuti in seguito all’immersione di una lente (per un’intera notte) in diverse soluzioni al fine di registrare la percentuale media di staining
corneale (per area) valutata il giorno successivo dopo 2
ore di porto. (Tab. 1).
Andrasko e Reyen4-5 hanno valutato ancora la comparsa di
staining mediante l’uso di un test provocativo eseguito a 2 e
4 ore di porto della lac. Prima dell’applicazione le lenti venivano bagnate nella soluzione per un tempo di 12 ore.
Le soluzioni usate nello studio sono riportate in tabella
(Tab.2). I pazienti, inoltre, prima di utilizzare le nuove lenti
dovevano immergerle nelle diverse soluzioni per almeno 12
ore. La severità degli staining (0-4) e le dimensioni dell’area
interessata (0-100%) sono state registrate per 5 diverse zone
della cornea in ogni occhio. Le combinazioni lente-soluzione
che mostravano l’area più estesa di staining erano:
• Complete® MoisturePLUS™/ PureVision™ at 2 hrs
(38%) and 4 hrs (33.7%)
53
ARTICO L O
La ricerca di nuovi materiali biocompatibili per la manutenzione
quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
Marche delle soluzioni
Renu
Fresch3
Renu
Sensitive3
5%
1%
1%
1%
1%
1%
1%
1%
1%
1%
2%
57%
23%
6%
12%
61%
54%
53%
42%
1%
1%
1%
73%
32%
17%
8%
66%
62%
63%
56%
1%
1%
1%
13%
4%
12%
2%
16%
13%
12%
12%
2%
1%
3%
5%
9%
5%
4%
3%
12%
8%
13%
10%
2%
2%
3%
2%
4%
2%
2%
2%
4%
3%
3%
2%
Unisol 4
Saline
Clear
Care4
Acuvue5 2
1%
1%
2%
Proclear
1%
1%
Soflens 66
1%
1%
Idrogel
Silicone Idrogel
6
3
Acuvue
Advance5
Acuvue
Oasys5
Biofinity6
* Private Label
Complete
MPS Easy
Rub2
1
Opti-free Opti-free
Replenisch1 Replenisch1
Aquify4
Walmart
Target
Walgreen
CVS MPS
MPS
MPS
MPS
(Renu M+)
(Renu M+) (Renu M+)
(Renu M+)
No test
No test
programmato programmato
Purevision
2%
1%
4%
7%
73%
43%
15%
21%
71%
76%
O2 Optix4
2%
1%
2%
5%
24%
7%
3%
3%
41%
28%
28%
24%
Night
& Day4
2%
1%
2%
3%
24%
11%
1%
3%
36%
24%
26%
22%
Salina
H2O2
3
POLYQUAD
Biguanide
Tabella 1
Griglia di Andrasko. In base al colore la percentuale media di staining corneale (per aerea) è cosi’ organizzata: verde = sotto il 10%;
giallo = dal 10% al 20% ; rosso = sopra il 20%
*Private Label o marche private sono prodotti o servizi solitamente realizzati o forniti da società terze (fornitore di marca industriale o
terzista vera e propria) e venduti con il marchio della società che vende/offre il prodotto/servizio (Distributore) (da Andrasho et al.,2006).
Soluzioni per la manutenzione delle lac usate nello studio di Andrasko e Reyen 4-5
Tipi di lenti utilizzate nello Studio IER Matrix
Soluzione
Marca
Molecola
Lente
Opti-Free Express
Alcon
polyquaternium-1
ACUVUE ADVANCE
ReNu MoistureLoc
B&L
alexidine
AQuify
Complete MoisturePLUS
CIBA
polyhexanide
polyhexamethylene
biguanide
AMO
Pure Vision
Marca
Vistakon, Johnson & Johnson,
Vision Care Inc
Vistakon, Johnson & Johnson,
Vision Care Inc
Baush & Lomb
AIR OPTIX
CIBA VISION
ACUVUE OASYS
Tabella 2
Le soluzioni riportate nello studio di Andrasko e Reyen (da
Andrasko et al., 2008).
Tabella 3
Le lenti utilizzate nello Studio IER Matrix (da Carnt et al.,2007).
• AQuify™/ PureVision™ at 2 hrs (21.3%) and 4 hrs
• ReNu® MoistureLoc®/ Oasys™ at 4 hrs (8.2%)
• ReNu® MoistureLoc®/ PureVision™ at 4 hrs (8%)
• ReNu® MoistureLoc®/ O 2Optix™ at 4 hrs (7.4%)
• AQuify™/ O 2Optix™ at 2 hrs (7.1%)
OPTI-FREE® EXPRESS® utilizzata con ogni tipo di lente
risultava determinare le aree di staining di dimensioni
minori (3.5% dopo 2 ore e 3.8% dopo 4).
Anche in questo caso i risultati dello studio dimostrano
come alcune combinazioni lente in silicone idrogel/soluzione unica (MPS) possano causare in maniera più o meno
importante staining a livello della cornea dei soggetti che le
utilizzano. Carnt et al. nel 20076 hanno continuato ad esaminare il variabile rapporto esistente tra i difetti dell’epitelio corneale indotti dal tipo di manutenzione utilizzata
per la cura delle lac e il legame con l’infiammazione della
cornea stessa. In un loro secondo studio (Studio IER Matrix)7 hanno raccolto e indagato i dati relativi a gruppi di
circa 40 pazienti seguiti per tre mesi durante l’utilizzo di
16 combinazioni “soluzione-lente in silicone idrogel”, per
un totale di 640 associazioni paziente-liquido-lente.
I partecipanti allo studio venivano visitati per un totale
di 4 volte durante lo studio: all’inizio, a due settimane, a
1 e a 3 mesi.
Le lenti e le soluzioni utilizzate nello studio sono riportate in tabella (Tab. 3 e 4).
Ai pazienti è stato chiesto di indossare le proprie lenti per
un minimo di 6 ore al giorno per 5 giorni la settimana. Lo
staining corneale è stato misurato sulla nuova scala di gradazione IER da 0 a 4 per estensione (0= nessuno,1= ≤5 %, 2
= 6 % -15 %, 3 = 16 % - 30 % e 4 = >30 % ) in ciascuna delle
5 zone della cornea. Inoltre, i clinici hanno indicato la presenza dei difetti epiteliali indotti dalla soluzione secondo
tale definizione: staining diffuso e puntato (grado di estensione 1 e superiori) in almeno 4 delle 5 regioni (centrale,
superiore, inferiore, nasale e temporale) della cornea. Può
essere presente anche staining congiuntivale che si estende dal limbus al bordo della lente. Una rappresentazione
di staining da lac è raffigurato in figura 1 (Fig.1).
I dati dello studio IER Matrix sono riportati nella tabella
5. I valori presentati indicano la percentuale di pazienti
con SICS (staining corneale indotto dalle soluzioni) per
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
54
Figura 1
Staining corneale (notare l’impronta causata dalla lente).
(Per gentile concessione Academy for Eyecare Excellence di CIBA
VISION).
mese durante i primi 3 mesi di utilizzo di una particolare
combinazione lente/soluzione. Il valore complessivo di
SICS per tutti i pazienti nelle 16 celle è stato del 4,9%. Nel
73% dei casi il difetto epiteliale corneale era bilaterale. La
maggioranza degli occhi (61%) presentava uno staining
diffuso,insieme ad un 39% che mostrava staining periferico. La probabilità di SICS non era influenzata dal tipo di
Tipi di soluzioni usate nello Studio IER Matrix
Soluzione
Marca
Agente disinfettante
AOSEPT plus
CIBA VISION
Solocare Aqua
CIBA VISION
OPTI-Free Express e
OPTI-Free RepleniSH
Alcon Laboratories
Inc
perossido di idrogeno
poliesametilene
biguanide
Polyquaternium e
miristilammidopropil
dimetilammina -1
Tabella 4
Le soluzioni utilizzate nello Studio IER Matrix (da Carnt et al.,2007)
Studio IER MATRIX: Staining corneale
Staining corneale indotto dal tipo di soluzione per mese
con la combinazione*
Lenti/
soluzione
AOSEPT
H2O2
SOLOCARE OPTI-FREE OPTI.FREE
AQUA
Express
RepleniSH
POLAYQUAD POLAYQUAD
PHMB
e ALDOX
e ALDOX
ACUVUE
ADVANCE
ACUVUE
OASYS
AIR OPTIX
0.0%
0.9%
0.0%
0.0% (2W)
0.9% (2W)
2.5% (2W)
6.2%
7.1% (2W)
0.5%
3.2%
5.9%
6.7%
Pure Vision
0.9%
23.2%
11.3%
20.9%
Tabella 5
Percentuali di pazienti per mese che hanno mostrato staining indotto
dal metodo di manutenzione delle lenti nei primi tre mesi di porto; 2W
( sostituzione dopo due settimane) (da Carnt et al.,2007).
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
lente. Il 23 % dei pazienti presentava staining diffuso in un
occhio e SICS con staining periferico nell’altro occhio.
Il perossido di idrogeno aveva determinato in misura minore l’insorgenza di difetto corneale quando associato con
il silicone idrogel rispetto a qualsiasi altro tipo di soluzione unica (p <0.001 ). Ciò suggeriva che questo fosse il sistema da prediligere al fine di evitare l’insorgenza di danno
corneale. Per quanto riguarda le lenti, Pure Vision aveva
presentato uno staining significativo con tutti i sistemi di
manutenzione fatta eccezione per il perossido di idrogeno,
mentre Acuvue Advance aveva avuto una frequenza più
bassa di staining con le soluzioni uniche (p<0.001).
Sono sorte delle difficoltà nel comparare le informazioni
dello Studio IER Matrix e quelle della griglia di Andrasko e ciò è dovuto al fatto che quest’ultima riporta l’interessamento di un’area media della cornea dopo due ore
di esposizione, mentre i dati IER riportano l’incidenza
osservata in uno studio clinico nel corso di tre mesi. Il
problema di tale approccio sta nel fatto che non ci sono
conferme che il risultato a due ore sia correlabile dopo
un periodo di porto più lungo. È chiaro dunque che per
tali ragioni la griglia di Andrasko non identifica le combinazioni lente-soluzione potenzialmente problematiche
nella realtà clinica.
Successivamente, nel 2009 Carnt et al.8 hanno ancora
studiato l’incidenza degli effetti collaterali dovuti all’uso
giornaliero di varie lenti in silicone idrogel combinate
con diverse soluzioni per la manutenzione.
I dati di questo lavoro sono relativi a gruppi di circa 40
pazienti seguiti per tre mesi durante l’utilizzo delle 16
combinazioni “soluzione-lente in silicone idrogel”, per
un totale di 640 combinazioni paziente-liquido-lente.
Tipi di lenti a contatto
Galyfilcon Lotrafilcon Lotrafilcon Senofilcon Balafilcon
Parametro
B
A
A
A
A
Contenuto
33
38
36
47
24
d’acqua,%
Raggio
8.7
8.6
8.6
8.8
8.6
base, mm
Diametro
della lente,
14
13.8
14.2
14
14
mm
Spessore
centrale a,
0.07
0.08
0.08
0.07
0.09
-3.00 D,
mm
Dk/t,
86
175
138
147
101
-3.00 D
Gruppo
1
1
1
1
3
FDA
Johnson &
CIBA
CIBA
Johnson & Baush &
Produttore
Johnson
VISION
VISION
Johnson
Lomb
Tabella 6
Parametri relativi alle lenti a contatto: D (Diottrie), Dk/t
(trasmissibilità all’ossigeno), FDA (Food and Drug Administration)
(da Carnt et al., 2009).
55
ARTICO L O
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
Le visite venivano eseguite nelle condizioni di base,
dopo 2 settimane, 1 mese e 3 mesi di porto.
Nello studio sono state utilizzate le seguenti lenti: ACUVUE ADVANCE® Galyfilcon A ( Johnson & Johnson), Air
Optix® Nigth & Day® Lotrafilcon A (CIBA VISION), Air
Optix® Aqua Lotrafilcon B (CIBA VISION), Senofilcon A
(Johnson & Johnson) e ACUVUE OASYS® Balafilcon A
(Bausch & Lomb). Le soluzioni usate invece erano: Aquify (CIBA VISION), Clear Care (CIBA VISION), OPTIFREE Express (Alcon) e OPTI-FREE RepleniSH (Alcon).
I dettagli sul tipo di lenti e sul tipo di soluzioni sono
elencati rispettivamente nelle tabelle 6 e 7.
Le complicanze osservate nei pazienti inclusi nei diversi
trials, in seguito all’utilizzo delle varie associazioni “lac
in silicone idrogel-soluzione”, sono state raggruppate clinicamente in sintomatiche e asintomatiche. I tipi di eventi
infiltrativi osservati nei soggetti arruolati nello studio nella metà dei casi erano eventi clinicamente asintomatici.
Nonostante tali eventi vengano considerati ad eziologia
sconosciuta e osservati anche in soggetti non caratterizzati dal porto giornaliero di lac in idrogel, si pensa che
possano essere comunque il risultato di insulti locali ai
quali potrebbe contribuire il tipo di lente o il particolare
tipo di combinazione “lente-soluzione” utilizzata.
Sono stati così evidenziati eventi infiltrativi corneali sintomatici (cheratite microbica MK, occhio rosso indotto da
lac CLARE, cheratite infiltrativa IK e ulcere periferiche
associate all’uso di lac CLPU), eventi infiltrativi asintomatici ( cheratiti infiltrative asintomatiche AIK e infiltrati
asintomatici) e complicanze di tipo meccanico (lesione
epiteliale arcuate SEAL, congiuntivite papillare indotta
dall’uso di lac CLPC).
Nei partecipanti sono stati osservati 70 CIE (eventi infiltrativi corneali) allo stadio iniziale, 18 SEAL, 1 erosione
corneale, 10 CLPC e 107 staining corneali.
I dati relativi all’ incidenza degli eventi infiltrativi, delle
complicanze meccaniche e degli staining corneali sono
riassunti rispettivamente nelle tabelle 8-9-10.
L’incidenza delle lesioni epiteliali arcuate superiori era influenzata in maniera significativa dal tipo di lente piuttosto che dal tipo di soluzione; Balafilcon A usata con
AQuify e Clear Care ha determinato una più alta incidenza di SEAL.
L’incidenza degli eventi infiltrativi, considerati come tali
sia quelli sintomatici che asintomatici, e della congiuntivite
papillare indotta da lac variavano in maniera significativa in relazione al tipo di soluzione usata: l’evidenza di
CIE con OPTI -FREE RepleniSH era più alta che con Clear Care e l’incidenza della CLPC era maggiore del 95%
dell’intervallo di confidenza (CI).
La comparsa di CIE sintomatici, invece, variava in maniera indipendente dal tipo di combinazione lente-soluzione usata. L’incidenza di CIE sintomatici con OPTI-FREE
RepleniSH era più alta che con Clear Care e OPTI-FREE
Express, con Lotrafilcon A era più alta piuttosto che con
Lotrafilcon B. Infine, l’incidenza degli staining corneali osservata variava in relazione al tipo di combinazione soluzione-lente in silicone idrogel. In particolare, l’uso del
perossido di idrogeno (Clear Care – CIBA VISION) ha
SOLUZIONI,N.di CIE totali e sintomatiche
(Incidenza per 100 partecipanti-mese)
Cleare Care, Aquify, OPTI-FREE Express, OPTI-FREE, RepleniSH
SOLUZIONI,N.delle complicanze meccaniche
(Incidenza per 100 partecipanti-mese)
Cleare Care, Aquify, OPTI-FREE Express, OPTI-FREE RepleniSH
Componenti delle soluzioni
Soluzione
Principio Attivo
Agente disinfettante
Poliesamide (PoliesaAquify
metilene biguanide)
CIBA VISON
0.001%
Perossido di idrogeno
Clare Care
CIBA VISION
3%
POLYQUAD (Poliquaternium -1) 0.001% e
OPTI-FREE Express ALDOX (miristilamAlcon
midopropil dimetilammina) 0.0005%
POLYQUAD 0.01% e
OPTI-FREE RepleniSH
Alcon
ALDOX 0.0005%
Tabella 7
Componenti delle soluzioni indagate nello studio (Carnt et al.,2009).
Lente a
contatto
Galyfilcon
A
Senofilcon
A
Balafilcon
A
Lotrafilcon B
Lotrafilcon A
CIE
tot.
CIE s.
CIE
tot.
CIE s.
CIE
tot.
CIE s.
CIE
tot.
CIE s.
1
0
4
3
1
1
4
3
0
0
8
2
2
1
6
1
0
0
3
1
4
1
9
7
2
0
1
1
2
0
3
2
1
1
7
3
1
1
11
11
Tabella 8
Incidenza degli eventi infiltrativi corneali (CIE) totali (asintomatici
e sintomatici) e CIE sintomatici (s.= sintomatici ; tot.= totali) (da
Carnt et al.,2009).
Lente a
CLPC SEAL CLPC SEAL CLPC SEAL CLPC. SEAL
contatto
Galyfilcon
0
1
0
0
2
0
1
0
A
Senofilcon
1
0
0
0
0
0
0
0
A
Balafilcon
2
2
0
8
0
1
1
0
A
Lotrafil1
0
0
0
0
0
1
1
con B
Lotrafil0
0
0
0
1
2
0
3
con A
Tabella 9
Incidenza delle complicanze meccaniche associate all’uso dei diversi
tipi di combinazioni lente-soluzione (CLPC: congiuntivite papillare,
SEAL: lesione epiteliale arcuata superiore) (da Carnt et al.,2009)
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
56
SOLUZIONI,N. di staining corneali (Incidenza per 100 partecipanti-mese)
Cleare Care, Aquify, OPTI-FREE Express, OPTI-FREE RepleniSH
Lente a
contatto
Galyfilcon A
0
1
0
0
Senofilcon A
1
3
7
8
Balafilcon A
1
24
11
15
Lotrafilcon B
1
3
6
8
Lotrafilcon A
2
1
8
7
Tabella 10
Incidenza degli staining corneali associati all’uso dei diversi tipi di
combinazioni lente-soluzione ) (da Carnt et al.,2009)
mostrato la più bassa incidenza di CIE e difetti dell’epitelio corneale. Questo studio mostra così chiaramente come
il tipo di lente e la soluzione, nonchè la loro particolare
combinazione, influenzano la comparsa e l’incidenza degli effetti avversi tra i soggetti che usano lac giornaliere
in silicone idrogel.Gli stessi risultati, inoltre, suggeriscono che il materiale, il disegno della lente e i componenti
delle soluzioni per la manutenzione sono tutti aspetti che
influiscono sul comfort dei pazienti e sul porto delle lac.
Con l’obbiettivo di eliminare i suddetti effetti avversi collegati al porto giornaliero di lenti a contatto in silicone
idrogel sarebbe di fondamentale importanza comprendere il tipo di relazione esistente tra le diverse combinazioni lente-soluzione e studiare i prodotti per la manutenzione delle lac al fine di valutarne la biocompatibilità
e favorirne la compliance.
La ricerca di nuovi materiali biocompatibili che possono
anche essere utilizzati come lac terapeutiche che rilasciano farmaci nell’occhio è quindi di grande attualità.
L’efficacia di tale mezzo di somministrazione è legata
alla scelta del materiale che costituisce la lente e alla sua
microstruttura studiate entrambe in relazione alle caratteristiche chimico-fisiche del farmaco.
I colliri somministrati sotto forma di gocce possono invece rivelarsi inadatti per una efficace somministrazione di
farmaci10. La biodisponibilità del principio attivo può essere molto limitata e possono esservi effetti collaterali legati
all’assorbimento sistemico del farmaco in questione. Le lac
come serbatoio di farmaco offrono il grande vantaggio di
permettere un aumento del tempo di residenza del farmaco nell’occhio. Questo grazie alla presenza della barriera
geometrica data dalla lente stessa al farmaco quando quest’
ultimo diffonde dalla matrice del gel nel film lacrimale.
La permanenza del farmaco nell’occhio è maggiore di 30
minuti in presenza di una lac 10-11 se confrontata con il
tempo di permanenza di 15 minuti quando si applicano
gocce di collirio 12-15. Inoltre, al fine di ottenere un rilascio
controllato del farmaco da parte delle lente, sarebbe ne-
cessario studiare la struttura del materiale di cui è composta la lac in termini di percorsi di diffusione: la struttura, essenzialmente costituita da nanopori più o meno
connessi, regola la velocità di rilascio della sostanza inizialmente caricata.
In base alla natura chimica del polimero e a i diversi rapporti con i vari elementi della struttura del principio attivo del farmaco, verrà modificata la caratteristica propria
di quest’ultimo di essere assorbito con diversa efficacia.
Negli ultimi anni diversi studi sono apparsi in letteratura che riportano interessanti risultati in questo campo
e recentemente Kapoor et al (2009) 16 si sono concentrati
sulla diffusione delle lenti a contatto in p-HEMA (polidrossimetil-metacrilato), ottenuto dalla polimerizzazione di 2 monomeri, che permettono il rilascio controllato
di Ciclosporina A (CyA).
Tale sostanza è un farmaco immunosoppressore che viene utilizzato per il trattamento di una varietà di malattie
e disturbi oculari. La CyA è comunemente fornita tramite
collirio, che è altamente inefficace a causa di una bassa
biodisponibilità (inferiore al 5%). La biodisponibilità dei
farmaci oftalmici può essere notevolmente migliorata di
circa il 50%, attraverso l’uso di lenti a contatto medicali17.
Questo lavoro si propone di indagare questa disponibilità utilizzando un tensioattivo quale il Brij 78 incorporato
nell’ idrogel al fine di creare micelle cariche di principio
attivo e ritardare i tassi di rilascio.
Il materiale è stato studiato mediante Microscopio a
Scansione Elettronica (SEM) con cryo-stage (Cryo-SEM)
per ottenere un’ evidenza diretta della presenza di aggregati di tensioattivo nel gel della lente al fine di modificarlo rendendolo più o meno affine al particolare polimero
che costituisce la lente. Le immagini risultanti mostravano una distribuzione di nanopori, più o meno connessi,
nei quali erano presenti aggregati di tensioattivo immersi
nella matrice del gel che molto probabilmente risultano essere veicoli con elevata affinità per le molecole idrofobiche
del farmaco. I risultati del lavoro hanno mostrato che i
tempi di rilascio della CyA possono essere significativamente aumentati grazie all’incorporazione all’interno di
micelle di tensioattivo disperso nel gel di poli-drossimetilmetacrilato. Tra i tipi di tensioattivo indagati nel lavoro
il Brij 78 sembra essere il più promettente per il rilascio
controllato di tale farmaco da lenti a contatto p-HEMA.
Tale conclusione non può essere al contrario raggiunta
per il rilascio di altri due tipi di farmaci idrofobici oftalmici, quali il desametasone (DMS) e desametasone acetato (DMSA), per l’insufficente e non adeguata partizione
all’interno degli aggregati di tensioattivo.
Diversi altri approcci sono stati testati per accrescere le
capacità di carico del farmaco delle lenti a contatto medicate al fine di ottenerne una migliore efficienza nel controllo del rilascio sulla superficie corneale.
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
57
ARTICO L O
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
Esempi ne sono la stabilizzazione del farmaco attraverso
la creazione di legami stabili covalenti18, la dispersione
in un gel acrilico o l’inclusione in nanopori della matrice
idrogel19-22 e tramite la formazione di recettori ad alta affinità attraverso imprinting molecolare23-26.
Un alternativa meno complessa e probabilmente più versatile potrebbe essere l’incorporazione della ciclodestrina (CD) alla struttura dell’idrogel delle lenti a contatto
morbide medicali. Le ciclodestrine, oligosaccaridi ciclici
naturali, possono formare complessi di inclusione con diversi farmaci attraverso legami reversibili non covalenti.
Generalmente, più alta è la costante di affinità del complesso CD-farmaco più bassa è la cinetica della reazione
di dissociazione27.
Quando però il complesso CD-farmaco viene diluito in
soluzione fisiologica la sua dissociazione è istantanea e
ciò non permetterebbe di ottenere un rilascio controllato del farmaco, come nel caso di soluzioni oftalmiche
contenenti ciclodestrine28-29. Al contrario, se la CD viene
inclusa nelle rete del polimero diminuisce la diluizione
e la formazione di un microambiente determinato dalla
struttura cava della ciclodestrina favorirebbe il rilascio
del farmaco con un tasso inversamente proporzionale
alla costante di affinità del complesso stesso 30-31. Polimeri
acrilici sono stati usati con successo come comonomeri al
fine di ottenere la formazione di una rete con un’ aumentata capacità di cattura del farmaco e al fine di sostenerne
il rilascio32-33. Tuttavia, il numero dei gruppi polimerizzabili in ogni CD e conseguentemente il grado di legame alla rete del polimero non è facile da regolare: ad alte
proporzioni di CD, infatti, la rete diventa eccessivamente
rigida per essere utilizzata come lente a contatto morbida.
Riguardo a tale questione Santos et al.(2009) descrivono
nel loro studio del 2008 lo sviluppo di un idrogel acrilico
con alte proporzioni di ß-ciclodestrina tramite una nuova
procedura al fine di conservarne le proprietà meccaniche,
la biocompatibilità e di rafforzare la capacità di carico del
farmaco, nonché migliorarne il controllo della velocità di
rilascio. Il metodo di preparazione consiste nella sintesi iniziale dell’idrogel al quale successivamente vengono fissate
Figura 2
Schema del polimero idrogel P-HEMA
copolimerizzato con GMA con i pendenti
di ciclodestrina ß-CDs (da Santos et al.,
2009)
Diclofenac
caricato
(mg/g)
GMA proportion
Figura 3
Diclofenac caricato sull’idrogel dopo immersione del farmaco
(colonna bianca) e quota di diclofenac che rimane sull’idrogel
dopo conservazione per 30 giorni in soluzione per lenti a contatto
(colonna nera) (da Santos et al.,2009)
molecole di CD attraverso i gruppi idrossilici. In tal modo
la CD non interferisce con la formazione della rete del polimero e perciò potrebbe non alterare significativamente le
sue proprietà strutturali. Tale meccanismo prevede la previa preparazione di poly-idrogel mediante la copolimerizzazione del glicil-metacrilato (GMA), mediante reazione
con i gruppi glicidici, a diverse proporzioni con monomeri
comunemente usati come componenti degli idrogel.
Tutto questo allo scopo di fornire alla rete del polimero
punti di legame per il successivo step di carico della betaciclodestrina. Quest’ ultima, infatti, in tal modo non entra a
far parte delle catene strutturali dell’idrogel, ma viene incorporata nella rete mediante legame con 2-3 gruppi etere
attraverso i gruppi idrossile (Fig. 2).
La beta-ciclodestrina “pende” dalla rete del polimero e non
ne modifica il coefficiente di trasmittanza alla luce (90% a
600 nm), la temperatura di transizione vetrosa, la viscoelasticità e la permeabilità all’ossigeno delle lenti a contatto
morbide ma, ne determina la diminuizione del coefficiente
di attrito del 50%, il miglioramento del carico del farmaco e
una sua maggiore affinità con la lente stessa.
Nello studio gli idrogel, ottenuti con la suddetta preparazione, sono stati immersi in una soluzione di diclofenac
sodico e successivamente misurata la concentrazione di
farmaco caricato. La concentrazione di diclofenac incluso
nel polimero era maggiore negli idrogel preparati attraverso la copolimerizzazione di GMA, caratterizzati dalla conseguente presenza di ß-CD pendente dalla struttura della
rete, piuttosto che negli idrogel preparati senza o con minor contenuto in GMA (Fig 3). Questo dimostra che il
farmaco può stabilire interazioni idrofobiche con la rete del
polimero, in quanto quest’ultimo ospitato nella struttura
cavitaria della ß-CD forma con essa un complesso stabile
di inclusione attraverso i suoi anelli aromatici. Il rilascio di
diclofenac dall’idrogel è stato valutato in un film lacrimale
artificiale ed è stato dimostrato come gli idrogel senza ß-CD
rilasciavano rapidamente la completa dose del farmaco per
diffusione nell’arco di 24 h. Al contrario gli idrogel con
ß-CD (in particolar modo quelli con più alte proporzioni)
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
58
erano in grado si sostenere il rilascio del farmaco per diversi giorni, fino a due settimane. L’alta affinità del farmaco
per l’idrogel ferma il rilascio del farmaco nel momento in
cui viene raggiunta una certa concentrazione dello stesso
nel microambiente formato. Questo ha dimostrato l’ottenimento dell’equilibrio tra rilascio e riassorbimento del farmaco attraverso le lenti a contatto in idrogel.
Conclusioni
Le conclusioni, dunque, evidenziano come le molecole di
ß-CD “pendenti” dalla struttura della rete del polimero
attraverso legami con i gruppi glicidici del GMA migliorino le capacità di carico degli idrogel e prevengano la
dispersione del farmaco sulla cornea durante la conservazione in soluzioni per lenti a contatto morbide.
Tali caratteristiche investono gli idrogel con beta-ciclodestrina di enormi potenzialità per lo sviluppo in futuro di
impianti medicali e dispositivi biomedicali.
Abstract
The authors reviewed some works of literature on the close evidence between the contact lens, lens solution used, as well as
their combination and the presence of ocular adverse events silicone hydrohel contact lens and daily wear related. Daily wear is
today the major mode of use for conventional hydrogel material.
Among the various associations' lens-solution” investigated in
several studies, hydrogen peroxide with any lens type showed
the lowest incidence of corneal infiltrative events, complications directly related to the discomfort and safety in the use of
lac always more consumers.
How to eliminate the complications associated with the use of
lac is of paramount importance to know the type of relationship among the different "lens-solution", so 'it is the search for
new biocompatible materials and the understanding of reaction mechanisms between drug and structure of the lens in the
production of new contact lenses medical.
Key words
Silicone hydrogel contact lens, daily wear care system used,
medicated contact lenses.
Bibliografia
1. Morgan P.B, Woods C.A, Tranoudis I.G. et al.: International
contact lens prescribling in 2008.Contact Lens Spectrum.,
2009;24:28-32
2. Jones L., Macdougail N.,Sorbara G.L.: Asymptomatic corneal
staining associated with the use of balafilcon silicone-hydrogel
contact lenses disinfected with a ply-aminopropyl biguanidepreserved care regimen. Optom. Vis. Sci., 2002;79:753-761
3. Andrasko G.J., Kelly M.S., Ryan A., Garofano R.J., Lemp J.M.:
Oculare Response Observed with Silicone Hydrogel Lenses and
Multi-Purpose Solution Combinations.Optometry,2006;79: 268
4. Andrasko G., Ryen K.: A series of evaluations of MPS and silicone hydrogel lens combinations. Review of Cornea and Contact Lenses, 2007:36-42
5. Andrasko G., Ryen K.: Corneal staining and comfort observed
with traditional and silicone hydrogel lenses and multipurpose
solution combinations. Optometry, 2008;79:444-454
6. Carnt N., Jalbert I., Stretton S., Naduvilath T., Papas E.: Solution toxicity in soft contact lens daily wear is associated with
corneal inflammation. Optom. Vis. Sci., 2007;84:309-315
7. Carnt N., Willcox M., Evans V. et al.:Corneal staining: The IER
matrix study. Contact Lens Spectrum, 2007:38-43
8. Carnt N.A., Evans V.E., Naduvilath T.J., Willcox M.D., Papas
E.B., Frick K.D., Holden B.A.: Contact lens-related adverse
events and the silicone hydrogel lenses and daily wear care
system used. Arch. Ophtalmol.,2009;127:1616-1623
9. Bourlais C., Acar L., Zia H., Sado P.A., Needham T., Leverge
R.:Ophthalmic drug delivery systems – recent advances. Prog.
Retin. Eye Res., 1998;17:33–58
10. McNamara N.A., Polse K.A., Brand R.J., Graham A.D., Chan
J.S., McKenney C.D.:Tear mixing under a soft contact lens: effects of lens diameter. Am. J. Ophthalmol., 1999;127:659–665
11. Creech J. L., Chauhan A., Radke C. J.: Dispersive Mixing in the
Posterior Tear Film Under a Soft Contact Lens. Ind. Eng. Chem.
Res., 2001;40: 3015–3026
12. Snibson G.R., Greaves J.L., Soper N.D., Prydal J.I., Wilson C.G.,
Bron A.J.: Precorneal residence times of sodium hyaluronate
solutions studied by quantitative gamma scintigraphy. Eye,
1990;4:594-602
13. Wilson C., Zhu Y. P., Frier M. et al.: Ocular contact time of a
carbomer gel (GelTears) in humans. Br. J. Ophthalmol., 1998;
82: 1131–1134
14. Ishibashi T., Yokoi N., Bron A.J. et al.: Retention of reversibly
thermo-gelling timolol on the human ocular surface studied by
video meniscometry. Curr. Eye Res., 2003;27:117-22
15. Yokoi N.,Komuro A.: Non-invasive methods of assessing the
tear film. Exp. Eye Res.,2004;78:399–407
16. Kapoor Y., Thomasabba J. C., Tan G.: Surfactant-laden soft
contact lenses for extended delivery of ophthalmic drugs. Surfactant-laden soft contact lenses for extended delivery of ophthalmic drugs. Biomaterials, 2009;30:867-878
17. Li C.C., Chauhan A.: Modeling Ophthalmic Drug Delivery by
Soaked Contact Lenses. Ind. Eng. Chem. Res., 2006;45:3718–
3734
18. Vairon J.P.,Yean L.,Meslard J.C.,Subira F.,Bunel C.: Immobilisation reversible sur polymers et liberation controlée. Application
aux lentilles cornéennes reservoirs de medicamento. L’actualité
Chimique, 1992, Septembre-Octobre: 330-335
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
59
ARTICO L O
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
La ricerca di nuovi materiali biocompatibili per la manutenzione quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
19. Gulsen D., Chauhan A.: Ophthalmic drug delivery through
contact lenses. Invest. Ophthalmol. Vis. Sci., 2004;45:2342-2347
20. Gulsen D., Chauhan A.: Dispersion of microemulsion drops in
HEMA hydrogel: a potential ophthalmic drug delivery vehicle.
Int. J. Pharm.,2005;292:95-117
21. Gulsen D.,Chauhan A.: Effect of water content on transparency, swelling, lidocaine diffusion in p-HEMA gels.Membr.
Sci.,2006;269:35-48
22. Danion A., Doillon C.J., Giasson C.J. et al.: Biocompatibility
and light transmission of liposomal lenses. Optom. Vis. Sci.,
2007;84:954-961
23. Alvarez-Lorenzo C., Hiratani H., Gómez-Amoza J.L. et al.:
Soft contact lenses capable of sustained delivery of timolol. J.
Pharm.Sci., 2002;91:2182-2192
24. Hiratani H., Mizutani Y., Alvarez-Lorenzo C.: Controlling drug
release from imprinted hydrogels by modifying the characteristics of the imprinted cavities. Macromol. Biosci., 2005;5:728-733
25. Alvarez-Lorenzo C., Yañez F., Barreiro-Iglesias R., Concheiro
A.: Imprinted soft contact lenses as norfloxacin delivery systems. J. Control. Release,2006;113:236-244
26. Venkatesh S., Sizemore S.P., Byrne M.E.: Biomimetic hydrogels
for enhanced loading and extended release of ocular therapeutics. Biomaterials, 2007;:717-724
27. Loftsson T., Duchêne D.: Cyclodextrins and their pharmaceutical applications. Int. J. Pharm., 2007;329:1-11
28. Uekama K.,Hirayana F., Irie T: Application of cyclodextrins in pharmaceutical preparations.Drug Target Deliv. Rev.,1994;3:411-456
29. Stella V.J., Rao V.M., Zannou E.A., Zia V. V.: Mechanisms of
drug release from cyclodextrin complexes. Adv. Drug. Deliv.
Rev.,1999;36:3-16
30. Rodriguez-Tenreiro C., Alvarez-Lorenzo C., Rodriguez-Perez
A. et al.: New cyclodextrin hydrogels cross-linked with diglycidylethers with a high drug loading and controlled release ability. Pharm. Res., 2006;23:121-30
31. Rodriguez-Tenreiro C., Alvarez-Lorenzo C., Rodriguez-Perez
A., Concheiro A., Torres-Labandeira J.J.: Estradiol sustained release from high affinity cyclodextrin hydrogels. Eur. J. Pharm.
Biopharm., 2007;66:55-62
32. Liu Y.Y., Fan X.D.: Synthesis, properties and controlled release
behaviors of hydrogel networks using cyclodextrin as pendant
groups. Biomaterials,2005;26:6367-6374
33. dos Santos J.F., Couceiro R., Concheiro A., Torres-Labandeira
J.J., Alvarez-Lorenzo C.: Poly(hydroxyethyl methacrylate-comethacrylated-beta-cyclodextrin) hydrogels: synthesis, cytocompatibility, mechanical properties and drug loading/release
properties. Acta Biomater., 2008;4:745-755
N. Pescosolido, C. Nardella / Lac Lenti a contatto 2010; 12 (2): 53-60
60
R U BR ICA
PILLOLE DI LAC
E DINTORNI
a cura di
Luigi Lupelli
È stato pubblicato...
Qualità della vita orientata
sull’aspetto visivo in portatori
di lenti a contatto in età
pediatrica
Rah MJ, Walline JJ, Jones-Jordan LA, Sinnott LT,
Jackson JM, Manny RE, Coffey B, Lyons S
Optometry & Vision Science 2010; 87: 560–566
Numerosi studi hanno riportato che
l’uso delle lenti a contatto, sia RGP
che morbide o ortocheratologiche,
può essere affrontato con successo
dai bambini che riescono a gestirle
correttamente e con successo. In questa ricerca, che ha avuto una durata
di tre anni, si è cercato di valutare se
l’uso di lenti a contatto nell’età che va
dagli 8 agli 11 anni può contribuire a
migliorare la qualità della vita.
Il questionario usato è stato The Pediatric Refractive Error Profile, che è uno
dei due questionari pediatrici orientati sull’aspetto visivo. È stato somministrato a 484 bambini miopi con assegnazione random a 247 di essi. Gli
altri hanno utilizzato occhiali.
Il risultati ottenuti, nello spazio di
tre anni, hanno mostrato che l’uso di
lenti a contatto, in confronto all’uso
degli occhiali, migliora la qualità
della vita. Le differenze principali
sono state ottenute in particolare per
i campi dell’Aspetto, della Soddisfazione e delle Attività svolte. In conclusione appare evidente che l’uso di
lenti a contatto va preso in seria considerazione anche nei miopi che in
età preadolescenziale possono avere
una certa avversione estetica per gli
occhiali e/o che partecipano ad attività ricreative.
Variazione diurna della funzione Bagnabilità delle lenti a contatto in
visiva e segni e sintomi
vitro: effetto dei surfattanti
Lin MC, Svitova TF
dell’occhio secco
Optometry & Vision Science 2010; 87: 440–447
Walker PM, Lane KJ, Ousler III GW, Abelson MB
Cornea 2010; 29: 607–612
I soggetti con occhio secco spesso
lamentano di avere disturbi visivi
con peggioramento dei sintomi al
mattino. Per verificare tale ipotesi
gli autori eseguono, prima al mattino e poi alla sera, una serie di esami
comprendenti, tra l’altro, la valutazione dell’acuità visiva con occhiali,
l’intervallo tra un ammiccamento e
l’altro come segno del decadimento
della funzione visiva, la velocità di
lettura, l’esame biomicroscopico e il
BUT lacrimale. Inoltre ai 21 soggetti
esaminati veniva somministrato una
versione modificata dell’Ocular Surface Disease Index.
I risultati mostrano che il deterioramento delle funzioni visive in relazione alla secchezza oculare (visione ridotta, annebbiata durante la lettura, la
visione della Tv, la guida) è maggiore
durante la sera. Anche i segni di iperemia bulbare e di staining dell’epitelio corneale sono più accentuati nelle
ore serali in confronto a quelli presenti al mattino. Il fatto che i sintomi correlati alla secchezza oculare vengano
riportati principalmente al mattino va
probabilmente posto in relazione con
la sensibilità corneale che si riduce
durante la giornata. Tale lavoro indica che il trattamento dell’occhio secco
non dovrebbe essere soltanto mirato a
ridurre i sintomi soggettivi di discomfort (più accentuati al mattino) e quelli oggettivi (più accentuati la sera, ma
anche teso a migliorare la performance visiva e in particolare a prevenire il
decadimento di tale funzione durante
le ore diurne.
La capacità del film lacrimale di distribuirsi uniformemente sulla superficie oculare dipende, tra l’altro,
dalla bagnabilità della cornea e, nel
caso di applicazione di lente a contatto, dalla bagnabilità della stessa.
Per migliorare la bagnabilità della superficie della lente a contatto
sono stati utilizzati vari approcci.
Con le lenti in idrogel si è aggiunto uno o più agenti umidificanti nel
blister e nella soluzione conservante
per variare la tensione superficiale.
Tali agenti adsorbiti sulla superficie
della lente sono ritenuti migliorare
la bagnabilità. I surfattanti possono
anche penetrare nella matrice del
materiale della lente per poi, presumibilmente, essere rilasciati durante
l’uso della lente.
Di dieci lenti morbide (quattro in
idrogel e 6 in silicone idrogel) gli
Autori hanno misurato sia la tensione superficiale, nell’interfaccia ariaacqua, che l’angolo di contatto sia
appena dopo aver rimosso la lente
a contatto dal blister, sia dopo aver
immerso la lente in una soluzione
senza surfattante. È stata anche misurata la tensione superficiale della
soluzione in cui erano conservate le
lenti nel blister.
I risultati hanno mostrato che la
tensione superficiale delle soluzioni presenti nei blister è più bassa di
quella dell’acqua purificata. Se le
lenti vengono prima immerse in una
soluzione che elimina il surfattante
l’angolo di contatto recedente aumenta mentre il valore del l’angolo
contatto recedente rimane invariato.
61
Pillole di lac e dintorni
Per le lenti in idrogel la bagnabilità di superficie dipende largamente
dalla presenza del surfattante presente nel blister mentre è interessante notare che per la maggior parte
delle lenti in silicone idrogel il surfattante non contribuisce a migliorare la bagnabilità in vitro. Ciò può far
ritenere che il risciacquo con soluzione salina prima dell’applicazione
può non alterare la bagnabilità e che
quindi può essere addirittura consigliato in caso si sospetti una ipersensibilità del portatore al surfattante. In conclusione si può affermare
che i surfattanti che si trovano nelle
soluzioni di conservazione poste nel
blister alterano l’idrofilia di superficie, anche se in modo diverso, per le
varie lenti a contatto.
Disfunzione lacrimale
post-LASIK
Disestesia
Nettune, G R.; Pflugfelder, S C.:
The Ocular Surface, 2010; 8: 135-145
Tra le complicanze post chirurgiche indotte dall’intervento di cheratomileusi in situ (LASIK) quella
più frequente è una disfunzione
lacrimale che appare presente nella
maggior parte dei pazienti operati. I
sintomi riportati da tali soggetti, che
contribuiscono a causare il discomfort oculare, non sono però sempre
gli stessi sia dal punto di vista qualitativo che quantitativo. Tale sindrome racchiude una componente
patologica neurotrofica, una instabilità lacrimale e una riduzione della
componente acquosa delle lacrime
accompagnata da un dolore di matrice neuropatica. I sintomi attribuibili alla secchezza oculare possono
essere, in molti casi, risolti con una
gestione appropriata che comprende un’ottimizzazione della superficie oculare sia prima che dopo l’intervento di chirurgia refrattiva. Nel
caso che i sintomi persistano anche
dopo nove mesi dall’intervento è
necessario adottare delle strategie
62
d’intervento molto più aggressive
in confronto a quelle convenzionalmente poste in atto.
L’atteggiamento verso le lenti a
contatto. Uno studio comparativo tra adolescenti e genitori
Zeri F., Durban JJ, Hidalgo F, Gispets J
Contact lens & Anterior Eye 2010; 33.119-123
È stato condotto un sondaggio, sia
in Italia che nella Penisola Iberica,
per comprendere quali siano gli
atteggiamenti degli adolescenti e
dei loro genitori che possono creare delle resistenze verso l’uso delle
lenti a contatto. In totale sono stati
raccolti 344 questionari compilati
dai genitori e 370 compilati dai figli.
In generale i genitori ritengono che
le lenti a contatto siano meno adatte
per gli adolescenti in confronto ad
una popolazione adulta. Comunque il giudizio assume una connotazione meno negativa se i genitori
sono anch’essi portatori di lenti a
contatto. Le preoccupazioni che più
frequentemente vengono espresse
dai genitori, in particolare le madri,
sono riferite a un maggior rischio
di danno oculare dovuto a una presunta minore attenzione all’igiene e
a una minore capacità nel rispettare
le indicazioni del contattologo, in
particolare per l’aspetto delle procedure di manutenzione. Il 78% degli
adolescenti che non usa le lenti a
contatto sarebbe favorevole a farne
uso specialmente per l’attività sportiva ma anche per ragioni estetiche
e per avere una maggiore libertà di
movimento.
Alessandro Fossetti è il nuovo
Direttore degli Studi dell’IRSOO
Attivo collaboratore della nostra rivista e membro del Comitato Scientifico, il dott. Alessandro Fossetti,
professore a contratto presso l’Università degli Studi di Padova, è stato nominato direttore dell’Istituto
Regionale degli Studi Ottici e Op-
tometrici di Vinci. La redazione si
complimenta con il nuovo direttore
e gli augura un proficuo lavoro.
RUBRICA
TIPS
& TRICKS
a cura di
Laura Boccardo
Quando tutto il resto fallisce,
seguite le istruzioni!
Ah, la primavera! Quest’anno il mio
programma di cura del giardino si è
focalizzato sulla lotta alle erbacce del
prato. Ho sparso un'intera confezione di diserbante, ma non ho ottenuto
alcun risultato. Perplesso, mi sono
deciso a leggere le istruzioni e ho
scoperto di aver saltato un passo importante: il prato doveva essere bagnato prima di spargere il prodotto.
Ho buttato via 30 dollari solo per non
aver seguito le istruzioni! Ho provato
di nuovo e ora le erbe infestanti sono
(per lo più) sparite. Perché vi racconto questo? Perché spesso le lenti che
applichiamo non funzionano, proprio
per il motivo che non vengono applicate come indicato dalle istruzioni. Le
aziende spendono un sacco di tempo
e denaro per ottimizzare le procedure
di impiego dei loro prodotti. Questa
dovrebbe bastare, come ragione per
seguire le istruzioni. Penso che sia più
forte di noi. Abbiamo applicato un
sacco di lenti multifocali: quanto mai
potrà essere diversa questa nuova
lente dalle altre? Se è un po' che non
tirate fuori un foglio illustrativo, iniziate a leggere. Rimarrete sorpresi e le
lenti che non funzionavano diventeranno vincenti.
J.M. Jacks, When All Else Fails, Follow
the Direction, CLSpectrum, giugno 2010
Una soluzione è meglio di due
Parlando di manutenzione durante
alcuni corsi, dei colleghi mi hanno
detto che preferiscono prescrivere
ai pazienti diversi tipi di soluzioni
per la manutenzione, alternandone
un mese una e un mese l’altra. Michael Mayers (One Lens Care Solution
is Enough, CLSpectrum Aprile 2010)
riferisce di aver sentito prescrivere
un'altra originale combinazione: una
soluzione unica per cinque notti e
un perossido due volte la settimana.
Quale messaggio arriva ai pazienti?
Prima possibilità: se una sola soluzione non basta, significa che non è
efficace, quindi si potrebbe provare
a mischiarne due insieme! Seconda
possibilità: se posso alternare questi prodotti, significa che sono equivalenti, quindi tutti i prodotti sono
uguali, quindi tanto vale che compri
il primo che mi capita o quello che
costa meno. I pazienti hanno già abbastanza confusione in testa riguardo
alla manutenzione, l'uso e la sostituzione delle lenti, senza bisogno di raccomandazioni strane da parte nostra.
Che occhi grandi che hai!
L’ultima trovata nel campo delle lenti
a contatto cosmetiche è un tipo di lenti
che ingrandiscono il diametro dell'iride, creando l'effetto degli "occhioni"
stile manga giapponese. Questo prodotto è stato originariamente inventato in Corea del Sud e, fino al 2009,
è rimasto appannaggio dei mercati
asiatici (Corea, Giappone, Pakistan e
Hong Kong), pressoché sconosciuto in
occidente, finché Lady Gaga non le ha
utilizzate nel video della canzone "Bad
Romance", dove appare con enormi
occhi da bambola. Si è così scatenata
la frenesia di molte adolescenti che
ammirano e copiano il look di questa
cantante. Attualmente queste lenti non
sono in commercio in nessun paese
occidentale, sono prive di marchio CE
e, quindi, possono solo essere comprate on-line. Le circle contact lenses sono
vendute come lenti a ricambio annuale. L’acquisto viene fatto sistematicamente senza alcun tipo di controllo
specialistico: le ragazze imparano ad
utilizzare queste lenti seguendo i tutorial su You Tube, che includono colliri
vasocostrittori per sbiancare l’occhio,
ciglia finte e dosi massicce di trucco
bianco sulle rime palpebrali. L’uso
sconsiderato delle lenti cosmetiche
da parte dei teenager, senza una prescrizione, senza controlli e senza una
seria istruzione alla manipolazione e
alla manutenzione delle lenti, li espone a seri rischi per la salute oculare. Se
quindi vedete una ragazza che sembra
Sailor Moon, partite dal presupposto
che non abbia ricevuto alcuna informazione sul corretto uso delle sue circle lenses. Non perdete mai l’occasione
per spiegare le norme basilari di igiene
e manutenzione delle lenti a contatto.
What Big Eyes You Have, Dear, but Are
Those Contacts Risky?”, The New York
Times, July 3, 2010.
Valutare le lenti morbide toriche
Quando si applicano delle lenti morbide toriche, non basta controllare la
posizione di riposo, ma è utile controllare anche la velocità di recupero
dopo una rotazione. Per valutare la
facilità di recupero rotazionale, la
lente può essere ruotata manualmente di 45° tempiali (nello studio hanno
usato un asciughino chirurgico). Una
lente mostra buone capacità di recupero alla rotazione se torna nella sua
posizione di riposo entro un minuto.
G. Cairns, P. China, T. Gree, Toric Lens
Performance: Insights Into Orientation
Stability, CLSpectrum, maggio 2010.
Avete un piccolo trucco o qualsiasi suggerimento che possa risolvere i problemi
più comuni che si incontrano nella pratica
contattologica di tutti i giorni?
Avete piacere di condividerlo con i colleghi?
Inviate i vostri Tips&Tricks alla redazione
di LAC.
63
R U BR ICA
IN LIBRERIA
DICTIONARY OF OPTOMETRY AND VISUAL SCIENCE
a cura di
Laura Boccardo
Michel Millodot
7a edizione
Butterworth-Heinemann, 2009
409 pagine, 89 tabelle,
241 illustrazioni
Lingua inglese
www.elsevier.com
Con quasi venticinque anni e sette
edizioni di storia, si può dire che
il “Dictionary of Optometry and
Visual Science” di Michel Millodot sia diventato un classico della
letteratura optometrica. Cresciuto
e rinnovato, edizione dopo edizione, l’attuale versione di questo dizionario contiene oltre 5.400
termini inerenti all’optometria, la
contattologia, l’ottica, l’ortottica,
l’anatomia, la fisiologia, la patologia, la farmacologia, le tecniche
di esame, la chirurgia refrattiva e
64
la percezione visiva. Per la prima
volta sono stati inseriti termini riguardanti la genetica oculare, i metodi di ricerca e le tecniche di neuroimmagine. All’inizio del testo è
inserito un glossario dei numerosi
acronimi, abbreviazioni e simboli
usati nell’ambito delle scienze visive. Inoltre, è indicata l’origine greca o latina di molti termini comuni
e il significato dei prefissi e suffissi
che vanno a formare le parole che
usiamo abitualmente nella nostra
pratica optometrica. Il “Dictionary
of Optometry and Visual Science”
diventa così una guida nel lessico
specifico delle scienze della visione, che con le dovute trasposizioni,
è fruibile anche a chi, come noi, non
è di lingua inglese.
Un dizionario si concentra in primo luogo sulle parole e sulle loro
definizioni e quindi fornisce solo le
informazioni essenziali relative al
contesto del vocabolo di cui tratta,
a differenza di un’enciclopedia, che
affronta ogni argomento in modo
dettagliato e completo. Molte voci,
comunque, sono collegate da riferimenti incrociati, che permettono di
approfondire diversi aspetti dello
stesso argomento. Malgrado ogni
voce sia trattata in modo relativamente breve e conciso, lo scopo ideale è quello di fornire almeno tutte
le informazioni più rilevanti di ogni
singolo termine. Per esempio, ogni
patologia è descritta illustrando la
sua eziologia, i principali segni e
sintomi e una nota sul trattamento.
Una struttura anatomica è descritta
in base alla sua struttura e alla sua
funzione.
Autore, insieme a Daniel Laby, anche di un “Dictionary of Ophthalmology” (2002), Michel Millodot
ammette di aver sviluppato una
passione quasi maniacale per la
compilazione e il perfezionamento
dei dizionari. Rispetto all’edizione
precedente, l’autore ha revisionato
quasi tutte le voci, ne ha ampliato
altre con informazioni più aggiornate, eliminando anche alcuni termini
obsoleti. Sono state aggiunte molte
nuove illustrazioni e le più vecchie
sono state sostituite, per adeguarsi
ad una grafica più moderna. Sono
state aggiunte sei nuove tabelle, che
non solo riassumono il testo scritto,
ma spesso sono essenziali nel completare la definizione.
La settima edizione del “Dictionary
of Optometry and Visual Science”
si presenta come un libro tascabile, con una robusta quanto insolita
copertina plastificata, pensata per
resistere a ripetute consultazioni e
anche a continui trasporti: non è un
libro destinato a riposare in libreria.
Grazie alla sua maneggevolezza il
dizionario di Millodot è diventato
uno strumento di lavoro indispensabile per tanti professionisti, oltre
ad essere compreso nei testi consigliati di un gran numero di corsi di
optometria in tutto il mondo.
Lenti a Contatto - Contact lenses
Agosto 2010, volume XII, numero 2
Prevenire la miopia con lenti a contatto morbide.
Attenzione alla retina periferica
Luigi Lupelli
Occhio secco e lenti a contatto
Gonzalo Carracedo OD, Msc
L’acido ialuronico e le sue applicazioni in contattologia
Matteo Fagnola, Marco Paolo Pagani, Silvio Maffioletti,
Silvia Tavazzi, Antonio Papagni
La ricerca di nuovi materiali biocompatibili per la manutenzione
quotidiana delle lenti a contatto in silicone idrogel
e per una nuova frontiera delle lenti a contatto medicali
03>
9 7 7 0 0 0 2 0 3 83 7 0
Poste Italiane. Spedizione in a. p. - 70% - DC/DCI/VC nr 2- 2010
Nicola Pescosolido, Chiara Nardella
dodicesimoanno
con il patrocinio di