CHIMICA ORGANICA I
Corso di laurea in CHIMICA (LT)
Esercitazione n. 14 - Reazioni e meccanismi dei composti aromatici.
TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERCIZI DI QUESTO FOGLIO: Reazione di
sostituzione elettrofila aromatica: alogenazione, nitrazione, solfonazione, alchilazione e acilazione di Friedel-Crafts;
meccanismo, addotti σ, orientamento, reattività. Metallazioni (mercuriazione e talliazione). Reazioni con elettrofili deboli
(sali di diazonio, reazione di Reimer- Tiemann, reazione di Kolbe, reazione di idrossimetilazione). Trasformazione dei
sali di diazonio. Sostituzioni elettrofile aromatiche del naftalene. Reazioni di antracene e fenantrene. Reazioni di
riduzione del benzene (con idrogeno, con sodio) e di ossidazione del benzene e di alchilbenzeni, del naftalene, di
antracene e fenantrene. Reazioni di sostituzione nucleofila di alogenobenzeni. Meccanismo di addizione-eliminazione e
meccanismo di eliminazione-addizione; benzino.
1. Dare la definizione ed un esempio per ciascuno dei seguenti termini: a) complesso σ; b)
solfonazione; c) nitrazione; d) gruppo orto,para orientante; e) alchilazione di Friedel-Crafts; f) gruppo
meta orientante.
2. Scrivere quale è e come si forma l'elettrofilo nelle seguenti reazioni aromatiche: a) nitrazione; b)
clorurazione; c) solfonazione; d) acilazione con cloruro di acetile; e) alchilazione con cloruro di
isobutile.
3. Scrivere il meccanismo della clorurazione del benzene, mettendo in evidenza il ruolo del
catalizzatore.
4. Il p-dimetilbenzene si nitra molto più facilmente del benzene. Spiegare.
5. Scrivere il meccanismo della bromurazione aromatica di: a) anilina (= benzenammina); b)
etossibenzene. Dimostrare l'orientamento, servendosi degli addotti σ.
6. Completare le seguenti reazioni del benzene: a) bromuro di terz-butile + AlCl3; b) 1-clorobutano +
AlCl3; c) bromo + un chiodo (...non di acciaio!); d) acido solforico fumante; e) iodio + HNO3; f)
cloruro di benzoile + AlCl3; g) acido nitrico + acido solforico; h) 1-cloro-2,2-dimetilpropano + AlCl3.
Scrivere in ogni caso il meccanismo.
7. Completare le seguenti reazioni dell'isopropilbenzene: a) Br2 alla luce; b) Br2 + FeBr3; c) SO3 in
acido solforico; d) cloruro di acetile + AlCl3; e) cloruro di propile + AlCl3.
8. Completare le seguenti reazioni, catalizzate da AlCl3: a) clorocicloesano + benzene; b) cloruro di
metile + fenil metil etere; c) 3-cloro-2,2-dimetilbutano + isopropilbenzene; d) 2-cloropropano +
nitrobenzene. Dimostrare in ciascun caso l'orientamento, servendosi degli addotti σ.
9. In ciascuna delle seguenti serie, ordinare i composti secondo la reattività decrescente nei confronti
della sostituzione elettrofila aromatica (spiegare), dopo aver individuato l'orientamento: a) triclorometilbenzene, metilbenzene, diclorometilbenzene, clorometilbenzene; b) etilbenzene, 1,1,1-tricloro2-feniletano, 2-fenil-1,1,1-trifluoroetano, 1-fenil-1,2-difluoroetano; c) metossibenzene, fenossido di
sodio, etanoato di fenile; d) feniletanone, benzammide, benzene.
10. Scrivere le reazioni di bromurazione, solfonazione e nitrazione dei seguenti composti, scrivendo in
ciascun caso il prodotto (o i prodotti) di reazione ed indicando se la reazione avviene più velocemente
o più lentamente della corrispondente reazione del benzene: a) metossibenzene; b)
difluorometilbenzene; c) etilbenzene; d) clorobenzene; e) nitrobenzene; f) acido benzensolfonico; g)
benzoato di etile; h) difenil etere; i) bifenile; j) terz-butilbenzene; k) fluorobenzene; l) metilbenzene;
m) acetato di fenile; n) acetilbenzene (= acetofenone, oppure fenil metil chetone oppure 1feniletanone); o) benzammide; p) benzonitrile; q) iodobenzene.
11. Il nitrobenzene viene trattato con la miscela solfonitrica (HNO3 + H2SO4). a) Scrivere l'equazione
chimica della reazione, dando il nome del prodotto. b) Scrivere il meccanismo, giustificando
l'orientamento. c) Prevedere l'ordine di reattività dei seguenti composti nella nitrazione aromatica:
nitrobenzene, fenolo, benzene, metilbenzene (spiegare).
12. a) Scrivere l'equazione chimica della reazione che avviene trattando il bromobenzene con acido
nitrico + acido solforico, giustificando l'orientamento. b) Spiegare l'ordine di reattività che si osserva
se, nelle condizioni di (a), si fanno reagire: benzene, bromobenzene, metilbenze-ne.
13. Disporre i seguenti composti in ordine di reattività crescente nei confronti dell'acido solforico
fumante (acido solforico + anidride solforica): fenolo, nitrobenzene, metilbenzene, clorobenzene.
Scrivere le reazioni corrispondenti e spiegare.
14. Quando il benzoato di fenile viene trattato con un agente nitrante, uno solo degli anelli benzenici
reagisce. Dire quale e perché.
15. Completare le seguenti reazioni di sostituzione elettrofila aromatica: a) N,N-dimetilanilina +
cloruro di acetile e cloruro di alluminio; b) clorobenzene + bromo e bromuro ferrico; c) propanoato di
fenile e acido nitrico + acido solforico; d) isopropilbenzene + acido solforico ed anidride solforica; e)
nitrobenzene + acido nitrico ed acido solforico; f) bifenile + anidride acetica e cloruro di alluminio.
16. Il bifenile si può considerare come un benzene con un fenile come sostituente. Dimostrare che la
reazione di un elettrofilo con il bifenile avviene con un orientamento orto+ para.
17. Spiegare perché il metilbenzene è orto+para orientante, mentre il triclorometilbenzene è meta
orientante.
18. Il vinilbenzene dà sostituzione elettrofila aromatica molto più facilmente del benzene ed i prodotti
sono i derivati orto + para. Spiegare, servendosi degli addotti σ.
19. a) Scrivere l'equazione chimica della reazione che avviene trattando l'acetanilide (= Nfeniletanammide) con bromo e giustificare l'orientamento. b) Spiegare l'ordine di reattività che si
osserva se con bromo si fanno reagire: anilina, acetanilide, benzene.
20. Il nitrobenzene viene talvolta usato come solvente nelle alchilazioni di Friedel-Crafts. Perché il
nitrobenzene non interferisce con la reazione desiderata?
21. a) Scrivere l'equazione chimica della reazione che avviene trattando il metilbenzene con cloruro di
propanoile e cloruro di alluminio, giustificando l'orientamento. Spiegare l'ordine di reattività che si
osserva se, nelle condizioni di (a) si fanno reagire: m-dimetilbenzene, metilbenzene, fluorobenzene,
benzene.
22. Quale composto in ciascuna delle seguenti coppie è più reattivo nella bromurazione aromatica?
(spiegare): a) acetanilide o benzene; b) bromobenzene o metilbenzene; c) p-dimetilbenzene o acido pmetilbenzoico; d) m-dinitrobenzene o m-metilnitrobenzene; e) clorobenzene o m-diclorobenzene; f)
metilbenzene o fenolo; g) fenolo o clorobenzene.
23. Il fenolo viene trattato con una soluzione acquosa di bromo; a) scrivere l'equazione chimica della
reazione, giustificandone l'orientamento. b) Commentare le condizioni in cui la reazione avviene,
confrontandole con quelle necessarie perché la reazione avvenga con il benzene.
24. Dare una spiegazione dei seguenti fatti sperimentali: a) Quando il benzene viene trattato con
metilpropene ed acido solforico, si ottiene terz-butilbenzene. b) La nitrazione del cloruro di
trimetilanilinio dà un prodotto nitrato in posizione meta. c) Quando l'anilina si tratta con acido nitrico
diluito, ad alta temperatura, si ottiene una miscela di orto- e para-nitroanilina; con acido nitrico
concentrato, invece, si ottiene solo la m-nitroanilina. d) Quando il benzene si tratta con una quantità
equivalente di cloruro di metile e cloruro di alluminio, si ottiene una miscela di benzene, metilbenzene
e dimetilbenzeni; quando invece il benzene si tratta con una quantità equivalente di cloruro di acetile e
cloruro di alluminio, il solo prodotto di reazione è il feniletanone. e) La bromurazione del terzbutilbenzene non dà prodotto di sostituzione in orto, ma solo in para.
25. Completare le seguenti reazioni, specificando i nomi dei composti organici che si formano: a)
metilbenzene + cloruro di isobutile + AlCl3 ; b) benzene + 1-cloro-2-butene e cloruro di alluminio; c)
benzene + cloruro di butanoile e cloruro di alluminio; d) benzene + anidride acetica + cloruro di
alluminio.
26. Il gruppo nitroso, -NO, come sostituente sul benzene orienta la sostituzione elettrofila aromatica in
orto + para ed è meno reattivo del benzene. Come potete spiegare questi dati sperimentali?
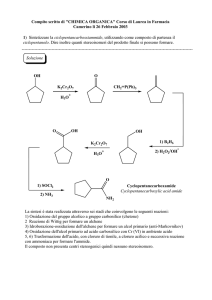
27. Il 4-metossifenilmetanolo contribuisce sia all'aroma della liquerizia che al profumo della lavanda.
Come si potrebbe ottenere questo composto a partire dal fenolo?
28. Preparate i seguenti composti, partendo da benzene o da metilbenzene e dai reagenti necessari: a)
butilbenzene; b) acido p-metilbenzensolfonico; c) p-cloronitrobenzene; d) m-cloronitrobenzene; e)
metil p-metilfenil chetone.
29. Scrivere i prodotti di mononitrazione dei seguenti composti, giustificando l'orientamento: a) ometilnitrobenzene; b) m-clorometilbenzene; c) acido o-bromobenzoico; d) acido p-metossibenzoico; e)
m-metilbenzenolo.
30. Scrivere i prodotti di bromurazione aromatica dei seguenti composti, giustificando l'orientamento:
a) p-cloronitrobenzene; b) p-cloroacetanilide (= N-(p-clorofenil)etanammide.
31. Quale dei tre trimetilbenzeni isomeri vi aspettate sia più reattivo in una sostituzione elettrofila
aromatica? Spiegare.
32. L'isopropilbenzene reagisce con il cloro in due modi diversi, a seconda delle condizioni. a) Scrivere
l'equazione chimica ed il meccanismo della reazione che avviene alla luce ultravioletta. b) Scrivere
l'equazione chimica ed il meccanismo della reazione che avviene in presenza di cloruro ferrico.
33 a) Scrivere la reazione dell'anilina con il cloruro di p-clorobenzendiazionio e spiegare perché questo
elettrofilo non reagisce con l'acetanilide (= N-feniletanammide). b) L'anilina reagisce più velocemente
con il cloruro di benzendiazonio o con il cloruro di 2,4-dinitrobenzendiazonio?
34. L'acido salicilico (= acido o-idrossibenzoico) e l'aldeide salicilica (= o-idrossibenzencarbaldeide)
si preparano dal fenolo. Scrivere le reazioni corrispondenti e spiegare perché gli stessi reagenti non
danno reazione con il benzene.
35. a) Scrivere l'equazione chimica ed il meccanismo della nitrazione aromatica del naftalene,
giustificandone l'orientamento. b) Scrivere l'equazione chimica ed il meccanismo della solfonazione a
bassa temperatura del naftalene. Spiegare perché a temperature più elevate si ottiene un isomero
diverso.
36. A differenza di benzene e naftalene, il fenantrene addiziona una molecola di bromo. Scrivere la
reazione e spiegare perché avviene, servendosi delle strutture di risonanza del fenantrene.
37. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a)
isopropilbenzene + permanganato di potassio (KMnO4), a caldo; b) vinilbenzene + acido cloridrico; c)
metilbenzene + cloro, alla luce ultravioletta; d) etilbenzene + cloro e cloruro ferrico; e) etilbenzene +
bromo, a caldo; f) vinilbenzene + permanganato di potassio, a caldo; g) metilbenzene + 1-cloropropano
e cloruro di alluminio; h) vinilbenzene + H2 (un equivalente) e Pt; i) vinilbenzene e bromo; j) 1,4diidrossi-2-metossibenzene + ossido di argento; k) benzene + sodio in ammoniaca ed etanolo; l)
vinilbenzene + H2 (in eccesso) e Pt.
38. Scrivere l'equazione chimica delle seguenti reazioni: a) benzene + ossigeno e pentossido di vanadio
(V2O5), ad elevata temperatura; b) antracene + anidride cromica (CrO3) ed acido solforico; c) pbenzendiolo + ossido di argento (Ag2O); d) propilbenzene + permanganato di potassio, a caldo.
39. Scrivere i prodotti delle seguenti reazioni del cloruro di p-metilbenzendiazonio con: a) KI; b)
CuCN; c) KOH; d) H2O, a caldo; e) CuBr; f) NaNO2, Cu; g) NaBF4 e poi aumentando la temperatura.
40. Per ognuno dei seguenti composti indicare un metodo di preparazione a partire dal benzene: a)
acido 3-amminobenzensolfonico; b) m-diamminobenzene; c) p-nitroanilina; d) m-nitroanilina.
41. Per ognuno dei seguenti composti indicare un metodo di preparazione a partire dal metilbenzene: a)
o-metilanilina; b) m-nitrometilbenzene; c) p-nitrometilbenzene; d) 4-cloro-2-nitrometilbenzene; e) 4cloro-2-metilanilina.
42. Scrivere i passaggi che permettono di effetturare le seguenti trasformazioni: a) da metilbenzene a 2bromo-4-metilanilina; b) da metilbenzene a 3,5-dibromometilbenzene, c) da anilina a 2,4,6-tricloroni-
trobenzene; d) da metilbenzene a 2-metil-4-nitrobenzonitrile; e) da metilbenzene a 3-bromo-4-iodometilbenzene.
43. Completare le seguenti reazioni di sostituzione nucleofila aromatica, specificando se avvengono
con meccanismo di addizione-eliminazione o di eliminazione-addizione (via benzino); spiegare il
perché della scelta. a) p-nitrobromobenzene + KOH; b) m-cloronitrobenzene + KOH; c) p-diclorobenzene + KOH (in eccesso); c) 2,4,6-trinitroclorobenzene + KOH; d) 4-ni-troclorobenzene + KOH;
e) m-clorometilbenzene + KOH; f) p-clorometilbenzene + KOH.
44. Scrivere equazione chimica e meccanismo delle seguenti reazioni: a) 2,4-dinitroclorobenzene +
sodioammide; b) 1,2-dicloro-3,5-dinitrobenzene + metossido di sodio (un equivalente) in metanolo; c)
1,2-dicloro-3,5-dinitrobenzene + metossido di sodio (due equivalenti) in metanolo; d) 4-clorometilbenzene + KOH ad elevata temperatura; e) 3-bromometilbenzene + dietilammide di litio [=
(CH3CH2)2N- Li+] in dietilammina.
45. Mettere i seguenti composti in ordine di reattività decrescente nei confronti della metanammina
(scrivere le reazioni corrispondenti e spiegare): 2-bromonitrobenzene, 3-bromonitrobenzene, 4bromonitrobenzene, 2,4-dinitrobromobenzene, 3,4-dinitrobromobenzene.
46. Il 2,4,6-trinitroclorobenzene reagisce con NaOH in acqua. a) Scrivere equazione chimica e
meccanismo della reazione. b) Il nome corrente del prodotto è "acido picrico", pur trattandosi di un
fenolo. Come mai?
47. Il m-clorometilbenzene reagisce con sodioammide in ammoniaca liquida, dando tre prodotti
isomeri. Scrivere l'equazione chimica della reazione e spiegare la formazione dei tre isomeri, sulla base
del meccanismo.
48. Il defoliante Agent Orange, usato nella guerra del Vietnam (e che è ritenuto responsabile della
malattia e della morte di molti reduci, anche a distanza di anni), contiene l'acido (2,4,5triclorofenossi)etanoico, indicato come 2,4,5-T. Questo acido si prepara per reazione parziale
dell'1,2,4,5-tetraclorobenzene con NaOH, seguita da reazione con cloroacetato di sodio.
a) Scrivere la reazione di sintesi del 2,4,5-T. b) Una delle impurezze contenute nell' Agent Orange
(probabilmente il principale componente tossico) era la 2,3,7,8-tetraclorodibenzodiossina, 2,3,7,8TCDD, spesso chiamata, impropria-mente, diossina. Indicare come 2,3,7,8-TCDD si forma nel corso
della sintesi di 2,4,5-T. c) Come si può eliminare la contaminazione da TCDD sia dopo il primo
passaggio che alla fine della sintesi?
Cl
O CH2 CO2H
Cl
Cl
Cl
O
Cl
Cl
O
Cl
2,3,7,8-TCDD
2,4,5-T
CHIMICA ORGANICA I
Corso di laurea in CHIMICA
Esercitazione n. 15 - Reazioni e meccanismi di aldeidi e chetoni.
TERMINI ED ARGOMENTI PER LO SVOLGIMENTO DEGLI ESERCIZI DI QUESTO FOGLIO: Meccanismo
generale dell'addizione nucleofila. Addizione di HCN. Addizione di acqua. Addizione di alcooli (formazione di
emiacetali e di acetali). Formazione di immine ed enammine. Addizione dei derivati dell'ammoniaca (idrossilammina,
idrazina, fenilidrazina, 2,4-dinitrofenilidrazina, semicarbazide). Reazione con i reattivi di Grignard ed i composti
litioorganici. Reazione di Wittig. Condensazione aldolica, aldolica incrociata, condensazione di Claisen-Schmidt.
Reazione di Cannizzaro. Reazione di ossidazione, reattivo di Tollens. Reazioni di riduzione: con idrogeno e
catalizzatore, con idruri, di Clemmensen, di Wolff-Kishner. Tautomeria. α-Alogenazione (promossa da basi ed acidocatalizzata); reazione dell'aloformio. Reazioni dei composti α,β-insaturi.
1. Dare la definizione ed un esempio per ciascuno dei seguenti termini: a) chetone; b) aldeide; c)
forma enolica; d) ione enolato; e) tautomeria; f) tautomero; g) idrogeno enolizzabile; h) cianidrina; i)
immina; j) ossima; k) fenilidrazone; l) enammina; m) acetale; n) emiacetale; o) 1,3-ditiano (= 1,3ditiaciloesano); p) saggio di Tollens; q) riduzione di Wolff-Kishner; r) riduzione di Clemmensen.
PER RICORDARE LE REAZIONI
2. Completare le equazioni chimiche per le reazioni del propanale con ciascuno dei seguenti
reagenti: a) NaBH4 (e poi H2O); bromuro di fenilmagnesio e poi acqua e HBr; c) OH-, H2O; d) 1,2etandiolo, in ambiente acido; e) bromo, in acido acetico; f) idrossilammina; g) fenilidrazina; h)
dietilammina; i) KMnO4, OH-; j) con piperidina (= azacicloesano); k) con pirrolidina (=
azaciclopentano).
3. Scrivere i prodotti che si ottengono per ciascuna delle seguenti reazioni della p-metilbenzencarbaldeide: a) con aldeide acetica (= etanale), in ambiente basico; b) con NaOH concentrata; c) con
KMnO4, a freddo; d) con KMnO4, a caldo; e) con etanammina.
4. Completare le seguenti reazioni del cicloesanone, specificando i nomi dei composti organici che si
ottengono: a) con 2,2-dimetil-1,3-propandiolo, in ambiente acido; b) con idrossilammina; c) con 1,2etandiolo, in ambiente acido; d) con LiAlH4 e poi acqua e acido.
5. Scrivere i prodotti che si ottengono da ciascuna delle seguenti reazioni dell'acetofenone (=
feniletanone): a) con cloro (in eccesso), in ambiente basico; b) con NaBH4, e poi acqua; c) con
HNO3 e H2SO4; d) con idrazina; e) con idrazina, in ambiente basico, a caldo; f) con bromuro di
fenilmagnesio, e poi acqua e HBr; g) con iodio, in ambiente basico; h) con Zn(Hg) e HCl.
6. Scrivere i prodotti delle reazioni del ciclopentanone con: a) bromo in acido acetico; b) NaBH4 e
successiva idrolisi; c) fenilidrazina; d) bromuro di isopropilmagnesio e poi acqua, H+; e) idrazina, in
ambiente basico a caldo.
7. Completare le seguenti reazioni, specificando i nomi dei composti organici che si formano: a)
cicloesancarbaldeide + HCN; b) ciclopentanone + NaCN + H2SO4; c) aldeide benzoica +
metanammina; d) ciclopentanone + anilina; e) ciclopentanone + piperidina (= azacicloesano); f) 4metil-3-penten-2-one + metanammina.
8. Per ciascuno dei seguenti composti indicare il gruppo funzionale e scrivere la reazione di idrolisi
completa.
HO
O CH2 CH3
a)
O
b)
CH3 CH2 C
O
O
d)
CH O CH3
CH3
O
c)
CH3
O
CH3
e)
CH3
HO
O
f)
HO
OH
OH
g)
O
N
O
N
h)
N
OH
9. Scrivere le reazioni per la formazione di emiacetali in soluzione acquosa di: a) 5-idrossi-2esanone; b) 1,3,4,5,6-pentaidrossi-2-esanone; c) 5-idrossipentanale; d) 2,4-diidrossipentanale. c)
Scrivere l'equazione chimica ed il meccanismo per la formazione di acetali con metanolo, a partire
dagli emiacetali precedenti.
10. Scrivere le reazioni del cicloesanone con i seguenti reagenti: a) metanammina, in ambiente acido;
b) metanolo, in ambiente acido anidro; c) idrossilammina, in ambiente acido; d) 1,2-etandiolo, in
ambiente acido; e) fenilidrazina, in ambiente acido; f) bromuro di fenilmagnesio, e poi acqua acida;
g) reattivo di Tollens; d) acetiluro di sodio e poi acqua acida; i) cianuro di sodio e poi acqua acida; j)
idrazina e poi KOH, a caldo.
11. Scrivere le reazioni della cicloesancarbaldeide con i seguenti reagenti: a) bromuro di
fenilmagnesio, e poi acqua acida; b) reattivo di Tollens; c) etanolo, in ambiente acido anidro; d) 1,3propanditiolo, in ambiente acido anidro; e) amalgama di zinco in HCl acquoso; f) fenilidrazina, in
ambiente acido.
12. Scrivere tutti i passaggi della reazione di Wittig servendosi di: a) trifenilfosfina, 1bromopropano, butillitio, benzaldeide; b) trifenilfosfina, 2-iodopropano, idruro di sodio, propanale.
13. Le seguenti reazioni sono usate per l'identificazione e l'analisi di aldeidi e chetoni. Scrivere le
reazioni corrispondenti: a) butanone + 2,4-dinitrofenilidrazina; b) benzaldeide + reattivo di Tollens;
c) cicloesanone + Br2, OH-.
14. Completare le seguenti reazioni: a) propanone + NH3, H2, Ni; b) propanale, H2, Pt; c)
cicloesancarbaldeide + KMnO4.
15. Scrivere i prodotti (specificandone il nome) delle seguenti reazioni: a) ciclopentanone + NaBH4 e
successiva idrolisi; b) benzaldeide + NaCN, HCl; c) pentanale + NaOH, H2O; d) 4-esenale +
metanolo e HCl anidro; d) 1,3-diossaciclopentano + H2O, H+ (ATTENZIONE: il gruppo funzionale
è del tipo C(OR)2 !).
16. Completare la seguente serie di reazioni: benzene + CH3CH2COCl + AlCl3 → A; A + NH2NH2,
OH-, a caldo → B; B + KMnO4, a caldo → C.
PER CAPIRE LE REAZIONI (MECCANISMI)
17. a) Scrivere il meccanismo della reazione tra idrossilammina ed un composto carbonilico. b)
Prevedere, spiegando, l'ordine di reattività delle seguenti aldeidi nei confronti dell'idrossilammina:
benzaldeide, p-nitrobenzaldeide, m-nitrobenzaldeide.
18. a) Mettere i seguenti composti in ordine di reattività nei confronti della reazione con idrazina
(spiegare): benzaldeide, p-metilbenzaldeide, p-metossibenzaldeide. b) Mettere i seguenti composti in
ordine di reattività nei confronti della reazione con 2,4-dinitrofenilidrazina: 2-pentanone, 3pentanone, 3-cloro-2-pentanone, pentanale (spiegare).
19. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene tra etanale e
metanolo, in presenza di acidi. b) Spiegare come varia la reattività se con metanolo si fa reagire
l'aldeide tricloroacetica.
20. a) Scrivere il meccanismo dell'idratazione di un composto carbonilico; b) mettere i seguenti
composti carbonilici secondo l'ordine decrescente delle loro costanti di equilibrio di idratazione:
CH3COCH2Cl, ClCH2CHO, CH2O, CH3COCH3, CH3CHO. (Spiegare).
21. a) L'1-fenil-2-propanone può dare due enoli diversi. a) Scrivere le strutture degli enoli. b)
Prevedere quale sarà presente all'equilibrio in quantità maggiore. c) Scrivere il meccanismo di
formazione dell'enolo in uno dei due casi.
22. Il 3-fenil-2-butanone potrebbe formare due enoli, ma in realtà ne forma uno solo. Quale?
Spiegare. b) Che cosa succede quando l'(R)-3-fenil-2-butanone si scioglie in soluzione acquosa acida
o basica? [suggerimento: tautomeria...]
23. Quando l'(R)-3-fenil-2-butanone si scioglie in etanolo acquoso contenente NaOH o HCl, il potere
rotatorio della soluzione diminuisce lentamente, fino a diventare zero. Evaporando il solvente, si
ottiene una miscela racemica di (R) e (S)-3-fenil-2-butanone. Spiegare e scrivere gli equilibri
corrispondenti.
24. Il 4-idrossibutanale esiste in soluzione essenzialmente in forma ciclica. a) Che tipo di composto
è? b) Scrivere l'equilibrio tra la forma aperta e la forma ciclica. c) Scrivere il meccanismo relativo
alla ciclizzazione.
25. a) L'1,1-dietossietano si idrolizza facilmente in acqua contenente un po' di acido solforico;
scrivere i prodotti di reazione ed il meccanismo. b) Un acetale si può formare in soluzione acida, ma
non in soluzione basica. Perché? c) L'etossicicloesano non dà reazione con HCl diluito, mentre l'1,1dietossicicloesano sì. Spiegare.
26. Nel tentativo di ottenere l'(R)-3-bromo-2-butanone, un chimico ha trattato l'(R,R)-3-bromo-2butanolo con acido cromico, ottenendo però una miscela racemica. Spiegare.
27. Quando il cis-2,4-dimetilcicloesanone si scioglie in etanolo acquoso contenente una traccia di
NaOH, si ottiene una miscela di isomeri cis e trans. Spiegare, servendosi del meccanismo.
28. a) La p-nitrobenzaldeide viene riscaldata in presenza di una base forte. Scrivere l'equazione
chimica ed il meccanismo della reazione. b) La benzaldeide viene fatta reagire con etanale in
ambiente acquoso basico. Scrivere l'equazione chimica ed il meccanismo della reazione, spiegando
la funzione della base e dei due carbonili.
29. a) Scrivere l'equilibrio che si stabilisce quando si scioglie l'etanale in acqua. b) Etanale,
tricloroetanale ed acetone si sciolgono in acqua: stabilire l'ordine decrescente di stabilità degli addotti
che si formano. Spiegare, sulla base del meccanismo.
30. Dire da quali dei seguenti composti si formano idrati stabili (scrivere gli equilibri corrispondenti
e spiegare): esacloropropanone, cicloesanone, benzaldeide, 2,2-dimetil-3-pentanone, formaldeide (=
metanale).
31. Mettere i seguenti composti in ordine di reattività verso HCN: difenil chetone, benzaldeide, fenil
metil chetone. Spiegare e scrivere le reazioni corrispondenti.
32. a) Perché una arilammina (per es. anilina) dà un'immina più stabile della isopropilammina? b)
Quale è la geometria di CH3CH=N-CH3? Vi aspettate che ci siano stereoisomeri? Da quali composti
si può ottenere?
33. a) Scrivere le equazioni chimiche della reazione del cicloesanone con le seguenti ammine:
metanammina, dimetilammina, piperidina (azacicloesano, C6H11N), pirrolidina (azaciclopentano,
C4H9N). b) Se si tratta con pirrolidina l'1-fenil-2-pentanone si forma una sola delle due enammine
regioisomere. Indicare quale e spiegare perché.
34. a) Scrivere gli equilibri tautomerici per i seguenti composti: cicloesanone, feniletanone, 1,3cicloesandione, 2,5-pentandione, 2,4-pentandione. b) Scrivere equazione chimica e meccanismo per
la clorurazione promossa da basi di (R)-1-fenil-2-metil-1-butanone. c) Scrivere gli equilibri
tautomerici per i seguenti composti carbonilici ed il meccanismo di formazione in ambiente acido e
basico: 3-ossobutanale, 3-metil-2,4-pentandione, 2-acetilcicloesanone.
35. La condensazione aldolica dei chetoni in genere non è un processo favorevole. La condensazione
aldolica intramolecolare di dichetoni, invece, è un metodo importante per la sintesi di composti
ciclici. Scrivere la reazione del 2,7-ottandione con KOH in acqua.
36. Ciascuno dei seguenti composti viene fatto reagire con HCN: etanale, D-gliceraldeide,
gliceraldeide racemica, propanone. a) Scrivere la reazione per ognuno dei composti. b) Se si fraziona
la miscela di reazione (cioè si separano i prodotti, sulla base delle diverse proprietà fisiche), quante
frazioni si ottengono in ciascun caso? Quali sono risolvibili (cioè sono miscele racemiche).
37. a) I metilchetoni vengono ossidati dagli ipoalogeniti (reazione dell'aloformio): scrivere
l'equazione chimica ed il meccanismo della reazione tra feniletanone ed ipoclorito di sodio
[ricordarsi che l'ipoclorito in ambiente basico è in equilibrio con cloro]. b) Dire quali dei seguenti
composti danno un saggio dello iodoformio positivo: iodoetanale; propanale, 2-butanolo,
feniletanone, 2-metil-3-pentanone. c) Da quale metil chetone si è ottenuto ciascuno dei seguenti
acidi, in seguito a reazione dell'aloformio:
HO
a) (CH ) CHCO H
32
2
b)
O
C
c)
C
C
OH
O
OH
O
38. Il testosterone (un ormone sessuale) contiene un raggruppamento -C=C-C=O, α,β-insaturo.
Perché sia il carbonio carbonilico che il carbonio in beta sono suscettibili di attacco da parte dei
reagenti nucleofili?
PER APPLICARE LE REAZIONI STUDIATE
39. a) Indicare nelle seguenti strutture i gruppi emiacetale ed acetale:
H3C
O
O
CH
OH
CH3
O
O
CH
OCH2CH3
CH2CH3
HO
CH3
O
HO
OH
b) Da quali alcooli ed aldeidi o chetoni si deve partire per ottenere i composti in (a)? Scrivere le
reazioni.
40. Da quali composti carbonilici ed ammine si ottengono le seguenti immine?
N
a)
b)
N
c)
CH3
C
CH3
N
d)
NH
e)
CH3
N
CH3
41. Da quale alogenuro alchilico potete partire per effettuare le seguenti reazioni di Wittig: a)
difenilchetone → 1,1-difeniletene; b) 2-pentanone → 4-metil-1,3-eptadiene; c) o-benzendialdeide →
o-divinilbenzene; d) metil (p-metossifenil) chetone → 1-metossi-2-(p-metossifenil)propene.
42. Indicare come si possa sintetizzare il 2-ottanone a partire dai seguenti composti e tutti i reagenti
necessari: a) eptanale; b) 2-ottanolo; c) 1-ottino.
43. Indicare come si possa sintetizzare l'ottanale a partire dai seguenti composti e tutti i reagenti
necessari: a) 1-ottanolo; b) 1-nonene (suggerimento: riguardare le reazioni degli alcheni!); c) 1ottino; d) 1,1-dicloroottano.
44. Dire quale tra i seguenti composti dà un saggio di Tollens positivo:
O
a) CH CHO
3
b) CH COCH
3
3
c)
OH
O
O
d)
CH3
45. Sia NaBH4 che NaBD4 sono disponibili commercialmente. Indicare come otterreste i seguenti
CH3CD(OD)CH2CH3,
composti
a
partire
dal
butanone:
CH3CD(OH)CH2CH3,
CH3CH(OD)CH2CH3.
46. Indicare come si possono effettuare le seguenti conversioni in modo efficiente (ricordate che le
aldeidi sono più reattive dei chetoni): a) da 3-ossociclopentancarbaldeide a 3-idrossimetilciclopentanone; b) 3-ossociclopentancarbaldeide a 3-idrossiciclopentancarbaldeide.
47. Scrivere le strutture dei seguenti derivati di composti carbonilici: a) il 2,4-dinitrofenilidrazone
della benzencarbaldeide; b) l'ossima del ciclopropanone; c) l'acetale etilenico del 3-esanone
(ciclico!); d) il dimetilacetale dell'etanale; e) il metil emiacetale del metanale; f) l'isomero E
dell'immina dell'1-fenil-1-propanone.
48. Sintetizzare i seguenti derivati, a partire dall'opportuno composto carbonilico:
a)
b)
d)
c)
N
N OH
f)
e)
N
N
H3C
O
O
CH3
N
49. Da quale alogenuro alchilico e da quale composto carbonilico si può partire per ottenere i
seguenti alcheni, mediante una reazione di Wittig:
50. a) Indicare due diversi modi per ottenere il 2-butanolo, usando reattivi di Grignard e gli
opportuni composti carbonilici.
51. Come si possono preparare i seguenti composti:
N
a) CH3CH2CH
d)
CH N(CH2CH3)2
N
e)
c)
b)
N
N
52. Come potete preparare i seguenti composti, a partire da ioduro di metile e reagenti opportuni: a)
3-metil-3-pentanolo; b) etanolo; c) 2-pentanolo; d) 1-feniletanolo; e) 1-fenil-2- butanolo.
53. Indicate come si possono effettuare le seguenti trasformazioni: a) da benzaldeide a 1-fenil-1butanolo; b) da cicloesanone a 1-butilcicloesanolo; c) da 1-butino a 2-pentin-1-olo; d) da
bromobenzene ad alcool benzilico.
54. Da quali composti i seguenti alcooli si possono ottenere per riduzione con NaBH4: 1-propanolo,
3-cicloesenolo, 1-cicloesiletanolo.
55. a) Con quale reattivo di Grignard si possono effettuare le seguenti trasformazioni: metanale in
alcool benzilico; cicloesanone in 1-propilcicloesanolo. b) Dire quali tra i seguenti composti non
possono essere usati in una sintesi di Grignard? (Attenzione: un reattivo di Grignard è
sostanzialmente un carbanione e quindi una base forte ...) 3-idrossibutanale, 3-ossobutanale, 3fenilpropanale, p-amminobenzaldeide, pentandiale, cicloesanone.
SPETTROSCOPIA
56. Dalle bottiglie che contenevano due composti, un’aldeide ed un chetone, entrambi di formula
molecolare C8H8O, si sono staccate le etichette. I composti sono stati provvisoriamente chiamati A e
B e si sono fatti gli spettri riportati di seguito. Sulla base degli spettri, identificate i composti e ...
rimettete a posto le etichette.
A
cm-1
B
CHIMICA ORGANICA I
Corso di laurea in CHIMICA (LT)
17. REAZIONI E MECCANISMI DI ACIDI CARBOSSILICI E DERIVATI
TERMINI ED ARGOMENTI DA CONOSCERE PER LO SVOLGIMENTO DEGLI ESERCIZI DI QUESTO
FOGLIO: Meccanismo di sostituzione nucleofila al carbonio acilico. Reazioni degli acidi carbossilici: riduzione,
conversione in alogenuri acilici, in anidridi, in esteri (formazione di lattoni e lattidi), in ammidi (formazione di
lattami). Reazioni degli alogenuri acilici: conversione in acidi, in anidridi, in esteri, in ammidi, in tioesteri; riduzione
(con LiAlH4 e con H2, Pd/BaSO4). Reazioni delle anidridi: conversione in acidi carbossilici, in esteri, in ammidi ed
immidi. Reazioni degli esteri: idrolisi acida e basica; transesterificazione; conversione in ammidi; riduzione. Reazioni
delle ammidi: idrolisi basica ed acida; conversione in nitrili, in ammine (riduzione,). Reazioni dei nitrili: idrolisi acida,
riduzione.
Reazioni specifiche delle singole classi: acidi carbossilici (α-alogenazione; reazione con diazometano; reazione con
DCC); cloruri acilici (reazioni con composti organometallici [reattivi di Grignard, cadmioorganici]; esteri (reazione
con i reattivi di Grignard, condensazione di Claisen); ammidi (trasposizione di Hofmann).
Reazioni di decarbossilazione. Uso degli esteri acetoacetico (= 3-ossobutanoato) e malonico (= propandioato) nella
sintesi organica.
PER RICORDARE LE REAZIONI
1. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'acido butanoico viene fatto
reagire con ciascuno dei seguenti composti: a) LiAlH4 e poi acqua; b) cloruro di benzoile; c)
etanolo, in ambiente acido; d) metanammina e poi riscaldamento.
2. Scrivere i prodotti (specificandone il nome) che si ottengono quando il cloruro di acetile viene
fatto reagire con ciascuno dei seguenti composti: a) ammoniaca (eccesso); b) acqua; c) 1-butanolo,
in presenza di piridina; d) toluene + AlCl3; e) H2 e Pd disattivato; f) metanammina (eccesso); g)
anilina (eccesso); h) dimetilammina (eccesso); i) etantiolo, in presenza di piridina; j) acetato di
sodio; l) acido acetico; m) fenolo, in presenza di piridina.
3. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'anidride acetica viene fatta
reagire con ciascuno dei seguenti composti: a) ammoniaca (eccesso); b) acqua; c) 1-propanolo; d)
benzene + AlCl3; e) etanammina (eccesso); f) dietilammina (eccesso); g) cicloesanolo; h) pbromofenolo; i) piperidina (azacicloesano); j) etossido di sodio in etanolo.
4. Scrivere le reazioni del cloruro di benzoile con ciascuno dei reagenti dell’Esercizio precedente.
5. Scrivere i prodotti (specificandone il nome) che si ottengono quando il propanoato di etile viene
fatto reagire con ciascuno dei seguenti composti: a) acqua, H+; b) acqua e OH-; c) 1-ottanolo + HCl;
d) metossido di sodio; e) metanammina; f) LiAlH4 e poi acqua.
6. Scrivere i prodotti (specificandone il nome) che si ottengono quando la propanammide viene fatta
reagire con ciascuno dei seguenti composti: a) acqua ed acido; b) acqua e OH-; c) LiAlH4 e poi
acqua.
7. Scrivere i prodotti di esterificazione di: a) acido p-metilbenzoico con 2-propanolo; b) acido pbenzendioico con etanolo (in eccesso); c) acido acetico con (R)-2-butanolo.
8. Scrivere la reazione di esterificazione acido catalizzata che porta ai seguenti esteri, suggerendo un
modo per portare la reazione a completamento: a) o-idrossibenzoato di metile; b) metanoato di
metile (punto di ebollizione, 32°C); c) benzoato di etile.
9. Scrivere i prodotti (specificandone il nome) che si formano per riscaldamento di: a) acido
propandioico; b) acido 2-metil-3-ossobutanoico; c) acido 2-etil-3-ossopentanoico; d) acido 5ossoesanoico.
10. Completare le seguenti reazioni: a) acido benzoico + 2-propanolo, in ambiente acido, a caldo; b)
acido benzoico + 1,2-etandiolo, in ambiente acido, a caldo; c) acido formico (metanoico) +
cicloesanolo, in ambiente acido; d) acido benzoico + (S)-2-pentanolo, in ambiente acido.
11. Completare le seguenti reazioni: a) soluzione concentrata di acido 10-idrossidecanoico, in
ambiente acido, a caldo; b) soluzione diluita di acido 10-idrossidecanoico, in ambiente acido, a
caldo; c) acido o-benzendioico + anidride benzoica; d) 3-ossobutanoato di etile + acqua, in ambiente
acido.
12. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a)
benzoato di fenile + metossido di sodio; b) cloruro di propanoile + metanammina; c) anidride
acetica + metanolo; d) acido benzoico + cloruro di tionile (SOCl2); e) propanoato di isopropile +
acqua, in ambiente acido; f) acido propanoico + metanolo, in ambiente acido; g) acetanilide + acqua,
in ambiente basico; h) anidride butandioica + ammoniaca (due equivalenti); i) 1-naftalenammina +
anidride acetica, in presenza di piridina.
13. Scrivere i prodotti che si ottengono per riscaldamento, in ambiente acido, dei seguenti composti:
a) acido ossalico (= acido etandioico); b) acido acetoacetico (= acido 3-ossobutanoico); c) acido
lattico (= acido 2-idrossipropanoico); d) acido ftalico (= acido o-benzendioico); e) acido 2idrossibutanoico; f) acido 3-idrossibutanoico; g) acido 4-idrossibutanoico; h) acido malonico (=
acido propandioico); i) acido 2-amminopentanoico; l) acido 3-amminopentanoico; m) acido 4amminopentanoico; n) acido piruvico (= acido 2-ossopropanoico).
14. Completare le seguenti reazioni, specificando i nomi dei composti organici che si ottengono: a)
cloruro di propanoile + diallil cadmio; b) cloruro di propanoile + diisopropil cuprato di litio; c)
cloruro di butanoile + dipropil cadmio.
15. Scrivere i prodotti (specificandone il nome) che si ottengono quando il cloruro di acetile viene
fatto reagire con ciascuno dei seguenti composti: a) ioduro di isopropilmagnesio e poi acqua ed
acido; b) difenil cadmio; c) dietilcuprato di litio.
PER CAPIRE LE REAZIONI (MECCANISMI)
16. Scrivere il meccanismo delle sostituzioni nucleofile al carbonio acilico che portano: a) al
benzoato di etile dal cloruro di benzoile; b) all'N-metiletanammide dal cloruro di acetile (= etanoile).
17. Scrivere il meccanismo della reazione acido-catalizzata dell'acido acetico con etanolo.
18. a) Quando l'acido maleico (= cis-butendioico) viene scaldato a 200°C, perde una molecola di
acqua e si trasforma in anidride maleica (= cis-butendioica). Il diastereomero dell'acido maleico,
l'acido fumarico, richiede una temperatura molto più alta per disidratarsi e quando lo fa, dà anch'esso
anidride maleica. Spiegare. b) L'acido o-benzendioico, scaldato a 200°C, forma un'anidride ciclica.
Quale ne è la struttura?
19. a) Perché il cloruro di benzoile è meno reattivo di altri alogenuri acilici (per esempio, cloruro di
butanoile) con i nucleofili? b) Perché non si può preparare un cloruro acilico da un acido e HCl? c)
Scrivere il meccanismo della reazione del cloruro di butanoile con il fenolo, in presenza di piridina.
20. Scrivere le equazioni chimiche per le reazioni dei seguenti derivati di acidi carbossilici con
NaOH acquoso, indicandone l'ordine di reattività; benzoato di etile, N-etilbenzammide, cloruro di
benzoile, anidride benzoica propanoica.
21. Scrivere equazione chimica e meccanismo per l'idrolisi basica del benzoato di metile; spiegare
l'ordine di reattività dei seguenti composti nell'idrolisi basica: benzoato di metile, p-bromobenzoato
di metile, p-nitrobenzoato di metile.
22. a) Scrivere il meccanismo di idrolisi basica degli esteri. Noto questo, si chiede se è possibile
esterificare un acido carbossilico in soluzione basica. b) Prevedere, spiegando, l'ordine di reattività
dei seguenti esteri nell'idrolisi basica: acetato di etile, 2-ossopropanoato di etile, 2-metilpropanoato
di etile.
23. Conoscendo il meccanismo di idrolisi basica degli esteri, si chiede se, partendo dal benzoato di
sec-butile di configurazione S, l'alcool che si forma dall'idrolisi ha subito racemizzazione, inversione
o ritenzione della configurazione. Spiegare.
24. Il benzoato di etile viene trattato con una soluzione acquosa di acido solforico. a) Scrivere
l'equazione chimica ed il meccanismo della reazione, mettendo in evidenza il ruolo dell'ambiente
acido. b) Spiegare l'ordine di reattività che si osserva sottoponendo ad idrolisi acida: benzoato di
etile, p-nitrobenzoato di etile, p-metossibenzoato di etile.
25. Scrivere i meccanismi delle seguenti reazioni: a) cloruro di benzoile + ammoniaca (in eccesso);
b) cloruro di esanoile + cicloesanammina (in eccesso).
26. a) Scrivere l'equazione chimica ed il meccanismo della reazione che avviene trattando il
propanoato di etile con etossido di sodio in etanolo. b) Dire se il 2,2-dimetilpropanoato di etile è più
o meno reattivo del propanoato di etile nella stessa reazione e spiegare perché.
27. a) Scrivere il meccanismo della reazione del cloruro di propanoile con bromuro di
fenilmagnesio. b) Scrivere il meccanismo della reazione del cloruro di propanoile con dietilcadmio;
c) il prodotto della reazione (b) si ottiene anche trattando il cloruro di propanoile con dietilcuprato di
litio: scrivere un meccanismo plausibile.
PER APPLICARE LE REAZIONI STUDIATE
28. Indicate come potete preparare i seguenti esteri, a partire da un cloruro acilico ed un alcool: a)
propanoato di etile; b) 3-metilesanoato di fenile; c) benzoato di benzile; d) cicloesancarbossilato di
ciclopropile.
29. Indicare come, partendo dagli opportuni cloruri acilici ed ammine si possano preparare le
seguenti ammidi: a) N,N-dimetiletanammide; b) acetanilide (= N-feniletanammide); c)
cicloesancarbammide.
30. Indicare come si possono sintetizzare i seguenti composti, (1) a partire da cloruro di benzoile e
tutti i reagenti necessari, (2) a partire da acido benzoico e tutti i reagenti necessari: a) N,Ndimetilbenzammide; b) benzoato di isopropile; c) benzoato di metile.
31. Scrivere le reazioni con cui è possibile trasformare l'etanoato di metile in: a) acido acetico; b)
etanolo; c) acetato di sodio; d) alcool terz-butilico; e) N-metiletanammide.
32. Indicate come si possa ottenere: a) l'acido esanoico dall'1-bromopentano; b) l'acido 2idrossiesanoico dal pentanale; c) l'N-metil-N-cicloesiletanammide dall'acido acetico.
33. Mostrare come si possono preparare i seguenti composti, a partire dagli opportuni cloruri acilici
e composti organometallici: a) 1-fenil-1-pentanone; b) 2-fenil-2-propanolo.
34. Gli acidi carbossilici reagiscono con due equivalenti di composto litioorganico, dando chetoni.
a) Scrivere un meccanismo plausibile per la reazione; b) scrivere la reazione dell'acido benzoico con
etillitio.
35. Mostrare come i seguenti chetoni si possano ottenere dagli acidi indicati: a) 1-fenil-1-propanone
da acido propanoico (due modi, uno dei quali un'acilazione di Friedel-Crafts); b) cicloesil metil
chetone, da acido cicloesancarbossilico.
36. Scrivere le reazioni che, partendo dagli opportuni alogenuri alchilici e cloruri acilici portano ai
seguenti chetoni, utilizzando cadmio-organici e/o cuprati: a) fenil isopropil chetone; b)
acetilcicloesano; c) 2,2-dimetil-3-pentanone; d) 2-fenil-4-metil-3-pentanone; e) 1-fenil-2-butanone;
f) 2-metil-3-pentanone; g) 1-fenil-2,2,4-trimetil-3-pentanone.
.
37. Un doppio legame coniugato con un carbonile aldeidico o chetonico può subire attacco da parte
di un reattivo di Grignard sulla posizione β. Che prodotti vi aspettate per reazione dell'acido 2pentenoico con bromuro di fenilmagnesio? [non siate precipitosi...].
38. Scrivere le reazioni che permettono di ottenere i seguenti alcooli, a partire dal propanoato di
metile: a) 2-metil-2-butanolo; b) 3-etil-3-pentanolo; c) 1,1-difenil-1-propanolo; d) 3-etil-2,4-dimetil3-pentanolo.
39. Mostrare come si possano effettuare le seguenti trasformazioni: a) da trans-1-bromo-2-butene ad
acido trans-3-pentenoico (due modi); b) da acido pentanoico a pentanoato di metile (due modi); c)
da 2-butenale ad acido 2-butenoico; d) da acido esanoico ad esanale; e) da 3-esene ad acido
propanoico (suggerimento: riguardare le reazioni degli alcheni...); f) da acido ciclopentancarbos-
silico a ciclopentilmetanolo; g) da acido 3-fenilpropanoico ad acido 2-ammino3-fenilpropanoico; h)
da 2-feniletanolo ad acido 3-fenilpropanoico; i) da metilenecicloesano ad acido 1metilcicloesancarbossilico; j) da metilenecicloesano ad acido cicloesiletanoico; k) da etanoato di
etile a 3-metil-3-pentanolo; l) da bromocicloesano a dicicloesilmetanolo; m) da metossibenzene a pmetossibenzammide.
40. Completare le seguenti reazioni, specificando i reagenti che occorrono per ciascuna trasformazione: a) alcool benzilico → cloruro di benzile → fenilacetonitrile → acido fenilacetico; b) cloruro
di terz-butile → cloruro di terz-butil magnesio → acido 2,2-dimetilpropanoico; c) 1-pentanolo →
acido pentanoico; d) 1-pentanolo → acido esanoico.
41. Per trasformare ciascuno dei seguenti composti nei prodotti richiesti, è necessaria una serie di
reazioni. Alcuni dei prodotti delle reazioni intermedie sono indicati, altri no. Scrivere le reazioni ed i
reagenti: a) 1-esanolo ad acido eptanoico, attraverso l'eptanonitrile; b) 1-esanolo ad acido 2metilesanoico, attraverso il 2-cloroesano.
SPETTROSCOPIA
42. Dalle bottiglie che contenevano tre composti, un acido carbossilico e due esteri, di formula
molecolare C8H8O, si sono staccate le etichette. I composti sono stati provvisoriamente chiamati A,
B e C e si sono fatti gli spettri riportati di seguito. Sulla base degli spettri, identificate i composti e ...
rimettete a posto le etichette.
A
B
C
solo per chi ha superato i tre compiti: PER L’ORALE (per gli appelli ufficiali anche questi sono
per lo scritto)
42. Scrivere i prodotti (specificandone il nome) che si ottengono quando l'acido butanoico viene
fatto reagire con ciascuno dei seguenti composti: a) PBr3 e bromo; b) dicicloesilcarbodiimmide e
poi etanammina; c) diazometano
43. Scrivere il meccanismo della reazione dell'acido propanoico con Br2, PBr3.
44. Scrivere equazione chimica e meccanismo della reazione tra butanammide ed ipobromito di
sodio (trasposizione di Hofmann). b) Il composto ottenuto in (a) si può avere anche per riduzione
dell'opportuno nitrile: scrivere la reazione corrispondente.
45. Scrivere le equazioni chimiche relative alle seguenti reazioni: a) acido propanoico + bromo e
PBr3; b) il composto (a) + ammoniaca (eccesso).
46. Completare le seguenti reazioni, specificando il nome dei prodotti organici: a) 3-fenilpropanoato
di argento + Br2, sottoposto a riscaldamento; b) ciclobutancarbossilato di piombo + I2, sottoposto a
riscaldamento; c) decanoato d'argento + bromo, a caldo; e) acido cicloottancarbossilico + ossido di
mercurio + bromo (suggerimento: prima far reagire HgO con l'acido). Scrivere il meccanismo in un
caso.
47. Scrivere il meccanismo della decarbossilazione dell'acido 2-etilpropandioico.
48. Completare le seguenti serie di reazioni, specificando i nomi dei composti organici che si
ottengono: a) acido acetico + SOCl2 → A; A + 2-propanammina → B. b) Acido cicloesancarbossilico + PCl3 → C; C + 2-butanolo → D. c) Acido 2-etilpentanoico + SOCl2 → E; E + metantiolo
F. d) Malonato dietilico (= propandioato dietilico) + acqua e acido → G; G sottoposto a riscaldamento → H. e) Anidride butandioica + metanolo (un equivalente) → I; I + SOCl2 → J; J + fenolo,
in presenza di piridina → K.
49. Scrivere i risultati attesi per la reazione di ciascuna delle seguenti molecole (o combinazioni di
molecole) con etossido di sodio in etanolo: a) butanoato di etile; b) 3-fenilbutanoato di etile; c) 3fenil-2-metilpropanoato di etile; d) esandioato dietilico; e) feniletanoato di etile + metanoato di etile;
f) benzoato di etile + butanoato di etile.
50. Come è possibile preparare i seguenti chetoni, servendosi della sintesi con l'estere acetoacetico?
a) 5-metil-2-esanone; b) ciclobutil metil chetone; c) 3-benzil-5-esen-2-one.
51. Come è possibile preparare i seguenti acidi, servendosi della sintesi con il malonato dietilico? a)
acido ciclopentancarbossilico; b) acido ottandioico; c) acido butandioico; d) acido 2-benzilesanoico.
52. Preparare i seguenti composti ( a partire dal malonato dietilico o dall'estere acetoacetico): a)
acido 2-metilbutandioico; b) 4-fenil-2-butanone; c) acido 3-ciclopentilpropanoico; d) acido 2-(3ossociclopentil)etanoico.
53. Come si può ottenere, dall'estere acetoacetico, il 3-chetoestere 1-acetilciclopentancarbossilato di
etile?
54. I seguenti chetoni non possono essere sintetizzati con il metodo dell'estere acetoacetico
(perché?), ma si possono preparare con una variante che prepara (condensazione di Claisen) ed
utilizza un 3-chetoestere opportuno, RCOCH2CO2CH2CH3, dove R è il gruppo che compare nel
chetone finale. Preparare i seguenti chetoni ed i 3-chetoesteri necessari per la loro sintesi: a) 3pentanone: b) 1-fenil-2-metil-3-esanone.
55. Completare le seguenti reazioni, scrivendo le strutture per ciascuno dei composti indicati: a)
estere malonico (in eccesso) con etossido di sodio e 1,2-dibromoetano → C16H26O8; b) C16H26O8
con etossido di sodio e 1,2-dibromoetano → C18H28O8; c) C18H28O8 + OH-, poi H+ ed infine
riscaldamento → C8H12O4.