Responsabile:
Dott. Massimo Valsecchi
Redazione:
NEWSLETTER
N. 3 - 2014
D.ssa Giuseppina Napoletano
[email protected] t
Dott. Federico Gobbi
[email protected]
Dott.ssa Emma Conti
[email protected]
Dott.ssa Chiara Postiglione
[email protected]
Recapiti:
tel. 045 8075918 – 5093
tel. 045 601 3563
Le newsletter e gli aggiornamenti in
epidemiologia sono reperibili nel sito
della Regione del Veneto al seguente
indirizzo:
http://www.regione.veneto.it/web/sanita/
viaggiare-in-salute
Nel sito del Dipartimento di Prevenzione
ULSS 20 all’indirizzo:
http://prevenzione.ulss20.verona.it/viagn
ews.html
Ha partecipato alla stesura di questa
newsletter la Dott.ssa Francesca Tognon
Supporto tecnico:
Lucrezia Tognon
Andrea Comin
AMEBA
Caso clinico
Un uomo di 35 anni si reca in guardia medica riferendo da circa 3 giorni una
fastidiosa sintomatologia caratterizzata da astenia intensa, nausea e dolore
addominale, meglio definito come senso di pesantezza al quadrante alto destro
dell’addome, che si irradia con una sensazione di dolore anche alla spalla destra.
Inoltre riferisce riscontro di puntate febbrili.
Il medico, visitato il paziente e riscontratagli una temperatura di 39°C, ritiene
opportuno inviarlo in Pronto Soccorso per effettuare accertamenti sierologici e
strumentali. Il paziente arriva così, attraverso il Pronto Soccorso, alla valutazione di
uno specialista infettivologo che di fronte ad un paziente con febbre accompagnata
da astenia intensa e sintomatologia gastro-intestinale effettua una domanda molto
importante per definire il quadro diagnostico: ha effettuato viaggi all’estero negli
ultimi 3 mesi? Il paziente riferisce di avere trascorso, circa un mese prima, 10 giorni
in Kenya per vacanza. Il primo test effettuato è una ricerca malaria, risultata
negativa. Si procede comunque al ricovero per ulteriori indagini.
Vengono effettuati esami ematochimici che mostrano alterazione degli indici di
flogosi con emocromo e formula nella norma, esami copro parassitologici che
risultano negativi; RX torace che non mostra niente di patologico; una ecografia
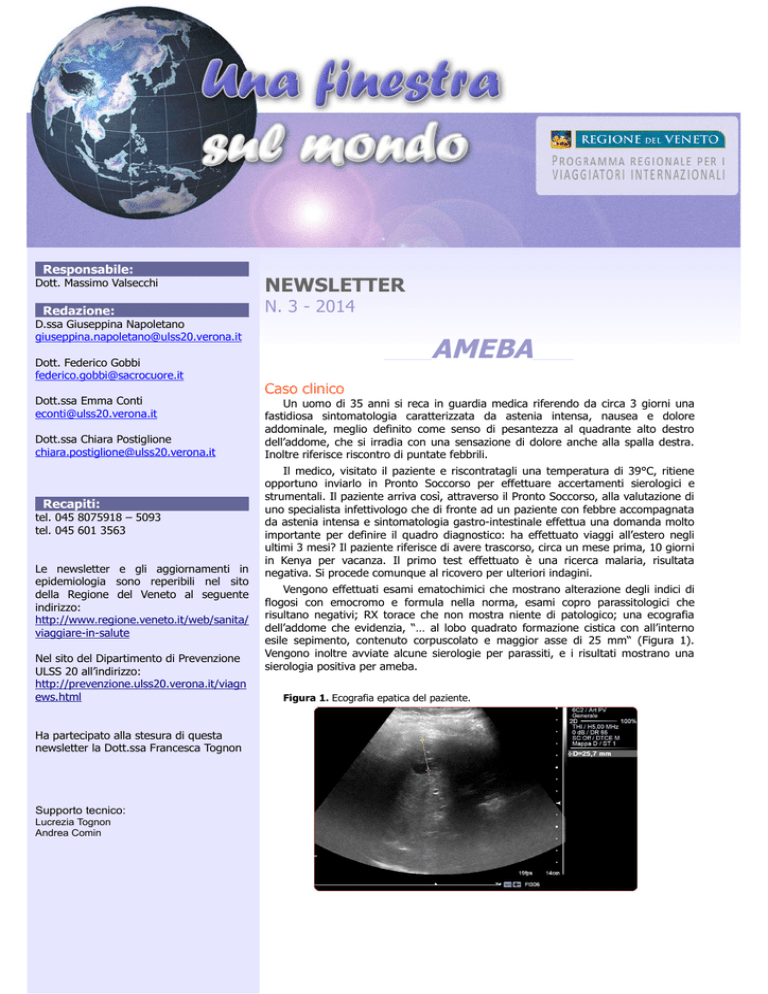
dell’addome che evidenzia, “… al lobo quadrato formazione cistica con all’interno
esile sepimento, contenuto corpuscolato e maggior asse di 25 mm“ (Figura 1).
Vengono inoltre avviate alcune sierologie per parassiti, e i risultati mostrano una
sierologia positiva per ameba.
Figura 1. Ecografia epatica del paziente.
Una finestra sul mondo
Si interroga il paziente sulle abitudini alimentari tenute durante il suo soggiorno
in Kenya, egli riferisce di avere sempre bevuto bevande da bottiglie sigillate e
mangiato pesce e verdure soltanto ben cotti. Riferisce però di avere consumato
macedonia di frutta già preparata… e di avere ogni tanto bevuto cocktail contenenti
cubetti di ghiaccio…
Si somministra quindi terapia specifica e si programmano con il paziente
appuntamenti successivi alla dimissione per il controllo ecografico del fegato.
ENTAMEBIASI
L’entamebiasi è l’infestazione causata da Entamoeba histolytica, protozoo
parassita intestinale obbligato. E’ dimostrata l’esistenza in natura di due specie
biologicamente ben differenziate ma morfologicamente identiche:
Entamoeba histolytica appunto, dotata di potere patogeno e in grado di dare
una malattia con grande variabilità clinica (dalle forme intestinali acute alle
complicanze extraintestinali potenzialmente fatali) e Entamoeba dispar che resta
sempre solo un semplice commensale intestinale. Nel descrivere le caratteristiche
morfologiche del parassita si parla quindi del complesso E. histolytica/E. dispar
(Eh/Ed).
Il parassita
L’Entameba presenta due stadi biologici, il trofozoita e la cisti.
I trofozoiti hanno dimensioni molto variabili da 14-16 µm ad un massimo di 5060 µm; le forme patogene che danno i segni della malattia sono di dimensioni
maggiori delle forme ritrovate nei portatori asintomatici.
I trofozoiti sono estremamente mobili grazie all’emissione di pseudopodi
globosi. Tale mobilità è influenzata da PH, temperatura e osmolarità del mezzo
ambiente ed è tipicamente monodirezionale e più veloce nelle forme patogene.
Il citoplasma presenta una porzione più periferica detta ectoplasma e una più
interna, l’endoplasma, che contiene il nucleo e numerosi vacuoli. (Figure 2a, 2b, 3 e
4).
Figura 2: Trofozoite di E. histolytica /E. dispar colorato con colorazione di iodio (2a) e
con colorazione tricromica (2b).
Fig. 2a
Fig. 2b
3 - 2014 – Ameba
2
Una finestra sul mondo
Figura 3: Trofozoiti di E. histolytica con eritrociti ingeriti, colorazione tricromica. Gli
eritrociti ingeriti appaiono come inclusioni scure. I parassiti mostrano nuclei con il tipico
piccolo cariosoma centrale e sottili filamenti di cromatina periferici.
Figura 4: Entamoeba histolytica: trofozoiti su sezione istologica di colon colorato con
ematossilina/eosina.
Le cisti mature di Eh/Ed sono tipicamente tetranucleate, hanno forma sferica od
ovalare e diametro massimo di 16-20 µm e rappresentano sia la forma infettante
che di resistenza ambientale. Sono in grado di rimanere vitali per varie settimane
nell’ambiente esterno. Lo sviluppo delle forme cistiche passa da uno stadio monobinucleato ad uno finale tetranucleato (l’unico con capacità infettante) che si può
completare già a livello dell’intestino, o nell’ambiente esterno con adeguate
condizioni di temperatura, Ph e umidità (Figure 5a, 5b e 6).
Figura 5: Cisti di E. histolytica/E. dispar con colorazione iodata (5a) e colorazione
tricromica (5b). La freccia evidenzia il corpo cromatoide, aggregato di ribosomi, tipico delle
forme immature.
Fig. 5a
3 - 2014 – Ameba
3
Una finestra sul mondo
Fig. 5b
Figura 6: Cisti di E. histolytica/dispar con colorazione tricromica. Sono visibili tre nuclei
(indicati con le frecce nere) e il corpo cromatoide con le tipiche estremità smussate (freccia
rossa).
Ciclo biologico
Il ciclo biologico inizia con l’ingestione di cisti inquinanti acqua o vegetali crudi.
Nello stomaco la parete cistica viene parzialmente digerita; la cisti arriva nel
duodeno e qui, da ogni cisti fuoriescono 4 piccoli trofozoiti che a loro volta si
dividono in 8 amebe che continuano il loro percorso nell’intestino fino ad arrivare al
cieco e al colon ascendente, dove trovano l’ambiente adatto alla maturazione
completa e si moltiplicano ripetutamente.
Nel tratto terminale del colon e nel sigma le condizioni ambientali cambiano e il
parassita si incista di nuovo e si ha così l’eliminazione di cisti con le feci.
Nelle forme diarroiche o dissenteriche è possibile trovare nelle feci anche le
forme vegetative.
Le complicanze extraintestinali, sempre secondarie ad una amebiasi intestinale
invasiva, sono dovute ad una disseminazione per via ematogena delle forme
vegetative amebiche: i trofozoiti di E. histolytica producono ulcerazioni della parete
intestinale attraverso le quali i trofozoiti stessi entrano nei capillari e migrano fino al
sistema circolatorio portale. (figura 7).
3 - 2014 – Ameba
4
Una finestra sul mondo
Figura 7: Cisti e trofozoiti sono eliminate attraverso le feci . Le cisti si trovano
tipicamente in feci formate, i trofozoiti in feci diarroiche. L’infestazione da Entamoeba
histolytica avviene per ingestione di cisti mature attraverso cibo, acqua o contatto con
mani contaminati. L’escistamento avviene nel piccolo intestino e vengono rilasciati i
trofozoiti , che migrano nel piccolo intestino. I trofozoiti si moltiplicano attraverso scissione
binaria e produzione di cisti , ed entrambi questi stadi passano nelle feci .
Grazie alla protezione conferita dalla loro parete, le cisti possono sopravvivere da giorni a
settimane nell’ambiente esterno e sono responsabili della trasmissione. I trofozoiti eliminati
con le feci sono rapidamente distrutti una volta fuori dall’organismo, e se ingeriti, non
sopravvivono all’ambiente gastrico.
In molti casi I trofozoiti restano confinati al lume intestinale ( A : infezione non invasiva) di
individui che sono portatori asintomatici e che eliminano le cisti con le loro feci. In alcuni
pazienti i trofozoiti invadono la mucosa intestinale ( B
malattia intestinale), oppure,
attraverso il circolo sanguigno, siti extraintestinali come il fegato, il cervello, e i polmoni ( C :
malattia extraintestinale), con le conseguenti manifestazioni patologiche. La forma invasiva è
data da E. histolytica e la forma non invasiva da E. dispar. Le due specie sono
morfologicamente indistinguibili se non per il fatto che a volte in E. histolytica si osservano
globuli rossi ingeriti (eritrofagocitosi). La trasmissione può avvenire anche attraverso
l’esposizione a materiale fecale durante pratiche sessuali (in tal caso non solo le cisti, ma
anche i trofozoiti potrebbero rivelarsi infestanti).
3 - 2014 – Ameba
5
Una finestra sul mondo
Epidemiologia
Il complesso Eh/Ed ha diffusione ubiquitaria, con aree di iperendemia nelle zone
della fascia intertropicale a basso tenore socio-economico e sanitario. Centro e sud
America, India ed Africa sono le regioni a più alta endemia. Si stima che circa 500
milioni di soggetti al mondo risultino semplici portatori di infezione o siano affetti da
malattia amebica, con 40 milioni di persone infettate ogni anno. Di queste, solo il
10-12% sviluppa forme cliniche di malattia. La malattia da E. histolytica causa da
40000 a 100000 morti ogni anno per infezione colitica o extraintestinale.
Nelle regioni a bassa endemia la maggior parte dei casi di amebiasi invasiva si
riscontra in immigrati da aree endemiche, ma si possono riscontrare anche in
viaggiatori che effettuano brevi soggiorni nelle suddette regioni. Unico serbatoio e
quindi fonte di infezione è l’uomo, che quando colonizzato elimina cisti nelle feci.
Manifestazioni cliniche
L’infezione da E. histolytica può variare da quadri totalmente asintomatici a
manifestazioni patologiche che coinvolgono solo il distretto intestinale distale (cieco
e colon) senza fenomeni di invasività, fino alla cosiddetta amebosi acuta invasiva o
retto colite amebica dissenterica. Questa, a sua volta, può comportare complicanze
secondarie extraintestinali per veicolazione delle forme vegetative con il circolo
ematico ad altri organi, principalmente il fegato, ma in teoria a qualsiasi altro
distretto corporeo compreso l’encefalo.
Amebiasi asintomatica. E’ una semplice colonizzazione sub-clinica. Nella
maggior parte dei casi la specie in causa è E. dispar, la cui diffusione nell’ambiente
è maggiore dell’E. histolytica: su circa 500 milioni di soggetti infetti il 75-80% delle
colonizzazioni umane sono ascrivibili a E. dispar e solo un 10-15% a E. histolytica.
Indagare le forme sub-cliniche facendo diagnosi di specie ha importanti ricadute dal
punto di vista epidemiologico e terapeutico. Infatti E. histolytica ha una elevata
potenzialità patogena per cui identificare e trattare i portatori, seppure asintomatici,
è importante in termini di salute pubblica.
Colite amebica non invasiva. La sintomatologia è soprattutto soggettiva con
diarrea contenuta e alvo irregolare, modico tenesmo, addominalgie saltuarie. E’
osservata soprattutto in soggetti autoctoni di zone endemiche che hanno già avuto
ripetuti contatti con il protozoo e che riescono a contenerne il quadro clinico.
Rettocolite acuta dissenterica. E’ il quadro clinico che caratterizza più
spesso l’amebiasi sintomatica (80-90% dei casi) e che si osserva nei soggetti che
sono al primo contatto con il parassita: bambini nei primi anni di vita, specie se ipomalnutriti, viaggiatori provenienti da area non endemica. L’esordio sintomatologico
è caratterizzato da crampi addominali, inappetenza, malessere generale e nell’arco
di alcune settimane può complicarsi con dolori addominali più intensi e frequenti, e
diarrea. Solitamente non c’è vomito e raramente c’è febbre. Con il passare di giorni
o settimane l’alvo da diarroico diventa dissenterico con presenza macroscopica di
sangue e muco. Questo pone diagnosi differenziale con altri patogeni invasivi
(Shigella spp, Salmonella spp, Campylobacter spp, E. coli enteroinvasivo ed
enteroemorragico) e altre cause non infettive come le malattie infiammatorie
croniche intestinali. La complicanza più frequente, seria e precoce, di questa forma
clinica è la perforazione intestinale con conseguente peritonite batterica, mentre
sono rari i quadri emorragici di una certa entità.
Colite amebica fulminante. Caratterizzata da profusa dissenteria, iperpiressia
e addominalgie, e sfociante in colite necrotizzante. Questa forma iperacuta è
fortunatamente rara e coinvolge per lo più i pazienti pediatrici. La morte
sopravviene nel giro di pochi giorni per perforazione e peritonite oppure per
megacolon tossico.
Ameboma. In non più del 1% dei pazienti con un’amebiasi intestinale attiva
può svilupparsi una reazione granulomatosa cospicua che nell’arco di alcune
settimane o pochi mesi porta alla formazione di una massa “tumor-like” che tende
ad estendersi verso il lume intestinale ed è denominata ameboma. In una certa
percentuale dei casi l’ameboma può svilupparsi in corso di infezione asintomatica e
in quel caso la diagnosi differenziale con una neoplasia si rende molto difficile, e
dirimenti saranno una sierologia e una valutazione istologica.
3 - 2014 – Ameba
6
Una finestra sul mondo
Amebiasi extra-intestinale. E’ sempre secondaria ad una retto-colite invasiva
e la patogenesi è da riferirsi alla veicolazione dei protozoi in forma vegetativa con il
torrente circolatorio. L’organo più frequentemente coinvolto è il fegato (80% dei
casi), verosimilmente attraverso la via ematogena portale che tende a far sì che il
parassita si localizzi prevalentemente al lobo destro. Entrando nella circolazione
portale i trofozoiti raggiungono e ostruiscono le venule portali intraepatiche e
digeriscono gli epatociti con enzimi proteolitici. Epatociti necrotici e detriti cellulari si
agglomerano a formare una cavità ascessuale contenente un fluido omogeneo di
color marrone classicamente definito “a pasta di acciuga”.
Gli ascessi epatici di solito insorgono da 2 a 5 mesi dopo il viaggio o il soggiorno
in area endemica, ma i sintomi possono manifestarsi anche prima e fino ad anni
dopo l’esposizione. Di solito non vi è alcuna concomitante colite amebica e la
diarrea è presente solo dal 18% al 33% dei casi al momento della diagnosi di
ascesso. Tra l’85% e il 90% dei pazienti presenta febbre e dolore ai quadranti
addominali di destra, iniziato di solito da non più di 10 giorni. Il dolore addominale
è il sintomo più precoce, descritto come una sensazione di peso in ipocondrio
destro, in zona sub-costale o in epigastrio e che può evolvere in un forte dolore che
si irradia alla spalla, al collo o alla schiena.
Può manifestarsi anche solo una sintomatologia sub-acuta caratterizzata da
nausea, inappetenza, febbricola. E’ presente epatomegalia dal 30 al 50% dei casi.
L’ascesso può comportarsi come una massa epigastrica ed esercitare una
compressione diaframmatica che si manifesta con dispnea. Molti pazienti
presentano rialzo dell’emidiaframma destro alla radiografia del torace e dal 10 al
30% dei casi lamentano tosse. Dal punto di vista bio-umorale si rileva leucocitosi
non eosinofila, anemia di grado medio-moderato e VES elevata. Può esserci un
lieve rialzo di transaminasi.
Solitamente non è presente ittero e quando è presente, è marker di uno stadio
di malattia più avanzata (pazienti con ascessi multipli o di grandi dimensioni). Una
corretta valutazione ecografica può indirizzare la diagnosi in un’elevata percentuale
di casi: l’indagine rileva una o più lacune pseudo-ascessuali, più spesso come detto
a livello del lobo destro caratterizzate da margini irregolari e completamente
sprovviste di pareti; le dimensioni sono molto variabili, la localizzazione, tipicamente
parenchimale, può spingersi fino alla zona sotto-capsulare. La mortalità è inferiore
all'1% con trattamento precoce, ma varia da 2% a 18% a seconda del contesto
clinico.
Le complicanze sono legate principalmente a rottura dell’ascesso. La rottura in
peritoneo avviene nel 2-7% dei casi e si manifesta con peritonite acuta seguita da
shock. La rottura in pericardio è rara ma può verificarsi con ascessi del lobo sinistro
ed è associata con pericardite, tamponamento cardiaco e un tasso di mortalità del
30%. Il coinvolgimento pleuro-polmonare, oltre che primario, può essere spesso
secondario ad una iniziale azione litica erosiva del protozoo nei confronti del
diaframma, dove si apre un varco per contiguità. La rottura in diaframma esita in
una amebiasi pleuropolmonare nel 10-20% dei casi e può essere complicata da
empiema e fistolizzazione epato-bronchiale. La rottura di ascesso nello spazio
pleurale con formazione di empiema è la complicanza più temibile, con mortalità
che raggiunge il 15-30% dei casi.
L’entamebiasi cerebrale, solitamente di riscontro autoptico, si osserva nel 1-2%
delle forme extraintestinali e la possibilità che vi sia un coinvolgimento encefalico va
tenuto in considerazione in tutti i casi di pazienti con amebiasi acuta che sviluppino
alterazione del quadro cognitivo e accusino anche cefalea, vomito, vertigini.
Tuttavia dall’introduzione dei derivati 5-nitroimidazolici in terapia, vista la loro
capacità di superare la barriera emato-encefalica, questo tipo di complicanza è
diventata sempre più rara.
Il coinvolgimento renale è raro e conseguente ad una estensione di una lesione
amebica epatica o ad una perforazione colonica peritoneale. Quest’ultima può
essere anche all’origine di un interessamento splenico, a sua volta anche
secondario ad una localizzazione epatica al lobo destro.
In pazienti malati che permettono che il quadro patologico si aggravi, anche in
relazione al basso livello igienico-sanitario che contraddistingue alcuni Paesi
endemici, si possono osservare forme di amebiasi cutanea o cutaneo-mucosa per
contiguità a livello perineale e genitale, contraddistinte da ulcerazioni estese e
molto dolorose, anch’esse ricche di protozoi.
3 - 2014 – Ameba
7
Una finestra sul mondo
Diagnosi
•
Esame microscopico diretto delle feci, preferibilmente su più campioni e dopo
metodiche di concentrazione per la ricerca di forme cistiche ed eventualmente
di trofozoiti su feci diarroiche. L’osservazione va fatta su preparati a fresco,
integrata eventualmente da colorazioni estemporanee (Lugol, Sargeaunt) e,
soprattutto, permanenti (tricromica, ematossilina ferrica). In questo modo si
possono distinguere le forme del complesso Eh/Ed dalle altre amebe non
patogene. Distinguere invece histolytica da dispar solo all’osservazione
morfologica non è possibile a meno che non si ritrovino trofozoiti con emazie
fagocitate intracitoplasmatiche, caratteristica specifica di E. histolytica.
•
Isolamento colturale da campioni di feci concentrati: questo esame risulta più
sensibile dell’esame diretto, ma non viene eseguito routinariamente in molti
laboratori per la complessità di preparazione del terreno richiesto per la
coltura. Sulla coltura inoltre è possibile effettuare in Centri di Riferimento la
tipizzazione isoenzimatica sec. Sargeaunt mediante gel-elettroforesi di 4
enzimi per differenziare, nell’ambito del genere histolytica, le popolazioni più o
meno patogene.
•
Ricerca antigenica su campione di feci. Si tratta di test ELISA, alcuni
permettono la rilevazione del complesso Ed/Eh, senza distinguere tra le due
forme, altri test permettono la differenziazione esclusivamente di E.
histolytica. Tuttavia tali test sono poco sensibili, infatti gli antigeni ricercati
sono espressi solo sulla membrana di trofozoiti e non delle cisti che possono
essere le uniche forme presenti in caso di infezione asintomatica.
•
Tecniche molecolari di PCR quali e quantitative su feci. Con metodiche di
“multiple PCR” è possibile identificare e tipizzare le due diverse specie.
•
Ricerca anticorpale su siero. Di solito una risposta anticorpale a titolo elevato
si sviluppa in corso di infezione da E. histolytica, ma non da E. dispar che dà
invece positività più deboli.
•
La diagnosi di ascesso epatico amebico viene posta con esame ecografico
(figura 8), che ha una sensibilità maggiore del 90%. Diagnosi differenziale va
fatta con ascessi piogeni batterici, la causa più comune di ascessi epatici in
zone dove non è endemica l’ameba. Di solito gli ascessi piogeni sono più
frequentemente multipli, insorgono in persone di età più elevata e che
presentano anche segni sistemici di infezione batterica. In caso di ascesso
epatico amebico la sierologia su sangue risulta fortemente positiva nel 8595% dopo una o più settimane dall’inizio dei sintomi. Può essere indicata
anche l’analisi del liquido ascessuale aspirato, sul quale è possibile effettuare
tecniche di sierologia e di biologia molecolare.
Figura 8 a e b: esempi di ascessi amebici del fegato all’ecografia.
Fig. 8a
3 - 2014 – Ameba
8
Una finestra sul mondo
Fig. 8b
Terapia
Nelle forme sintomatiche di amebiasi acuta ed in quelle extraintestinali i farmaci
di prima scelta sono i derivati 5-nitroimidazolici:
•
Metronidazolo in ciclo di 750 mg x 2 /die per 14 giorni oppure
•
Tinidazolo in dose di 2 g / die per 3-5 giorni
A tale trattamento va fatto seguire un ciclo di terapia con un amebicida luminale
per evitare che forme cistiche vitali possano residuare in qualche plica intestinale,
reiterando eventualmente a distanza anche di mesi la malattia. Si procede quindi
con
•
Paromomicina solfato 1.5-2 g/die in tre-quattro somministrazioni refratte
per ciclo di 7 giorni.
Nelle infezioni in cui si sia potuto accertare che la specie in causa è sicuramente
dispar, il trattamento non è richiesto; al contrario nei portatori asintomatici di
histolytica è indicato il trattamento, soprattutto per motivi di salute della comunità.
Diversi studi, tra cui una review Cochrane del 2009, hanno evidenziato che non
ci sono evidenze di vantaggio nel drenare un ascesso epatico amebico non
complicato, rispetto al solo trattamento farmacologico per os. Pertanto solo per le
formazioni ascessuali a rischio di rottura (sottocapsulari, di diametro ≥ 8-10 cm) è
opportuno ricorrere anche allo svuotamento della zona ascessualizzata,
eventualmente integrato da immissione “in loco” di un nitroimidazolico in
formazione parenterale.
Prevenzione
Visto che E. histolytica, come molti patogeni diffusi nelle aree del mondo a
basso reddito, ha un ciclo di trasmissione fecale-orale, i viaggiatori e turisti che si
recano in zone tropicali devono aderire a buone norme di igiene alimentare
prestando molta attenzione a cibi crudi (vegetali) e bevande non sigillate “a rischio”
(in particolare l’acqua di rubinetto) o con ghiaccio in cubetti.
La trasmissione interpersonale può essere evitata attuando misure igieniche
personali, come il frequente e accurato lavaggio delle mani e l’uso di guanti per il
personale che opera in strutture pubbliche quali Divisioni di Malattie Infettive
ospedaliere o Istituti di ricovero per pazienti con deficit mentali. Attualmente sono
allo studio vaccini, tra cui uno in formulazione orale che stimola l’immunità cellulare
e mucosale, ma al momento è stato testato solo su animali.
3 - 2014 – Ameba
9
Una finestra sul mondo
Bibliografia
•
Scaglia M., Gatti S., Sargeaunt P.G., Rondanelli E.G. Parassiti e parassitosi
umane . Selecta Medica, pag 141-155.
•
Shannonb N. Moonah, et al., Host Immune Response to Intestinal Amebiasis,
PLOS Pathogens, August 2013/volume 9/Issue 8
•
Cecilia Ximenez et al., Human Amebiasis: Breaking the Paradigm? Int. J.
Environ. Res. Public Health 2010, 7, 1105-1120; doi:10.3390/ijerph7031105
•
Terry Wuerz MD et al., A review of amoebic liver abscess for clinicians in a
nonendemic setting Can J Gastroenterol Vol 26 No 10 October 2012
•
Wilson W. Chan et al., Parasitic Liver Disease in Travelers Infect Dis Clin N Am
26 (2012) 755-780 http://dx.doi.org/10.1016/j.idc.2012.05.006
33- -2014
2014––Ameba
Ameba
10