Prof. Giorgio Sartor
Nucleotidi e coenzimi
Copyright © 2001-2012 by Giorgio Sartor.
Versione 1.6.2 – apr 2012
All rights reserved.
Basi azotate
• Le basi azotate coinvolte nella formazione di
nucleotidi e coenzimi appartengono a due
famiglie principali:
6
5
– Purine
N1
N
7
8
9
3
2
4
N
N
H
4
– Pirimidine
N
2
V.1.6.2 © gsartor 2001-2012
5
3
1
6
N
Nucleotidi e coenzimi
-2-
1
Purine
• Le basi puriniche sono:
NH2
6
Adenina - A
N
N
6-amminopurina
N
N
H
OH
6
Guanina - G
N
N
6-idrossi-2-aminopurina
2
N
H 2N
V.1.6.2 © gsartor 2001-2012
N
H
Nucleotidi e coenzimi
-3-
Purine
• La struttura delle basi puriniche è legata alla
tautomeria cheto-enolica:
H
H3C
O
H 3C
CH3
CH3
H 3C
H
O
CH3
Guanina - G
OH
N
N
H2N
V.1.6.2 © gsartor 2001-2012
N
O
O
N
H
N
HN
H 2N
N
Nucleotidi e coenzimi
N
H
N
HN
HN
N
H
N
H
-4-
2
Pirimidine
• Le basi pirimidiniche sono:
Timina - T
O
CH3
HN
2,4-diidrossi-5-metilpirimidina
O
N
H
NH2
Citosina – C
N
2-idrossi-4-amminopirimidina
O
N
H
O
Uracile - U
HN
2,4-diidrossipirimidina
O
V.1.6.2 © gsartor 2001-2012
N
H
Nucleotidi e coenzimi
-5-
Pirimidine
• Anche la struttura delle basi puriniche è legata
alla tautomeria cheto-enolica:
H
Timina
(Uracile)
H 3C
O
H 3C
CH3
CH3
OH
HO
O
CH3
HN
N
HO
Citosina
O
N
N
H
NH2
N
N
HO
CH3
HN
NH2
V.1.6.2 © gsartor 2001-2012
CH3
O
CH3
N
H
H 3C
O
N
Nucleotidi e coenzimi
O
N
H
-6-
3
Solubilità
• Le basi azotate sono insolubili in acqua, la loro
solubilità è aumentata dal legame con molecole
molto idrosolubili:
CH2OH
O
OH
OH
O
HO
• ribosio
OH
HO
OH
OH
CH2OH
O
• 2-deossiribosio
OH
O
OH
HO
HO
OH
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
-7-
Ribosio e 2-deossiribosio
β-ribosio
CH2OH
O
OH
V.1.6.2 © gsartor 2001-2012
2-deossi-β-ribosio
CH2OH
OH
O
OH
OH
OH
Nucleotidi e coenzimi
-8-
4
Nucleosidi
• Il legame si forma tra il C1 dello zucchero e con
l’atomo di azoto non coinvolto nella tautomeria.
• Si formano i nucleosidi, in questo caso
l’adenosina.
NH2
NH2
N
N
N
CH2OH
OH
NH2
N
CH2OH
O
N
HO
1'
4'
N
O
OH
O
N
N
H
5'
N
N
N
N
OH
2'
3'
OH
OH
OH
OH
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
-9-
Nucleotidi
• La funzione alcolica primaria rimasta libera può essere
esterificata con l’acido fosforico (fosfoestere), per
esempio con l’adenosina, si ottiene una molecola
idrosolubile e carica. Adenosinmonofosfato (AMP)
NH2
P
O
O
P
HO
O
5'
N
3'
2'
OH
Nucleotidi e coenzimi
N
O
5'
O
1'
4'
OH
V.1.6.2 © gsartor 2001-2012
O
O
O
N
N
O
N
N
O
NH2
N
N
1'
3'
OH
OH
- 10 -
5
Nucleotidi
• Più in generale:
O
P
O
BASE AZOTATA
O
O
BASE AZOTATA
--O3PO
5'
5'
O
O
1'
1'
3'
3'
OH
V.1.6.2 © gsartor 2001-2012
OH
OH
OH
Nucleotidi e coenzimi
- 11 -
Deossinucleotidi
• Più in generale:
O
P
O
O
V.1.6.2 © gsartor 2001-2012
BASE AZOTATA
O
BASE AZOTATA
--O3PO
5'
O
5'
O
1'
3'
3'
OH
OH
Nucleotidi e coenzimi
1'
- 12 -
6
Nucleotidi ciclici
• Anche la funzione alcolica in 3’ può essere esterificata con
una funzione acida libera dello stesso acido fosforico, si
ottengono i nucleotidi ciclici: cAMP
NH2
N
N
N
N
O
5'
O
O
P
O
3'
O
OH
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 13 -
Nucleotidi e acidi nucleici
• Il legame può anche avvenire tra nucleotidi diversi attraverso
esterificazioni in 3’ e 5’ per formare catene polinucleotidiche (acidi
nucleici).
NH
NH
2
Nucleotide
P
O
O
P
O
O
O
N
N
5'
O
NH2
O
N
N
O
O
O
NH2
OH
P
N
N
N
N
5'
O
2
Deossinucleotide
N
N
N
O
O
N
P
O
O
O
O
O
P
Nucleotide
O
Acido ribonucleico (RNA)
V.1.6.2 © gsartor 2001-2012
N
3'
OH
P
N
O
O
3'
O
N
N
Nucleotidi e coenzimi
O
Deossinucleotide
O
Acido deossiribonucleico (DNA)
- 14 -
7
Nucleotidi e acidi nucleici
RNA
V.1.6.2 © gsartor 2001-2012
DNA
Nucleotidi e coenzimi
- 15 -
Nucleotidi liberi
NH2
O
P
O
O
P
O
• I monofosfonucleotidi
hanno la possibilità di
essere ulteriormente
fosforilati per formare i
difosfonucleotidi (ADP) e i
trifosfonucleotidi (ATP)
N
N
O
N
N
O
O
5'
O
1'
3'
OH
OH
NH2
O
O
P
O
O
O
P
O
O
P
O
N
N
O
N
N
O
5'
O
1'
3'
OH
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
OH
- 16 -
8
Nucleotidi liberi
• I monofosfonucleotidi
hanno la possibilità di
essere ulteriormente
fosforilati per formare i
difosfonucleotidi (ADP) e i
trifosfonucleotidi (ATP)
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 17 -
Nucleotidi liberi
• I legami che tengono insieme i residui di
fosfato sono legami di tipo anidridico.
NH2
O
P
O
O
P
O
N
N
O
N
N
O
O
5
O
1
3
OH
O
V.1.6.2 © gsartor 2001-2012
O
O
P
O
OH
O
+ 3H2O
P
O
2
P
OH
O
+ 4 H+
O
Nucleotidi e coenzimi
- 18 -
9
ADP e ATP
• Legami di tipo anidridico
• Legami di tipo fosfoestereo
NH2
O
O
P
P
O
O
O
NH2
N
N
O
N
P
O
O
O
O
OH
P
O
P
O
O
OH
N
N
O
O
OH
ADP
V.1.6.2 © gsartor 2001-2012
N
N
O
N
O
O
O
OH
ATP
Nucleotidi e coenzimi
- 19 -
A cosa servono i nucleotidi
• Trasporto di energia
– ATP (GTP), ADP, AMP,
• Segnali intracellulari
– cAMP
• Trasporto di equivalenti ridotti
– NAD+/NADH, NADP+/NADPH
– FAD/FADH2
• Trasporto di acili
– CoA
• …
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 20 -
10
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 21 -
Energia
O
O
P
• ATP
O
O
O
O
P
P
O
N
O
O
O
O
NH 2
N
N
N
HO
OH
∆G0’ = -7.3 kcalmole-1
O
• ADP
O
P
O
O
N
P O
O
O
O
NH2
N
N
N
HO
OH
∆G0’ = -15.3 kcalmole-1
O
• AMP
O
P
N
O
O
O
NH2
N
N
N
HO
• GTP
O
P
O
O
O
O
P
O
OH
O
O
P
N
O
O
O
O
N
N
HO
NH
OH
NH2
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 22 -
11
Trasporto di energia
ATP + H2O → ADP + PO43∆G°’ = -7.3 kcalmole-1 (-30.6 kJmole-1) a pH 7
∆G° = -10 kcalmole-1 (-42 kJmole-1) a pH 9
O
P
O
O
O
O
O
P
O
P
..
O
H
N
O
O
O
O
N
HO
H
O
O
O
P
NH2
N
O
+
O
P
O
N
OH
O
O
N
P O
O
O
O
N
HO
V.1.6.2 © gsartor 2001-2012
NH2
N
N
OH
Nucleotidi e coenzimi
- 23 -
∆G°’
• Il valore di ∆G°’ dipende da:
– Forza ionica
– Concentrazione di Mg++
– Concentrazione di Ca++
• Nelle normali condiziono cellulari vale circa:
-12 kcalmole-1
• I nucleotidi sono contemporaneamente:
–
–
–
–
Stabili
Solubili
Carichi
Reattivi
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 24 -
12
∆G°’
• Altre molecole fosforilate hanno ∆G°’ negativo
O
P
O
O
O
O
P
O
O
O
O
P
O
O
..
O
H
N
O
N
O
P
+
O
O
P
O
O
O
N
P O
O
O
NH2
N
O
N
N
HO
H
O
NH2
N
HO
OH
N
OH
∆G°’ = -7.3 kcalmole-1
O
O
H
H
H
HO
H
OH
HO
H
H
H
HO
OH
O
OH
H
H
+
O P
OH
O
O
O
O
∆G°’ = -3.3 kcalmole-1
H
HO
P
OH
O
O
..
O
H
H
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 25 -
Perché il ∆G°’ dell’ATP vale -30.6 kJmole-1?
• Repulsione tra cariche
– Maggiore in ATP che in ADP
O
O
P
P
O
O
O
P
O
O
O
N
O
O
NH2
N
O
N
N
HO
O
O
P
O
OH
O
O
P
N
O
O
O
NH2
N
N
HO
V.1.6.2 © gsartor 2001-2012
N
OH
Nucleotidi e coenzimi
- 26 -
13
Perché il ∆G°’ dell’ATP vale –7.3 kcalmole-1?
• Stabilizzazione per risonanza
– Del fosfato
3-, H+
O
O
O
P
O
P
O
O
O
O
=
O
P
O
O
P
O
P
O
O
O
O
3-, H+
O
O
O
O
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 27 -
Trasporto di energia
ATP + H2O → AMP + P2O74- → 2PO43∆G0’ = -7.3 kcalmole-1 ∆G0’ = -8 kcalmole-1
O
O
O
P
P
O
O
O
O
P
O
..
O
H
N
O
O
O
N
N
HO
H
NH2
N
OH
O
O
N
P O
O
O
NH2
N
+
N
HO
V.1.6.2 © gsartor 2001-2012
OH
N
O
O
O
P
P
O
O
Nucleotidi e coenzimi
O
O
O
2
O
P
O
O
- 28 -
14
ATP e Mg++
• Nella cellula l’ATP è spesso complessato con lo
ione Mg++
O
O
P
P
O
O
O
O
O
O
P
N
O
O
O
NH2
N
N
HO
Mg++
N
OH
• Per formare un complesso ibridizzato …
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 29 -
Altre molecole “energetiche”
• Hanno ∆G0’ negativo nella reazione di idrolisi del gruppo
fosfato.
∆G°’= -14.8 kcalmole-1
∆G°’= -10.3 kcalmole-1
∆G°’= -10.3 kcalmole-1
O
O
P
O
O
O
N
O
O
H
O
P
P
O
O
H
NH2+
H
H 3C
O
O
O
N
H
O
O
O
Fosfoenolpiruvato
V.1.6.2 © gsartor 2001-2012
Acetilfosfato
Nucleotidi e coenzimi
Fosfocreatina
- 30 -
15
Come si fa a “ricaricare” l’ADP per formare ATP
• Attraverso la catalisi di un enzima (piruvato chinasi)
ADP
PEP
O
O
P
O
O
O
+
H
P
O
O
O
O
N
P O
O
O
O
H
O
O
P
P
O
O
O
O
OH
O
O
O
NH2
N
N
O
OH
N
P O
O
HO
N
OH
ATP
V.1.6.2 © gsartor 2001-2012
piruvato chinasi
N
N
HO
O
NH2
N
+
O
H
H
O
H
H
O
EP
H
O
Piruvato
Nucleotidi e coenzimi
- 31 -
Reazioni accoppiate
• L’idrolisi del fosfato permette, attraverso
l’accoppiamento, ad altre reazioni NON SPONTANEE di
avvenire ugualmente.
• L’ATP viene in genere usato dalla cellula come
trasportatore di fosfati e come donatore di energia
(sottoforma di ∆G).
• Per produrre ATP un modo consiste nell’accoppiarne la
sintesi (da ADP e Pi) all’idrolisi di molecole con ∆G di
idrolisi maggiore (in valore assoluto).
• Tutto ciò avviene attraverso…
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 32 -
16
…gli
V.1.6.2 © gsartor 2001-2012
ENZIMI
Nucleotidi e coenzimi
- 33 -
Enzimi
• Permettono l’accoppiamento di reazioni
chimiche:
–Nello stesso posto
–Nello stesso momento
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 34 -
17
Reazioni accoppiate
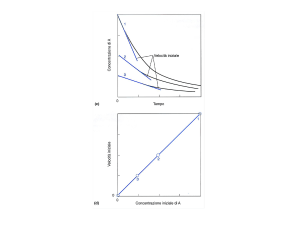
• Consideriamo l’equilibrio
A
[B]eq
Keq =
∆G°' = 4 kcal mole -1
B
= 10
[A]eq
-
∆G°'
RT
= 1.15 10-3 (a 25°C)
• Se la reazione è accoppiata all’idrolisi di ATP attraverso un
enzima:
A + ATP + H2O
B + ADP + Pi + H+
∆G°' = -3.3 kcal mole -1
[B]eq [ADP]eq [Pi]eq
Keq =
[B]eq
[A]eq
V.1.6.2 © gsartor 2001-2012
= 2.67 102
[A]eq [ATP]eq
=
[ATP]eq
[ADP]eq [Pi]eq
Keq
Nucleotidi e coenzimi
- 35 -
Reazioni accoppiate
• Nella cellula il rapporto:
[ATP]
[ADP] [Pi]
[B]eq
[A]eq
~ 500
= 2.67 102 x 500 = 1.34 105
1.34 105
1.15 10-3
~108
• In presenza di idrolisi di ATP la Keq di una reazione può
aumentare di 108 volte;
• Se l’idrolisi di una mole di ATP (-7.3 kcal) non bastano più
moli di ATP possono essere impiegate.
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 36 -
18
Reazioni accoppiate
AeB
• Non sono necessariamente due composti
chimici ma possono essere:
– differenti conformazioni di una molecola;
– differenti concentrazioni di uno ione ai lati di una
membrana,
– ecc…
– … stati iniziali e finali di una TRASFORMAZIONE!
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 37 -
Trasporto di elettroni
NAD+
nicotinamide adenindinucleotide
Acido nicotinico
O
O
OH
NH2
N
H
Nicotinamide
N
O
NH2
N
+
O
O
O
HO
O
P
O
O
P
O O
N
O
OH
NH2
N
N
HO
Nicotinamide
N
OH
Adenina
Dinucleotide
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 38 -
19
Trasporto di elettroni
Come funziona il NAD+
O
H
NH2
+
N
Stato ossidato
O
O
O
HO
O
P
O
O
NAD+
P
O O
N
O
OH
NH2
N
+ H+ + 2eN
N
HO
H
H
(H-)
OH
O
NH2
Stato ridotto
N
O
O
O
HO
O
P
O
O
NADH
P
O O
N
O
OH
NH2
N
N
HO
V.1.6.2 © gsartor 2001-2012
N
OH
Nucleotidi e coenzimi
- 39 -
Trasporto di elettroni
Come funziona il NAD+
Stato ossidato
V.1.6.2 © gsartor 2001-2012
Stato ridotto
Nucleotidi e coenzimi
- 40 -
20
Trasporto di elettroni
H
O
H
NH2
N
O
H
NH2
+ H+ + 2e-
+
N
(H-)
R
R
NAD+
NADH
• Trasporta DUE elettroni per molecola
• Reazione catalizzata dalle DEIDROGENASI
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 41 -
Gliceraldeide-3-fosfato deidrogenasi (EC 1.2.1.12)
∆G°' = +6.3 kJ mol-1
come H
H
3-fosfogliceraldeide
GAP
H
S
O
R
O
H
2
H
Intermedio
tioacetalico
NAD+
OH
CH2OPO3-HPO4
B
3
+
NADH
NAD+
--
NAD+
H
S
H
O
Complesso
Enzima-substrato
O
Intermedio
aciltioestere
R
S
R
H
B
NAD H
O
1
NADH
GAP
NAD+
O
5
OH
CH2OPO3-S
1,3-bifosfoglicerato
1,3BPG
O
NAD+
NAD+
H
+
4
H+
--O3P
B
O
O
S
H
P
O
OH
R
B
PO3-O
O + H+
H
B
+
R
1,3BPG
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 42 -
21
Gliceraldeide-3-fosfato deidrogenasi (EC 1.2.1.12)
NAD+
Cys
carbossimetilata
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 43 -
Trasporto di elettroni
NADP+
nicotinamide adenindinucleotide fosfato
H
O
NH2
+
N
O
O
O
HO
O
P
O
O
P
O
O
N
O
OH
NH2
N
N
HO
O
O
P
N
O
O
Adenina Fosfato
Nicotinamide
Dinucleotide
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 44 -
22
Trasporto di elettroni
FAD (flavinadenindinucleotide)
(Forma ossidata)
O
H3C
N
H3C
N
Base di Shiff
ridotta
NH
N
H
H
Ribosio in
forma aperta
O
H
HO
OH
H
H
HO
O
O
O
P
O
O
P
O O
N
O
NH2
N
N
N
HO
V.1.6.2 © gsartor 2001-2012
OH
Nucleotidi e coenzimi
- 45 -
Trasporto di elettroni
FAD (flavinadenindinucleotide)
(Forma ossidata)
O
H3C
N
H3C
N
Base di Shiff
ridotta
Ribosio in
forma aperta
NH
N
O
H
H
H
HO
OH
H
H
HO
O
O
O
P
O
O
P
O O
N
O
NH2
N
N
HO
V.1.6.2 © gsartor 2001-2012
N
OH
Nucleotidi e coenzimi
- 46 -
23
Trasporto di elettroni
Come funziona il FAD
H
O
H3C
N
H3C
N
H
NH
N
O
H3C
H
O
N
NH
R'
+
R
H3C
H
N
H
R
N
H
H
R'
R
H
+
O
R
FADHz
(ridotto)
FAD
(ossidato)
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 47 -
Trasporto di elettroni
Il FAD è legato alle
proteine,
(in questo caso la
alcolvanillilico ossidasi)
H
H
OH
O
H
O
OH
CH3
Alcool Vanillico
V.1.6.2 © gsartor 2001-2012
O
OH
CH3
Aldeide Vanillica
(Vanillina)
Nucleotidi e coenzimi
- 48 -
24
Trasporto di acili
O
• Gli acili e
R
• gli acetili
H 3C
O
• Vengono trasportati dal coenzima A (CoA)
acido pantotenico
HS
H
H
N
N
ADP
O
H OH
O
P
O H3C CH3
O
O
O
O
P
O O
N
O
NH2
N
β -mercaptoetilamina
N
HO
V.1.6.2 © gsartor 2001-2012
N
OH
Nucleotidi e coenzimi
- 49 -
Trasporto di acili
• Attraverso la formazione di un legame tioestere
O
R
S
H
H
N
N
O
O
H OH
O
O H3C CH3
P
O
O
P
O O
N
O
NH2
N
N
Legame tioestere
V.1.6.2 © gsartor 2001-2012
O
HO
Nucleotidi e coenzimi
N
OH
- 50 -
25
Proteina acil-CoA
• Complesso tra la proteina legante acil-CoA, Coa e
palmitoile
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 51 -
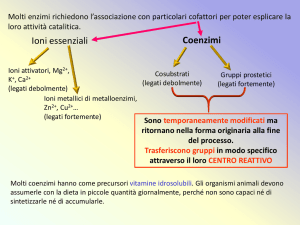
Coenzimi
• Molecole non proteiche legate che permetto a
proteine di svolgere attività enzimatiche:
–
–
–
–
–
–
–
–
–
Tiamina (Vit. B1) → Tiamina pirofosfato
Riboflavina (Vit. B2) → FAD e FMN
Acido Nicotinico (niacina; Vit. B3) → NAD+ e NADP+
Piridossina, piridossale, piridossamina (Vit. B6) →
Piridossalfosfato
Acido pantotenico → Coenzima A
Biotina → legata alla carbossilasi
Acido folico → Tetraidrofolato
Cobalamina (Vit. B12) → coenzimi a cobamide
Acido ascorbico (Vit. C) → antiossidante
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 52 -
26
Tiamina (Vit. B1)
H
N
N
S
+
OH
H3C
N
NH2 CH
3
O
H
N
N
O
S
+
N
O
O
O
O
O
H3C
P
P
NH2 CH
3
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 53 -
Piridossina, piridossale, piridossamina
Piridossalfosfato (Vit. B6)
H
OH
H
OH
HO
N
+
H
H
O
H
OH
HO
CH3
N
H
+
CH3
H
O
P
O
NH2
OH
HO
N
+
CH3
H
H
O
O
OH
O
N
+
CH3
H
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 54 -
27
Piridossina, piridossale, piridossamina
Piridossalfosfato
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 55 -
Biotina
OH
S
O
CH3
H3C
NH
HN
O
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 56 -
28
Acido folico e acido tetraidrofolico
O
N
N
H2N
N
N
O
N
H2N
OH
N
H
O
O
OH
H
N
O
H
OH
N
O
H
O
H
N
N
H
N
H
N
H
H
H
OH
O
H
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 57 -
Cobalamina (Vit. B12)
H2N
O
NH2
O
H3C
H 2N
NH2
O
CH3
H3C
N
O
H3C
H2N
N
H
N
3+
H
Co
N
HN
HO
CH3
NH2
N
R
OH
N
N
CH3
CH3
CH3
CH3
O
O
HO
CNHN
O
H3C
HO
P
O
O
O
OH
H2N
O
HN
CH3
N
CH3
O
HO
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 58 -
29
Acido ascorbico (Vit. C)
OH
O
OH
H
H
HO
O
H
+
H O
H
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 59 -
V.1.6.2 © gsartor 2001-2012
Nucleotidi e coenzimi
- 60 -
30
Crediti e autorizzazioni all’utilizzo
• Questo materiale è stato assemblato da informazioni raccolte dai seguenti testi di Biochimica:
– CHAMPE Pamela , HARVEY Richard , FERRIER Denise R. LE BASI DELLA BIOCHIMICA [ISBN 9788808-17030-9] – Zanichelli
– NELSON David L. , COX Michael M. I PRINCIPI DI BIOCHIMICA DI LEHNINGER - Zanichelli
– GARRETT Reginald H., GRISHAM Charles M. BIOCHIMICA con aspetti molecolari della Biologia
cellulare - Zanichelli
– VOET Donald , VOET Judith G , PRATT Charlotte W FONDAMENTI DI BIOCHIMICA [ISBN 9788808-06879-8] - Zanichelli
• E dalla
–
–
–
–
consultazione di svariate risorse in rete, tra le quali:
Kegg: Kyoto Encyclopedia of Genes and Genomes http://www.genome.ad.jp/kegg/
Brenda: http://www.brenda.uni-koeln.de/
Protein Data Bank: http://www.rcsb.org/pdb/
Rensselaer Polytechnic Institute:
http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb1/MB1index.html
• Il materiale è stato inoltre rivisto e corretto dalla Prof. Giancarla Orlandini dell’Università di Parma alla
quale va il mio sentito ringraziamento.
Questo ed altro materiale può essere reperito a partire da:
http://www.ambra.unibo.it/giorgio.sartor/ oppure da http://www. gsartor.org/
Il materiale di questa presentazione è di libero uso per didattica e ricerca e può essere usato senza
limitazione, purché venga riconosciuto l’autore usando questa frase:
Materiale ottenuto dal Prof. Giorgio Sartor
Università di Bologna a Ravenna
Giorgio Sartor - [email protected]
31