Tematica 6
TEMATICA 6
RADIOFARMACI NELLA DIAGNOSTICA E TERAPIA TUMORALE
Alla realizzazione di questo progetto di Ricerca concorreranno tre unità operative, in cui sono
localizzati gruppi di ricerca con competenze specifiche e complementari, in particolare:
UNITÀ OPERATIVA DI PADOVA,
UNITÀ OPERATIVA DI FERRARA,
UNITÀ OPERATIVA DI SIENA.
Composizione e Settore di Indagine
La Tematica sui radiofarmaci nella diagnostica e terapia tumorale si avvale del contributo delle
Unità di ricerca di Padova, Ferrara e Siena. La ricerca è orientata ai vari aspetti inerenti la
progettazione, la sintesi, la caratterizzazione chimico fisica e la determinazione delle proprietà
biologiche di radiofarmaci sia per il loro impiego nella diagnostica per immagini che nella
radioterapia dei tumori.
Le Unità del CIRCMSB si avvale di innumerevoli collaborazioni con Dipartimenti di diverse
Università italiane ed europee.
UNITÀ DI RICERCA DI PADOVA
E.Zangoni, L.Melendez-Alafort, U.Mazzi
Nuovi analoghi della Somatostatina e derivati della biotina coniugati con agenti chelanti per
l’imaging nucleare e l’applicazione radioterapeutica.
Gli isotopi radioattivi di metalli di transizione offrono molte opportunità nello sviluppo di
radiofarmaci, e tra di essi il tecnezio-99m ed il renio-186/188 giocano un ruolo importante in
ambito, rispettivamente, diagnostico e terapeutico. A differenza di isotopi di atomi naturalmente
presenti nelle molecole biologiche (O, C, N), che possono essere incorporati nelle molecole
direzionatrici attraverso la formazione di un legame covalente, gli isotopi di natura metallica per
essere incorporati nelle biomolecole devono essere stabilizzati da un sistema chelante in un
complesso di coordinazione.
Nell’ultimo decennio è stata sviluppata un’ampia gamma di tecniche per la marcatura di
biomolecole con radiometalli, ma la metodica più ampiamente studiata e impiegata consiste
nell’approccio del chelante bifunzionale (Bifunctional Chelating Agent, BFCA). Il chelante
bifunzionale presenta da un lato un set coordinativo in grado di stabilizzare il metallo, dall’altro un
gruppo funzionale per l’ancoraggio covalente della biomolecola, che può essere diretto oppure
mediato da uno spaziatore (linker), a dare il derivato BFCA(-linker)-BM. La scelta accurata del
BFCA è uno degli aspetti fondamentali nella progettazione di radiofarmaci target-specifici.
BM
Un BFCA ideale dovrebbe garantire la formazione di un complesso con alta resa e a concentrazioni
molto basse del coniugato BFCA-BM. Tale complesso non dovrebbe sottostare a reazioni di
115
Tematica 6
ossidoriduzione, dovrebbe essere termodinamicamente stabile e cineticamente inerte e presentare un
basso numero di isomeri, in quanto tutte questi parametri possono influenzare notevolmente le
caratteristiche biologiche e farmacocinetiche del coniugato BFCA-BM. Infine, l’attacco del BFCA
alla biomolecola dovrebbe essere facilmente realizzabile.
La selezione del BFCA dipende dal tipo di radiometallo e dal suo stato di ossidazione. Il core
[M=O]3+ viene largamente impiegato per la marcatura di biomolecole con 99mTc- e 186/188Re e negli
ultimi 15 anni sono stati sintetizzati e valutati molti chelanti bifunzionali, la maggior parte dei quali
possiede un set coordinativo di tipo NxS(4-x). Questi chelanti, sebbene abbiano trovato applicazione,
soffrono di alcune limitazioni quali l’elevata lipofilia, una scarsa flessibilità strutturale, più forme
isomeriche spesso difficili da separare e limitata stabilità in vivo. Inoltre la loro marcatura richiede
spesso condizioni drastiche. Lo sviluppo di BFCA più efficienti resta quindi uno degli interessi
principali nell’ambito della medicina nucleare.
Con lo sviluppo di un precursore di Tc-99m e di Re-188 prodotto da TcO4- con il Kit denominato
Isolink di struttura M(CO)3(H2O)3+ si è aperta la strada ad una nuova serie di radiofarmaci target
specifici nei quali il tracciante radioattivo viene fissato attraverso una reazione di sostituzione delle
tre molecole di acqua del precursore con differenti serie di set coordinativi uno dei quali porta la
biomolecola. Attraverso tale nuovo approccio sono in corso una notevole quantità di studi per
trovare il complesso più stabile e che venga fissato in una posizione della biomolecola che non
modifichi le sue proprietà sia biologiche generali che quelle che tereminano la sua specificità.
L’Unità del CIRCMSB di Padova nel prossimo triennio sposterà l’obiettivo della ricerca dagli
aspetti prettamente chimici e di ricerca di nuovi complessi di coordinazione del Renio e del
Tecnezio agli aspetti applicativi, ovvero avrà quale primario obiettivo quello di utilizzare i risultati
della precedente ricerca chimica di sintesi e caratterizzazione di complessi di Renio e Tecnezio per
la produzione di radiofarmaci target specifici.
In particolare saranno sviluppati due approcci di marcatura, sperimentati nell’Unita del
CIRCMSB di Padova, uno utilizzante il legante bifunzionale PN2S che stabilizza il metallo in un
complesso neutro di struttura MO(PN2S) e consente contemporaneamente, attraverso il gruppo
carbossilico laterale non coordinato, la facile coniugazione del centro radioattivo ad un gruppo NH2
terminale della biomolecola, ed un altro che utilizza l’approccio del tricarbonile, anch’esso
sperimentato nell’Unità del CIRCMSB di Padova, con il sistema cosìdetto del (2+1) in cui i gruppi
sostituenti le molecole di H2O nel precursore M(CO)3(H2O)3+ sono il dietilditiocarbammato
(chelante bidentato SS) e un gruppo fosfinico (P) che è coniugato alla biomolecola.
Tali approcci di marcatura dovranno essere adattati alle biomolecole in funzione della loro struttura
ed in funzione delle loro proprietà biologiche ed ogni radiofarmaco verrà testato in vitro ed in vivo
per determinare la possibile applicazione nell’imaging diagnostico, se il radionuclide è il Tc-99m o
nella radioterapia se il radionuclide è il Re-188.
R'
O
O
O
NH
PN 2S
NH
HN
HN
NH
H
O
NH
O
H
O
H
N
NH
HO
N
H
HO
O
CH 3
R
NH 2
1
Figure 1. X = L -Phe (1), X = L-1Nal (2)
E’ nostra intenzione utilizzare le metodologie messe a punto dall’Unità di ricerca di Padova nel
campo delle infezioni, marcando una molecola peptidica quale l’UBI29–41 che ha già evidenziato con
116
Tematica 6
la marcatura diretta (99mTc-UBI29–41) una buona fissazione nei siti di infezione ed insieme una
rapida e prevalente escrezione renale e la mancanza di effetti collaterali .
Ma gli sforzi maggiori saranno orientati verso il progetto legato alla marcatura con Tc-99m e
Re-188 di nuovi analoghi della somatostatina per l’imaging nucleare e l’applicazione
radioterapeutica dei tumori esprimenti recettori SSTR1-5. Uno dei derivati già in corso di studio è
quello descritto in Fig. 1.
Il progetto è stato inserito nel WG5 del COST D38 e si avvarrà della collaborazione del gruppo di
Basilea con i Proff J.Reubi e H.Maecke.
BIBLIOGRAFIA
1.
R.Visentin, R.Rossin, M.C.Giron, A.Dolmella, G.Bandoli, U.Mazzi, Synthesis and
Characterization
of
Rhenium(V)
Oxo
Complexes
with
N-[N-(3Diphenylphosphinopropionyl)glycyl]cysteine Methyl Ester. X-ray Crystal Structure of
{ReO[Ph2P(CH2)2C(O)-Gly-Cys-OMe(P,N,N,S)]}, Inorg. Chem., 42, 950-959, (2003).
2.
R.Visentin, M.C.Giron, M.Bello, U.Mazzi, Technetium-99m labeling of N-[N-(3diphenilylphosphinopropio-nyl)glycyl]cysteine (PN2S-OH) and its methyl esther derivetive
(PN2S-OMe), Nucl.Med.Biol.,31, 655-662, (2004).
3.
R. Visentin, G. Pasut, F.M. Veronese, U. Mazzi, Highly Efficient Technetium-99m Labeling
Procedure Based on the Conjugation of N-[N(3Diphenylphosphinopropionyl) glycyl]cysteine
Ligand with Poly(ethylene glycol..) Bioconj. Chem., 15, 1046-1054, (2004)
4.
M. Riondato, D.Camporese, D.Martin, J.Suades, A.Alvarez-Larena, U.Mazzi. Synthesis
and Characterisation of [Re(CO)3(SS)(P)] Complexes: A [2+1] Concept for 99mTc- and 188ReRadiopharmaceutical Applications. Eur.J.Inorg.Chem., 20, 4048-4055, (2005) .
L.Melendez-Alafort, E.Zangoni, U.Mazzi
Studi di marcatura, biodistribuzione ed efficacia radioterapeutica di
188
Re-HA (Acido Ialuronico)
L'acido ialuronico (HA) è uno dei componenti fondamentali dei tessuti connetivi dell'uomo e
degli altri mammiferi. Chimicamente è definibile come un glicosaminoglicano dalla catena
polisaccaridica non ramificata prodotta dall'aggregazione di migliaia di unità disaccaridiche
formate a loro volta da residui di acido glucuronico (un derivato del glucosio) e Nacetiglucosamina. Entra nella costituzione della sostanza fondamentale del tessuto connettivo della
pelle, il quale contiene il 63% di acqua, il 32% di collagene e l'1% di acido ialuronico. E' contenuto
in concentrazioni elevate nell' umor vitreo, nel cordone ombelicale, nei liquidi delle articolazioni. Si
presenta come una sostanza amorfa, solubile in acqua. Regola il contenuto idrico della sostanza
intracellulare e la permeabilità del tessuto connettivo. Funge da sostanza cementante dei tessuti ai
quali conferisce la tipica plasticità. E' contenuto nel collagene, nel quale ha la funzione di catturare
e trattenere l' acqua. Per costruire il collagene le cellule impiegano molta vitamina C. Ha proprietà
antinfiammatorie. Oltre che idratare la pelle possiede anche la proprietà di cicatrizzare le ferite. Nel
derma ha un' azione plastica e permette una migliore diffusione delle sostanze.
Inoltre l'acido ialuronico lega con dei recettori cellulari denominati CD44, ben conosciuti dagli
studiosi del sistema immunitario per la loro presenza nella pelle, tra l'altro sulla superficie delle
cellule cheratiniche, inclusi i follicoli piliferi. I CD44 sono anche sovraespressi in diversi tipi di
tumore e ciò ha sviluppato l’impiego dell’HA quale veicolante chemioterapici per tali tipi di
tumore.
Sulla base delle proprietà dell’HA sopra descritte sono stati eseguiti nell’Unità di Ricerca di
Padova del CIRCMSB diversi studi di marcatura con Tc-99m [1] su acido ialuronico sostituito con
acido butirrico [2], o con tassolo [3-5] per determinare la loro distribuzione in vivo, e definire le
capacità dell’HA di veicolare questi chemioterapici sul tumore
117
Tematica 6
Weight (g)
E’ stato inoltre definito un metodo di marcatura con Tc-99m dell’acido ialuronico (HA) semplice e
con alta resa che è risultato adatto per studi radioterapeutici nei topi [1].
Ultimamente il metodo di marcatura con Tc-99m dell’HA è stato trasferito al Re-188, con lo scopo
di utilizzare le proprietà veicolanti dell’HA per trasportare il radionuclide Re-188 sul tumore
affinché esplichi la sua azione radioterapica[6,7].
Dai dati preliminari in nostro possesso sull’efficacia delle radiazioni del Renio-188 sulle cellule
del carcinoma epatocellulare (HCC) nel topo si può dedurre che trattamenti di tale tipo di tumore
consentono prolungati aumenti di sopravvivenza. Sono stati già riportati in letteratura altri
promettenti risultati utilizzando il 131I-lipiodol [8], ma si può pensare che il 188Re, per le sue migliori
proprietà fisiche e chimiche quali la più alta energia delle emissioni beta, la più breve emivita e la
concomitante emissione di una componente gamma di energia paragonabile a quella del Tc-99m,
che consente di eseguire l’imaging durante il trattamento terapeutico, sia più promettente per il
trattamento di questi tipi di tumore.
E’ stato pertanto deciso di affrontare uno studio sistematico sulle proprietà radioterapeutiche su
questo come su altri tipi di tumore esprimenti alte quantità di CD44, di derivati dell’HA a diversa
massa molecolare.
Al momento gli studi si sono focalizzati su HA di ∼70 kDalton.
Studi di biodistribuzione in topi sani di 99mTc-HA hanno mostrato che 25 minuti dopo la
somministrazione intravenosa, più dell’80% del radiofarmaco si trova nel fegato e nella milza in
seguito al binding selettivo dell’HA su recettori specifici [1].
Basandoci su tali indicazioni, cellule di carcinoma epatocellulare sono state indotte nel fegato del
topo e trattate con HA marcato direttamente con 188Re.
La biodistribuzione di 188Re-HA è stata studiata in femmine sane di topi neri C57BL/6 trattati con
50 µL (3 MBq) di marcato purificato con iniezione nella vena caudale.
Trenta minuti dopo l’iniezione le dosi accumulate nel fegato e nella milza hanno raggiunto il valore
massimo e rimangono poi costanti per più di 72 h senza clearance renale.
Per verificare l’efficacia terapeutica del 188Re-HA sulle metastasi de fegato, i topi C57BL/6 sono
stati iniettati i.v. con cellule tumorali M5076, un fibrosarcoma che metastatizza specificatamente
nel fegato, e trattati 7 giorni più tardi con 9.2, 7.4, 4.5, e 2.2 MBq di 188Re-HA. Due settimane più
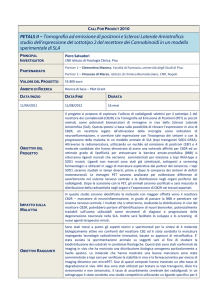
tardi i topi sono stati sacrificati per valutare l’impatto terapeutico. Mentre I fegati dei topi non
trattati mostravano un grande aumento di peso (Fig. 1) ed esibivano una massiva infiltrazione
neoplastica (Fig. 2) gli organi degli animali
5
trattati erano macroscopicamente normali.
spleen weight
Pochi foci metastatici erano visibili solo nei
liver weight
topi
che
avevano
ricevuto
minor
4
attività.Risultati simili sono stati anche ottenuti
in un modello di topo xenogenico con metastasi
3
a livello del fegato di coloncarcinoma umano
impiegando cellule tumorali HT-29impiantate
*
2
*
in topi SCID. Degno di nota è anche che il
188
Re-HA ha portato ad un
trattamento con
1
aumento della sopravvivenza di questo modello
di topi. Inoltre l’approccio radioteraputico con
*
188
0
Re-HA è stato ben tollerato ed associato con
Positive Control
60 µCi
120 µCi
una leggera tossicità nel fegato e a livello di
midollo osseo. Ora si stanno verificando le
Fig. 1. La figura mostra il peso (medio ± SD)
potenzialità
terapeutiche
usando
della milza e del fegato di topi con metastasi di
somministrazioni multiple di basse dosi di
attività di radiofarmaco per determinare tumore M5076 e trattate con 120 µCi o 60 µCi
l’effetto curativo a tempi lunghi, per poi di 188Re-HA.
definire tutte le condizioni sperimentali per il potenziale a livello clinico.
118
Tematica 6
Si può concludere dicendo che questi studi di biodistribuzione hanno dimostrato che il
complesso188Re-HA è più stabile rispetto al Re-188-HDD/lipiodol che è tuttora sotto
sperimentazione clinica. Inoltre, al contrario del Re-188-HDD/lipiodol, che deve essere
somministrato via intra-arteria, il 188Re-Ha può essere somministrato per semplice iniezione
intravenosa ed è rapidamente concentrato nel fegato e nella milza, senza eliminazione, riducendo
così il rischio di danno agli atri organi. Il trattamento delle metastasi al fegato nei topi ha rivelato
che il coniugato mostra un forte effetto terapeutico anche in presenza di bassa attività. E’ inoltre
importante notare che le attività qui usate sono simili a quelle già in uso nei trial clinici. Infine
l’efficacia terapeutica del trattamento è anche confermata in un modello di topo xenogenico con
metastasi al fegato di coloncarcinoma umano usando cellule tumorali HT-29 impiantate in topi
SCID, e non associate con rilevante tossicità al fegato ed al midollo spinale.
Nel prossimo triennio si porteranno avanti analoghi studi su derivati di HA da 5, 10, 200, 500 Mda
per applicazioni anche in sedi diverse dal fegato, e contemporanemente si proseguiranno gli studi
per la preparazione della sperimentazione clinica.
A
B
Fig. 2. La figura mostra le foto della milza e del
fegato espiantate da topi iniettati con cellule
tumorali M5076 al giorno 0 e trattate al giorno +7
con soluzione fisiologica (A), 60 µCi (B) o 120
µCi (C) di 188Re-HA. Gli animali furono
sacrificati al 21° giorno dall’iniezione del tumore.
C
BIBLIOGRAFIA
[1] A.Banzato, M.Bello, D.Bernardini, P.Boccaccio, D.Bollini et al. Annual Report 2006 LNLINFN, Legnaro,PD, pp 63,64
[2] Coradini D., Zorzet S., Rossin R., Scarlata I., Pellizzaro C., Turrin C., Bello M., Cantoni S.,
Speranza A., Sava G., Mazzi U., Perbellini A. - Clinical Cancer Research, 2004, 10, 48224830.
[3] A. Banzato, M. Rondina, L. Meléndez-Alafort, A.Nadali, E. Zangoni, D. Renier, G. Moschini,
U. Mazzi, P. Zanovello, A. Rosato. Scintigraphy Imaging of in Vivo Drug Biodistribution
Dictates Regional Therapeutic Efficacy of a Paclitaxel-Hyaluronic Acid Bioconjugate, J.
Label.Compd & Radiopharm. 2008
119
Tematica 6
[4] A. Banzato, M. Rondina, L. Meléndez-Alafort, A.Nadali, E. Zangoni, D. Renier, G. Moschini,
U. Mazzi, P. Zanovello, A. Rosato. Scintigraphy Imaging of in Vivo Drug Biodistribution
Dictates Regional Therapeutic Efficacy of a Paclitaxel-Hyaluronic Acid Bioconjugate, J.
Label.Compd & Radiopharm. 2008
[5] A.Banzato, S. Bobisse, D. Renier, F. Bettella, G.Esposito, L. Quintieri, U. Mazzi, P. Zanovello,
A.Rosato. Paclitaxel-Hyaluronan Bioconjugate Targeting Ovarian Cancer Affords a Potent In
Vivo Therapeutic Activity. Clinical Cancer Research (2008) in press
[6] A.Antoccia, A. Banzato, M. Bello, D. Bollini ,F. De Notaristefani, C. Giron, U. Mazzi, L.
Melendez Alafort, G. Moschini, A. Nadali, F. Navarria, A. Perrotta, A. Rosato, C. Tanzarella,
N. Uzunov. 188Rhenium-induced cell death and apoptosis in a panel of tumour cell lines Nuclear Instruments and Methods in Physics Research A.; 571: 471-474. 2007
[7] A.Antoccia, A. Banzato, M. Bello, D. Bollini ,F. De Notaristefani, C. Giron, U. Mazzi, L.
Melendez Alafort, G. Moschini, A. Nadali ,F. Navarria ,A. Perrotta, A. Rosato, C. Tanzarella,
N. Uzunov. 188Rhenium-induced cell death and apoptosis in a panel of tumour cell lines Nuclear Instruments and Methods in Physics Research A.; 571: 471-474. 2007
[8] E. Garin, H. Rakotonirina, F. Lejeune, B. Denizot, et al - Nucl. Med. Commun. 2006, 27, 363
369.
UNITÀ DI RICERCA DI FERRARA
Gruppo: Gruppo Prof. Marchi, Dott. Bergamini, Dott. Marvelli
Preparazione di nuovi complessi di Renio e Tecnezio solubili in acqua per la radiofarmacia
Collaborazioni: Dip. Scienze farmaceutiche Univ. Padova, Dip. Scienze farmaceutiche Univ.
Ferrara, Dip. Medicina Clinica e Sperimentale Univ. Ferrara.
Tra gli isotopi radioattivi di metalli di transizione utilizzati nello sviluppo di radiofarmaci, il
tecnezio-99m ed il renio-186/188 giocano un ruolo importante sia in ambito, il primo, diagnostico
che terapeutico. Inoltre, la disponibilità di un generatore portatile sia per il Tc-99m che per il Re188, fa sì che questi due radionuclidi occupino una posizione predominante in radiofarmacia.
Poiché i due elementi appartengono al medesimo gruppo della tavola periodica, la chimica
sviluppata per uno può essere da guida per il design di radiofarmaci dell’altro.
Come noto, le specie eluite dai generatori sono costituite dagli osso-anioni permetallato [MO4]-; lo
studio della loro chimica ha riguardato principalmente complessi in cui il metallo è nello stato di
ossidazione +5 e caratterizzati dalla presenza dei raggruppamenti Tc/Re(V)-oxo [M=O]3+ e -nitruro
[M≡N]2+ e solo più recentemente Tc/Re(I)-carbonile fac-[M(CO)3]+.
I composti maggiormente utilizzati nello studio della chimica del Re(V) sono rappresentati dai ben
noti complessi [ReOCl3(PPh3)2] e [ReNCl2(PPh3)2]. Questi precursori contengono PPh3 nella loro
sfera di coordinazione che, come noto, presenta elevata tossicità, non è solubile in acqua, a meno
che non vengano inseriti gruppi idrofili nelle loro struttura, ha un elevato peso molecolare ed
ingombro sterico. Per queste ragione, i due precursori sopra riportati non sono propriamente indicati
per gli scopi della medicina nucleare. La sostituzione di PPh3 con fosfine solubili in acqua e
maggiormente biocompatibili può rappresentare un importante punto di partenza nello sviluppo di
futuri radiofarmaci.
La solubilità in acqua di composti di coordinazione può essere ottenuta impiegando la fosfina 1,3,5triaza-7-fosfoadamantano (PTA ). Fu sintetizzata da Daigle in 1974, ma il suo interesse è stato
rivolto recentemente alla realizzazione di composti di coordinazione per la catalisi in fase acquosa.
Per applicazioni in medicina and biologia, l’attenzione è stata principalmente rivolta a complessi di
rutenio e platino. L’elevata idrofilicità, le piccole dimensioni insieme alla sua stabilità chimica e
termica la rendono unica in confronto alle altre alchil o aril-fosfine.
120
Tematica 6
P
N
N
N
PTA - (1,3,5-triaza-7-phosphaadamantane)
Sulla base di queste brevi considerazioni è stato iniziato negli anni precedenti uno studio per la
sintesi di precursori di Re(V) contenenti PTA solubili in acqua. I complessi [ReNCl2(PTA)3] e
trans-[ReO2Cl(PTA)3] sono stati ottenuti mediante reazioni di semplice sostituzione dai
corrispondenti precursori [ReNCl2(PPh3)2] e [ReOCl3(PPh3)2]; essi presentano una elevata solubilità
in acqua essendo rispettivamente di ca. 0.5gmL-1 e ca. 0.36gmL-1. E’ stato poi intrapreso uno studio
preliminare della loro reattività scegliendo come legante modello il sale sodico dell’acido
ditiocarbammico. Tale scelta è stata dettata dal fatto che complessi non solo di Re e Tc con
ditiocarbammato sono stati estesamente studiati poiché questo legante permette di includere nella
sua struttura una varietà di sostituenti organici che possono determinare il destino biologico dei
complessi. Ad esempio, complessi del tipo [TcN(S2CNR2)2] sono stati studiati nell’imaging del
miocardio.
Per il prossimo triennio ci si propone di:
ampliare lo studio della reattività dei complessi di renio sopra citati verso altre classi di leganti,
estendere le conoscenze acquisite al tecnezio-99,
progettare idonee vie di sintesi dei precursori a partire dall’anione [MO4]- (M=Re, Tc) che
costituiscono la specie eluite dai generatori di Re-188 e Tc-99m.
Per quanto riguarda il punto 3) è da tenere presente che il PTA, contrariamente alle altre fosfine,
non è in grado di strappare l’ossigeno allo ione permetallato provocando la riduzione del metallo da
+7 a +5, e che il renio è più difficile da ridurre rispetto al tecnezio. Sarà quindi necessario
progettare adeguate reazioni di riduzione/sostituzione che siano efficaci, con rese elevate e in
condizioni sperimentali idonee al loro trasferimento ai corrispondenti radionuclidi Re-188 e Tc99m.
UNITÀ DI RICERCA DI SIENA
“Radiofarmaci nella diagnostica e terapia tumorale”
Gruppo di ricerca dei Proff. Vomero, Anzini, Cappelli
Composizione e Settore di Indagine
L’Unità di Siena propone un nuovo progetto inerente la Tematica 6 che implementa le potenzialità
della tematica stessa nei suoi vari aspetti inerenti la progettazione, la sintesi, la caratterizzazione
chimico fisica e la determinazione delle proprietà biologiche di radiofarmaci sia per il loro impiego
nella diagnostica per immagini che nella radioterapia dei tumori.
Il gruppo di ricerca opera presso il Dipartimento Farmaco-Chimico-Tecnologico, collabora con il
gruppo del Professor F.Fazio dell’Ospedale San Raffaele di Milano.
Più in generale, all’interno del CIRCMSB, l’Unità di Siena porta avanti collaborazioni con l’Unità
di Ricerca di Padova e di Firenze.
Il presente gruppo di ricerca dell’Unità di Siena porterà avanti ricerche sulla sintesi di nuovi leganti
del recettore benzodiazepinici periferico (PBR) marcati con tecnezio, renio e rame con l’obiettivo di
sviluppare nuovi traccianti SPECT potenzialmente utili per la diagnosi di tumori e di malattie
neurodegenerative.
Il recettore PBR è stato originariamente scoperto per mezzo del diazepam marcato con trizio e
questo importante risultato ha stimolato la ricerca focalizzata alla caratterizzazione di questo
recettore. Il PBR è principalmente localizzato nei tessuti periferici e nelle cellule della glia ed è
altamente espresso nei tessuti steroidogenici come le ghiandole surrenali. Inoltre esso è
121
Tematica 6
sovraespresso in molti tessuti tumorali (per esempio in alcuni tumori del cervello, nei tumori delle
ovaie, in quelli del fegato, della mammella, nel cancro colorettale, ecc.) e l’espressione sembra
essere correlata con il grado di malignità del tumore. Inoltre, elevate concentrazioni di PBR sono
state osservate in aree lesionate del cervello in una grande varietà di neuropatologie come la sclerosi
multipla, la malattia di Alzheimer e quella di Huntington.
A livello subcellulare il PBR è localizzato nella membrana mitocondriale più esterna.
Dal punto di vista fisiologico, il PBR è coinvolto in meccanismi regolatori che variano secondo il
tipo di tessuto considerato: per esempio tra gli effetti mediati dal PBR c'è l'omeostasi del calcio, il
metabolismo lipidico, l'ossidazione mitocondriale, l'inibizione della proliferazione cellulare, ma il
coinvolgimento del PBR nella regolazione della biosintesi di steroidi nel sistema nervoso centrale è
probabilmente il più interessante aspetto del suo ruolo biologico con riferimento alle possibili
applicazioni terapeutiche.
Il PBR rappresenta un sistema fondamentale nel trasferimento di colesterolo dall'esterno all'interno
del mitocondrio rendendolo disponibile alla trasformazione da parte del citocromo P450 a
pregnenolone, che poi successivamente è metabolizzato ad altri ormoni.
Il derivato
isochinolincarbossamidico PK11195 è stato il primo legante non benzodiazepinico che è stato
scoperto legare il PBR e facilitare il trasporto del colesterolo dalla membrana più esterna del
mitocondrio a quella più interna, incrementando così la velocità di sintesi del pregnenolone.
Il PK11195 è oggi il composto più utilizzato nello studio dell’espressione e delle funzioni del PBR
(per esempio la steroidogenesi e l’apoptosi). Il PK11195 marcato con il carbonio-11 è stato
utilizzato nell’imaging dei tumori del cervello, nella sclerosi multipla, nell’ischemia cerebrale, ecc.,
attraverso la tomografia ad emissione di positroni (PET).
Recentemente un nuovo legante del recettore PBR, il DAA1106, è stato proposto come tracciante
PET per l’imaging dei PBR nel cervello umano.
Nell’ambito di un progetto attivo nei nostri laboratori già da diversi anni, è stato sintetizzato un gran
numero di leganti dotati di elevata affinità per i PBR. Alcuni dei composti sintetizzati sono stati
sottoposti a marcatura con carbonio-11 al fine di studiarne la biodistribuzione in vivo. Gli studi
effettuati hanno dimostrato per i composti selezionati un elevato legame specifico ai PBR ed elevati
rapporti tessuto/sangue cosicchè tali composti si candidano quali interessanti leganti PET per la
visualizzazione dei PBR in vivo.
La valutazione di tali traccianti in un modello eccitotossico della malattia di Huntington ha rivelato
che tali composti possono essere considerati degli interessanti candidati per la diagnosi dei processi
neurodegenerativi attraverso la PET. L’ulteriore esplorazione delle relazioni struttura-affinità in
questa classe di composti ha condotto alla scoperta di leganti PBR dotati di affinità subnanomolare.
La marcatura con carbonio-11 di una di queste molecole ha consentito di ottenere un nuovo
tracciante PET molto promettente che potrà essere utilizzato nella diagnosi di importanti patologie
come quelle citate sopra.
Il progetto di ricerca ha come scopo lo sviluppo di nuovi leganti PBR marcati con tecnezio, renio o
rame potenzialmente utili nella diagnosi e nella terapia delle citate patologie.
Nella prima fase del progetto verranno sintetizzati derivati chinolincarbossamidici recanti differenti
gruppi chelanti al fine di valutare gli effetti delle caratteristiche chimico-fisiche del gruppo chelante
nell’interazione con i PBR. Durante la seconda fase del progetto, i leganti più promettenti dal punto
di vista dell’affinità recettoriale verranno marcati con l’introduzione dell’opportuno radionuclide e
valutati in studi di biodistribuzione in vivo.
BIBLIOGRAFIA
1) Cappelli, A.; Anzini, M.; Vomero, S.; De Benedetti, P. G.; Menziani, M. C.; Giorgi, G.;
Manzoni, C., “Mapping the Peripheral Benzodiazepine Receptor Binding Site by
Conformationally Restrained Derivatives of 1-(2-Chlorophenyl)-N-methyl-N-(1-methylpropyl)3-isoquinolinecarboxamide (PK11195)”, J. Med. Chem. 1997, 40, 2910-2921.
122
Tematica 6
2) Matarrese, M.; Soloviev, D.; Cappelli, A.; Todde, S.; Moresco, R. M.; Anzini, M.; Vomero, S.;
Sudati, F.; Carpinelli, A.; Perugini, F.; Galli Kienle, M.; Fazio, F., “Synthesis of the Novel
[11C]-Labelled Quinoline Carboxamides: Analogues of PK-11195 as Putative Radioligands for
PET Studies of Peripheral Type Benzodiazepine Receptors”, J. Labelled Cpd. Radiopharm.
1999, 42, S397-S399.
3) Anzini, M.; Cappelli, A.; Vomero, S.; Seeber, M.; Menziani, M. C.; Langer, T.; Hagen, B.;
Manzoni, C. Bourguignon, J.-J., “Mapping and Fitting the Peripheral Benzodiazepine Receptor
Binding Site by Carboxamide Derivatives. Comparison of Different Approaches to Quantitative
Ligand-Receptor Interaction Modeling”, J. Med. Chem. 2001, 44, 1134-1150.
4) Matarrese, M.; Moresco, R. M.; Cappelli, A.; Anzini, M.; Vomero, S.; Simonelli, P.; Verza, E.;
Magni, F.; Sudati, F.; Soloviev, D.; Todde, S.; Carpinelli, A.; Galli Kienle, M.; Fazio, F.,
“Labeling and Evaluation of N-[11C]Methylated Quinoline-2-carboxamides as Potential
Radioligands for Visualization of Peripheral Benzodiazepine Receptors”, J. Med. Chem. 2001,
44, 579-585.
5) Cappelli, A.; Pericot Mohr, G.; Gallelli, A.; Giuliani, G.; Anzini, M.; Vomero, S.; Fresta, M.;
Porcu, P.; Maciocco, E.; Concas, A.; Biggio, G.; Donati, A., “Structure-Activity Relationships
in Carboxamide Derivatives Based on the Targeted Delivery of Radionuclides and Boron Atoms
by Means of Peripheral Benzodiazepine Receptor Ligands”, J. Med. Chem. 2003, 46, 3568.
6) Belloli, S.; Moresco, R. M.; Matarrese, M.; Biella, G.; Sanvito, F.; Simonelli, P.; Turolla, E.;
Olivieri, S.; Popoli, P.; Cappelli, A.; Vomero, S.; Galli-Kienle, M.; Fazio, F., “Evaluation of
Three Quinoline-2-carboxamide Derivatives as Potential Radioligands for the in Vivo PET
Imaging of Neurodegeneration”, Neurochem. Int. 2004, 44, 433–440.
7) Cappelli, A.; Matarrese, M.; Moresco, R. M.; Valenti, S.; Anzini, M.; Vomero, S.; Turolla, E.
A.; Belloli, S.; Simonelli, P.; Filannino, M. A.; Lecchi, M.; Fazio, F., “Synthesis, Labeling, and
Biological Evaluation of Halogenated Quinoline-2-carboxamides as Potential Radioligands for
Visualization of Peripheral Benzodiazepine Receptors”, Bioorg. Med. Chem. 2006, 14, 40554066.
8) Cappelli, A.; Giuliani, G.; Valenti, S.; Anzini, M.; Vomero, S.; Giorgi, G.; Sogliano, C.;
Maciocco, E.; Biggio, G.; Concas, A., “Synthesis and Structure-Activity Relationship Studies in
Peripheral Benzodiazepine Receptor Ligands Related to Alpidem”, Bioorg. Med. Chem., in
press (doi: 10.1016/j.bmc.2007.06.044).
9) Cappelli A., Mancini A., Sudati F., Valenti S., Anzini M., Belloli S., Moresco R. M., Matarrese
M., Vaghi M., Fabro A., Fazio F., Vomero S., “Synthesis and Biological Characterization of
Novel 2-Quinolinecarboxamide Ligands of the Peripheral Benzodiazepine Receptors Bearing
Technetium-99m or Rhenium,” Bioconj. Chem., submitted (2008).
123