Chimica Organica
Informazione Scientifica sul Farmaco
Capitolo 15
Carboidrati
Organic Chemistry, 5th Edition
L. G. Wade, Jr. Prentice Hall
Organic Chemistry, 3rd Edition
Paula Y. Bruice, Prentice Hall
Carboidrati
•
•
•
•
Sintetizzati dalle piante utilizzando la luce per convertire CO2 e
H2O in glucosio e O2 (fotosintesi).
Formano polimeri, tra i quali amido e cellulosa.
La maggior parte degli zuccheri hanno formula Cn(H2O)n, “idrati di
carbonio”
Sono poliidrossialdeidi, poliidrossichetoni o sostanze che per
idrolisi formano composti di questo tipo
OH OH
OH OH
CH2CHCHCHCHCHO
OH
OH OH
HO
OH OH O
OH OH
HO
H
* * * *
OH OH O
H
D-glucosio
24=16 stereoisomeri
H
HO
H
H
CHO
OH
H
OH
OH
CH2OH
Classificazione dei carboidrati
•
•
•
Monosaccaridi o zuccheri semplici
Poliidrossialdeidi o aldosi
Poliidrossichetoni o chetosi
Disaccaridi: possono essere idrolizzati ottenendo due
monosaccaridi
Polisaccaridi: per idrolisi formano molte molecole di monosaccaride.
Es., amido e cellulosa hanno più di 1000 unità di glucosio
H
HO
H
H
CHO
OH
H
OH
OH
CH2OH
Glucosio: aldoso
H OH
HO
HO
HO
H
H
HOH2C
H
OH
O
O
H
OH
H
CH2OH
OH H
Saccarosio: disaccaride
Cellulosa: polisaccaride
3
Monosaccaridi
•
Classificati come:
aldosi o chetosi
Numero di carboni della catena (pentosi, esosi)
Configurazione del centro di chiralità più lontano dal gruppo
carbonilico
glucosio,
D-aldoesoso
fruttosio,
D-chetoesoso
4
Classificazione D, L
• Sono definiti zuccheri di tipo D quelli che hanno la configurazione del
centro di chiralità più lontano dal carbonile come la (+) gliceraldeide.
• Zuccheri L corrispondenti alla (-) gliceraldeide.
Gli aldosi della serie D
I chetosi della serie D
7
Epimeri
• Composti con più centri di chiralità che differiscono per la
configurazione di uno solo di essi.
8
Struttura emiacetalica: glucosio
• L’emiacetale si forma per reazione del gruppo -CHO con il
gruppo -OH al C5.
D-glucopiranosio
Anomero b
Anomero a
9
Fruttosio
•
Si forma per reazione del C=O al C2 con il gruppo -OH al C5.
D-fruttofuranosio
O
furano
O
pirano
10
Anomeri
• Il carbonio emiacetalico può avere configurazione R o S, si formano
quindi due emiacetali
• Si tratta di una caso particolare di diastereoisomeri; il carbonio
emiacetalico è anche chiamato anomerico
• Le due forme anomeriche (a e b) sono in equilibrio
11
Mutarotazione
• L’equilibrio tra le forme anomeriche determina il fenomeno della
mutarotazione
• Sciogliendo l’anomero a (o b) in acqua, si ha una variazione del
potere rotatorio fino al valore della miscela anomerica
• Attenzione: non si tratta del valore medio perché gli anomeri sono
presenti all’equilibrio in percentuali diverse (sono diastereoisomeri!)
12
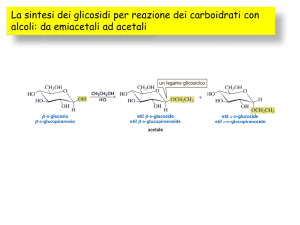
Glicosidi
• Lo zucchero in forma emiacetalica può reagire con un alcol e
formare un acetale (glicoside).
• Gli emiacetali a- e b- (anomeri) formano due acetali anomeri a- e
b- glicosidi.
• Il gruppo R- legato all’ossigeno anomerico si chiama aglicone.
HOH2C
CH2OH
O
O
HO
HO
OH
salicina
13
Disaccaridi
• Tre possibili legami glicosidici:
• Legame 1-4’: il carbonio anomerico è legato all’ossigeno
al C4 di una seconda molecola di zucchero.
• Legame 1-6’: il carbonio anomerico è legato all’ossigeno
al C6 di una seconda molecola di zucchero.
• Legame 1-1’: due carboni anomerici legati da un atomo
di ossigeno.
14
Cellobiosio
•
•
•
•
Si ottiene per idrolisi parziale della celulosa
Due molecole di glucosio con legame b-1,4’.
Stesso tipo di legame della cellulosa.
Dà mutarotazione.
15
Maltosio
• Si ottiene per idrolisi parziale dell’amido
• Due molecole di glucosio con legame a-1,4’.
16
Lattosio
•
•
•
Galattosio + glucosio, legame b-1-4’.
Zucchero principale del latte (4-8%)
Galattosemia: mancanza dell’enzima capace di isomerizzare il
galattosio a glucosio
17
Saccarosio
•
•
•
Zucchero da tavola
Glucosio + fruttosio,
legame 1-1’
100 milioni di tonnellate
all’anno (canna da
zucchero, barbabietola)
18
Polisaccaridi: cellulosa
•
•
•
•
Polimero del D-glucosio.
Legame di tipo b-1,4’
Fibre robuste (legno, cotone, lino, canapa …)
L’uomo ed alcuni animali digeriscono l’amido ma non la cellulosa
19
Amilosio
• Frazione solubile dell’amido, polimero del D-glucosio.
20
Amilopectina
• Frazione insolubile dell’amido
21
Glicogeno
• Polimero del glucosio simile all’amilopectina ma ancora
più ramificato.
• Riserva di energia nei tessuti dei muscoli e del fegato.
• Le numerose terminazioni delle catene costituiscono un
mezzo per riversare rapidamente glucosio nel sangue.
22
Acidi nucleici
• Polimero del ribosio, molecole
legate da gruppi fosfato.
• Ogni ribosio è legato ad una
base.
• Acido ribonucleico (RNA)
• Acido deossiribonucleico (DNA)
23
Fine del capitolo 15
24