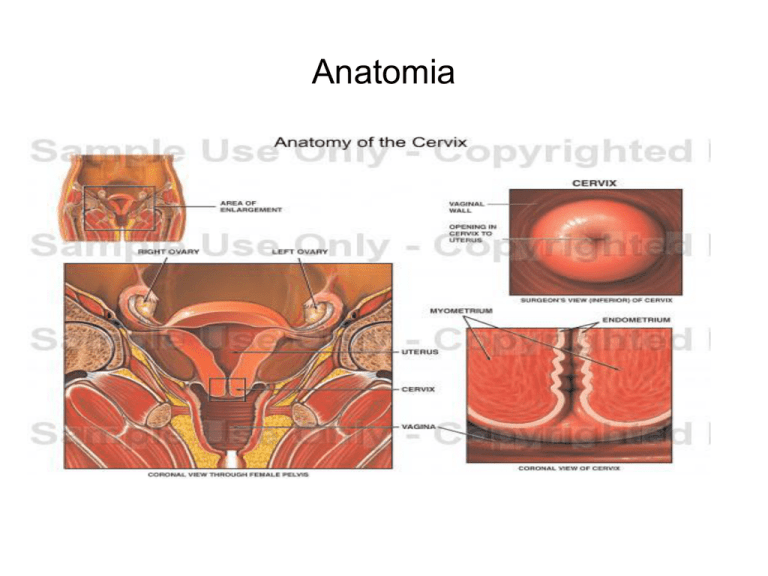
Anatomia
Lesioni preneoplastiche portio
Giunzione squamo-colonnare
Colposcopia
La Giunzione SquamoColonnare
• nella donna in età fertile è sull’ esocervice
• nella donna in menopausa è endocervicale
Bethesda Sistems
• Lesioni squamose atipiche di significato non determinabile (ASCUS)
• Lesione ghiandolare atipiche di significato non determinabile (AGUS)
• Lesione Intraepiteliale Squamosa (SIL)
SIL di basso grado = lesione squamosa di basso grado comprende
- la displasia lieve (CIN1)
- la lesione da HPV
SIL di alto grado = lesione squamosa di alto grado
comprende
- la displasia moderata (CIN2)
- la displasia grave (CIN3)
Infezione da HPV
Molto diffusa : 75%
Alta prevalenza tra i giovani
E’ Transitoria : 80% delle donne è
negativa dopo 18mesi dall’infezione
Solo una piccola parte progredisce verso
carcinoma, ed è dovuto al HRHPV
• La maggior parte dell’infezione è
transitoria.
• Il rischio è aumentato solo nelle
pazienti con infezione persistente.
• la Persistenza è tipica dei ceppi ad alto
rischio
ALTO E BASSO RISCHIO
11*
6*
57
2*
10*
3*
7*
13*
44*
40*
42*
32*
43*
HPV cutanei
(*basso rischio)
HPV mucosali
(†alto rischio)
34
16†
†
58† 52† 45†
68†
†
33
39†
18†
35† 31
51†
53
66†
26
30
56†
Adapted from Wieland U and Pfister H. In: Gross, Barrasso Eds. Ullstein Mosby; 1997.
Lui J et al (Eds): IDEAL 2003. Springer-Verlag, Berlin Heidelberg 2003.
HPV
CONDILOMI GENITALI
90% dei casi 6 e 11
10% di
e
nel corso della vita
LESIONI CERVICALI
CIN 1 (4 - 25%)
PAPILLOMATOSI RICORRENTE DELLE
ALTE VIE RESPIRATORIE (JORRP)
0.1-2.1/100.000 nati
1/400 parti in pz. con condilomatosi florida
HPV
,
,31, 33, 35, 39, 45, 51, 52,
55, 56, 58, 59, 66
% attribuibile a HPV
Carcinoma cervicale
Carcinoma vagina
Carcinoma vulva
Carcinoma ano
100%
64-91%
40%
88-94%
Carcinoma faringe
25%
Carcinoma cavità orale
10%
Carcinoma pene
40%
Raffigurazione del meccanismo
oncogeno di HPV
Lesioni virali da HPV
Primo presidio diagnostico:
Pap test
coilocitosi
Atipia Coilocitotica
•
•
•
Il coilocita è
definito come una
cellula squamosa
superficiale o
intermedia
caratterizzata da:
Ampio alone
paranucleare a
margini
netti,otticamente
vuoto
Nucleo ingrandito
18
Pap test: sensibilità
15-30%
Coilociti e discheratociti non sono presenti in tutte
le infezioni produttive
Poche cellule alterate con caratteristiche non
sempre evidenti
Tali modificazioni cellulari non sono evidenti nelle
infezioni latenti e quando il virus è integrato nel
genoma della cellula ospite.
19
Pap test: sensibilità
La sensibilita del pap test nella diagnosi delle
lesioni virali della cervice è abbastanza bassa.
Ciò è dovuto non tanto al test ma alla natura
della infezione stessa. Infatti gli ECV non
sempre sono presenti in quanto si verificano
solo nelle infezioni produttive, mentre quando
il virus si integra con il DNA della cellula
ospite, quindi possibile oncogenesi, il pap test
potrebbe anche essere negativo.
•
•
•
•
•
•
•
La cellula infettata da HPV è detta COILOCITA (= cellula col buco): è
una cellula squamosa, epiteliale, con un nucleo ipercromico (scuro) e un
alone nucleare intorno (chiaro). Si parla di "coilocitosi". L'HPV promuove,
nelle cellule squamose, una marcata IPERPROLIFERAZIONE, per cui
troviamo anche alterazioni di tipo strutturale, tissutale, di tipo
papillomatoso.
Il coilocita ha aspetto fusato. Normalmente il nucleo di una cellula
squamosa è centrale vescicoloso, ricco di nucleoli. Una volta infettata,
questa cellula presenta un nucleo allungato, a volte bitorzoluto, con
l'acido nucleico concentrato. Attorno si crea un alone chiaro (che poi
sarebbe il buco) costituito dai virioni in replicazione.
Il corrispettivo istologico di questa lesione è dovuto alla
iperproliferazione: si formano delle lesioni in cui l'epitelio (come se non
trovasse più spazio sul piano) inizia ad ispessirsi e a formare le
PAPILLE, che si portano dietro il loro asse fibrovascolare, per
assicurarsi il nutrimento. Il tessuto è caratterizzato da:
PAPILLOMATOSI
IPERCHERATOSI =aumento della produzione di cheratina.
PARACHERATOSI =cheratinizzazione di epiteli normalmente non
cheratinizzati.
DISCHERATOSI =cheratinizzazione parziale.
Alterazioni cellulari
acantosi
discheratosi
Acantosi: aumento delle cellule che compongono lo
strato spinoso
Evidenza di ECV da HPV può
essere presenti nelle CIN 1 e 2
meno frequentemente nelle CIN3
in questi casi la lesione viene
classificata come
CIN con evidenza di infezione da
HPV( Richart, 1999)
Di regola la evidenza di ECV da
HPV è inversamente
proporzionale al grado di CIN e
può non essere evidente nelle
lesioni di alto grado/CIS
L’assenza di antigeni strutturali virali e quindi di
ECV è relativamente frequente nel CIS ed è la
regola nel ca invasivo
Quindi con la trasformazione maligna, che in
genere correla con la integrazione del DNA
virale nel DNA dell’ospite, vengono persi i
marcatori morfologici ed ogni informazione sulla
presenza del virus è legata all’analisi molecolare
Pap test + colposcopia
accuratezza diagnostica
Lesioni preneoplastiche della portio
diagnosi
Pap Test
Colposcopia
L’associazione pap test
colposcopia porta a risultati corretti nel 9097%.
Accuratezza
diagnostica :
colposcopia
90 %
Dipartimento di Scienze Ginecologiche-Università
di Catania- ambulatorio di colposcopia prof.
M.T.Bruno
colposcopia
•
•
•
•
Individuare le lesioni
definirne i limiti topografici
Esprimere un grading
Indicare la sede o le sedi della biopsia
Colposcopia
l’epitelio cilindrico con l’acido
acetico assume un aspetto
a “ chicco d’uva”. E la zona di gsc
è ben individuabile, se la donna è
giovane.
Epitelio acidopositivo
•
Le aree di epitelio atipico assumono invece un
colorito bianco in quanto il
citoplasma delle cellule atipiche è ricco di proteine
che a contatto con acido acetico si coagulano danno
nell’ insieme l’aspetto biancastro tipico.
Colposcopia
• Spesso all’ area acidopositiva si associa un
aspetto:
a”mosaico” dato dai capillari che assumono un
andamento parallelo all’epitelio per cui danno
un aspetto quadrettato;
a “puntato” dato da papille connettivali con il
contenuto vascolare.
Se l’atipia interessa le ghiandole da’ origine allo
“sfondato ghiandolare ispessito”.
Mosaico
Colposcopia
• Il test diSchiller viene
utilizzato solo ai fini didattici
e si basa sul fatto che l’epitelio
maturo è ricco di glicogeno
per cui lo iodio lo
colora uniformemente color
mogano. L’epitelio atipico non
contiene glicogeno per cui non
si colora. E’ poco specifico.
Colposcopia
La colposcopia mette in evidenza eventuali
•
- lesioni atipiche della portio,
•
- studia la sua estenzione
•
- permette di eseguire la biopsia mirata
•
- indica il tipo di terapia, infatti
se la lesione è tutta esocervicale ed è una SIL di basso
grado PERSISTENTE basta fare una laserterapia ,
se la lesione è endocervicale per avere la certezza
diagnostica bisogna eseguire un prelievo del
canale cervicale o addirittura una conizzazione
Biopsia portio
• Individuata la zona sospetta si esegue
la biopsia mirata della portio. Consiste nel
prelevare un frammento di tessuto sotto
visione colposcopica, quando la lesione è
interamente visibile.
• Si esegue con una apposita pinza,
ambulatoriamente e senza anestesia
Biopsia portio
Scarsa accuratezza diagnostica della biopsia target
Biopsia target= prelievo escissionale
accuratezza
43-51%
107
b
i
o
p
s
i
a
CIN1
conizzazione
CIN 2-3
65%
Zuchna C. 2010
Incrementare il numero di biopsie target a
due/tre
Accuratezza diagnostica
Sensibilità
Specificità
Conizzazione
Se la lesione non è
interamente visibile, ma si estende nel
canale cervicale allora è consigliabile la
conizzazione diagnostica.
Conizzazione
Consiste nell’asportare un cono di tessuto
cervicale il cui apice coincide con il
canale cervicale e la base con l’esocollo.
Se la lesione è SOPRATTUTTO
esterna l’altezza del cono è minima,
se la lesione si estende SOPRATTUTTO
dentro il canale cervicale l’ altezza del cono
è massima.
Conizzazione
E’ indicata, quando
• - l ’ intera area non è visibile al colposcopio,
ma risale dentro il canale cervicale;
• - l’esame istologico ha messo in evidenza un
CIN3-Carcinoma in situ;
• - la biopsia ha dato esito negativo in
una paziente con paptest
ripetutamente positivo
Conizzazione
Si esegue in anestesia generale.
Si delimita la zona atipica con la soluzione di Lugol.
Si danno due punti di sutura a ore 3-9 per bloccare le
cervicali e diminuire l’emorragia.
Si comincia ad incidere e ad asportare il cono la cui
profondità è legata alla localizzazione della lesione.
Nella donna fertile il tratto di cono asportato non deve
superare i 2.5 cm di canale cervicale lasciando intatta
la parte superiore del canale cervicale e l’orifizio
uterino interno.
Conizzazione
Nella donna in postmenopausa invece, nella quale la gsc si trova dentro il
canale cervicale, è bene asportare un cono il cui apice
raggiunga anche l’orificio cervicale interno.
Asportato il cono, veniva coperta la perdita di sostanza con
la mucosa cervicale residua mediante due punti alla Sturmdorf.
Attualmente ciò non si fa in quanto è più facile controllare eventuali
focolai di neoplasia residua con il pap test e la colposcopia.
Il cono asportato dopo averlo orientato con una sutura a ore 12,
viene inviato al patologo. Quanto più elevato è il numero delle
sezioni tanto più non sfuggiranno piccole aree di neoplasia.
Trattamento CIN1
Lesione CIN1
follow-up
SICPCV linee guida
Il trattamento è indicato se la lesione di
basso grado persiste per più di due anni
ZTN completa
ATZ2 GSC non visibile
CIN3
Pap Test
LSIL
Conizzazione
ATZ1 gsc Parzialmente visibile
cheratosi
Vantaggi della colposcopia
• Scarsa invasività
• accuratezza diagnostica: colposcopia+ pap test= 100
• Sensibilità
colposcopia+ biopsia target
Limiti della colposcopia
•Impossibilità di identificare lesioni endocervicali
•Bassa sensibilità qualora non sia seguito da biopsia
•Esame operatore dipendente
Limiti della colposcopia ,
la lesione esocervicale si
continua nel canale cervicale.
-
- la gsc non è visibile
59
ambulatorio di ColposcopiaProf. M.T. Bruno- Università di
Catania
Lesioni virali da HPV
diagnosi:
Pap test
Colposcopia
• HPV test
HPV test
Vanno mandate a colposcopia tutti i casi
di pap test anomalo
Bethesda Sistem
National Cancer Institute Workshop on Cytopathology (1988,1991)
Cellule squamose
• S.I.L. Lesione Intraepiteliale Squamosa
•A.S.C.U.S.Cellule Squamose Atipiche
LSIL (di
basso
grado)
HSIL
(di alto
grado)
di significato indeterminato
Cellule ghiandolari
CIN 1 (displasia
lieve)
CIN 1 + HPV
CIN 2
(displasia
moderata)
CIN 3
(displasia
grave e Ca in
situ)
• A.G.U.S Cellule Ghiandolari Atipiche di significato indeterminato
Dipartimento di Scienze Ginecologiche-Università
di Catania- ambulatorio di colposcopia prof.
M.T.Bruno
Il motivo più frequente di invio a
colposcopia è un referto citologico
ASCUS
ASCUS
Obbiettivo principale
l’identificazione di lesioni CIN2,
lesioni usualmente trattate.
ASCUS
3 8 %
CIN2
Quindi non bisogna sottovalutare un referto citologico
ASCUS
La gestione della citologia
ASC-US (SICPCV)
1. Colposcopia immediata
2. Ripetere pap test dopo sei mesi
3. HPV test
Protocollo ASCUS
ASCUS
HPV test
screening
colposcopia
HPV test nello screening
• La logica è quella di rovesciare
l’attuale algoritmo
• Pap Test• Test HPV• Colposcopia
• eseguendo prima il test più sensibile
(test HPV) e successivamente il test
più specifico (Pap Test).
Protocollo di screening
Test di primo livello
HPV
Pap test
Rip a 3 aa
Negativa
HPV a 1 anno
>Ascus
colposcopia
L’HPV test nello screening
primario
Pap test+ HPV test donne> 30 anni
ogni 3 anni
HPV test nel follow-up della
terapia escissionale per CIN2-3
Perché la sorveglianza dopo trattamento per
CIN2-3
Le pazienti hanno un rischio aumentato di
sviluppare una neoplasia cervicale
La maggior parte delle recidive si osserva
nei primi due anni dal trattamento
Definizione di m.Residua/ recidiva: CIN2-3
confermato con istologia
Follow- up dopo trattamento per CIN2-3
• Problemi
Adesione al follow-up
Visita ogni 6
mesi per 2 o
piu aa
Quali test usare
Pap test
HPV test
6
mesi
negati
vi
12 mesi
Aderenza al followup e meno costi
Follow- up dopo trattamento per
CIN2-3
HPV test con tipizzazione
la Persistenza /Recidiva di CIN
Associati alla
Persistenza di HPV 16/18
HPV test
La tipizzazione permette una accurata
identificazione delle infezioni persistenti
Se HPV test negativo si puo allungare
l’intervallo di follow-up fino a 5 anni
HPV test
Molto sensibile
Poco specifico
VPP basso
VPN alto
Sensibilità HPV test capace di
diagnosticare tutti i casi in cui l’HPV
infetta la cellula ma è bassa la
specificità
HPV test positivo
Allarme nella paziente
Risvolti psicologici nella donna e
nella coppia
Aumento indiscriminato di
indagini di secondo livello:
colposcopia, biopsia, laser ecc
Con danno alla sanità pubblica
Come aumentare la specificità dell’HPV test?
Test di
Rischio
oncogeno
HPV test
genotipizzazione
mRNA E6 E7
Proteina p16
Fish test
HPV test
genotipizzazione
La genotipizzazione
è eseguita con il metodo della PCR, che
ha una sensibilità per l’infezione molto
elevata.
Secondo studi prospettici il rischio di
persistenza e progressione delle lesioni
HPV correlate è notevolmente diverso
secondo del genotipo virale
Quindi la tipizzazione fornisce
informazioni aggiuntive sul rischio
individuale di sviluppare lesioni
preneoplastche
Distribuzione percentuale dei carcinomi del
collodell’utero,pertipodiHPVinEuropa
HPV type prevalence in Cervical carcinomas* in Europe (% of all HPV+ cases treated)
1616
58,1
1818
3333
3131
4545
3535
5858
5656
5252
7373
66
6868
1111
5151
3939
6666
5959
7070
8282
15,7
4,4
4,0
2,9
1,6
1,2
1,0
0,6
58.1%
73.8%
78.2%
82.2%
85.1%
86.7%
87.9%
88.9%
0,6
0,3
0,3
0,3
0,2
8 tipi di HPV sono responsabili del0,290%
deicancridelcollodell’utero0,2
0,1
0,0
0,0
0
20
40
60
80 *
Casi di carcinoma della cervice attribuiti ai genotipi di HPV (%)
100
Smith JS, Lindsay L, Hoots B et al. Int J Cancer 2007;121:621-32
HPV ad alto rischio: diversa
capacità oncogena
• Numerosi studi hanno rilevato che le donne con
citologia ASCUS/LSIL positive per HPV 16-18 hanno
un rischio aumentato rispetto a quelle con positività
per altri tipi oncogeni di HPV ( studio ALTS).
• Il rischio di CIN3 è risultato 5 volte più alto nelle
donne HPV 16 positive rispetto alle donne positive per
gli altri sottotipi virali ad alto rischio.
• Quindi la tipizzazione di HPV 16-18 consente di
identificare le donne con rischio più elevato di
sviluppare un CIN2
Genotipizzazione: HPV 16
HPV ad alto rischio: HPV 16
• Studi sugli HPV 16 hanno scoperto che
le proteine E6/E7 del genotipo 16 ha
una maggiore adesivita alla proteina p53
e alla proteina del gene dei retino
blastoma- Per cui esplica una maggiore
attività oncogena. I tipi a basso rischio
invece producono proteine E6 e E7 con
bassa affinità di legame per p53 e pRb e
non ne attivano la degradazione;
HPV ad alto rischio: HPV 16
• inoltre Indagini recenti hanno
dimostrato, utilizzando tecniche capaci
di determinare la carica virale (Hibryd
Capture), che il genotipo 16 ha una
carica virale circa 60 volte maggiore
nelle HSIL rispetto alle LSIL e agli altri
HRHPV 31, 33, 18, 45.
HPV ad alto rischio: HPV 16
• Questi studi hanno identificato l’HPV 16 come
il più aggressivo.
• Sembra che sia utile riconoscere le pazienti
con ASCUS o LSIL con infezione da HPV16 da
quelle con altri HPV ad alto rischio, in quanto
hanno un rischio maggiore a due anni di CIN3
o più.
mRNA E6-E7
• L’iperespressione di E6/E7 di HPV ad
alto rischio è associata al
cervicocarcinoma e alle sue lesioni
precancerose. L’analisi dell’espressione
dei trascritti E6/E7 di HPV 16, 18, 31,
33, 45 con il test commerciale Pr tect
HPV Proofer ha dimostrato una buona
specificità nell’identificare le lesioni
CIN2+.
mRNA E6-E7
• Pazienti con CIN1 istologico e HPV test
positivo per uno degli HPV test ad alto
rischio vengono inviate a trattamento se
mRNA positivo.
• Donne positive all’HPV 16-18 e positive al
mRNA sono ad altissimo rischio di
sviluppare un cervicocarcinoma.
• Donne con pap test negativo, ma positive
all’HPV test 16-18 persistente sono a
rischio di sviluppare una CIN3
la ricerca del mRNA di E6-E7.
la positività di questo test sottolinea la
avvenuta integrazione del virus .
Ne consegue che la transcriptasi di E6 ed
E7 può essere utilizzato come markers di
progressione della lesione
mRNA E6-E7
la ricerca dell’RNA messaggero è
limitata solo ai principali tipi oncogeni
16, 18, 31, 33, 45, espressione di una
fase virale attiva.
Il test è molto
sensibile ed è quindi in grado di rilevare
le infezioni allo stadio iniziale, molto
prima che le alterazioni cellulari siano
visibili in un normale campione di cellule
studiato al microscopio.
Proteina p16
La proteina p16 è un regolatore del ciclo
cellulare che interrompe il segnale di
transizione della cellula dalla fase G1 verso la
fase S, fasi durante le quali la cellula prima
sintetizza le proteina e poi replica il DNA. La
p16 inibendo le Kinasi ciclino dipendenti
responsabili della fosforilazione del pRB
(retinoblastoma) e quindi della conseguente
trascrizione del fattore E2F che regola la
produzione delle proteina specifiche della
fase S. La sintesi di p16 è regolata da un
meccanismo feed back negativo con lo stesso
E2F.
Proteina p 16
L’oncogene E7 del HPV interagisce con pRB cellulare
inducendo l’espressione del fattore E2F, a
prescindere
dall’azione
delle
Kinasi
ciclino
dipendenti con conseguente aumento della p16.
L’iperespreeione della p16 evidenzia una alterazione
del ciclo cellulare e quindi una maggiore probabilità
di trasformazione neoplastica. In
particolare
lìiperespressione della proteina p16 nelle cellule
displastiche
indica
una
attiva
espressione
dell’oncogene virale E7
La p16 non è espressa nelle cellule epiteliali normali
e nelle cellule infiammatorie e metaplastiche delle
cervice
Proteina p16
Proteina p16
FISH
TEST
( Fluorescent in Situ Hybridization)
un HPV ad alto rischio persistente può
integrarsi nelle cellule cervicali e
causarne la trasformazione neoplastica
attraverso due diversi meccanismi:
Fish Test
meccanismo oncogeno di HPV
HPV
Fish test
Amplificazione del gene delle
telomerasi, situato nel locus 26 del
braccio lungo del cromosoma 3 (3q26).
Iperproduzione di telomerasi
Immortalizzazione della cellula
infettata
cromosoma
La telomerasi
La telomerasi ha il compito di riparare le
estremità dei cromosomi (telomeri) che
normalmente con l’invecchiamento
cellulare tendono ad accorciarsi.
• Questo meccanismo per la sua semplicità, è
molto più diretto del primo, fallisce meno
facilmente e giustifica la velocità di
progressione ( anche meno di un anno) che
qualvolta si osserva clinicamente.
• Mediante la tecnica FISH è possibile contare
le copie del gene3q26 nelle cellule cervicali
prelevati
FISH test
L’amplificazione del gene della telomerasi è stata riscontrata nel
LSIL 22%
HSIL 52%-80%
Carcinoma 100%
Se FISH positiva predisporre controlli ravvicinati ( pap testcolposcopia)
Se FISH negativa, la probabilità che una LSIL regredisca
spontaneamente è pressochè assoluta
In quest’ultimo caso la paziente non necessita di ulteriori
controllo e può rientrare nei normali protocolli di screening