1. I carboidrati
I carboidrati (o saccaridi, zuccheri, o glucidi
sono un gruppo molto vasto di sostanze
organiche, costituite nella maggior parte solo da
tre elementi, carbonio, idrogeno ed ossigeno.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
1. I carboidrati
I carboidrati nel mondo vivente assumo due funioni
principali:
Di tipo energetico: sono la sorgente primaria di
energia per gli organismi viventi.
Di tipo strutturale (principalmente in pareti cellulari,
rivestimenti cellulari, tessuti connettivi).
Inoltre i carboidrati possono aggregarsi alle proteine
della superficie cellulare formando le glicoproteine.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
1. I carboidrati
Possiamo classificare i carboidrati in base alla loro
complessità chimica in:
Monosaccaridi (Monomeri)
Oligosaccaridi, associazioni di poche unità di
monosaccaridi, come i Disaccaridi (Dimeri)
Polisaccaridi, costituiti da centinaia o migliaia di
unità (Polimeri)
I monosaccaridi sono le unità fondamentali degli
zuccheri, i carboidrati più semplici (monomeri),
con formula generale (CH2O)n
.
I monosaccaridi sono polialcoli aldeici (poliidrossialdeidi)
o chetonici (poliidrossichetoni) di brevi catene
idrocarburiche (comprendenti da 3 a 7 o più atomi di C).
Quindi in un monosaccaride sono compresi:
•
•
un certo numero di gruppi ossidrilici (-OH) che
conferiscono allo zucchero caratteristiche alcoliche;
un gruppo carbonilico (>C=O) che, a seconda di dove è
posizionato nella molecola, conferisce caratteristiche
aldeidiche o chetoniche.
1. I carboidrati
A seconda del numero di atomi di carbonio da cui
sono composti, i monosaccaridi si classificano in
triosi, tetrosi, pentosi, esosi.
A seconda del gruppo funzionale:
Aldosi
gruppo aldeidico —CHO
Copyright ©2009 Zanichelli
editore
Chetosi
gruppo chetonico —C=O
Le idee della chimica
I due monosaccaridi più semplici sono:
Il diidrossiacetone non presenta centri chirali e
quindi non presenta isomeria ottica.
1. I carboidrati
L’atomo di carbonio centrale della gliceraldeide
è un centro chirale, quindi il composto
presenta due enantiomeri.
La gliceraldeide prende il nome di L- o Dgliceraldeide a seconda il gruppo —OH si trovi
a sinistra oppure a destra del carbonio,
secondo le formule di Fisher.
1. I carboidrati
L’assegnazione della lettera si effettua a partire
dalle formule di Fisher.
La configurazione degli zuccheri si ricava per
confronto con la gliceraldeide.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
In campo biologico hanno importanza solo i
monosaccaridi della serie D.
Si definiscono epimeri molecole con più centri
chirali che differiscono per la posizione di un
solo centro.
aldosi
chetoesosi
– I monosaccaridi glucosio e fruttosio sono zuccheri a 6 atomi
di carbonio (esosi).
– Queste molecole contengono lo stesso numero e tipo di
atomi ma in disposizioni differenti: sono isomeri.
aldeide
C6H12O6
H
O
H
C
Glucosio
C
OH
C
O
HO
C
H
H
C
OH
H
H
C
OH
HO
C
H
H
C
OH
H
C
OH
H
C
OH
H
C
OH
H
C
OH
H
Fruttosio
H
chetone
Il ribosio è un esempio di zucchero a 5 atomi
di carbonio:
forme cicliche e semiacetali
In soluzione acquosa la maggior parte dei
monosaccaridi esiste in forma ciclica, a causa
della reazione tra il gruppo aldeico o
chetonico ed uno dei gruppi ossidrile.
In chimica questo tipo di reazione produce
composti detti semiacetali.
Struttura ciclica o ad anello del D-glucosio:
6 CH2OH
H
5C
H
H
4C
OH
CH2OH
O
H
C 1
OH
3C
H
OH
O
H
OH
O
H
OH
HO
C2
H
H
H
OH
Formula di
struttura
OH
Formula semplificata
(proiezione di Hawort)
Struttura
semplificata
Proiezione di Haworth
Nella proiezione di Haworth il bordo più vicino al
lettore è evidenziato con un tratto più spesso.
Anomeri e
Per effetto del processo di ciclizzazione si forma
un nuovo centro chirale (il primo atomo di
carbonio, il C-1).
Si producono due nuovi isomeri ottici, detti
anomeri e , tra di loro in equilibrio.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
anomeri e del D-glucosio
Le idee della chimica
-D-glucosio
-D-glucosio
L’esistenza di due forme anomeriche del
D-glucosio è di grande importanza biologica.
L’-D-glucosio è il costituente dell’amido e del
glicogeno e rappresenta il “combustibile” della
respirazione cellulare.
Il -D-glucosio è il costituente della cellulosa.
I monosaccaridi
1. I carboidratipresentano anelli a sei (piranosi)
oppure a cinque (furanosi) atomi di carbonio.
Il glucosio è un piranoso:
Il fruttosio è un furanoso:
Copyright ©2009 Zanichelli
editore
Le idee della chimica
monosaccaridi derivati
monosaccaridi derivati
Alcuni molecole derivate dai monosaccaridi
sono di grande importanza biologica.
Il 2-desossi-D-ribosio è un costituente del DNA.
Un amminozucchero acetilato, la
N-acetil-glucosammina, è costituente della
chitina.
L’acido N-acetilneuramminico è presente nei
rivestimenti polisaccaridici degli animali
superiori, nelle glicoproteine e glicolipidi.
1. I carboidrati
disaccaridi
Quando due monosaccaridi condensano per
reazione dell’—OH anomerico di un
monosaccaride con l’ —OH alcolico dell’altro
monosaccaride si ha la formazione di un
disaccaride con liberazione di una molecola
d’acqua.
Il legame che si forma prende il nome di legame
O-glicosidico.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
1. I carboidrati
I principali disaccaridi sono:
• saccarosio (-D-glucosio + -D-fruttosio)
• maltosio (-D-glucosio + -D-glucosio)
• lattosio ( -D-galattosio + D-glucosio)
• cellobiosio ( -D-glucosio + -D-glucosio)
Copyright ©2009 Zanichelli
editore
Le idee della chimica
maltosio
-D-glucosio + -D-glucosio
CH2OH
H
HO
CH2OH
O
H
OH
H
O
H
H
H
OH
H O
OH
H
H
H
OH
Glucosio
OH
H
OH
Glucosio
H2 O
CH2OH
H
HO
CH2OH
O
H
OH
H
H
H
H
O
OH
O
H
OH
H
Maltosio
H
OH
H
OH
saccarosio
-D-glucosio + -D-fruttosio
Il Saccarosio è il comune zucchero da tavola o zucchero di canna.
lattosio
-D-galattosio + -D-glucosio
Quanto è dolce il sapore dolce?
Oltre agli zuccheri, molti tipi di molecole hanno
un sapore dolce perché si legano ai recettori del
«dolce» presenti sulla lingua.
polisaccaridi
– I polisaccaridi sono polimeri formati da centinaia
o migliaia di molecole di monosaccaridi, unite tra
loro per condensazione.
Granuli di amido in
cellule di tubero di
patata
O
O
O
Granuli di glicogeno
nel tessuto muscolare
Monomeri
di glucosio
Amido
O
O
O
O O
O
O
O
Glicogeno
O
O O
Fibre di cellulosa nella parete di
una cellula vegetale
Molecole
di cellulosa
O
O
O
O
O
O
O
O
O
O
Cellulosa
OO
OO
OO
OO
O OH
O OH
O
OO
OO
O O
O O
O
O O
O
amido
1. I carboidrati
• l’amido, riserva energetica delle piante, è un
polimero formato da monomeri di -D-glucosio in
forma di amilosio, a catena pressoché lineare, e di
amilopectina a catena ramificata.
Le idee della chimica
glicogeno
1. I carboidrati
• il glicogeno, riserva energetica negli organismi
animali, è un polimero formato da monomeri di
-D-glucosio, ha una struttura molto ramificata
ed è costituito da più di 100.000 unità di
glucosio.
cellulosa
1. I carboidrati
• la cellulosa, costituente principale del mondo
vegetale, è formata da lunghissime catene
lineari di -D-glucosio, con massa molecolare
media di 500.000 u.
La linearità delle molecole di cellulosa ne
determina la possibilità di essere fascicolate in
modo da ottenere dei cavi resistenti.
La cellulosa è la sostanza organica più diffusa in
natura.
Solo alcuni microorganismi presentano l’enzima
cellulasi, che ne permette la digestione.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
1. I carboidrati
L’amido
e la cellulosa, formati da differente
anomeri del D-glucosio, differiscono per il tipo di
legame glicosidico che forma fra le molecole di
glucosio.
Copyright ©2009 Zanichelli
editore
Le idee della chimica
chitina
• E’ un polisaccaride formato da monomeri di
n-acetil-glucosammina, è uno dei principali
componenti dell'esoscheletro degli insetti e
degli altri artropodi, e della parete cellulare di
funghi. Dopo la cellulosa, la chitina è il più
abbondante biopolimero presente in natura.
lipidi
I lipidi sono un gruppo di molecole eterogenee dal punto
di vista chimico, ma tutte con un carattere più o meno
spiccatamente idrofobo.
Ad una più o meno totale insolubilità in acqua segue una
marcata solubilità nei solventi organici (cloroformio,
acetone, etere, benzene, ecc.)
I lipidi comprendono diversi composti di dimensioni
relativamente modeste se paragonati ai polisaccaridi o
alle proteine, formati prevalentemente da atomi di
carbonio e di idrogeno.
Funzioni dei lipidi nei processi biologici:
1. Fonte di energia (1 g lipidi → 9 kcal)
2. Riserva di energia
3. Componenti delle membrane cellulari
4. Protezione ed isolamento
5. Ormoni stereoidei
6. Vitamine liposolubili (A, D, E, K) ed il
loro assorbimento
7. Trasporto
Appartengono alla famiglia dei lipidi:
Trigliceridi (che includono i grassi animali e
gli oli vegetali, che sono le tra le
principali molecole energetiche
metaboliche)
Fosfolipidi (formano le membrane
biologiche), Sfingolipidi
Cere
Molecole Isoprenoidi: Terpeni e derivati
(vitamine), Steroidi (colesterolo e alcuni
ormoni)
Classificazione lipidi
Saponificabili
NON
Saponificabili
Acidi grassi
• insaturi
• saturi
acido palmitico (C16:0)
CH3(CH2)14CO2H
Acido oleico (18:1)
acido oleico (C18:1)
CH3(CH2)7CH=CH(CH2)7COOH
ω (posizione doppi legami)
Gli acidi grassi insaturi sono classificati in base al
numero e posizione dei doppi legami.
La posizione dei doppi legami è indicata dalla
loro distanza dall’ultimo carbonio della catena,
il carbonio ω.
La maggior parte degli acidi grassi monoinsaturi più
comuni sono ω-9, come l’acido oleico.
La presenza di un doppio legame in
configurazione cis determina un brusco
piegamento nella catena idrocarburica,
responsabile di un punto di fusione più basso
del corrispondente acido grasso saturo.
acido palmitico (C16:0)
CH3(CH2)14CO2H
I lipidi: quali sono
β-carotene
Steroidi
Doppio strato lipidico
Fosfatidilcolina
51
Sadava et al. Biologia La scienza della vita © Zanichelli editore 2010
acidi grassi essenziali
• Gli acidi grassi linoleico (C18:2) e linolenico (C18:3)
sono esempi di acidi grassi essenziali, così
denominati perché l’organismo non è in grado di
sintetizzarli.
Precursori
delle
prostagland
ine
acidi grassi essenziali ω-3
• Il nome di questi composti deriva dalla posizione
del primo doppio legame, iniziando il conteggio dal
carbonio terminale ω.
acido α-linolenico
Riducono la formazione di coaguli nel sangue e abbassano la
probabilità di attacchi di cuore. Ne sono ricchi la frutta secca e il
pesce.
Gli acidi grassi insaturi hanno temperatura di
fusione inferiore a quella degli acidi grassi saturi.
A Tamb gli acidi grassi insaturi sono liquidi, quelli
saturi sono solidi.
Ciò è dovuto al diverso numero di interazioni di
Van der Waals. Nei gli acidi grassi insaturi tali
interazioni sono impedite dal doppio legame cis.
La temperatura di fusione di un trigliceride
quindi dipende dagli acidi grassi che lo
compongono.
La prevalenza nei trigliceridi di acidi grassi
insaturi caratterizza gli oli vegetali.
La prevalenza di acidi grassi saturi invece
caratterizza il burro e in genere i grassi animali.
I trigliceridi
reazioni dei trigliceridi
1: Idrogenazione degli oli: da acidi grassi
insaturi ad acidi grassi saturi.
Es. Margarine da acidi grassi saturi
oli idrogenati
• L’idrogenazione aiuta a prevenire i danni agli
oli vegetali, infatti i doppi legami reagiscono
lentamente con l’ossigeno atmosferico
ossidandosi. Questo fenomeno è detto
irrancidimento.
• Gli oli idrogenati, in particolare se contengono
acidi grassi trans, sembrano essere molti
dannosi alla salute.
Le reazioni dei trigliceridi
2: Idrolisi dei trigliceridi:
mediante base forte → saponificazione
• Nella maggior parte dei fosfolipidi la testa
polare contiene un amminoalcol come la
serina o la colina
acido grasso
glicerolo
acido grasso
gruppo fosfato
colina
cere
Le cere sono lipidi solidi a Tamb e sono esteri di
un acido grasso con un alcol monovalente
alifatico a lunga catena, o con uno sterolo.
molecole isoprenoidi
Gli isoprenoidi contengono isoprene.
Gli isoprenoidi si classificano in:
1. Terpeni e loro derivati
2. Steroidi
Isoprene
molecole isoprenoidi:
vitamine liposolubili
Le vitamine liposolubili derivano dai terpeni:
• Vitamina A
• Vitamina D
• Vitamina E
• Vitamina K
Una vitamina è una sostanza indispensabile al
nostro organismo, ma non prodotta da esso. Deve
essere introdotta con la dieta.
Trans-Retinolo. Liposolubile. Presente in frutta e verdure, fegato e formaggi.
Forma i pigmenti visivi, aiuta la protezione dei tessuti epiteliali e delle mucose.
Sintomi da carenza: secchezza pelle e occhi, cecità notturna, sterilità maschile
vitamina A
Colecalciferolo. Liposolubile. Presente in prodotti caseari, pesce e cereali.
Sintetizzata dalla pelle in seguito all’esposizione solare. Funzione:
assorbimento calcio e fosforo. Sintomi da carenza: rachitismo.
vitamina D
Tocoferolo La vitamina E agisce come antiossidante, protegge da ossidazione
e radicali liberi. La carenza porta a sterilità, pelle secche e atrofia muscolare.
Presente nei vegetali.
vitamina E
La vitamina K regola la formazione di una proteina necessaria per la
coagulazione del sangue. La carenza comporta rischi di emorragie.
Escherichia coli
vitamina K
molecole isoprenoidi:
steroidi
Gli steroidi sono un gruppo di lipidi isoprenoidi che
che presentano una struttura di base formata da 4
anelli di atomi di carbonio, il nucleo steroideo,
l’idrocarburo saturo ciclopentanoperidofenantrene.
• In natura esistono moltissimi steroidi diversi
per struttura e funzione, il più comune e
abbondante negli animali è il colesterolo.
Gran parte del colesterolo prodotto dal fegato è
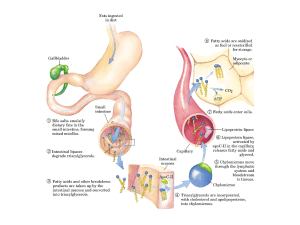
convertito in acidi biliari, componenti della bile.
La bile serve per emulsionare i grassi durante la
loro digestione nell’intestino
Il colesterolo può trasformarsi anche in ormoni
steroidei
• Ormoni steroidei femminili sono estrogeni e
progestinici
• Ormoni steroidei maschili sono gli androgeni
• Regolano la concentrazione di ioni e acqua i
mineralcorticoidi
• Regolano i livelli di glucosio, amminoacidi e
acidi grassi i glucocorticoidi