Capitolo 69.fm Page 1899 Thursday, April 26, 2007 9:33 AM
CAPITOLO
Augusta Balzarini
Salvatore Ferla
69
Principi di riabilitazione
del paziente oncologico
Introduzione
Le recenti acquisizioni nella prevenzione e nella diagnosi
precoce dei tumori, il miglioramento delle tecniche chirurgiche e l’impiego di nuovi farmaci chemioterapici hanno portato
a un incremento significativo dei sopravvissuti e a un aumento
della vita media dei pazienti con patologie tumorali. Di pari
passo è aumentata l’attenzione alle problematiche funzionali
legate agli esiti dei trattamenti causali e all’evoluzione della
malattia oncologica. La riabilitazione è diventata in questi anni
parte integrante dell’iter terapeutico del paziente, fornendo gli
strumenti più idonei per la prevenzione e la cura delle sequele
iatrogeniche, per il recupero delle funzioni lese, per la riduzione degli esiti cronici, per il miglioramento del benessere fisico,
per l’acquisizione di nuove abilità e di nuovi equilibri psicofisici, per la riscoperta di potenzialità residue e per il mantenimento di una qualità di vita al più alto livello possibile.
Il cancro e i trattamenti conseguenti (chirurgia, chemioterapia, radioterapia) sono responsabili in una percentuale rilevante di pazienti di lesioni anatomiche più o meno importanti
(dovute al coinvolgimento diretto o indiretto di strutture
vascolari, muscolari, nervose, ossee) che in molti casi determinano danni funzionali invalidanti e permanenti (compromissione della funzione respiratoria, fonatoria, deglutitoria,
minzionale, deambulatoria, ecc.). A questi vanno aggiunte le
problematiche psicologiche indotte dalla diagnosi di cancro
e dovute alla paura della morte e dell’evoluzione della malattia, alla perdita dell’integrità psico-corporea, al disfiguramento, ai cambiamenti della relazione con il partner e i
familiari, alla perdita del proprio ruolo all’interno della famiglia e nell’ambito sociale e lavorativo.
Tutti questi aspetti, insieme alla valutazione funzionale del
paziente e dello stato di malattia, vanno tenuti in considerazione nella definizione del programma riabilitativo che sarà
di necessità individuale e multidisciplinare, coinvolgendo a
seconda dei bisogni più figure professionali (fisiatra, fisioterapista, linfologo, neurologo, ortopedico, psicologo, tecnico
ortopedico, logopedista, enterostomista, assistente sanitario,
ecc.).
La conoscenza delle caratteristiche della neoplasia (tipo
istologico, sede, stadio, possibilità terapeutiche, prognosi,
ecc.) è di estrema importanza dal momento che lo stato di
malattia può condizionare il lavoro riabilitativo e richiedere
adeguamenti del programma, degli obiettivi e delle scelte
terapeutiche. Diversi saranno infatti gli interventi e le finalità
nei pazienti a buona prognosi (in cui sarà previsto un trattamento intensivo di carattere funzionale) rispetto a quelli con
limitata aspettativa di vita (in cui il trattamento potrà essere
esclusivamente di tipo palliativo).
Una corretta valutazione clinico-funzionale è sempre necessaria e va effettuata durante tutto l’iter della malattia per
meglio adattare l’intervento riabilitativo all’evolversi della
patologia e ai bisogni del paziente. Indispensabile quindi una
valutazione delle condizioni generali del paziente, delle patologie concomitanti, un esame muscolare e articolare completo
ma con particolare riguardo al territorio sede della neoplasia,
una analisi dei deficit precoci e tardivi, una valutazione della
postura generale, delle modalità di carico, della tipologia di
deambulazione, della presenza di dismorfismi/paramorfismi a
carico della colonna e degli arti, della dinamica respiratoria di
base, delle funzioni cognitive, delle abilità e capacità a svolgere attività complesse. Particolare attenzione dovrà essere
posta anche alla valutazione della personalità del paziente, al
suo ruolo sociale e lavorativo, alle aree di maggiore interesse,
alle motivazioni e alle aspettative, al grado di collaborazione,
alle potenzialità che saranno di grande aiuto per lo sviluppo di
strategie alternative in caso di deficit funzionali permanenti.
Sulla base di tutti questi dati il fisiatra insieme al fisioterapista e al paziente potrà definire il programma riabilitativo,
le modalità e il tipo di intervento, i tempi e le possibilità di
recupero, coadiuvato quando necessario dagli altri componenti dell’équipe.
Data l’ampiezza dell’argomento – ogni neoplasia si presenta infatti con quadri riabilitativi peculiari – abbiamo scelto di
prendere in considerazione quelli di maggiore interesse riabilitativo e di più frequente osservazione nella pratica clinica.
Neoplasie della mammella
L’introduzione di tecniche chirurgiche meno demolitive, il
ricorso sempre più frequente alla metodica della biopsia del
linfonodo sentinella (BLS), la riduzione delle dosi e dei
campi di radioterapia, la maggiore informazione alle pazienti
Capitolo 69.fm Page 1900 Thursday, April 26, 2007 9:33 AM
1900
69. PRINCIPI DI RIABILITAZIONE DEL PAZIENTE ONCOLOGICO
e la continua sensibilizzazione dei chirurghi hanno portato
negli ultimi anni a una progressiva diminuzione dell’ incidenza e dell’entità degli esiti iatrogenici. Problematiche riabilitative sono comunque di osservazione frequente nelle pazienti sottoposte a chirurgia mammaria con dissezione ascellare
ed è compito dello staff riabilitativo prevenirle e trattarle
precocemente per salvaguardare la qualità di vita della paziente e per facilitarne la ripresa funzionale, sociale e lavorativa (Tab. 69.1)
La prevenzione delle sequele inizia in sala operatoria: il
chirurgo dovrebbe limitare il più possibile, pur nel rispetto
della radicalità chirurgica, i danni funzionali ed estetici, evitando di posizionare l’arto in iperabduzione, conservando
strutture muscolari e nervose, riducendo l’uso dell’elettrobisturi, evitando la tensione dei lembi di chiusura, confezionando medicazioni non troppo costrittive e limitanti.
Allo staff riabilitativo spetta invece la valutazione precoce
dei deficit funzionali e il loro trattamento specifico.
Il dolore, sintomo di più comune osservazione (85% dei
casi) nell’immediato postoperatorio, viene riferito dalla maggior parte delle pazienti all’articolazione scapolo-omerale,
alla scapola, all’ascella, alla parete toracica, al braccio. È in
genere dovuto alla posizione dell’arto durante la seduta
operatoria, al trauma chirurgico, alla flogosi della capsula
articolare e della cuffia dei rotatori (in particolare del sovraspinato), alle lesioni nervose, alle exeresi muscolari, alla
presenza del drenaggio.
Il posizionamento dell’arto in iperabduzione può determinare lo stiramento dei muscoli flessori del braccio con retrazione muscolo-tendinea, limitazione ai movimenti di flessione e abduzione del braccio e di estensione del gomito, dolore
alla palpazione lungo i muscoli interessati. In alcuni casi può
associarsi la retrazione della fascia muscolare o la flogosi dei
linfatici in forma di sottili cordoni dolorosi visibili e palpabili al di sotto della cute dall’ascella al gomito. Sono anch’essi causa di dolore e limitazione al movimento della spalla e
del gomito.
Le limitazioni articolari coinvolgono sia l’articolazione
scapolo-omerale che la scapolo-toracica. La loro incidenza
varia dal 15 al 50% dei casi. Ne sono causa le flogosi della
capsula e della cuffia dei rotatori, il dolore locale, la tensione
della ferita, la paura di sentire dolore, la presenza del drenag-
Tab. 69.1. Esiti riabilitativi nel carcinoma mammario.
Chirurgia
Chirurgia ricostruttiva
Radioterapia
Chemioterapia
Evoluzione
Dolore
Limitazioni articolari
Retrazioni fasciali
Lesioni nervose
Linfedema
Dolore
Limitazioni articolari
Alterazioni posturali
Radiodermite acuta
Fibrosi cutanee
Plessopatia
Linfedema
Neuropatie
Flebiti chimiche
Metastasi ossee
Plessopatie evolutive
Compressioni midollari
Sindromi da allettamento
Linfedema maligno
gio, le lesioni nervose (toracico lungo, toracici anteriori,
intercostobrachiale, plesso brachiale), la sclerosi dei linfatici,
le cicatrici retraenti e aderenti, le retrazioni fasciali.
Per favorire la ripresa funzionale dell’arto e per evitare
l’instaurarsi di atteggiamenti di protezione rigidamente antalgici è buona norma iniziare già nei primi giorni successivi
all’intervento una mobilizzazione attiva e passiva dell’arto
superiore e del rachide cervico-dorsale, sia al letto della
paziente sia in palestra. La mobilizzazione non dovrà superare all’inizio i 90° di flessione per evitare l’eccessiva trazione
dei lembi e la maggiore produzione di siero. In questa fase
potranno essere impiegati farmaci antinfiammatori, terapie
fisiche (laser, magnetoterapia, ultrasuoni) o manuali per ridurre il dolore e per favorire la circolazione linfatica e venosa.
Retrazioni fasciali, dolore, limitazioni articolari e sclerosi
linfatiche si possono osservare anche dopo BLS, ma in una
limitatissima percentuale di pazienti e solo nelle prime settimane dopo l’intervento.
La lesione del nervo toracodorsale è assai poco frequente
e comporta deficit del muscolo grande dorsale con limitazione ai movimenti di adduzione e rotazione interna del braccio.
La sofferenza dei nervi toracici anteriori causa ipovalidità
dei muscoli grande e piccolo pettorale, con riduzione nell’immediato della mobilità della spalla e del braccio. A più lunga
distanza l’ipotrofia dei muscoli può compromettere un successivo intervento ricostruttivo.
Il deficit del toracico lungo si verifica nel 17-30% dei casi.
L’incidenza risulta più elevata negli interventi conservativi
per una maggiore difficoltà a isolare il nervo in un campo
operatorio più ristretto. Il deficit nervoso comporta alaggio
del margine mediale della scapola, spostamento mediale e
superiore del suo angolo inferiore, dolore in regione scapolare, contrattura dei muscoli agonisti e antagonisti (trapezio,
elevatore della scapola, romboidi), limitazione all’elevazione
dell’arto al di sopra della testa con gomito esteso. Il deficit è
in genere completamente recuperabile entro 6 mesi dall’intervento. Per facilitare questo recupero andranno impostati
precocemente esercizi di attivazione della muscolatura funzionalmente valida e di rilassamento di quella contratta per
evitare l’instaurarsi di blocchi articolari, di dolori cronici e di
alterazioni posturali.
La lesione del nervo intercostobrachiale, presente nel 5070% delle pazienti subito dopo l’intervento, è responsabile di
una sintomatologia algico-disestesica variabile per intensità,
durata e distribuzione. Le pazienti riferiscono ipoestesia o
anestesia al cavo ascellare e alla faccia mediale del braccio,
sensazione di intorpidimento, di cuscinetto, di spillo. Queste
sensazioni tendono a diminuire gradualmente nel corso del
primo anno, ma nel 5-7% possono peggiorare con comparsa
di iperestesia, allodinia, dolore costrittivo, lancinante, a
morso di cane. Il dolore, se particolarmente intenso, può
comportare limitazioni articolari e/o posizioni antalgiche,
può interferire nelle attività quotidiane, può provocare o
aggravare uno stato ansioso-depressivo. Le terapie fisiche
(magnetoterapia, elettrostimolazioni transcutanee) e quelle
farmacologiche (antidepressivi triciclici, L-acetilcarnitina,
gabapentina) danno risultati in genere soddisfacenti ma duraturi solo in una percentuale limitata di pazienti.
Lo stiramento del plesso brachiale si verifica nello 0,5-1%
dei casi ed è dovuto all’abduzione dell’arto oltre i 90° e alla
rotazione controlaterale del capo. Coinvolge i contingenti alti
del plesso: n. muscolocutaneo (m. bicipite e coracorachiale),
meno frequentemente l’ascellare (m. deltoide) e il mediano
(m. flessori dell’avambraccio).
Capitolo 69.fm Page 1901 Thursday, April 26, 2007 9:33 AM
1901
Neoplasie della mammella
Le plessopatie brachiali sono di comparsa tardiva e riconoscono per lo più una genesi postattinica. I sintomi più
caratteristici sono deficit motorio da coinvolgimento dei
contingenti alti del plesso, ad andamento prossimo-distale,
alterazioni sensitive (ipoestesia, parestesie), linfedema a
lento sviluppo e di consistenza fibrosa e dolore di comparsa
tardiva e di intensità lieve-moderata. Nei casi particolarmente compromessi si potrà arrivare alla plegia dell’arto e alla
comparsa di distrofie cutanee e ungueali. Le modalità di
insorgenza, le caratteristiche del dolore e del linfedema saranno di grande aiuto nella diagnosi differenziale con le
forme evolutive (Tab. 69.2). Il trattamento riabilitativo delle
plessopatie postattiniche sarà diretto al contenimento
dell’edema e al recupero della funzionalità dell’arto, facendo
ricorso a terapie motorie, neuromotorie, drenanti, compressive-contenitive, ortesiche.
Il linfedema costituisce la complicazione tardiva più frequente degli interventi di dissezione ascellare.
L’incidenza varia dal 20 al 30% dopo sola chirurgia e dal
50 al 60% dopo chirurgia e radioterapia sulle stazioni linfonodali limitrofe alla sede di intervento (sovraclaveari, ascella,
catena mammaria). Dopo biopsia del linfonodo sentinella
l’incidenza di linfedema varia dal 3 al 5%.
Sul piano fisiopatologico le conseguenze della chirurgia e
della radioterapia si traducono in un sovraccarico funzionale
del circolo linfatico, che porta a un accumulo anomalo di
liquido e macromolecole proteiche a livello dell’interstizio,
il cui ristagno richiama per effetto osmotico altro liquido
nell’interstizio e causa, nei componenti connettivali, una
reazione infiammatoria locale con iperproduzione di tessuto
connettivo e ispessimento fibrotico dei tessuti. La stasi linfatica crea inoltre un ottimo terreno per lo sviluppo di infezioni
batteriche acute e croniche che portano a fenomeni perilinfangiosclerotici e ostruzioni endoluminari, con conseguente
ulteriore aggravamento dell’edema.
Nei casi sottoposti a radioterapia, la fibrosi dei tessuti
cutanei e sottocutanei provoca ostacolo al flusso linfatico,
compromissione della contrattilità del vaso linfatico e inibizione della rigenerazione dei linfatici superstiti.
Oltre alla chirurgia e radioterapia, altri fattori possono
giocare un ruolo predisponente o favorente: le variazioni anatomiche del sistema linfatico, la presenza o assenza delle vie
collaterali, il numero di linfonodi asportati, alcune complicazioni postoperatorie (sieroma, ematomi, infezioni, ritardo di
cicatrizzazione, trombosi venose profonde, limitazioni e blocchi articolari), le linfangiti ricorrenti, i dismetabolismi (ipertensione arteriosa, obesità, diabete), le attività lavorative faticose e ripetitive, i traumi e i microtraumi ripetuti. La diagnosi
Tab. 69.2. Diagnosi differenziale nelle plessopatie brachiali.
Plessopatia postattinica
Deficit sensitivi
(ipoestesia, parestesie)
Deficit motori prossimali
(deltoide, bicipite, tricipite)
Coinvolgimento contingenti alti
Linfedema a componente
linfatica
Dolore
di linfedema è soprattutto clinica e strumentale. La valutazione delle modalità di insorgenza, dell’intervallo di comparsa,
delle dimensioni dell’arto e della consistenza, del colore, della
presenza di calore, di dolore, di sclerosi tissutale, di fovea,
della funzionalità del cingolo superiore, del trofismo muscolare, dello stato della cute, di eventuali patologie concomitanti
potrà fornire importanti informazioni per un corretto inquadramento diagnostico e per la definizione del piano di trattamento. A completamento dell’esame clinico potranno essere effettuate indagini strumentali, quali ad esempio l’ecografia ad alta
risoluzione (per definire sede, entità dell’edema, grado di
imbibizione e/o di fibrotizzazione), l’eco-color-Doppler (nei
casi di sospetta compromissione del circolo venoso) e la
linfoscintigrafia (per lo studio anatomico e funzionale del
circolo linfatico superficiale e profondo). TC e RM andranno
invece riservate ai casi in cui vi sia il sospetto clinico di una
recidiva loco-regionale di malattia come causa del linfedema.
Il trattamento del linfedema deve essere personalizzato,
individualizzato e prevedere l’impiego di più metodiche
(manuali, meccaniche, compressive, contenitive, motorie,
farmacologiche) tra loro variamente combinate (Tab. 69.3).
Il linfodrenaggio è sicuramente il trattamento di scelta nei
linfedemi di qualsiasi stadio e dimensione, in quanto in grado
di favorire il riassorbimento dei liquidi e delle proteine
dall’interstizio e di accelerare il flusso linfatico. Le tecniche
possono essere diverse (Vodder, Foldi, Leduc), ma se correttamente applicate risultano ugualmente efficaci. La terapia
deve essere completata dall’applicazione di un bendaggio
multistrato, confezionato utilizzando bende monoelastiche, a
medio o corto allungamento, applicate in strati sovrapposti in
modo da realizzare la massima azione di compressione durante il lavoro muscolare. In alcuni casi al di sotto del bendaggio
possono essere usati degli spessori in lattice per ridurre la
pressione in corrispondenza di eminenze ossee (gomito, polso) o per aumentare la compressione nelle aree in cui l’edema
è di maggiori dimensioni e consistenza. Se ben tollerato, il
bendaggio va mantenuto in sede fino alla seduta successiva.
Al termine del ciclo di trattamento il bendaggio verrà
sostituito da un tutore elastico il cui scopo è quello di mantenere e migliorare i risultati ottenuti. Sono disponibili in commercio bracciali al polso, al metacarpo, guanti confezionati
su misura o preconfezionati, a pressione graduata da distale
a prossimale e di diversa classe di compressione (dalla I che
esercita pressioni distali di 20-30 mmHg, fino alla III con
pressioni di 40-50 mmHg). Nella scelta del tipo e della classe
di compressione vanno tenuti in considerazione l’entità, la
distribuzione dell’edema, l’età della paziente, lo stile di vita,
l’attività lavorativa.
Nei casi in cui il linfodrenaggio non dia risultati soddisfacenti e duraturi nel tempo si può associare la pressoterapia
sequenziale. Il trattamento prevede sedute giornaliere di 3060 minuti ciascuna con pressioni variabili da 40 a 50 mmHg:
Plessopatia evolutiva
Dolore
Tab. 69.3. Terapia del linfedema.
Deficit sensitivi
Terapia di attacco
Linfedema a componente venosa
Deficit motori
Terapia di mantenimento
Coinvolgimento C8-T1
Sindrome Claude Bernard-Horner
Linfodrenaggio manuale
Bendaggio multistrato
Chinesiterapia
Linfodrenaggio manuale
Supporto elastico
Chinesiterapia
Terapia farmacologica
Terapia meccanica
Capitolo 69.fm Page 1902 Thursday, April 26, 2007 9:33 AM
1902
i tempi di applicazione, le pressioni e la durata del trattamento
vanno definiti sulla base delle dimensioni e della consistenza
dell’edema. Per evitare fenomeni di ingorgo linfatico e fibrosi
alla radice dell’arto, la pressoterapia sequenziale non deve
mai essere impiegata da sola ma sempre in associazione a
linfodrenaggio, bendaggio o altri trattamenti drenanti.
La terapia motoria viene utilizzata per facilitare il flusso
linfatico attraverso la contrazione muscolare e le variazioni di
pressione endoaddominale ed endopleurica indotte dagli atti
respiratori. Consente di migliorare il trofismo muscolare
dell’arto e la funzionalità del cingolo scapolare e di correggere
eventuali alterazioni posturali. Viene in genere effettuata al
termine delle sedute di trattamento e sotto elastocompressione.
Per mantenere e migliorare i risultati ottenuti dalle terapie
può essere utile, in alcuni casi, ricorrere a un trattamento
farmacologico di supporto. Gli α-benzopironi (cumarina e
derivati) e i y-benzopironi (diosmina, rutina) si sono dimostrati i farmaci più attivi, specie se utilizzati negli stadi iniziali
del linfedema quando la parete del vaso ha conservato la sua
contrattilità e quando non si sono ancora instaurati fenomeni
fibrotici a carico dell’interstizio.
Le eparine a basso peso molecolare trovano indicazione
nella terapia e nella profilassi delle trombosi venose profonde.
Gli antibiotici e gli antinfiammatori vanno prescritti in caso
di complicazioni flogistiche, linfangiti, erisipela. Sono da preferire le penicilline, le cefalosporine e i macrolidi, somministrati a dosaggio pieno per almeno 7-10 giorni, in associazione
ad antipiretici e antinfiammatori. Nei casi gravi può essere
utile uno steroide: betametasone 4 mg per 3 giorni e successivamente 2 mg per 4 giorni. Nelle forme ricorrenti (più di tre
episodi acuti l’anno) è indispensabile instaurare un trattamento
preventivo con penicillina ad azione prolungata, alla dose di
1.200.000 UI ogni 15-21 giorni per almeno un anno.
Problematiche funzionali si possono osservare anche dopo
interventi ricostruttivi con protesi a espansione o con lembi
miocutanei di retto addominale o grande dorsale.
Nel primo caso è frequente la presenza di dolore in sede di
intervento, limitazione nei movimenti della spalla e nella
dinamica respiratoria, con atti respiratori più brevi e superficiali, contratture muscolari e posture scorrette. Un adeguato
controllo del dolore con farmaci antinfiammatori e miorilassanti, associato a una rieducazione motoria precoce, consente
di riprendere e mantenere la funzionalità del cingolo scapolotoracico e di ridurre lo stato miotensivo.
Negli interventi di ricostruzione con lembi miocutanei il
trattamento riabilitativo deve essere diretto soprattutto al
controllo del dolore locale, generalmente avvertito al torace
e alla scapola nelle ricostruzioni con grande dorsale, alla
colonna e all’addome in quelli con retto addominale. In
questi ultimi il dolore può essere di maggiore intensità e
durata ed è legato alla necessità di mantenere, nei primi
giorni, posizioni obbligate semisedute e con arti inferiori
flessi. Esercizi attivi e passivi, di rinforzo e di rilassamento,
esercizi respiratori e deambulazione assistita andranno impostati per il ripristino della funzionalità dei cingoli, superiore per gli interventi con grande dorsale e inferiore per gli
interventi con retto addominale, della deambulazione e della
dinamica respiratoria e per evitare retrazioni tissutali e alterazioni posturali del rachide.
Nelle pazienti sottoposte a radioterapia possono comparire manifestazioni cutanee locali che vanno dall’eritema
all’edema, alla desquamazione secca e umida fino alle ulcere.
In alcuni casi può essere necessaria la sospensione temporanea del trattamento, ma nella maggior parte delle pazienti il
69. PRINCIPI DI RIABILITAZIONE DEL PAZIENTE ONCOLOGICO
quadro si risolve spontaneamente o ricorrendo all’applicazione di creme emollienti, pomate cortisoniche o a sedute di
laser e magnetoterapia.
Più tardivamente possono comparire iperpigmentazione,
teleangectasie, fibrosi cutanee e sottocutanee responsabili a
volte di blocchi o limitazioni articolari, plessopatie brachiali,
linfedema e, meno frequentemente, fibrosi polmonari, polmoniti, pericarditi (1%). Tutte queste complicazioni possono
essere evitate, o ridotte di intensità, instaurando o proseguendo anche durante la radioterapia un programma motorio che
consenta di mantenere la funzionalità articolare, la circolazione linfatica e venosa e l’elasticità tissutale. In caso di
fibrosi marcata e di cicatrici retraenti può risultare utile
associare terapie fisiche (magnetoterapia, ultrasuoni) o manuali (massaggio di scollamento, linfodrenaggio, stretching,
chinesiterapia).
L’impiego di alcuni chemioterapici (cisplatino, taxani)
può determinare la comparsa di neuropatie periferiche, per
lo più di tipo sensitivo, con parestesie, iperestesia alle mani e
ai piedi, disturbi dell’equilibrio e della deambulazione, impaccio motorio, diminuzione dei riflessi profondi. Il danno
sensitivo è in genere completamente reversibile a distanza di
alcuni mesi dall’interruzione della terapia. Il recupero può
essere accelerato da un trattamento motorio-propriocettivo e
dall’impiego di farmaci quali antidepressivi triciclici (amitriptilina) e antiepilettici (gabapentina, pregabalin).
Le flebiti chimiche da fuoriuscita accidentale di chemioterapici possono presentarsi con quadri diversi in relazione al
tipo, alla quantità di farmaco stravasato, alla sensibilità locale
e allo stato generale del paziente. Si potrà avere dolore,
arrossamento, edema, necrosi. Tardivamente potranno comparire fibrosi, retrazioni, limitazioni articolari. La terapia
dovrà essere instaurata precocemente e dipenderà dal tipo di
lesione: laser, magnetoterapia, antinfiammatori, antibiotici,
antidolorifici; in caso di fibrosi o retrazione: terapie motorie,
massaggio di scollamento, ultrasuoni.
Neoplasie dei tessuti molli
L’introduzione di tecniche chirurgiche conservative ha permesso di ricorrere sempre meno a interventi demolitivi e
invalidanti (amputazioni, disarticolazioni) ma non ha ridotto
l’incidenza delle complicazioni. L’importanza delle strutture
anatomiche coinvolte dall’intervento (ossee, nervose, muscolari, vascolari) e dalle terapie complementari richiede che il
fisiatra lavori in stretta collaborazione con l’équipe chirurgica e con i radioterapisti per ridurre al minimo i danni funzionali pur nel rispetto della radicalità oncologica. In quest’ottica il chirurgo può essere considerato il primo riabilitatore, dal
momento che deve porre particolare attenzione alla conservazione delle strutture nervose, vascolari e muscolari necessarie alla stabilità di un’articolazione o all’allestimento di un
moncone funzionalmente valido, alla salvaguardia dei muscoli agonisti, al ripristino delle linee di trazione dopo trasposizione di fasci muscolari, all’integrità delle strutture ossee
indispensabili al carico o all’utilizzo di un arto.
Nelle amputazioni le problematiche riabilitative sono soprattutto quelle legate alla necessità di arrivare a una protesizzazione rapida ed efficace. Questa richiede da un lato
l’allestimento di un moncone adeguato e di un livello ottimale
di amputazione e dall’altro un programma riabilitativo mirato
e impostato precocemente. Terapie motorie, fisiche, manuali
Capitolo 69.fm Page 1903 Thursday, April 26, 2007 9:33 AM
1903
Neoplasie del distretto cervico-facciale
(massaggio di sfioramento, linfodrenaggio), contenitive
(bendaggio elastico) e farmacologiche andranno messe in
atto per il controllo del dolore postoperatorio e da arto fantasma, per evitare posizioni scorrette del moncone, per mantenere tono e trofismo muscolare e per prevenire l’edema. A
partire dalla 20a-30a giornata potrà essere utilizzata la protesi:
inizialmente fornita di una invasatura provvisoria per adattarsi alle eventuali modifiche del moncone e per rendere la cute
anelastica nei punti di appoggio, successivamente modificata
e sostituita da quella definitiva. Le protesi classiche ad armatura metallica hanno subito una progressiva evoluzione grazie alle nuove acquisizioni tecnologiche e all’uso di materiali
(fibre di carbonio, polipropilene, leghe di titanio) che uniscono caratteristiche di leggerezza, robustezza, resistenza e durata. Particolarmente interessanti si sono dimostrate le protesi
mioelettriche e quelle “intelligenti” capaci di adattarsi automaticamente alle diverse velocità di cammino.
Anche gli interventi conservativi possono portare a sequele riabilitative importanti ed estremamente diversificate a
seconda della sede interessata. Le demolizioni in regione
glutea causano destabilizzazione dell’articolazione coxofemorale, mancato controllo del bacino in stazione eretta e
durante la deambulazione, ipovalidità all’estensione, abduzione e rotazione esterna della coscia, difficoltà a fare le scale
e nel passaggio dalla posizione seduta a quella eretta. L’exeresi parziale o totale del quadricipite o la lesione completa
del nervo femorale può compromettere pesantemente lo
svolgimento delle attività quotidiane, quali deambulazione,
salita e discesa delle scale e corsa, a causa della mancata
stabilità del ginocchio. Al contrario, le demolizioni della
regione adduttoria non alterano la funzionalità dell’arto ma
comportano sierosità abbondanti, flogosi locali, infezioni che
riducono l’autonomia dei pazienti nei mesi immediatamente
successivi all’intervento. Anche se meno frequenti le exeresi
a carico delle formazioni muscolari dell’arto superiore possono coinvolgere i muscoli che hanno inserzione sulla scapola (sovra e sottospinato, sottoscapolare, grande e piccolo
rotondo, romboidi, trapezio, deltoide, dentato anteriore),
sulla clavicola (scaleni, sternocleidomastoideo) e sull’omero
prossimale (grande dorsale, grande pettorale). In questi casi,
oltre a un marcato deficit funzionale a carico del cingolo
scapolo-toracico, si potranno avere ripercussioni funzionali
gravi sia sull’assetto del cingolo stesso sia sulla colonna,
specie a livello cervico-dorsale.
La complessità e la variabilità di questi quadri clinici
richiede programmi riabilitativi precoci, precisi e mirati, tali
da consentire una rapida risoluzione del deficit o un suo
adeguato compenso. Potranno essere impiegate tecniche motorie, di facilitazione muscolare, propriocettive, di rilassamento, esercizi specifici per la muscolatura residua, per i
passaggi posturali, per il controllo del cammino e della stazione eretta. Dove necessario si potrà ricorrere ad ausili
ortesici quali canadesi, stabilizzatori di ginocchio, carrozzine, reggibraccia, immobilizzatori, o a bendaggi elastici per
favorire il ritorno venoso ed evitare l’edema. L’intervento
riabilitativo sarà ancora più efficace se nella fase preoperatoria è stata fornita un’adeguata informazione al paziente sui
possibili danni funzionali, sulle possibilità di compenso, sugli
eventuali deficit residui permanenti e soprattutto se è stata
effettuata un’accurata valutazione fisiatrica relativa all’assetto e alla funzionalità della colonna, del bacino, delle principali articolazioni e strutture muscolari, alle modalità di innervazione, alla tipologia di cammino, alla presenza di dolore.
Neoplasie del distretto
cervico-facciale
La complessità anatomica della regione cervicale rende ragione della maggior parte delle sequele postchirurgiche.
Strutture muscolari, nervose e vascolari possono essere interessate direttamente o indirettamente dall’atto chirurgico o
dalle terapie complementari ad esso associate. Disfunzioni
uditive e vestibolari possono conseguire al trattamento chemioterapico. Gusto e olfatto possono essere alterati dalla
radioterapia e da alcuni farmaci chemioterapici. Il cambiamento dell’aspetto fisico, il disfiguramento conseguente ad
alcuni interventi ampiamente demolitivi, la perdita della
voce, delle capacità lavorative o socio-relazionali possono
instaurare stati depressivi fino all’autoisolamento e rendere
difficile il rapporto con i terapeuti. Le funzioni motorie, la
masticazione, la deglutizione, la fonazione possono essere
compromesse dalla radioterapia, ma soprattutto dalla chirurgia. I quadri clinici potranno essere di entità differente a
seconda che l’intervento sia conservativo (del nervo accessorio-spinale e delle strutture muscolari) o demolitivo. Sia in un
caso che nell’altro avremo deformazione del profilo del collo,
rigidità ai movimenti del rachide cervicale, contrattura da
stiramento dei muscoli romboidi, angolare della scapola, dei
legamenti dell’articolazione scapolo-omerale, delle radici del
plesso cervicobrachiale, dolore al collo, alla scapola, al moncone della spalla, amiotrofia da paralisi (in caso di sezione
del nervo spinale) della porzione superiore del trapezio, abbassamento del moncone della spalla, scapola alata, limitazione dei movimenti di flessione e abduzione del braccio,
parestesie, disestesie in regione laterocervicale e deltoidea,
edema localizzato al volto. Nei casi in cui all’intervento
chirurgico faccia seguito la radioterapia, i quadri clinici sopra
ricordati possono subire aggravamenti più o meno marcati.
Al deterioramento funzionale possono associarsi manifestazioni quali mucosite, disfagia, disgeusia, xerostomia ed
edema locale, che portano ad un ulteriore peggioramento
della deglutizione, dell’alimentazione e delle condizioni generali del paziente. Data la complessità delle problematiche
è sempre necessario ricorrere a un trattamento riabilitativo
adeguato alle necessità del paziente, mirato alla prevenzione
e riduzione dei danni iatrogenici e, dove possibile, multidisciplinare, coinvolgendo figure come il logopedista, il dietologo, lo psicologo. Potranno essere impiegate tecniche respiratorie (per migliorare la ventilazione, la dinamica toracica e
addominale, favorire l’eliminazione delle secrezioni in assenza del riflesso della tosse); esercizi attivi e passivi per il
cingolo scapolare (per favorire il rilassamento, evitare posture scorrette, contratture muscolari, per il recupero della funzionalità della spalla e del collo); metodiche quali lo
stretching multidirezionale, il pompage, il massaggio, il linfodrenaggio; terapie fisiche (magnetoterapia, laser, ultrasuono) per ridurre i tempi di recupero, evitare l’instaurarsi di
dolori cronici, prevenire e ridurre le fibrosi cutanee e sottocutanee da radioterapia. Nei pazienti con problemi di deglutizione l’impiego di tecniche logopediche e di strategie compensatorie è di fondamentale importanza per il recupero della
funzione e per eliminare il rischio di complicazioni da aspirazione. Il trattamento prevede esercizi attivi e passivi per
mantenere e incrementare la funzionalità delle strutture residue, il tono muscolare, l’elasticità dei tessuti, procedure di
integrazione motoria, stimolazioni tattili e termiche, manovre
Capitolo 69.fm Page 1904 Thursday, April 26, 2007 9:33 AM
1904
specifiche di deglutizione, nonché strategie di compenso
posturale, miglioramento degli imput sensitivi, cambiamenti
nelle caratteristiche dei cibi (viscosità, consistenza, volume,
temperatura, sapore).
Neoplasie polmonari
In questi tipo di neoplasie il trattamento riabilitativo riveste
un ruolo fondamentale per la prevenzione di complicazioni a
breve e lungo termine.
In tutti i pazienti candidati a chirurgia il piano di trattamento deve prevedere una fase preoperatoria e una fase da proseguire nel postoperatorio e durante le eventuali terapie complementari.
Prima dell’intervento occorre valutare le condizioni generali del paziente, lo stato cardiocircolatorio, le pregresse
patologie respiratorie (asma, enfisema, bronchite cronica),
gli esami ematochimici (emoglobina, ematocrito, elettroliti
plasmatici), lo stadio della malattia, la presenza di metastasi
a distanza. In modo specifico andrà studiata la dinamica
respiratoria di base, il tipo di respiro (toracico, diaframmatico), la validità della tosse, la presenza e il tipo di secrezioni,
la postura, gli eventuali dimorfismi della colonna. Il paziente
andrà istruito sulle principali tecniche respiratorie e ne andrà
spiegata l’utilità in modo chiaro e facilmente comprensibile.
La presa di coscienza del proprio respiro, la comprensione
delle tecniche e la collaborazione del paziente saranno fondamentali nella fase postoperatoria per migliorare la dinamica respiratoria, per facilitare la tosse e l’eliminazione delle
secrezioni, per controllare il dolore, per ridurre il rischio di
complicazioni broncopneumoniche. Subito dopo l’intervento
il programma riabilitativo andrà proseguito con esercizi specifici, impiego di incentivatori respiratori, terapie farmacologiche (mucoliti, fluidificanti, espettoranti), manuali e fisiche
in presenza di dolore, contratture muscolari antalgiche, esercizi per gli arti superiori e inferiori, tosse assistita, umidificazione, controllo della postura.
Neoplasie colo-rettali
Solo gli interventi che comportano l’allestimento di una colostomia rappresentano indicazione al trattamento riabilitativo.
A causa della rilevanza del danno subito dal paziente e
dell’entità delle sequele, il trattamento riabilitativo deve essere multidisciplinare per garantire al paziente stomizzato un
regime di vita il più normale possibile e per aiutarlo nell’accettazione della menomazione. Presupposto fondamentale
dell’intervento riabilitativo deve essere una corretta informazione al paziente e alla sua famiglia sul tipo di intervento, sulle
sue complicazioni, sulla funzione della colostomia, sulle possibilità riabilitative e la scelta di una idonea posizione della
stomia, elemento indispensabile per la sua gestione e la riabilitazione postoperatoria. Il primo passo della riabilitazione è
quello di far prendere confidenza al paziente con la propria
stomia e insegnarne la gestione, ad esempio istruendolo sulle
manovre di preparazione e di pulizia della cute, di applicazione e di sostituzione della sacca. Per venire incontro alle
diverse esigenze dei pazienti sono stati messi in commercio
vari tipi di presidi stomali: sacche impermeabili agli odori,
antifruscio, con filtro per i gas, con adesivi meno allergizzanti,
con barriere protettive totali. La scelta del prodotto dipenderà
69. PRINCIPI DI RIABILITAZIONE DEL PAZIENTE ONCOLOGICO
dal tipo di stomia, dal tipo di pelle, dalla quantità del materiale
evacuato, dai “gusti” del paziente, dall’utilizzo o meno dell’irrigazione. Quest’ultima rappresenta infatti il mezzo migliore
per il controllo delle evacuazioni e per la regolarizzazione
delle funzioni intestinali. La metodica dovrebbe essere iniziata solo quando la stomia è meglio consolidata (circa un mese
dopo l’intervento) e il paziente più collaborante. All’inizio
dovrebbe essere effettuata quotidianamente per un periodo di
10-15 giorni per valutarne l’efficacia e la tollerabilità. In
seguito, la frequenza andrà adattata alle esigenze del paziente
e all’attività intestinale (ad es., ogni 2-3 giorni).
Anche l’alimentazione può giocare un ruolo terapeutico
importante, soprattutto per prevenire problemi quali eccessiva eliminazione di gas, cattivi odori, scarsa continenza ed
eccessiva frequenza delle evacuazioni, stipsi. L’alimentazione dovrà essere il più libera possibile e adattata ai gusti e alle
abitudini del paziente, pur tenendo conto di eventuali intolleranze e restrizioni specifiche legate a patologie concomitanti.
Saranno da evitare regimi dietetici troppo restrittivi, mentre
andranno favoriti l’introduzione di fibre grezze e di un corretto apporto di liquidi per facilitare la motilità intestinale e
prevenire la stipsi.
La resezione del retto può comportare inoltre complicazioni minzionali, in particolare ritenzione e incontinenza urinaria. Nel primo caso le cause vanno ricercate nel trauma della
vescica e dell’uretra con conseguente deficit neurologico
parziale, nella lesione del pavimento pelvico o nell’interruzione intraoperatoria delle fibre autonome con denervazione
totale della vescica, perdita della sensibilità e della motilità
del detrusore, impossibilità alla minzione se non con l’ausilio
del torchio addominale e con la pressione manuale in ipogastrio. L’incontinenza (da stress o da urgenza) può essere
dovuta alla lesione delle fibre simpatiche e parasimpatiche e
alla dislocazione della vescica. Sia in un caso sia nell’altro
andranno diagnosticate precocemente mediante esame urodinamico per monitorarne l’evoluzione e per valutare l’efficacia delle terapie. In caso di ritenzione il paziente andrà istruito
a mingere a intervalli regolari, a controllare giornalmente il
bilancio idrico e periodicamente il residuo postminzionale e
andrà instaurata una terapia farmacologica per aumentare la
capacità contrattile del detrusore. Il trattamento dell’incontinenza sarà invece basato sull’impiego di miolitici vescicali e
sulla rieducazione dei muscoli del pavimento pelvico per
migliorare il controllo volontario della continenza.
Neoplasie del sistema nervoso
Il sistema nervoso può essere sede di tumori primitivi o metastatici. Anche se la prognosi di questi tumori è in genere
infausta, molti pazienti possono avere sopravvivenze relativamente lunghe. Durante questo tempo la riabilitazione gioca un
ruolo importante nel ridurre i deficit neurologici e le disabilità
derivanti, migliorando la qualità di vita. I danni dovuti alla
presenza di una lesione encefalica o midollare potranno essere
di tipo motorio, sensitivo o misto: l’entità, la tipologia e la
prognosi di questi deficit dipenderanno sostanzialmente dalla
localizzazione e dal tipo del tumore primitivo. Il danno motorio potrà presentarsi come emiparesi, paraparesi o tetraparesi,
a seconda che sia coinvolto un emisoma, gli arti inferiori o i
quattro arti. I disturbi potranno andare da una lieve paresi di
uno o più gruppi muscolari a una franca e grave plegia. Accanto ai disturbi motori potranno essere presenti alterazioni delle
Capitolo 69.fm Page 1905 Thursday, April 26, 2007 9:33 AM
1905
Neoplasie in fase avanzata
funzioni cognitive, del linguaggio e della parola (afasia, disartria), della memoria, della personalità, deficit sensitivi e di
coordinazione, turbe del controllo sfinterico. Nel caso di compressione midollare le problematiche neurologiche saranno
diverse a seconda del livello di lesione: dolore locale, radicolare o riferito a distanza, deficit motori (paraparesi flaccida o
spastica, tetraparesi nelle lesioni da C1 a C6), sensitivi, sfinterici (precoci nel coinvolgimento della cauda) (Tab. 69.4).
Nelle lesioni centrali il trattamento riabilitativo dovrebbe
essere preceduto da un esame fisiatrico e neurologico completo, anche attraverso test specifici di valutazione del linguaggio, della scrittura, dell’attenzione, della memoria, i cui
risultati serviranno per formulare il piano di trattamento
individuale e per valutarne i progressi.
Le strategie riabilitative non saranno dissimili da quelle
utilizzate per il trattamento di altre sindromi neurologiche:
esercizi passivi, attivi assistiti, facilitazioni neuromuscolari,
esercizi propriocettivi, esercizi di riadattamento alla stazione
eretta e al cammino, tecniche logopediche, terapie fisiche e
manuali. Nei casi di recupero parziale della motilità o di gravi
disabilità potranno essere impiegati ausili ortesici e protesici
(canadesi, deambulatori, carrozzine, ausili ergonomici) e attrezzature speciali all’interno degli ambienti domestici.
Nelle compressioni midollari il trattamento riabilitativo
sarà soprattutto indirizzato al controllo del dolore, al recupero
della motilità, dell’autonomia, della stazione eretta e della
deambulazione. Il piano di trattamento andrà definito sulla
base delle condizioni generali del paziente, sull’entità del
deficit neurologico e del coinvolgimento metastatico e dovrà
comprendere esercizi attivi e passivi, passaggi posturali, deambulazione assistita, uso di ortesi. Nei casi di grave danno
neurologico il trattamento riabilitativo avrà il solo scopo di
mantenere il trofismo muscolare, evitare posture scorrette e
prevenire lesioni da decubito.
Nelle lesioni a carico del sistema nervoso periferico (plessopatie e neuropatie) da compressione/infiltrazione di masse
tumorali, da esiti di chemio e radioterapia, si potranno ottenere risultati significativi quando il trattamento motorio, propriocettivo e farmacologico sia associato a quello della malattia di base.
Tab. 69.4. Presidi ortesici.
Lesione ossea C1-C2 Collare Philadelphia
Immobilizzatore cervicale Minerva
Lesione C3-C6
Collare in plastica
Collare in gommapiuma
Lesione C7-T1
Collare Philadelphia
Immobilizzatore cervico-dorsale
Immobilizzatore Minerva
Lesione T1-T3
Immobilizzatore cervico-sternale
Supporto sternotoracico per collare Philadelphia
Corsetto semirigido dorsolombare con/senza
Lesione T5-T12
spallacci
Corsetto semirigido dinamico
Corsetto elastico toracolombare
Busto rigido Taylor
Busto rigido per iperestensione a 3 punti
Corsetto semirigido lombare e lombosacrale
Lesione L1-S1
Corsetto semirigido dinamico
Corsetto elastico lombare
Busto rigido Knight
Neoplasie in fase avanzata
Anche nei pazienti con cancro avanzato la riabilitazione ha
un ruolo importante nel ripristinare l’autonomia, nel recuperare le funzioni danneggiate dalla malattia e dalle terapie, nel
preservare una qualità di vita accettabile e garantire una
morte dignitosa. In questa fase della malattia il programma
terapeutico riabilitativo dovrà essere individualizzato e definito sulla base dello stadio della malattia, sull’aspettativa di
vita, sulla presenza di complicazioni neurologiche od ortopediche, sulle condizioni generali del paziente, sui sintomi
presentati, sulle patologie concomitanti. La valutazione del
paziente e del suo stato di malattia consentirà di individuare
il livello funzionale, i bisogni e i sintomi più problematici.
L’allettamento è sicuramente il problema più importante da
affrontare in questi pazienti. La prolungata immobilità cui
spesso sono costretti a causa del dolore, di lesioni neurologiche, di fratture patologiche, può portare ad alterazioni funzionali anche gravi a carico dell’apparato cardiocircolatorio
(ipotensione, edemi da non uso, trombosi venose profonde),
respiratorio (atelettasie, ridotta clearance bronchiale, stasi di
secrezioni, fenomeni broncopneumonici), muscolo-scheletrico (ipercalcemia, rigidità articolari, retrazioni muscolotendinee, posture scorrette, sindromi dolorose, ipotrofia muscolare). Per prevenire e ridurre l’entità di queste complicazioni
occorre impostare precocemente un programma riabilitativo
mirato a mantenere e facilitare le funzioni respiratorie e
cardiocircolatorie, a recuperare il tono e il trofismo muscolare, a ripristinare la funzionalità articolare, a prevenire lesioni da decubito. Del programma dovranno far parte esercizi
attivi assistiti e contro resistenza, esercizi passivi, rieducazione al cammino, passaggi posturali, esercizi respiratori, istruzione all’uso di presidi ortesici. Durata, numero e cadenza
delle sedute andranno valutate di volta in volta e comunque
non dovranno superare la tolleranza del paziente per evitare
dolore o affaticamento. Particolare attenzione andrà posta
alla posizione del paziente: dovrà essere confortevole, anche
con l’aiuto di sostegni esterni, dovrà consentire la mobilizzazione e favorire l’espansibilità toracica, facilitare il ritorno
linfatico e venoso. Nei soggetti defedati, con disturbi cognitivi o con lesioni ossee a rischio di frattura andrà preferita una
chinesiterapia passiva per mantenere la funzionalità articolare, per prevenire contratture e posture scorrette. Gli esercizi
attivi andranno impiegati nei soggetti giovani o in quelli in
condizioni generali non particolarmente compromesse e potranno essere effettuati anche contro resistenza o con l’ausilio
di macchine, quali ad esempio una cyclette statica a bassa
resistenza. Indispensabile per il ripristino della deambulazione e per il recupero dell’autonomia sarà la rieducazione al
cammino. A seconda delle necessità potranno essere impiegati bastoni, canadesi o deambulatori. Per il trattamento delle
contratture muscolari, dei dolori di intensità non elevata,
degli edemi declivi potranno trovare indicazione il massaggio di sfioramento, tecniche di rilassamento, il linfodrenaggio manuale, terapie strumentali (ultrasuoni, laser, elettroterapia, TENS).
Le complicazioni respiratorie potranno essere prevenute e
trattate attraverso esercizi di mobilizzazione globale, tecniche di respirazione toracica, addominale, umidificazione,
tosse assistita. Nei casi in cui questa risulti ipovalida, si potrà
ricorrere a manovre di clapping, di vibrazione, a tecniche di
espirazione forzata, se tollerate e se non inducono dolore o
dispnea. Saranno invece da evitare il drenaggio posturale e la
Capitolo 69.fm Page 1906 Thursday, April 26, 2007 9:33 AM
1906
broncoaspirazione in quanto causa di disagio per il paziente
e di possibili episodi di ipossia. Viceversa, potranno essere
utili l’aerosolterapia con farmaci mucolitici e gli umidificatori d’ambiente. Del programma riabilitativo dovranno infine
far parte l’istruzione del paziente e dei familiari all’uso dei
presidi ortesici per gli spostamenti, dentro e fuori casa, e dei
sistemi antidecubito (materassi, cuscini) e l’impiego di accorgimenti o attrezzature speciali (maniglioni, docce manuali,
sedili) per facilitare i movimenti all’interno della casa.
Un altro problema di frequente riscontro nei pazienti terminali è costituito dalle ulcere da decubito. La loro prevenzione è possibile ricorrendo ad alcune semplici pratiche infermieristico-riabilitative: mobilizzazione sistematica del paziente con cambi di postura ogni 2-3 ore, controllo periodico
delle condizioni della biancheria del letto, dello stato della
cute, utilizzando in casi di necessità creme emollienti o idratanti, pulizia della regione genitale e perineale nei soggetti
incontinenti, controllo della reclinazione del letto e della
posizione del tronco, utilizzo di cuscini sotto la schiena, le
ginocchia e i piedi per evitare scivolamenti, frizione della
cute, impiego di materassi antidecubito (in schiuma di lattice,
in gel, ad aria, ad acqua, fluidizzati), correzione degli squilibri
elettrolitici, metabolici e nutrizionali, istruzione dei familiari
sull’uso dei presidi, sulla gestione dei cateteri e dei drenaggi
e sulle tecniche di medicazione. Il trattamento delle ulcere da
decubito è soprattutto topico e basato sull’impiego di sostanze enzimatiche (collagenasi, fibrinolisina), battericide (iodopovidone, ipoclorito di sodio), batteriostatiche, cicatrizzanti
(idrocolloidi). Anche le terapie fisiche (magnetoterapia, laserterapia) si sono dimostrate utili nell’accelerare i processi
riparativi e favorire la produzione del tessuto di granulazione.
Nei pazienti con metastasi ossee le problematiche che
richiedono un intervento riabilitativo sono quelle legate al
rischio di fratture patologiche e/o di compressioni midollari,
al dolore, alla perdita della capacità a deambulare in modo
autonomo, all’immobilità (ipotrofia muscolare, limitazioni
articolari, contratture muscolari, retrazioni tendinee, posture
scorrette). Nella scelta del tipo di programma si dovrà tener
conto delle variabili connesse alla morfologia delle lesioni
(litiche, addensanti, miste), alla sede (rachide, ossa lunghe,
bacino), alla diffusione (unicità, molteplicità delle localizzazioni), alla sintomatologia algica (intensità, sede, irradiazione), alla evolutività della malattia, alle condizioni generali del
paziente, all’aspettativa di vita. Il programma si basa sull’impiego di presidi ortesici, terapie motorie e neuromotorie,
terapie fisiche strumentali, farmacologiche.
Qualunque sia il tipo prescelto (Tab. 69.4), il presidio
ortesico deve garantire la stabilità della struttura ossea interessata, limitare la mobilità del segmento coinvolto, controllare il dolore, ma al contempo deve essere leggero, modellabile per adattarsi alle variazioni di peso e forma del paziente,
di facile impiego e facilmente estraibile. Il suo utilizzo è
indicato durante tutto il periodo delle terapie complementari,
chemio e radioterapia, e comunque fino al consolidamento
dell’osso. Una volta raggiunto un sufficiente grado di riparazione, il presidio semirigido o rigido può essere sostituito da
un tipo più leggero e se ne può limitare l’uso solo in determinate situazioni (durante l’attività lavorativa, negli spostamenti in auto, in caso di stazione eretta prolungata).
Nelle lesioni al rachide cervicale, a seconda della localizzazione, possono essere utilizzati collari in polietilene, immobilizzatori cervicali (controindicati in caso di lesioni allo
sterno o alla mandibola) o cervicosternali, collari in plastica
con o senza appoggio mentoniero, collari in gommapiuma
69. PRINCIPI DI RIABILITAZIONE DEL PAZIENTE ONCOLOGICO
sagomati (indicati nei pazienti con modesta sintomatologia
dolorosa o quando non sia consentito l’utilizzo di altri tipi di
presidio).
La stabilizzazione della colonna dorsolombare può essere
ottenuta con corsetti semirigidi o busti rigidi. I primi comprendono i tipi lombari, lombosacrali, dorsolombari, con o
senza spallacci, in stoffa o in tessuto elastico più leggeri e più
facili da indossare. Tra i busti rigidi, quelli di più frequente
impiego sono il dorsolombare alto con spallacci (Taylor) e
senza (Knight) e quello per iperestensione a 3 punti (C35).
Nei casi in cui vi siano lesioni costali o quando non sia
tollerata la compressione addominale è da preferire il C35.
In caso di coinvolgimento del bacino e/o dei femori, con
dolore al carico o rischio di frattura, vanno impiegati 1 o 2
bastoni canadesi con appoggio antibrachiale. Nei pazienti
debilitati o in quelli con difficoltà di coordinazione si deve
ricorrere all’uso di un deambulatore con o senza ascellari o a
una carrozzina ortopedica nei casi di fratture inoperabili, nei
deficit neurologici gravi e nel coinvolgimento massivo degli
arti superiori e inferiori.
Oltre ai presidi ortesici, la terapia motoria è parte integrante del trattamento riabilitativo. In presenza di lesioni a rischio
di frattura, complicazioni neurologiche e di sindromi algiche
che condizionano prolungati allettamenti è buona norma
impostare un programma motorio basato sul controllo della
postura per evitare rigidità articolari e contratture muscolari,
su esercizi attivi isometrici, con o senza resistenza (per il
recupero della stenia e dei deficit motori e per la prevenzioni
di complicazioni tromboemboliche), su esercizi passivi che
coinvolgano anche il segmento interessato, sulla massoterapia per migliorare la circolazione locale e per mantenere il
trofismo cutaneo e muscolare, sui passaggi posturali, sulla
rieducazione al cammino. Nella fase di attesa della risposta
delle terapie causali, l’impiego di terapie strumentali (ultrasuoni, laser, magnetoterapia, elettrostimolazioni transcutanee) si è dimostrato utile per il controllo di dolori derivanti
da contratture muscolari o malposizioni o per il trattamento
dei disturbi neurologici da chemioterapia e degli esiti cutanei
della radioterapia (radiodermiti acute, fibrosi cutanee e sottocutanee).
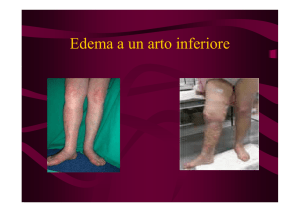
Molti tumori in fase avanzata si complicano con un linfedema evolutivo maligno. È per lo più dovuto alla compressione linfatica e/o venosa a opera di adenopatie metastatiche o
di masse neoplastiche, all’infiltrazione dei vasi linfatici cutanei e sottocutanei, a trombosi neoplastiche, a tromboflebiti
migranti. L’edema evolutivo compare per lo più acutamente,
progredisce rapidamente e molto spesso è accompagnato o
preceduto da dolore neuropatico e sintomi neurologici (ipostenia prossimo-distale a carico dei cingoli scapolare e pelvico, parestesie, iperestesia, allodinia). Si presenta con cute
tesa, traslucida, di colorito eritematoso o subcianotico, di
consistenza molle con fovea marcata. Sono in genere presenti
teleangectasie e circoli collaterali alla radice dell’arto, alla
parete toracica o addominale. I quadri clinico e sintomatologico sono, nella maggior parte dei casi, sufficienti a porre
diagnosi di linfedema evolutivo. Nei casi dubbi la TC o la RM
forniscono importanti informazioni circa la sede e l’entità del
coinvolgimento metastatico.
Il trattamento del linfedema maligno non è dissimile da
quello del linfedema postchirurgico, anche se in questi casi
sarà soprattutto diretto al controllo dei sintomi di accompagnamento, a prevenire ulteriori incrementi dimensionali, a
mantenere e recuperare la funzionalità dell’arto. Le terapie
potranno essere manuali, contenitive, compressive, motorie,
Capitolo 69.fm Page 1907 Thursday, April 26, 2007 9:33 AM
1907
Neoplasie in fase avanzata
farmacologiche, ortesiche. Dovranno tenere conto delle condizioni generali del paziente e locali dell’arto e andranno di
volta in volta adattate e modificate nelle loro modalità di
applicazione.
In questo tipo di pazienti particolare attenzione andrà
posta all’igiene della cute per evitare lesioni, escoriazioni,
sovrainfezioni batteriche o fungine, specie nei casi di linforrea abbondante. Il linfodrenaggio manuale o il massaggio
leggero possono essere utilizzati per ridurre le dimensioni
dell’edema, le sensazioni di tensione dolorosa, anche se per
alcuni autori la presenza di una ripresa di malattia ne controindica in modo assoluto l’effettuazione. Solo in caso di
massivo coinvolgimento cutaneo o di lesioni ulcerative e
sanguinanti il linfodrenaggio non dovrà essere effettuato.
L’impiego del bendaggio e/o del tutore elastico si è dimostrato particolarmente utile per ridurre il disagio del paziente a
causa dell’eccessivo peso e della tensione dell’arto, per evitare ulteriori incrementi dimensionali e per controllare la
linforrea. Sono da preferire supporti elastici di bassa classe
di compressione (I o II) e bendaggi monostrato o leggeri. In
caso di intolleranza potranno essere utilizzate bende tubolari
elastiche, facili da indossare, morbide e poco traumatizzanti
per la cute, anche in doppio strato. Esercizi attivi e passivi
trovano specifica indicazione per prevenire rigidità articolari, posture scorrette, la comparsa di ulcere da decubito nei
pazienti allettati e per favorire il ritorno linfatico e venoso.
Nei casi di edema di grosse dimensioni potranno essere
impiegati presidi ortesici: reggibraccia per l’arto superiore
quando è associata una plessopatia brachiale, canadesi per la
deambulazione per l’arto inferiore, carrozzine per gli spostamenti fuori casa. La terapia meccanica (pressoterapia), utilizzata a bassi regimi pressori e per tempi di seduta non
superiori ai 30 minuti, andrà effettuata solo in casi selezionati
e con particolare cautela specie se è presente una documentata ostruzione al circolo linfatico e/o venoso (impegno adenopatico delle stazioni sovraclaveari, ascellari, inguinali,
pelviche, ecc.).
Per il controllo del dolore potranno essere somministrati
diuretici, eparine a basso peso molecolare, antinfiammatori,
cortisonici, antidepressivi triciclici, antiepilettici e analgesici
oppiodi. Dosi, tempi e durata della terapia andranno definiti
sulla base del quadro sintomatologico.
BIBLIOGRAFIA
AA.VV. Cancer Rehabilitation in the New Millennium: Opportunities and Challenges. Cancer Suppl. 92(4), 969-1052, 2001.
BALZARINI A., Riabilitazione. In: AMADORI D., DE CONNO F. (Eds.)
Libro Italiano di Cure Palliative. Poletto Editore, Milano, 290298, 2003.
BALZARINI A., BORDET V., I presidi ortesici. In: MERCADANTE S.,
RIPAMONTI C. (Eds.), Valutazione, diagnosi e trattamento del dolore da cancro. Masson, Milano, 313-320, 2000.
BUONOCORE M., BONEZZI C., Principi di riabilitazione del paziente
neoplastico. In: BONADONNA G., ROBUSTELLI DELLA CUNA G.
(Eds.), Medicina Oncologica. Masson, Milano, 1627-1633, 1999.
CARACENI A., Le compressioni midollari metastatiche. In: MERCADANTE S., RIPAMONTI C. (Eds.), Valutazione, diagnosi e trattamento del dolore da cancro. Masson, Milano, 156-168, 2000.
CHEVILLE A., Cancer Rehabilitation. Semin. Oncol. 32, 219-224,
2005.
DELISA J., GANS B., CURRIE D. (Eds.), Rehabilitation Medicine:
Principles and Practice, 2nd Ed. Lippincott Company, Philadelphia, 1993.
DEVITA V.T. JR., HELLMAN S., ROSENBERG S.A., (Eds.), Cancer:
Principles & Practice of Oncology, 5th. Lippincott-RavenPublishers, Philadelphia, 1997.
GANZ P.A., Current Issues in Cancer Rehabilitation. Cancer 65,
742-751, 1990.
MELLETTE S.J., BLUNK K.L., Cancer Rehabilitation. Semin. Oncol.
21(6), 779-782, 1994.
RONKA R., VON SMITTEN K., TASMUTH T. E COLL., One-year morbidity after sentinel node biopsy and breast surgery. The breast
14, 26-36, 2005.
TWYCROSS R., JENNS K., TODD J. (Eds.), Lymphoedema. Radcliffe
Medical Press, Abingdon Oxon, 2000.
PARTE I.fm Page 2 Thursday, April 12, 2007 4:29 PM