I LEGAMI CHIMICI
Attività 1
Prerequisiti:
conoscenza
della tavola periodica e delle sue caratteristiche (elettronegatività, numero atomico, valenza,
numero di ossidazione)
regola dell’ottetto
Obiettivi: conoscenza dei legami chimici forti (ionico, covalente e metallico)
Classe IV scuola primaria.
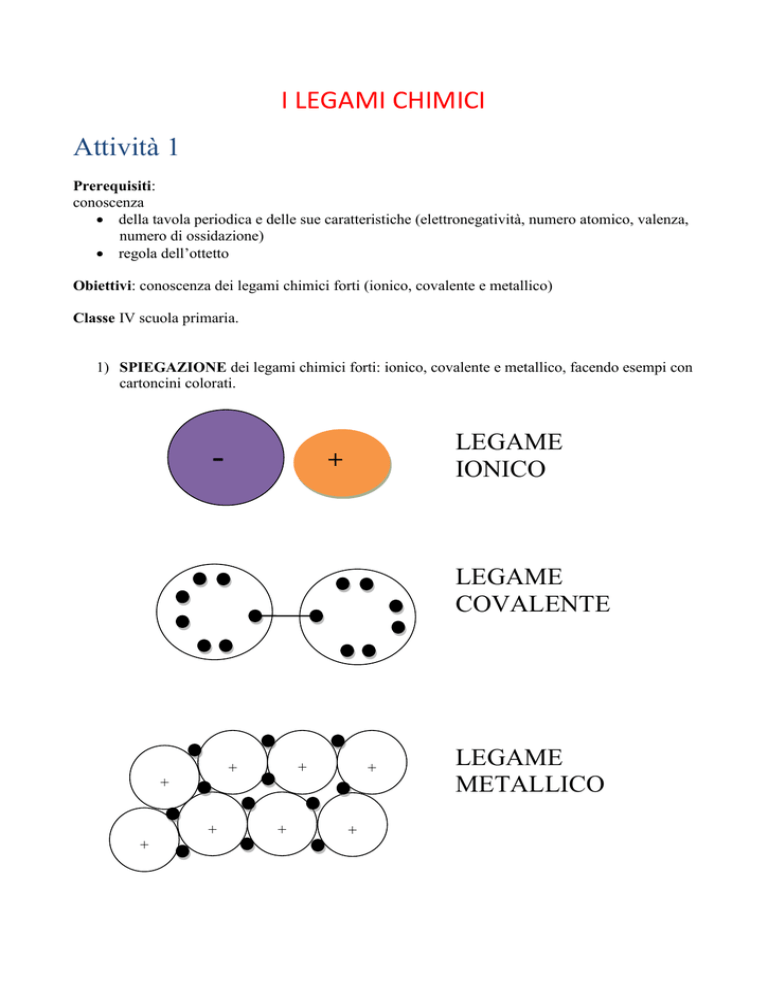
1) SPIEGAZIONE dei legami chimici forti: ionico, covalente e metallico, facendo esempi con
cartoncini colorati.
-
LEGAME
IONICO
+
LEGAME
COVALENTE
+
+
+
+
+
+
+
+
+
LEGAME
METALLICO
2) ATTIVITÀ.
Si prepara un bussolotto contenente delle tessere sulle quali sono indicati: il nome
dell’elemento, il simbolo dell’elemento, la sua elettronegatività e il numero di
ossidazione. Gli elementi vengono assegnati a ogni bambino pescando la tessera nel
bussolotto. I bambini devono raggrupparsi in base all’elettronegatività dell’elemento
assegnato e in base alle richieste dell’insegnante, dovranno formare così i legami della
tipologia richiesta.
Esempi di tessere:
H
Na
Cl
2,20
0,93
3,16
±1
+1
±1 +3 +5 +7
idrogeno
sodio
cloro
3) VERIFICA
La verifica consiste in due domande aperte:
Che tipo di legame si realizza quando due atomi di fluoro, ognuno con 7 elettroni di
valenza, mettono in comune un elettrone ciascuno?
(Legame COVALENTE)
Che tipo di legame si forma quando la differenza di elettronegatività tra i due
elementi del legame è maggiore di 1,7?
(Legame IONICO)
E nella compilazione della seguente scheda:
+
-
Na
Cl
Legame ____________
Legame ____________
+
+
+
+
Legame ____________
+
+
+
+
Attività 2
Prerequisiti:
conoscenza
della tavola periodica e delle sue caratteristiche (elettronegatività, numero atomico, valenza,
numero di ossidazione)
legami forti
regola dell’ottetto
Obiettivi: conoscenza del legame ponte di idrogeno
Classe IV scuola primaria.
1) SPIEGAZIONE del legame ponte di idrogeno attraverso l’utilizzo di Geomag ( gioco di
costruzioni magnetiche).
2) ATTIVITÀ. Si forniscono a ogni bambino 6 biglie metalliche di due colori diversi: due
rosse che rappresentano l’Ossigeno e quattro blu che rappresentano l’Idrogeno e quattro
barrette magnetiche verdi, che rappresentano i legami covalenti tra gli atomi di idrogeno e
gli atomi di ossigeno. Andando a unire alle barrette verdi le biglie blu e una rossa si formerà
così l’ipotetica molecola d’acqua. A questo punto con due “molecole” si può verificare la
forza attrattiva tra due biglie (una rossa e una blu).
Atomo di H
Atomo di 0
Con la linea
tratteggiata si indica
il LEGAME A
IDROGENO
che i bambini
possono
sperimentare tramite
la forza attrattiva tra
le due biglie: rossa
(O) e blu (H).
3) VERIFICA.
La verifica consiste in domande a risposta chiusa (V/F)
Il legame a idrogeno
consiste nell’attrazione tra due dipoli negativi V/F
è un legame debole V/F
esiste tra l’atomo di O di una molecola e l’atomo di H di un’altra V/F
è un legame forte V/F
Attività proposte da:
Cecilia Gaeta
Francesca Fallani
Ilaria Mammola
Mirko Picchi