Uso appropriato delle tecnologie
genomiche sul territorio
Dott. Antonio
Oliveriommg
– MMG
D.ssa
Paola Iaricci
Roma
aprile
2014
Roma
12 12
aprile
2014
• CON LA CRESCENTE DIFFUSIONE DI
INFORMAZIONI SANITARIE,SI SVILUPPA UNA
FORMA SOGGETIVA DELLA SALUTE E SI
ACCENTUA LA DISUGUAGLIANZA IN TERMINI
NON SOLO DI ACCESSO QUANTO
SOPRATTUTTO DI ESITO
la possibilità di prevedere la comparsa di una
malattia in una persona asintomatica è
un’acquisizione recente e coincide con la
diagnostica genetico-molecolare.
I precedenti sistemi di screening, dalle
schermografie toraciche ai test per
lafenilchetonuria ai PAP-test,
erano tutte analisi presintomatiche
in senso lato, in quanto precedevano la comparsa
dei sintomi clinici, ma erano solo rivelatori precoci
di un’alterazione già in atto.
• I test genetici costituiscono il prodotto più
importante della ricerca genetica applicata
alla medicina e hanno potenziali ricadute
• sulla diagnosi
• e sulla prevenzione
• in questo contesto la figura del medico di
mmg ha una funzione di tramite informativo
tra l’utente e chi gestisce il test
la possibilità di prevedere la comparsa di una
malattia in una persona asintomatica è
un’acquisizione recente e coincide con la
diagnostica genetico-molecolare.
I precedenti sistemi di screening, dalle
schermografie toraciche ai test per
lafenilchetonuria ai PAP-test,
erano tutte analisi presintomatiche
in senso lato, in quanto precedevano la comparsa
dei sintomi clinici, ma erano solo rivelatori precoci
di un’alterazione già in atto.
• Per il tumore alla mammella la prevenzione
si basa sull'identificazione del tumore già
presente, e quindi la sua efficacia è
condizionata dai tempi della diagnosi e dalla
sua tempestività.
RUOLO DEL M.M.G.
Educazionale
Intervento sui
fattori di rischio
modificabili
Contraccettivi orali
Terapia estrogenica
sostitutiva
Dieta
Obesità
Fumo
Esposizione alle
radiazioni
RUOLO DEL M.M.G.
Educazionale
Stimolo alla
accettazione di
metodiche di
prevenzione
secondaria
Autoesame del seno
Consulto senologico
Indagini diagnostiche
Percorsi di screening
TEAM TERAPEUTICO
M.M.G.
RADIOLOGO
RADIOLOGO INTERVENTISTA
GENETISTA
MEDICO NUCLEARE
CHIRURGO
PATOLOGO
BIOLOGO MOLECOLARE
ONCOLOGO
RADIOTERAPISTA
CHIRURGO PLASTICO
PSICOLOGO
FISIATRA
Al centro dell'attenzione
• l'innovazione nelle cure e nella ricerca, a
partire dalle ultime scoperte nel campo della
genetica a quelle della prevenzione primaria,
fino alle ultime metodiche radiologiche per
l'anticipazione diagnostica.
• Per arrivare, infine, a definire i traguardi
raggiunti in chirurgia, anatomia patologica,
biologia molecolare e radioterapia.
• TEST GENETICI E MEDICINA
ANTICIPATORIA
Test genetici
• L’UTILITA’ DEI TEST PREDITTIVI E’ IN QUESTO
MOMENTO LIMITATA,FATTA ECCEZIONE PER QUELLI
CHE RIGUARDANO ALCUNE PATOLOGIE NELLE QUALI
ESISTE L’EFFETTO DI UN GENE PRINCIPALE, CHE LE
RENDE ASSIMILABILI ALLE MALATTIA
MENDELIANE,COME IL TUMORE DELLA MAMMELLA
DA MUTAZIONE DEL GENE BCRA1 BRCA2
• (Negli ultimi anni, sono stati identificati almeno 5 geni
responsabili della trasmissione ereditaria del carcinoma
mammario: BRCA1, BRCA2, P53, PTEN, ATM)
BRCA1 BRCA2
10%
14%
Tunori mammella
Tumori ovarici
LA DIMENSIONE PSICOLOGICA E SOCIO-CULTURALE
DELLA MALATTIA CANCRO,
L’OFFERTA O LA POTENZIALE OFFERTA DI TEST
GENETICI (SPECIE IN AMBITO PREVENTIVO),
SUSCITA UNA VASTA ECO NELL’OPINIONEPUBBLICA.
CIO’ PONE PARTICOLARI PROBLEMI, SIA DI
VALIDAZIONE, SIA DI UTILIZZO DEI TEST GENETICI.
DOMANDA
• Considerando l'aspetto bioetico, i risvolti
psicologici del test genetico, considerando una
storia familiare variabile in quanto dinamica,
la valutazione formale del rischio eredofamigliare quando è appropriata?
L’utilizzo dei test genetici BRCA1/2 e le forme
eredo-familiari di carcinoma mammario e/o
ovarico
Dott. LILIANA
Antonio Oliverio
– MMG
D.ssa
VARESCO
aprile
2014
IRCCSRoma
AOU 12
SAN
MARTINO
Roma 12 aprile 2014
Raccomandazioni USPSTF 2013
raccomandato l’invio alla Consulenza Genetica Oncologica
sulla base di una
“moderata certezza”
“moderato”
che
vi
sia
un
beneficio
netto
(nuove informazioni potrebbero cambiare la grandezza o la
direzione degli effetti dell’azione e queste modificazioni
potrebbero portare ad una conclusione diversa da quella
attuale)
CONSULENZA GENETICA
Atto medico che
• fornisce all’utente INFORMAZIONI sulla malattia genetica
(diagnosi genetica incluso test genetico , rischio di trasmissione
ereditaria, interventi medici disponibili)
•
con lo scopo di AIUTARE la persona ad acquisire ‘AUTONOMIA’
decisionale rispetto alle opzioni disponibili
(fare o meno il test genetico, diagnosi prenatale/test predittivo,
prevenzione secondaria)
all’interno di processo di comunicazione
“a più tappe”
si crea uno spazio di Dialogo / Relazione in cui è
possibile esprimere le proprie idee / emozioni
Approccio alla problematica:
la PERSONA (non la malattia) è
al centro della consulenza genetica
(counselling)
Condividere le incertezze scientifiche
Dare le informazioni necessarie per poter
Evidenze
scientifiche
Più di ‘basso livello’
opzioni
disponibili
effettuare una scelta personale consapevole
Dare ascolto (e aiuto) alle motivazioni/interessi/
situazioni personali e familiari che entrano in
gioco nella scelta di se/come affrontare
il discorso del rischio ereditario
Monitorare il risultato delle azioni mediche
P.I.
QUALI I CRITERI ?
• L.V.
SOGGETTO CON STORIA PERSONALE DI TUMORE:
Maschio con carcinoma mammario
Donna con carcinoma mammario e carcinoma ovarico
Donna con carcinoma mammario:
< 36 anni,
< 50 anni con carcinoma bilaterale,
< 50 anni e storia famigliare di > 1 parente di primo grado* con:
- carcinoma mammario < 50 anni
- carcinoma ovarico a qualsiasi età
- carcinoma mammario bilaterale
- carcinoma mammario maschile
> 50 anni solo se storia famigliare di carcinoma mammario o ovarico in > 2 parenti
in primo grado tra di loro* (di cui uno in primo grado con lei)
< 60 anni con carcinoma mammario “triplo-negativo” [2013]
-ad ogni età con storia famigliare di carcinoma esocrino del pancreas in > 2 parenti in primo grado
tra di loro* (di cui uno in primo grado con lei) [2013]
Donna con carcinoma ovarico/tuba/primitivo del peritoneo a qualsiasi età [2013]
Soggetto con carcinoma esocrino del pancreas e storia famigliare di carcinoma della mammella o
dell’ ovaio o esocrino del pancreas in > 2 parenti in primo grado tra di loro* (di cui uno in primo grado
con lei/lui) [2013]
SOGGETTO CON SOLA STORIA FAMIGLIARE DI TUMORE:
che rientri in uno dei punti sopra elencati a partire da un parente di primo grado *
con precedente identificazione in famiglia di una mutazione ereditaria in un gene predisponente (BRCA1,
BRCA2, P53, PTEN, ecc.)
Situazioni di storia famigliare oncologica in cui siano presenti casi di carcinoma mammario e pattern
complicati di tumori multipli insorti in giovane età (tra cui in particolare: sarcomi, carcinoma gastrico
diffuso, carcinoma prostatico aggressivo, tumori primitivi multipli, tumori rari)
*genitore, fratello, figlio e, per il lato paterno della famiglia, considerare anche familiari di
secondo grado
P.I.
domanda :
Chi va inviato in consulenza genetica?
Qual è la modalità con cui si trasmette nelle famiglie
una mutazione BRCA?
• L.V.
POTENZIALE UTILITA’
DEL TEST GENETICO BRCA
Gene mutato
PREVENZIONE ad hoc
dalla giovane età?
TERAPIE MIRATE?
Prevenzione per
“ rischio eta’ “
Identificazione donne BRCA +
Valutazione storia famigliare
Criteri
Cascade testing
Identificazione delle
donne a rischio della famiglia
Test completo
BRCA1 e BRCA2
Test mutazione specifico
Su soggetto
con tumore
con % più alta
Donna BRCA+
(20%)
Donna BRCA+
Donna BRCA-
No informazioni
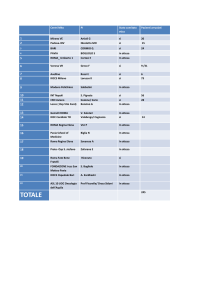
No informazioni
1900
(66)
(80)
1946
1903
(77)
(80)
Mamm 50
(52)
Ovaio 55 (58)
1941
Mamm 42
1967
1975
1939
=
Mamm sn 38
Mamm ds 40
(40)
1965
Trasmissione anche attraverso il ramo paterno
Famigliari di I grado: 50% probabilità di condividere la mutazione
18-25
25-30
40-45
• P.I.
Quali sono i limiti del test genetico BRCA oggi ?
Prelievo di sangue
Estrazione DNA
Piastre con primer con M13
Mix PCR + DNA
Amplificazione
Purificazione prodotti
PCR Biomek 2000
Mix Big Dye
M13 UP / M13RP
Purificazione sequenze
Biomek 2000
Analisi sequenze:
•2 operatori
•SeqScape
•MutationSurveyor
ABI3130
Referto
I geni sono unità complesse
Esone 1
Esone 2
RNA messaggero
Esone 3
Proteina
BRCA1
BRCA2
Mutazioni troncanti
Mutazioni missense
Delezioni/Riarrangiamenti
Varianti di incerto significato biologico !!!!
I test genetici attuali esaminano
solo una parte del gene
Esone 1
Esone 2
Esone 3
Zone
esaminate
Zone non
esaminate
Secondo alcune stime nei geni BRCA
«non possiamo vedere»
circa 10 mutazioni su 100
Eterogeneità genetica
• P.I.
Quali sono i rischi di cancro associati alle
mutazioni
BRCA1 e BRCA2?
Solo mammella e ovaio?
• L.V.
Rischio di cancro BRCA-associato
Famiglie con tanti
casi di tumore
Età giovane
Rischio di Ca Mamm 40-80%
iceberg
?
Popolazione
generale
Stima del rischio di cancro
NON è (ancora) “personalizzata”
Rischio di cancro
Meta-analysis of BRCA1 and BRCA2 penetrance. Chen S,
Parmigiani G. J Clin Oncol. 2007. 25:1329-33
Rischio di cancro cumulativo a 70 anni:
BRCA1
BRCA2
Carcinoma mammario 57% (95% CI, 47%-66%)
Carcinoma ovarico* 40% (95% CI, 35%-46%)
Carcinoma mammario 49% (95% IC, 40-57%)
Carcinoma ovarico* 18% (95% CI, 13%-23%)
* Carcinoma ovarico e tubarico
Rischio di Carcinoma mammario controlaterale
in donne con mutazione BRCA1/2
Controlateral breast cancer risk in BRCA1 and BRCA2 Mutation
Carrier. Greaser MK et al, J Clin Oncol, 2009
Rischio cumulativo a 75 anni:
BRCA1: 30.4% (95% CI, 29.3%-36,9%)
BRCA2: 20,1% (95% CI, 12,1%-28,1%)
BRCA1
BRCA2
30 anni, sana BRCA1…. a 40 anni?
PANCREAS
RR 4
BRCA2 PROSTATA
RR 6
BRCA
MELANOMA UVEALE
RR 99
? ESOFAGO
RR 2-4
? STOMACO
RR 2-3
Rischio di cancro in donne BRCA varia
anche all’interno della stessa famiglia (i.e. stessa mutazione)
Studi di segregazione indicano che
gran parte di questa variabilità è genetica
(polimorfismi comuni? varianti poco frequenti?)
• P.I.
Quali sono le opzioni mediche che
vengono oggi discusse con le donne
sane portatrici di mutazione BRCA?
• L.V.
Opzioni -> scelte
delle donne BRCA
Non fare niente
Chirurgia profilattica
Mastectomia e
(Istero)salpingooforectomia
(Istero)salpingooforectomia
Mastectomia
Le tre età della vita, G. Klimt
Sorveglianza
RNM mammaria, Mx, Eco
Ecografia TV + Ca125
Farmacoprevenzione
18-25
25-30
40-45
Chirurgia profilattica
ginecologica
•
↓ rischio di ca mammario
•
↓ rischio di ca ovarico
desiderio di maternità
gestione sintomi della menopausa
prevenzione malattie cardiovascolari/osteoporosi
Chirurgia profilattica mammaria
Donne sane
Mastectomia
bilaterale
Donne affette da ca mammario
Chirurgia
radicale
vs
Chirurgia
conservativa
Mastectomia
controlaterale
Mastectomia profilattica
Bermejo-Perez, Int J.Cancer, 2007
Limiti:
Mancanza dati sulla ↓ mortalità
Tecniche di esecuzione mastectomia diverse
Tempi d follow-up brevi
Svantaggi
Aspetti estetici,funzionali
e psicologici
Complicanze chirurgiche
Non reversibilità
ormonale L’utilizzo della HRT deve essere attentamente valutato su base clinica e
Terapia
ormonale L’utilizzo della HRT deve essere attentamente valutato su base clinica e devono
essere illustrati i potenziali vantaggi e svantaggi della terapia in discussione.
sostitutiva (HRT)
L’uso della HRT nelle donne a rischio deve essere limitato il più possibile, nel
tiTeraHRT
tempo e nel tipo di dosaggio.
sibile, nel tempo e nel tipo di dosaggio.
Terapia
Contraccettivi
orali
ontraccettirali
dDonne con più di 35 anni con storia familiare di carcinoma mammario devono
essere informate dell’aumento di rischio di carcinoma mammario associato con
l’assunzione della pillola contraccettiva. Per le donne portatrici di mutazione
BRCA, devono essere discussi gli effetti opposti della pillola contraccettiva sul
rischio di carcinoma mammario e ovarico (aumento di rischio mammario,
protezione contro tumore ovarico). Tuttavia, generalmente, l’assunzione di
contraccettivi orali non deve essere presa in considerazione solo come opzione
di riduzione del rischio di carcinoma ovarico.
rio associato con l’assunzione della pillola contraccettiva. Per le donne portatrici
di mutazione BRCA, devono essere discussi gli effetti opposti della pillola
contraccettiva sul rischio di carcinoma mammario e ovarico (aumento di rischio
mammario, protezione contro tumore ovarico). Tuttavia, generalmente,
l’assunzione di contraccettivi orali non deve essere presa in considerazione solo
come opzione di riduzione del rischio di carcinoma ovarico.
Commenti: Il fatto che, sia il NICE che l’ASCO (Visvanathan K et al, JCO
31, 2013), a fronte dei risultati di una meta-analisi aggiornata (Cuzick J et al,
The Lancet April 2013) e di una revisione sistematica della letteratura
rispettivamente, abbiano deciso di raccomandare la prevenzione
farmacologica con i modulatori selettivi degli estrogeni ha (ri)aperto un fronte
di discussione che riguarda gli stessi obiettivi della chemioprevenzione
(diminuire l’incidenza o la mortalità?). Non vi sono evidenze di una
riduzione di mortalità mentre la riduzione di incidenza è molto significativa
(anche se confinata ai tumori ER+). Gli effetti negativi della prevenzione
farmacologica con SERMs (aumento del rischio di eventi tromboemolici,
infarto, tumore dell’endometrio) devono essere compresi dalle donne ed è
ancora presto per poter stabilire se vi sia un profilo di effetti
complessivamente favorevole.
modello di analisi decisionale
parametri derivati dalla letteratura
simula storie di vita di una coorte del 1980
di 1.000.000 donne BRCA1 o BRCA2
dall’età di 25 ai 100 anni o alla morte
Interventi considerati:
screening mammella con mammografia + MRI dai 25 anni
CPG (chirurgia profilattica ginecologica) a varie età
CPM (chirurgia profilattica mammaria) a varie età
(No chemioprevenzione, CA125+EcoTV, qualità di vita)
DONNE BRCA1
Probabilità di sopravvivenza a 70 aa:
( US population 84%)
senza interventi
53%
solo CPG a 40 anni
+15%
(68%)
solo CPM a 25 anni
+13%
(66%)
solo CPG a 50 anni
+8%
(61%)
solo screening mammella
+6%
(59%)
CPM a 25 anni e CPG a 40 anni
+26% (79%)
screen mamm dai 25, CPM e CPG a 40 anni
+24% (77%)
screen mamm dai 25 e CPG a 40 anni
+21% (74%)
screen mamm dai 25 e CPG a 50 anni
+16% (69%)
DONNE BRCA2
Probabilità di sopravvivenza a 70 aa:
( US population 84%)
senza interventi
71%
solo CPM a 25 anni
solo CPM a 40 anni
+8%
+7%
(79%)
(78%)
solo CPG a 40 anni
solo CPG a 50 anni
solo screening mammella
+6%
+4%
+4%
(77%)
(75%)
(75%)
CPM a 25 anni e CPG a 40 anni
+12% (83%)
screen mamm dai 25, CPM e CPG a 40 anni
+11% (82%)
screen mamm dai 25 e CPG a 40 anni
+9%
(80%)
screen mamm dai 25 e CPG a 50 anni
+8%
(79%)
P.I.
DOMANDA
• Come possiamo seguire prospetticamente
donne ad alto rischio genetico in un
programma multidisciplinare ?
• L.V.
Programma alto rischio genetico
Radiologi
Chirurghi
Ginecologi
Oncologi
MMG
Accesso spontaneo
CGO
Valutazione
storia familiare
Genetista
No
test
Test BRCA
Non conclusivo
Valutazione life time risk
- Basso rischio
- Medio rischio
- Alto rischio
Test BRCA +
Test BRCA –
predittivo
Psicologo
BRCA+
Follow-UP
CLINIC
Oncologo
Ginecologo
Infermiere
case manager
Chirurgo
senologo
Radiologo
senologo
GENETIC NURSE
• Coordina e programma gli esami previsti mediando tra le
esigenze della persona e quelle delle strutture coinvolte
• Rappresenta il punto di riferimento per i medici coinvolti nei
diversi aspetti del programma di prevenzione
• Facilita gli aspetti organizzativi
• Facilita gli aspetti comunicativi medico-paziente
• Svolge attivita’ di counselling al paziente durante gli esami
diagnostici, nell’attesa dei risultati e in caso di malattia
Infermiere Case Manager
L’infermiere case manager dalla teoria alla prassi
P. Chiari A. Santullo
Mac Graw Hill ed. 2011
P.I.
Quindi….
• UNA VALUTAZIONE FORMALE DEL RISCHIO EREDOFAMIGLIARE E’ APPROPRIATO SOLO SE SONO
DISPONIBILI :
• INTERVENTI DI PREVENZIONE SPECIFICI IN BASE AL
LIVELLO DI RISCHIO E DI DIMOSTRATA UTILITA’ PER
• IL/I TUMORI COMPRESI NELLA STORIA FAMIGLIARE
• ( ES. CA COLON-RETTO,CA MAMMELLA,CA OVAIO, )
• L’esecuzione del test porta in sé alcuni risvolti
• psicologici importanti:
• Ansia per i propri familiari
• Difficolta’ a progettare il proprio futuro
• Necessita’ di scelte terapeutiche
• L.V.
DAL RISCHIO GENETICO AI
MALATI DI RISCHIO
I vissuti delle giovani donne che si
sono sottoposte al test BRCA
PERCEZIONE DI RISCHIO E
PESO DELLA STORIA FAMIGLIARE
Anna, 35 anni
"La mia storia familiare è molto negativa, cioè, indubbiamente mi avrebbe
influenzato a prescindere dai risultati del test”
“Infatti il ragionamento che ho fatto quando non avevo ancora i risultati è stato
questo: quanto poi ti cambia questo risultato? Relativamente, perchè se tu hai un
risultato negativo, comunque sei portata a fare una prevenzione maggiore, e quindi
tanto vale da un lato rientrare in questo programma"
" Perchè alla fine se fosse stato negativo, anzi sarei stata più in difficoltà,
perchè a quel punto lì dici è negativo però io voglio fare lo stesso la profilassi... per
cui ho preferito così"
Irene , 39 anni
PESO DELLA
STORIA
FAMILIARE
" Non ritengo che questa mutazione
abbia cambiato il mio modo di vedere le
cose, è stato il vivere quello che ho
vissuto. Una volta che mia mamma si è
ammalata e ho saputo che comunque
non sarebbe riuscita ho cambiato
proprio modo di pensare, non è stato
assolutamente dovuto al test. Non ti
abituano all'idea che quando nasci
comunque hai una fine.. pensi sempre di
essere eterno, e questa eternità forse
non è giusto che sia inculcata. Devi
viverla bene finchè ne hai la possibilità"
INFLUENZA SUL
DESIDERIO DI
MATERNITA’
" Forse l'unica cosa che mi lega un
po' di questa cosa è se avere o non
avere figli. Ecco, questo mi da un
po'... la paura c'è. Il discorso è sulla
mia pelle, ma su dei figli, lì è più
pesante. E' l'unico neo che posso
trovare in sta cosa è di saperlo. Se
non lo sapessi, probabilmente
avrei già dei figli... più
inconsapevolmente.
Dovessi
ammalarmi e io non ci sono più...
rimane proprio da solo. E questo
sì, questo limita molto la cosa..."
Barbara , 35 anni
“Sapere che è aumentato del tot per cento, non ti fa
stare tranquillo naturalmente. Comunque c'è
un'altissima percentuale di rischio già quando non
hai niente quindi figurati, se hai anche questo fattore
nel sangue, si ti fa pensare, a me ha pian piano fatto
entrare nell'idea che avrò una buona probabilità
di avere un cancro al seno, e quindi di
prepararmi psicologicamente (...) Devo fare i
controlli e sperare di non incontrare nessuna
malattia, anche se a stare a sentire tutte le storie,
effettivamente è come vincere alla lotteria... però c'è
chi vince"
"Avere più consapevolezza può aiutarti a prepararti mentalmente a delle brutte cose che
possono capitare, una preparazione psicologica. Poi hai già a chi fare riferimento se capita
qualcosa, hai a chi telefonare, fare domande, invece di sbattere la testa qua e là, magari
andando dalla persona sbagliata. In questo modo qua noi abbiamo già preparato tutto per
l'eventualità che poi speriamo che non viene, però se dovesse venire, mi sento
abbastanza preparata"
Esperienza (medici superspecialisti in TE)
Organizzazione del lavoro (setting e tempi adeguati)
Ricerca (reti;registri; di base)
Informazioni
Aiuto empatico
(promozione
dell’autonomia
decisionale)
parole
Informazioni
Emozioni
parole
&
gesti
Paura del fallimento
Fiducia nuove terapie
Proprio vissuto
Senso del limite
Paura
Negazione
Senso di colpa
Speranze
Gioia
Grazie per l’attenzione!