Politecnico di Bari
Facoltà di Ingegneria-Taranto
Corso di Laurea (interfacoltà)
in Ingegneria per l’Ambiente e il Territorio
(ex DM 270/2004)
CHIMICA
A.A. 2011-2012 (6 CFU)
Il docente
Dr. Giuseppe Romanazzi
Introduzione
Che cos’è
cos’è la CHIMICA?
Disciplina scientifica che studia: composizione, proprietà, struttura e
trasformazioni della materia, spontanee o provocate dall’Uomo.
Scienza che più di ogni altra ha influenzato la civilizzazione dell’uomo
dell’uomo.
Al contrario di quanto possa pensare l’opinione pubblica, vi é una
strettissima correlazione tra chimica e sviluppo positivo delle
condizioni di vita dell’uomo.
Introduzione
La straordinaria ampiezza di questo campo di studio, l’incessante sviluppo delle
acquisizioni teoriche, il continuo affinamento dei dati sperimentali forniti da
apparecchiature sempre più sofisticate e la limitatezza della mente umana, hanno
portato nel corso degli ultimi 60 anni ad una inevitabile, progressiva specializzazione.
Oggi, anche raggruppando le specializzazioni affini, esistono numerose branche della
chimica: Chimica inorganica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
Chimica
organica
organo-metallica
inorganica industriale
organica industriale
delle corrosioni (elettrochimica)
analitica
biologica (biochimica)
farmaceutica
ambientale (include la Chimica degli ecosistemi)
delle combustioni
dello stato solido
dei Materiali ……..etc…… etc…..
Tutte hanno però una base comune di leggi fondamentali che viene indicata
come chimica-fisica o chimica generale a seconda del livello più o meno
avanzato della trattazione.
Argomento del nostro corso è appunto questa base comune che tratteremo
ad un livello intermedio fra chimica generale e chimica-fisica, anche se
assai più vicino alla prima.
Testo consigliato e altro materiale didattico:
Franco Nobile e Piero Mastrorilli
La chimica
di base
con esercizi
CASA EDITRICE AMBROSIANA
Seconda edizione: giugno 2006
+ (almeno) 20 lezioni in formato PDF (fornite dal docente);
+ dispense per argomenti speciali (fornite dal docente);
+ appunti di lezione ed esercitazioni;
È obbligatorio procurarsi una TAVOLA PERIODICA DEGLI ELEMENTI
Consiglio caldamente a tutti di procurarsi un libro di testo
UNIVERSITARIO. Qualunque testo di Chimica per la Facoltà
di Scienze e/o Ingegneria va bene purché non sia di indirizzo
biomedico. Altresì sconsiglio l’uso del libro delle scuole medie
superiori.
Notare che non impongo l’acquisto di un libro, ma ribadisco
che l’esame di Chimica va preparato anche con l’ausilio di un
libro di testo. Quindi, se decidete di non acquistare il libro,
sfruttate le biblioteche, fatevelo prestare da un amico,
escogitate altri mezzi (legali! Fotocopiare integralmente un
libro è un reato) ma studiate anche sul libro di testo. Il libro
di testo è parte integrante del corso. tempo di illustrare. Ci
sono esempi svolti ed esercizi risolti che, spesso, il docente
non ha
Non fidatevi dei soli appunti. Tenete conto che il docente,
per quanto preparato possa essere, è un essere umano
soggetto a strafalcioni (spero rari!). Il libro di testo, prima
di essere pubblicato, è soggetto a revisione da parte di molte
persone, quindi “formalmente libero da errori (ovvero
macroerrori)”.
Il materiale didattico lo trovate sul sito della facoltà
previa iscrizione:
http://www.fataing.poliba.it/
Modalità dell’esame:
L’esame consiste in una prova scritta che può
comprendere anche quesiti di teoria:
se il voto della prova scritta è compreso tra 15 e 22
è necessario
sostenere un colloquio (prova orale) per
superare l’esame;
se il voto della prova scritta è ≥ 23, l’esame è
superato e si può verbalizzare direttamente.
N.B.: in caso di colloquio, il voto finale sarà la media
fra il punteggio della prova scritta e il voto del colloquio.
Chimica
(A.A. 2011/2012, 6CFU)
• Stati di aggregazione della materia
• Trasformazioni di stato
• Sistemi omogenei ed eterogenei. Fasi di un sistema
• Natura atomica della materia. Leggi fondamentali della Chimica
Stati di aggregazione della materia:
La materia si può presentare in diversi stati fisici, o stati di aggregazione. Essi sono il risultato di due
proprietà caratteristiche delle particelle che costituiscono la materia:
• il movimento (moti traslazionali dati dall’energia cinetica);
• le forze di reciproca interazione (determinano l’energia potenziale).
Il moto traslazionale è in relazione diretta con la temperatura; le forze di interazione, oltre a
dipendere da diversi parametri (struttura, composizione, etc), sono spesso correlate con la pressione. A
seconda del tipo di energia che prevale (cinetica o potenziale), la materia si può presentare in tre
diversi stati di aggregazione: gassoso, liquido, solido. Modificando opportunamente i parametri che
agiscono su un sistema, si può avere la trasformazione fisica del suo stato di aggregazione (passaggio di
stato).
MATERIA
(Tutto ciò che occupa spazio e possiede massa)
STATO SOLIDO
STATO LIQUIDO
STATO GASSOSO
forze di interazione >>
moti traslazionali e rotazionali
forze di interazione ~
moti traslazionali
forze di interazione <<
energia cinetica
• distribuzione ordinata (cristalli)
• rigido
• incomprimibile
• volume e forma propri
• distribuzione disordinata
• non rigido
• incomprimibile
• volume, ma non forma, proprio
• distribuzione disordinata
• non rigido
• comprimibile
• volume e forma non propri
La stessa sostanza può presentarsi nei tre diversi stati di aggregazione, in funzione della sua
temperatura e pressione
Condizioni standard
(P =1 atm, t =25 °C)
Condizioni normali
(P =1 atm, t =0 °C)
Trasformazioni (o passaggi) di stato:
GASSOSO o DI VAPORE
evaporazione
o gassificazione
sublimazione
condensazione
LIQUIDO
liquefazione
fusione
brinamento
solidificazione
congelamento
Particelle “congelate”
in una struttura caotica
Vetroso (metastabile)
devetrificazione
SOLIDO
Cristallino (stabile)
Particelle regolarmente impaccate
in una struttura cristallina
Sistemi omogenei ed eterogenei:
OMOGENEO
SISTEMA
(le sue proprietà sono le stesse in ogni suo
punto :costituito da un’unica fase)
(porzione di universo sottoposta
ad osservazione)
a Costituito da una singola
specie atomica presente
in uno specifico stato di
aggregazione : Cu, Hg, He
a Costituito da un singolo
composto chimico presente
in uno specifico stato di
aggregazione : C12H24O11 , H2O, N2
ETEROGENEO
(le sue proprietà non sono le stesse in ogni
suo punto:costituito da più fasi)
aspugne e fumi:
aschiume e nebbie:
amiscugli meccanici:
asospensioni:
aemulsioni:
a Soluzioni costituite da più
specie atomiche e/o composti
chimici:
8 gassose gas in gas
aria (N2 80%, O2 20%)
8 liquide gas in liquido
CO2 in H2O
liquido in liquido Alcool etilico (C2H6O) in H2O
solido in liquido
saccarosio (C12H24O11) in H2O
8 solide solido in solido
ottone (Zn in Cu), bronzo (Sn in Cu)
solido - gas
liquido - gas
solido - solido
liquido - solido
liquido - liquido
Le grandezze che caratterizzano
un sistema possono essere:
ESTENSIVE
(dipendono dall’ estensione del sistema.
Es.: lunghezza, massa, tempo,
volume, quantità di calore che interviene
in una reazione chimica, etc.)
INTENSIVE
(non dipendono dall’estensione del sistema.
Es.: densità, temperatura di fusione, viscosità,
indice di rifrazione, etc.)
Le grandezze estensive possono essere rese intensive riferendone il valore ad una
determinata quantità di sostanza .
Natura atomica della materia:
ELEMENTO: sostanza costituita da atomi tutti uguali
alcuni elementi esistono come molecole discrete,
ad esempio H2 O2 N2 F2 Cl2 Br2 I2 P4 S8
Li
C
S
COMPOSTO: sostanza che contiene atomi diversi
NaCl
acido oleico C18H34O2
Natura atomica della materia:
La teoria atomica di Dalton:
1. Tutta la materia è composta da atomi
indivisibili. Un atomo è una particella
estremamente piccola che mantiene la sua
identità durante le reazioni chimiche.
2. Un elemento è un tipo di materia composto
da un solo tipo di atomo. Tutti gli atomi dello
stesso elemento hanno la stessa massa e le
stesse proprietà
3. Un composto è un tipo di materia costituito
da atomi di due o più elementi chimicamente
uniti in proporzioni fisse. Due tipi di atomi in
un composto si legano in proporzioni espresse
da numeri semplici interi
4. Una reazione chimica consiste nella
ricombinazione degli atomi presenti nelle
sostanze reagenti in modo da dare nuove
combinazioni chimiche presenti nelle sostanze
formate dalla reazione
John Dalton (1766-1844)
“Un nuovo sistema di filosofia
chimica” (1808)
Natura atomica della materia:
Leggi fondamentali della chimica
Legge della conservazione delle masse
(A. L. Lavoisier)
Legge delle proporzioni definite
LEGGI PONDERALI
(J. L. Proust)
Legge delle proporzioni multiple
(J. Dalton)
Legge delle proporzioni multiple in volume
(J. L. Gay-Lussac)
Legge di Avogadro
(A. Avogadro)
LEGGI
VOLUMETRICHE
TRATTATO
ELEMENTARE
DI CHIMICA
PRESENTATO IN UN NUOVO ORDINE
E SECONDO LE MODERNE SCOPERTE,
Con Figure
1789
Legge della conservazione delle masse (1789)
“in ogni reazione chimica la massa totale
dei reagenti è uguale alla massa totale
dei prodotti della reazione”
A.L. Lavoisier (1743-1794)
reagenti
2 g di idrogeno + 16 g di ossigeno
prodotti
⇒
18 g di acqua
⇒
2 g di idrogeno + 18 g di acqua
oppure
4 g di idrogeno + 16 g di ossigeno
“La materia non si crea né si distrugge ma si trasforma”
Legge delle proporzioni definite (1806):
“in un dato composto gli elementi costituenti sono
sempre presenti in rapporti ponderali costanti,
indipendentemente dall’origine o dal modo di
preparazione del composto stesso”
in 100 g di H2O ci sono:
J. L. Proust
(1754-1826)
11,1 g di H
88,9 g di O
l’anidride carbonica CO2 è costituita da:
carbonio C 27,3% in peso
ossigeno O 72,7% in peso
per formare il cloruro di sodio NaCl devo far reagire:
23 g di Na e 35,5 g di Cl
4,6 g di Na e 7,1 g di Cl
1 g di Na e 1,54 g di Cl
(il rapporto ponderale Na/Cl resta sempre 1/1,54)
“Ogni composto ha una composizione ben precisa e invariabile”
Legge delle proporzioni multiple (1808):
“quando due elementi entrano a far parte di
diversi composti, le quantità in peso dell’elemento
che si combina con una quantità costante dell’altro
stanno tra loro in rapporti semplici, definiti da
numeri interi piccoli”
J.Dalton (1776-1844)
% in peso
% in peso
di azoto
di ossigeno
8g
63,6
36,4
N2O
14 g
16 g = 2 x 8 g
46,7
53,3
NO
C
14 g
24 g = 3 x 8 g
36,8
63,2
N2O3
D
14 g
32 g = 4 x 8 g
30,4
69,6
NO2
E
14 g
40 g = 5 x 8 g
25,9
74,1
N2O5
azoto
ossigeno
A
14 g
B
Per ogni composto al rapporto ponderale corrisponde un definito rapporto atomico.
“Ogni elemento è costituito da particelle elementari, dette
atomi, che entrano intere e indivise nelle reazioni”
Legge delle proporzioni multiple in volume (1808):
“quando due gas reagiscono tra di loro, il rapporto tra i loro
volumi misurati nelle stesse condizioni di temperatura e
pressione è definito da numeri interi piccoli …………………..
……………… se il prodotto della reazione è anch’esso un gas, il
rapporto tra il suo volume e quello di ciascuna delle specie
gassose reagenti è ancora definito da numeri interi piccoli”
1 volume di
idrogeno
idrogeno + azoto → ammoniaca
3 litri
1 litro
2 litri
H2/N2=3/1, H2/NH3=3/2, N2/NH3=1/2
→
+
1 volume di
cloro
J. L.Gay-Lussac
(1778-1850)
2 volumi di
cloruro di idrogeno
volume di N2
che reagisce
volume di O2
che reagisce
volume fisso
di N2
volume di O2 che
reagisce
con il volume fisso di N2
N2O
2
1
2
1
NO
1
1
2
2
N2O3
2
3
2
3
NO2
1
2
2
4
N2O5
2
5
2
5
Legge di Avogadro (1811):
“volumi uguali di gas diversi, misurati nelle stesse
condizioni di temperatura e pressione, contengono
un uguale numero di particelle (molecole)”
A. Avogadro (1776-1856)
H + Cl →
x HCl
H3 + Cl3 x
→ 2 H3/2Cl3/2
H2p + Cl2q → 2 HpClq
H2 + Cl2 → 2 HCl
Molecola: la più piccola particella di un composto o di un elemento capace di
esistenza indipendente. La molecola di un elemento è costituita da atomi uguali. La
molecola di un composto contiene gli atomi che lo compongono in un rapporto fisso e
costante.
Legge di Avogadro (1811):
“volumi uguali di gas diversi, misurati nelle stesse
condizioni di temperatura e pressione, contengono
un uguale numero di particelle (molecole)”
A. Avogadro
(1776-1856)
idrogeno + cloro → cloruro di idrogeno
1 vol
1 vol
2 vol
n mol.
n mol.
2n mol.
H2 + Cl2 → 2 HCl
idrogeno + ossigeno → acqua
2 vol
1 vol
2 vol
2n mol.
n mol.
2n mol.
2 H2 + O2 → 2 H2O
idrogeno + azoto → ammoniaca
3 vol
1 vol
2 vol
3n mol.
n mol.
2n mol.
3 H2 + N2 → 2 NH3
Molecola: la più piccola particella di un composto o di un elemento capace di
esistenza indipendente. La molecola di un elemento è costituita da atomi uguali. La
molecola di un composto contiene gli atomi che lo compongono in un rapporto fisso e
costante.
Chimica
(A.A. 2011/2012, 6CFU)
• U.m.a. Peso atomico. Grammo atomo. Numero di Avogadro.
• Peso molecolare. Grammo molecola. Mole.
• Formule minime. Formule molecolari. Formule di struttura
• Esercitazione (alla lavagna … NO SLIDE..!)
ATOMO:
Nucleo, formato da
protoni e neutroni
Guscio di elettroni
in movimento
nucleo
protoni
neutroni
mp
mn
elettroni
me
mp : mn : me ≅ 1 : 1 : 0,00054
Dimensioni atomiche:
massa atomo
da 1,673·10-24 (H) a 250 x 1,673·10-24 g
raggio atomo
0,5·10-8 ÷ 3·10-8 cm
massa elettrone
1/1836 della massa del protone
raggio elettrone
2,8·10-13 cm (2,8·10-5 Å)
raggio protone
10-12 cm (10-4 Å)
carica elettrone
e- = -1,602·10-19 coulomb
1 Å = 1·10-8 cm
La dimensione dell’atomo
Grandezze che caratterizzano gli elementi:
NUMERO ATOMICO Z
Indica il numero di protoni nel nucleo
Si scrive in basso a sinistra del simbolo
NUMERO DI MASSA A
È la somma del numero dei protoni e di quello di neutroni (N)
12
C
6
Si scrive in alto a sinistra del simbolo
ISOTOPI
atomi aventi lo stesso numero di protoni (Z) ma diverso numero di neutroni
Isotopo (ισο+τοποσ)
(ισο+τοποσ) = stesso posto
1H
2H
3H
12C
13C
14C
12C
13C
14C
Stabile
Stabile
Instabile
Protoni e Neutroni
I neutroni sono una sorta
di collante per il nucleo.
L’energia che tiene
assieme le particelle del
nucleo è enorme.
DIFETTO DI MASSA
La massa di un atomo dovrebbe consistere della somma
delle masse di Z protoni + N neutroni, trascurando la
piccola massa degli elettroni. Invece la massa di un
atomo è minore di questa somma. La differenza fra i
due valori è detto.
Difetto di massa
Equazione di Einstein: E = mc2
Il difetto di massa è dovuto a quella parte della massa
dei nucleoni che si è trasformata in energia di legame
fra i protoni e i neutroni di un atomo (0,1-0,7%)
Peso atomico, peso molecolare, peso formula
Con la dizione peso atomico (PA) (oppure massa atomica) viene indicato
il rapporto tra massa dell’atomo e una massa scelta arbitrariamente
come massa unitaria, tale massa è pari ad 1/12 della massa dell’atomo di
carbonio (isotopo 12) e vale:
u.m.a. (unità di massa atomica)
1/12 della massa di
12
6
C = 1,6605 ·10-24 g
(dalton)
1
1 u.m.a = ⋅ m 12 C
6
12
Analogamente il peso molecolare (PM) di un elemento o composto è uguale al
rapporto tra la massa di una molecola dell’elemento o del composto e quella
dell’unità di misura ed è, pertanto, un numero puro che indica quante volte la
molecola pesa in più dell’unità di misura: poiché per il peso molecolare e per il
peso atomico si fa riferimento alla stessa unità di misura, è di tutta evidenza
che il peso molecolare è uguale alla somma dei pesi degli atomi che la
costituiscono. Per composti, come i sali, che non presentano molecole discrete,
si deve parlare di peso formula.
Peso atomico, peso molecolare, peso formula
PESO ATOMICO
È il rapporto tra massa dell’atomo
e massa dell’unità di misura.
mE
E u.m.a =
(1/12) ⋅ m 12 C
6
PESO MOLECOLARE
È la somma dei pesi degli
atomi che costituiscono la molecola*.
PESO FORMULA
È il rapporto tra la massa della formula
e la massa dell’unità di misura
(per composti non molecolari*).
Dove
m 12 C
6
E n u.m.a =
(1/12) ⋅ m
A a Bb u.m.a =
è la massa del isotopo 12 del carbonio
* sarà più chiaro dopo lo studio del legame chimico
mEn
12
6C
m A a Bb
(1/12) ⋅ m
12
6C
Osservazione
:
Le dizioni peso atomico e peso molecolare sono in realtà
improprie, perché tali valori non esprimono dei pesi (peso=
massa X accelerazione gravitazionale = m·g), ma sono
numeri adimensionali.
Negli ultimi 30 anni sono state proposte da organismi
internazionali definizioni formalmente più corrette, che
mettono in evidenza l’adimensionalità della grandezza, come
massa atomica relativa e massa atomica media relativa, ma
in pratica non sono state adottate e si sono conservate le
secolari dizioni peso atomico e peso molecolare.
Unità di massa atomica (uma
(uma oppure u):
1/12 della massa di 12C ( = 1,6606×
1,6606×10-24 g)
Alcuni pesi atomici (ovvero massa atomica media relativa):
H
He
Li
Be
B
C
N
O
F
1,008
4,003
6,941
9,012
10,811
12,011*
14,007
15,999
18,998
* perché? Non è 12 uma
Ne
Na
Mg
Al
Si
P
S
Cl
Ar
20,180
22,990
24,305
26,982
28,086
30,974
32,066
35,453
39,948
* perché? Non è 12 uma
La massa relativa (peso atomico) di un dato elemento chimico è una media
ponderata delle masse relative dei suoi isotopi: in particolare è la sommatoria del
prodotto tra la massa relativa di ciascun isotopo e la relativa abbondanza isotopica.
Tralasciando l’isotopo 14 del carbonio (che è instabile*) in natura si trova che ogni 112
atomi di carbonio isotopo 13 ce ne sono 10000 di carbonio isotopo 12
abbondanza isotopica
10000
abbondanza C =
≅ 0,98892
10000 + 112
12
abbondanza 13C =
112
≅ 0,01108
10000 + 112
(Quindi il 98,892 % è di
12C)
(Quindi lo 1,108 % è di
13C)
massa (relativa) isotopica del C = 12,000000
12
massa (relativa) isotopica del C = 13,003354 =
13
(per definizione deve
essere esattamente 12 )
m 13 C
6
(1/12) ⋅ m
12
6C
Peso atomico di C = 12,000000 ⋅ 0,98892 + 13,003354 ⋅ 0,01108
Peso atomico di C ≅ 12,011
* Esiste anche un isotopo 11 del carbonio anch’esso instabile!
(valore tabulato del peso atomico medio)
Peso (massa) atomico ed abbondanza isotopica
Calcolo della massa atomica media di un elemento note le abbondanze
relative (= frazione del numero totale di atomi costituiti da un dato
isotopo) degli isotopi costituenti.
Cloro:
isotopo
35
17
Cl
37
17
Cl
massa isotopo
34,96885
36,96590
abbondanza relativa
0,75771
0,24229
34,96885 uma x 0,75771 = 26,49625 uma +
36,96590 uma x 0,24229 = 8,95647 uma
_____________
Peso (massa) atomico medio
= 35,45272 uma
Lo stesso procedimento può essere applicato ad elementi costituiti da tre
o più isotopi di cui sono note le abbondanze relative.
N.B.: La somma delle abbondanze relative di tutti gli isotopi di
un dato elemento è uno.
Peso (massa) atomico ed abbondanza isotopica. Altri esempi:
isotopi = elementi con stesso Z e diverso N
elemento
carbonio
isotopi
12C
13C
14C
ossigeno
16O
17O
18O
potassio
39K
40K
41K
piombo
204Pb
206Pb
207Pb
208Pb
abbondanza
relativa (%)
Z
A
N=A–Z
6
6
6
6
7
8
8
8
8
19
19
19
12
13
14
16
17
18
39
40
41
8
9
10
20
21
22
98,89
1,11
tracce
99,759
0,037
0,204
93,138
0,012
6,800
82
82
82
82
204
206
207
208
122
124
125
126
1,3
26,0
20,7
52,0
peso
atomico (tabulato)
12,011
15,9994
39,0983
207,19
Oggi è possibile misurare accuratamente le masse atomiche tramite
uno strumento chiamato spettrometro di massa
Sui testi di chimica trovate
tabelle che già tengono conto
dall’ abbondanza isotopica.
Qui, ad esempio, è riportata la
tabella 1.7 del libro di testo
Nobile-Mastrorilli.
Come vedremo in seguito
piuttosto
che
usare
una
tabella del genere è meglio
usare una tavola periodica
degli elementi che contiene
ulteriori
informazioni
e
proprietà degli atomi.
16
Peso molecolare = somma delle massa atomiche (pesi atomici)
della molecola
Esempi:
H2SO4 (formula dell’acido solforico):
solforico):
peso molecolare = 2×
2×1,008 + 32,066 + 4×
4×15,999 = 98,078 u.m.a.
C6H12O6 (formula del glucosio):
glucosio):
peso mol. = 6×
6×12,011 + 12×
12×1,008 + 6×
6×15,999 = 180,156 u.m.a.
Grammo-atomo. Numero di Avogadro.
Peso molecolare. Grammo-molecola. Mole.
Corrispondentemente al peso atomico e al peso molecolare si definisce il grammo-atomo,
la grammo-molecola come la quantità di una specie chimica il cui peso in grammi è
numericamente uguale al valore, rispettivamente, del PA, del PM.
In base a questa definizione ogni grammo-molecola o grammo-atomo contiene un
ugual numero di particelle.
Nel linguaggio chimico si tende oggi a sostituire alle dizioni grammo-atomo o grammomolecola la dizione mole. La definizione di mole (Comité International des Pois et
Mesures; 1971) è la seguente:
“Mole è la quantità di materia di un sistema che contiene tante entità
elementari quanti atomi sono contenuti in 0,012 Kg (12 g) di carbonio
(isotopo 12)”
Questo numero di atomi è il numero di Avogadro:
N = 6,022·1023
N particelle (atomi, molecole, ioni, etc.) = 1 mole
Il numero di Avogadro è un numero grandissimo
7 × 1022
stima del numero di stelle nell' universo osservabile.
1023
stima del numero di granelli di sabbia di tutte le spiagge del mondo.
N ≈ 6,022×1023
è il numero di atomi in 12 grammi di
12C
1024
è il numero totale di connessioni sinaptiche presenti nel cervello
umano.
Il numero di Avogadro è un numero grandissimo
È,quindi, difficile cogliere la reale entità del numero di Avogadro se non
si simula un esperimento quale potrebbe essere quello di calcolare il
tempo necessario per contarlo con, per esempio, una velocità costante di
150 numeri al minuto.
Con tale velocità si conterebbero:
150 numeri/minuto · 60 minuti/ora · 24 ore/giorno · 365 giorni/anno =
= 7,884 · 107 numeri/anno
6,022 · 1023 numeri/7,884 · 107 numeri/anno ≈ 1016 anni
!!!
TABELLA: Unità di misura del Sistema Internazionale.
La mole è una delle sette grandezze fondamentali.
Osservazione:
N=
12 g di carbonio isotopo 12 = numero di atomi
12 uma
=
12 g
12 x 1,6605·10-24 g
1
=
1,6605·10-24
=6,022·1023
Moli di elementi
Grammo-atomo. Numero di Avogadro.
u.m.a. (unità di massa atomica)
1/12 della massa di
12
6
12
6
C = 1,6605 ·10-24 g
C = 12 u.m.a.; C = 12,011 u.m.a.
peso atomico
12
6
C = 98,89 %
13
6
C=
1,11 %
“quantità in grammi pari al peso atomico”
grammo atomo
12
1 grammo atomo 6 C = 12 g
1 grammo atomo
1 grammo atomo
C = 12,011 g
W = 183,85 g
1/ 1,6605 ·10-24 = NA (numero di Avogadro) = 6,022 ·1023
Peso molecolare. Grammo-molecola. Mole.
peso molecolare (peso formula)
“somma dei pesi atomici”
“quantità in grammi pari al peso molecolare”
grammo molecola
1 grammo molecola
1 grammo molecola
mole
CO2
NH3
= (12 +16 + 16) = 44 g
= (14 +1 + 1 + 1) = 17 g
“quantità di sostanza che contiene un numero di particelle
pari ad un numero di Avogadro NA”
m (g)
n (mol) =
M (g/mol)
(questa è la definizione operativa (cioè in formula
matematica) della mole; e sarà fondamentale per risolvere
qualsiasi esercizio o problema chimico che incontrerete)
Dove m simboleggia la massa della sostanza (elemento, molecola,
sale ione. etc) ed M simboleggia
il peso di una mole di tale
sostanza: peso molare.
Mole e peso molare
Una mole di sostanza diverse ha peso diverso !
In una reazione o in una formula chimica contano le moli, non i grammi!
Riepilogando:
u.m.a. (dalton): unità di misura usata per le masse atomiche
1 u.m.a. = 1/12 della massa del 12C = 1,6605·10-24 g
m (g)
n (mol) =
M (g/mol)
peso atomico/molecolare (relativo): indica quante volte
l’atomo/molecola pesa più dell’unità di misura (cioè del peso di
riferimento)
12C = 12 u.m.a.
grammo-atomo/molecola:
quantità
in
grammi
di
elemento/molecola pari al suo peso atomico/molecolare relativo
1 grammo-atomo di 12C = 12 g
un
NUMERO PURO!
u.m.a.
dalton
MASSA!
g
numero di Avogadro: numero di atomi contenuti in 1 grammoatomo
NA = 6,022 ·1023
mole: quantità di materia contenente NA = 6,022 ·1023 particelle
mole ≡ grammo-atomo/molecola
Esempio per CO2:
peso molecolare: (12 + 16 + 16) u.m.a. = 44 u.m.a. ≡ 44 dalton
1 grammo-molecola: 44 g (contengono 6,022 ·1023 molecole)
1 mole: 44 g (contiene 6,022 ·1023 molecole)
peso molare: 44 g/mol
Determinazione dei pesi molecolari di sostanze volatili
attraverso la densità gassosa relativa.
Se si considerano volumi uguali (V) di due gas diversi A e B alla stessa
temperatura e pressione, le quantità (in grammi) dei due gas in essi contenuti,
rispettivamente MA e MB, contengono lo stesso numero N di molecole.
Indicando con mA il peso in grammi di una molecola di A e con mB quello di una
molecola di B, le due quantità MA e MB risulteranno essere date da:
La densità relativa del gas A rispetto al gas B è:
Semplificando e dividendo mA a numeratore e mB a denominatore per
l’unità delle masse atomiche, si ottiene la relazione cercata:
Usando come riferimento l’idrogeno molecolare, di peso molecolare 2,016
dalton:
il peso molecolare del gas A è uguale a 2,016 volte la sua densità relativa
rispetto all’idrogeno:
Composizione ponderale
La formula di un composto fornisce in maniera immediata e diretta la sua
composizione atomica. Una mole di un composto di formula AaBbCc contiene a moli
di atomi dell’elemento A, b moli di atomi dell’elemento B e c moli di atomi
dell’elemento C; in modo equivalente si può dire che il rapporto atomico tra gli
elementi che formano il composto è:
a:b:c
La formula consente anche di ricavare in maniera molto semplice la composizione
del composto sotto forma di rapporto ponderale o di percentuale in peso.
Una mole di composto, pari a AaBbCc grammi, contiene mA, mB e mC grammi degli
elementi A, B e C corrispondenti rispettivamente ad a moli di atomi di A, b moli di
atomi di B e c moli di atomi di C:
mA (g) = a (mol) · A (g/mol)
mB (g) = b (mol) · B (g/mol)
mC (g) = c (mol) · C (g/mol)
Il rapporto ponderale che caratterizza il composto è:
mA : mB : mC
Le espressioni con le quali si calcolano le percentuali in peso degli
elementi nel composto si ricavano con le proporzioni:
Esercizio: Un miscuglio di perclorato di potassio (KClO4) e di cloruro di
sodio (NaCl) contiene il 36,11% in peso di cloro. Calcolare la percentuale
dei due composti nel miscuglio.
Svolgimento
Le percentuali di cloro nel perclorato di potassio e nel cloruro di sodio
sono rispettivamente:
Indicando le quantità di perclorato di potassio e di cloruro di sodio contenute in 100 g
di miscuglio rispettivamente con x (%KClO4) e y (%NaCl), la massa di cloro contenuta in
ciascuna di esse si ottiene dalla proporzione:
Le quantità mClx e mCly possono essere ottenute anche in maniera più diretta:
I valori di x e y, e quindi la composizione della miscela, si ottengono risolvendo il
sistema:
Esercizi analoghi:
Esercizi analoghi con “difficoltà maggiore”:
Formule minime. Formule molecolari.
Formule di struttura
formula minima
“indica, con numeri interi più piccoli possibili, i rapporti
con cui gli atomi si legano tra loro in un composto”
H2O
CH
acqua
acetilene
benzene
“indica l’esatto numero di atomi che si legano tra loro
in un composto”
formula molecolare
H2O
acqua
formula di struttura
C2H2
C6H6
acetilene
benzene
“indica le posizioni steriche relative degli atomi che si
legano tra loro in un composto”
H
O
H
H
H
acqua
H C
C H
acetilene
H
C
C
C
C
H
C
C
H
benzene
H
Formule minime e Formule molecolari.
Studiare gli esercizi svolti del libro di testo a pag, 43-49
Esercizi:
ESERCITAZIONE (alla lavagna … NO SLIDE..!)
1° esercizio.
esercizio.
50 g di un miscuglio di CaBr2 e LiBr contengono il 84,77 % in peso di bromo. Calcolare
la composizione percentuale del miscuglio.
2° esercizio.
esercizio.
20,0 g di una lega di magnesio e zinco, bruciati con un eccesso di aria, formano una
miscela dei relativi ossidi (MgO e ZnO) che pesa 30,684 g. Determinare la composizione
percentuale in peso della lega.
3° esercizio.
esercizio.
L’analisi di una sostanza organica costituita da carbonio, idrogeno e ossigeno ha fornito
i seguenti risultati: per combustione di 1,101 g si sono ottenuti 2,646 g di anidride
carbonica e 0,540 g di acqua. Ricavare la formula minima della sostanza. Sapendo,
inoltre, che la densità gassosa della sostanza relativa all’idrogeno molecolare è 54,624
stabilirne la formula molecolare.
4° esercizio.
esercizio.
L’analisi di una sostanza organica costituita da carbonio, idrogeno, azoto e ossigeno ha
fornito i seguenti risultati: per combustione di 8,972 g si sono ottenuti 21,125 g di
anidride carbonica, 7,206 g di acqua e 896,6 mL di azoto molecolare raccolto a
condizioni normali. Ricavare la formula minima e la formula molecolare della sostanza
sapendo che la sua densità relativa al gas elio (dr→He) è pari a 56,04.
5° esercizio.
esercizio.
Un composto organico è costituito da carbonio, idrogeno, azoto e ossigeno. Per
analizzare carbonio e idrogeno, 2,404 g di composto vengono bruciati con un eccesso di
ossigeno. Dalla combustione si ottengono 3,521 g di diossido di carbonio e 2,163 g di
acqua. Per l’analisi dell’azoto si pesano 3,606 g di composto, che sviluppano 672,1 mL di
azoto a c.n. La densità relativa del composto rispetto all’ossigeno è dr→O2= 3,756.
Ricavare la formula minima e la formula molecolare del composto.
Chimica
(A.A. 2011/2012, 6CFU)
• Come
introduzione a questa lezione potete studiare da soli il cap3 del libro di testo
• Modello atomico di Thomson
• Il nucleo atomico (esperienza di Rutherford)
• Modello atomico di Rutherford
• Radiazioni elettromagnetiche. Spettro delle radiazioni elettromagnetiche.
Fenomeni di interferenza e diffrazione
• Interazione tra luce e materia (spettri atomici)
• Modello atomico di Bohr. Numeri quantici
Modello atomico di J. J. Thomson (1897)
Thomson misurò con opportuni esperimenti
il rapporto carica/massa dell’elettrone:
J. J. Thomson
(1856-1940)
Nobel 1906
e/m= 1,76 ×1011 C/Kg
da cui si dedusse * :
m= 9,11×
×10-31 Kg= 9,11×
×10-28 g
Un valore circa 1800 volte* più piccolo della massa dell'idrogeno. Quasi tutta la
massa atomica è, quindi, associata alla carica positiva (cioè, come vedremo, è
concentrata nel nucleo)
Egli ipotizzò il suo modello: “Tutta la massa e la carica positiva sono
distribuite uniformemente in una sfera di raggio ∼ 1Å (10-10 m). Gli
elettroni sono distribuiti in questa sfera agendo da collante per le cariche
positive, e sono in numero tale da rendere neutro l’atomo”
++
+ + +
-+ - + -
*Fu in seguito Robert Andrews Millikan (1868-1953) con l’esperimento
della “goccia cadente” (1909) a misurare la carica dell’elettrone.
La radioattività
• “Raggi” α: particelle con carica positiva (nuclei di elio con 2 protoni e 2 neutroni)
• “Raggi β”: elettroni
• “ Raggi γ”: radiazioni elettromagnetiche ad alta energia
La radioattività è il fenomeno per cui alcuni nuclei, non stabili, si trasformano in altri emettendo
particelle. La scoperta della radioattività avvenne alla fine dell’800 ad opera di Henry Bequerel e dei
coniugi Pierre e Marie Curie, che ricevettero il Premio Nobel per la Fisica per le loro ricerche. Essi
scoprirono che alcuni minerali, contenenti uranio e radio,avevano la proprietà di impressionare delle
lastre fotografiche poste nelle loro vicinanze. Le lastre fotografiche, una volta sviluppate,
presentavano delle macchie scure.
Modello atomico di Rutherford (1911)
Un fascio di particelle α viene fatto
passare attraverso una lamina di oro. Le
particelle che attraversano la lamina
colpiscono uno schermo fluorescente
illuminandolo.
Se la distribuzione di carica e massa
negli atomi di oro della lamina fosse
omogenea,
tutte
le
particelle
dovrebbero attraversarla senza subire
deviazioni.
Invece Rutherford osservò che:
• la maggior parte delle particelle attraversa la lamina senza subire deviazioni;
• alcune subiscono deviazioni di varia ampiezza;
• una certa porzione di particelle viene respinta.
Modello atomico di Rutherford (1911)
Ernest Rutherford
(1871-1937)
Nobel 1908
(Modello dinamico basato sulla meccanica newtoniana)
tutta la carica positiva e quasi tutta la massa sono
concentrate in un “nucleo” di raggio ~10-4Å. Atomo
«vuoto»
gli elettroni, in numero uguale alla carica nucleare, ruotano
intorno al nucleo
+
+
Rappresentazione del modello di atomo che
spiega l’esperimento di Rutherford
+
+
+
+
+
+
+
+
+
+
+
+
+
+
Modello atomico di Rutherford (1911)
Ernest Rutherford
(1871-1937)
Nobel 1908
Dimensioni atomiche: circa 1 Å = 10-10 m
Dimensioni nucleari: circa 10-5 Å = 10-15 m
La maggior parte dell'atomo è vuoto
Quasi tutta la massa atomica è quindi
concentrata nel nucleo
Modello atomico di Rutherford (1911)
Hendrik Antoon Lorentz, fisico olandese, critica il modello di
Rutherford applicando la teoria elettromagnetica classica
all’elettrone.
Limiti alla teoria di Rutherford:
Gli elettroni, oscillando attorno alla loro
posizione di equilibrio e girando attorno
al nucleo, per le leggi di Maxwell e di
Hertz, avrebbero dovuto emettere una
radiazione elettromagnetica, e quindi
ridurre la loro energia.
Gli elettroni perderebbero rapidamente
la loro energia irradiandola e quindi
cadrebbero a spirale verso il nucleo,
cioè collasserebbero sul nucleo.
Ma gli atomi sono stabili!
Come mai?
Ernest Rutherford
(1871-1937)
Nobel 1908
Modello atomico di Rutherford (1911)
Limiti alla teoria di Rutherford:
Ernest Rutherford
(1871-1937)
L’elettrone movendosi di moto Nobel 1908
-
+
circolare perderebbe energia
cinetica avvicinandosi
progressivamente
al nucleo (in circa 10-11s)
-
Le leggi dell’elettromagnetismo
stabiliscono che quando una carica
elettrica subisce una qualsiasi
accelerazione perde energia
Radiazioni elettromagnetiche
Una radiazione elettromagnetica è una radiazione caratterizzata da un campo
elettrico E e uno magnetico H perpendicolari tra loro e perpendicolari alla
direzione di propoagazione. La sua velocità nel vuoto è c = 2,9979·108 m/sec.
Vettore
elettrico
Sorgente
Rappresentazione di un onda elettromagnetica.
Vettore
magnetico
Direzione di
propagazione
Grandezze caratteristiche di un onda elettromagnetica.
A
λ Lunghezza d’onda: rappresenta la distanza tra due
minimi o due massimi (unità di lunghezza: m, cm,
nm, A, …)
ν Frequenza: ν=c/λλ, rappresenta nell’unità di tempo
λ
il numero di vibrazioni di un onda di lunghezza
d’onda λ (unità di tempo-1: sec-1, Hz)
E = h·ν
ν
A Ampiezza: rappresenta l’altezza di una cresta ed è
indicativa dell’intensità dell’onda
h = 6.626·10-34 J ·s (costante di Planck)
Radiazioni elettromagnetiche
Un’onda è caratterizzata dalla sua lunghezza e, quindi, dalla sua frequenza. In
alcuni casi è più comodo usare al posto di λ il suo reciproco, che viene indicato
~ e prende il nome di numero d’onda:
con v
1
~
v=
Poiché la frequenza ν :
λ
c
1 ν
ν=
⇒
=
λ
λ c
la relazione tra il numero d’onda e la frequenza è
ν
~
v=
c
Quindi il nome di numero d’onda come la frequenza è proporzionale
all’energia della radiazione elettromagnetica.
Spettro delle radiazioni elettromagnetiche
Le onde elettromagnetiche sono classificabili in base alla loro lunghezza d’onda:
La luce viaggia in pacchetti di energia chiamati fotoni o quanti.
L’energia quindi non varia in maniera continua ma viene trasportata in
quantità discrete e dipende dalla frequenza della radiazione.
Il fotone associato ad un’onda di frequenza υ trasporta un’energia
pari a E = h υ.
L’intensità della radiazione è proporzionale al numero di fotoni.
E=hυ
h = 6,62·10-34 J·s
1 nm = 10-9 m
1 Å = 10-10 m = 0,1 nm
Interazioni tra luce e materia
Spettro (continuo) della luce bianca
Spettro: insieme delle frequenze che compongono la radiazione
analizzata dallo spettrometro
Interazioni tra luce e materia
Un prisma è un oggetto in
grado di disperdere la luce
bianca nelle sue componenti
monocromatiche
Rifrazione della luce
Hydrogen
gas
Se la luce bianca viene analizzata
dopo aver attraversato un’ampolla
trasparente che contiene un
elemento
tenuto
allo
stato
gassoso,
lo
spetto
colorato
continuo
della
luce
bianca
presenta delle righe nere; queste
denunciano il mancato arrivo di
radiazioni che, pertanto, sono
state assorbite dall’elemento
Spettro di assorbimento
Gli elementi, portati allo stato gassoso e
riscaldati ad alta temperatura, emettono una
luce che, analizzata, dà uno spettro
costituito da righe di un colore caratteristico
dell’elemento eccitato su fondo nero
Spettro di emissione
Spettro di assorbimento
Spettro di emissione
Interazioni tra luce e materia. Spettri atomici
Interazioni tra luce e materia
Spettro dell’idrogeno: eq. di Balmer-Ritz
Nello spettro di emissione si notano tre gruppi di righe, detti serie: la serie di Lyman,
quella di Balmer e quella di Paschen: tutte le righe di Lyman e la prima di Balmer sono
nella zona dell’ultravioletto, le rimanenti righe di Balmer e la prima di Paschen cadono
nel visibile, tutte le altre nell’infrarosso. Nonostante che lo spettro di emissione
dell’idrogeno appaia complicato, una semplice relazione matematica correla la posizione
di tutte le righe. Tale relazione è
1
1
~
ν = RH 2 − 2
n1 n2
RH costante di Rydberg (109678 cm-1)
n1 e n2 interi con n1<n2
1
~
ove v è il numero d' onda ed è uguale a
λ
Tuttavia, nessuna teoria atomica era in grado di spiegare e predire spettri atomici
fino a quando Niels Bohr non introdusse il suo modello atomico….
Modello atomico di Bohr (1913)
(Atomi idrogenoidi H, He+, Li++, …)
Niels Bohr
(1885-1962)
Nobel 1922
1° postulato l’atomo si trova in uno stato stazionario che non irradia energia
2° postulato le orbite permesse all’elettrone di massa m e di velocità v, in ogni
stato stazionario sono circolari e solo quelle aventi un raggio r
tale da rendere il suo momento angolare mvr pari a un multiplo
intero del quanto di momento angolare h/2π
π
mvr
3° postulato
= n
h
2π
l’atomo può assorbire o irradiare energia solo quando
passa da uno stato stazionario ad un altro
Modello atomico di Bohr
(Atomi idrogenoidi H, He+, Li++, …)
QUANTIZZAZIONE DEL RAGGIO
Fd 'attrazione = Fcentrifuga
(1)
⇒
e2
v2
=m
2
r
r
Evidenziando r del secondo membro
mv 2 r 2
r=
e2
(2)
Moltiplicando il numeratore e il denominatore per m
Tenendo conto del secondo
2 2 2
m
v r
(3)
r=
me 2
2
h
h
postulato: mvr = n
⇒ m 2v 2 r 2 = n 2
2π
4π 2
(4)
Sostituendo la relazione (4) nella (3) si ottiene:
r = n2
h2
4 π 2 me
quantizzazione del raggio
2
(n=1, 2, 3, … numero quantico principale)
Modello atomico di Bohr (1913)
(Atomi idrogenoidi H, He+, Li++, …)
QUANTIZZAZIONE DELL’ENERGIA
Energia = Energia potenziale + Energia cinetica
Tenendo
e2 1 2
E = V + T = − + mv
(7)
r 2
conto della (1) e 2
v 2 possiamo
=m
2
r
r
Sostituendo la relazione (8) nella (7) si ottiene:
Sostituendo la quantizzazione del raggio
e2
E=− =−
2r
r = n
2
ricavare la
E =V +T
(6)
1 2 e2
mv =
2
2r
(8)
e2 e2
e2
E=− +
=−
r 2r
2r
h2
4 π 2 me
2
(9)
nella (9) si ottiene:
e2
2π 2 me 4
=− 2 2
2
h
nh
2n 2
4π 2 me 2
2π 2 me 4
1
E n = − 2 2 = − 2 E0
nh
n
quantizzazione dell’energia
(n=1, 2, 3, … numero quantico principale)
Modello atomico di Bohr
(Atomi idrogenoidi H, He+, Li++, …)
E
16r1=r4
n=∞
∞
0
E4= -1/16 E0
∆E4-1= E4 – E1
E3= -1/9 E0
n=4
9r1=r3
n=3
4r1=r2
r1
∆E3-1= E3 – E1
E2= -1/4 E0
n=2
(n=1), E1
Serie di Balmer
(UV-VIS)
(n=2), E2
∆E2-1= E2 – E1
(n=3), E3
E1= - E0
n=1
Serie di Lyman
(lontano UV)
ν
E = h ⋅ν
∆E3-
∆E3-
∆E2-
1
1
1
(n=4), E4
Modello atomico di Bohr
(Atomi idrogenoidi H, He+, Li++, …)
Derivazione teorica della costante di Rydberg
2π 2 me 4
1
E n = − 2 2 = − 2 E0
nh
n
∆E = E2 − E1 = ( −
1
~
v=
λ
1
1
1
1
+
)
E
=
(
−
) E 0 = hν
0
2
2
2
2
n2 n1
n1 n2
v
c = λv = ~
v
1
1
~
hcv = ( 2 − 2 ) E0
n1 n2
1 1
~
v = RH 2 − 2
n1 n2
v = cv~
1
1 E0
~
v =( 2 − 2)
n1 n2 hc
E0
RH ≡
hc
E
E
E
0
E4
E3
0
E4
E3
E2
E2
E
0
E4
E3
•
E2
E
E1
•
E1
stato fondamentale
E assorbita
E1
stato eccitato
•
stato fondamentale
E emessa
1
1
1
1
∆E = E 2 − E1 = − 2 + 2 E 0 = 2 − 2 E 0
n 2 n1
n1 n 2
∆E = h ⋅ν
Modello atomico di Bohr
(Atomi idrogenoidi H, He+, Li++, …)
n=5
=4 =3
=2 =1
E = hc/
c/λ
λ
Spettro di emissione
Questa transizione
non è possibile
Limiti del modello atomico di Bohr
Il modello di Bohr, per quanto stimolante,
ha delle limitazioni:
incapacità di interpretare i risultati spettroscopici di
atomi polielettronici
incapacità di offrire qualsiasi base teorica per
interpretare le proprietà direzionali dei legami chimici
intrinseca contraddizione (si postula che l’elettrone non
ubbidisce alle leggi della fisica classica e si usano
proprio queste leggi per definire il raggio delle orbite e
l’energia del sistema)
Estensione del modello atomico di Bohr
(Atomi polielettronici) numeri quantici l ed m
Le orbite descritte dal moto dell’elettrone intorno al nucleo sono ellittiche, con
una eccentricità quantizzata (Sommerfeld: numero quantico l) e assumono
orientazioni nello spazio quantizzate (effetto Zeeman: numero quantico m).
n=1, 2, 3, … numero quantico principale
l=0, 1, … (n-1) numero quantico secondario
m=0, ±1, … ± l numero quantico magnetico
Estensione del modello atomico di Bohr
(Atomi polielettronici) numeri quantici l ed m
n = 1, 2, 3, …
numero quantico principale ⇒ determina l’energia dell’orbita
l = 0, 1, … (n-1) numero quantico secondario ⇒ determina l’energia e la forma dell’orbita
m = 0, ±1, … ± l numero quantico magnetico ⇒ determina l’orientazione dell’orbita
Chimica
(A.A. 2011/2012, 6CFU)
• Ipotesi di De Broglie. Principio di indeterminazione di Heisenberg.
• Modello atomico ondulatorio. Equazione d’onda di Schrödinger.
• Orbitali atomici e numeri quantici. Energia degli orbitali atomici.
• Principio di esclusione di Pauli. Regola di Hund.
• Aufbau: costruzione della tabella periodica degli elementi.
• Proprietà periodiche degli elementi.
Dualismo onda-particella
Ipotesi di De Broglie (1924)
Fenomeni fisici:
di carattere corpuscolare
di carattere ondulatorio
(fenomeni connessi con l’esistenza di
particelle discrete)
(fenomeni che mostrano proprietà
continue proprie delle onde)
•leggi classiche del moto
•diffrazione della luce
Meccanica classica
Teoria ondulatoria classica
di carattere dualistico onda-corpuscolo
Moderna teoria quanto-meccanica
(Il carattere corpuscolare o il carattere
ondulatorio di un fenomeno sono due
aspetti di una stessa realtà)
natura dualistica delle particelle microscopiche
natura dualistica della luce
Relazione di Planck
E = hν = h
Relazione di Einstein
c
λ
E = mc 2
λ=
h
mc
Ipotesi di De Broglie
a qualsiasi particella di massa m e di velocità v può
essere associata un’onda di lunghezza d’onda pari
a:
λ=
h
mv
•Diffrazione di un fascio di elettroni ad opera
di un reticolo di diffrazione costituito da un
cristallo di Ni
Dualismo onda-particella
Ipotesi di de Broglie (1924)
Per i fotoni:
Relazione di Planck
Relazione di Einstein
c
E = hν = h
λ
E = mc 2
h
λ=
mc
A. Einstein
(1879-1955)
Nobel 1921
M. Planck
(1858-1947)
Nobel 1919
Per un qualsiasi corpo in movimento:
h
λ=
mv
Natura dualistica dell’elettrone
(Esperimenti chiave)
L. De Broglie
(1892-1987)
Nobel 1929
• Effetto
fotoelettrico
e
termoelettrico:
natura
corpuscolare dell’elettrone
• Davisson e Germer, 1927: Diffrazione di un fascio di
elettroni ad opera di un reticolo di diffrazione costituito da un
cristallo di Ni
Dualismo onda-particella
Ipotesi di De Broglie 1924
L’ipotesi del dualismo onda-particella ricevette la conferma sperimentale nel
1927 e, nel 1929, De Broglie fu insignito del premio Nobel per la fisica.
•Davisson e Germer, 1927: Diffrazione di un fascio di elettroni ad opera di un reticolo di
diffrazione costituito da un cristallo di Ni
Raggi X
Elettroni
Un fascio di elettroni era diretto verso un cristallo di nichel, che poteva essere ruotato per misurare la
distribuzione angolare degli elettroni. Si trovò che a certi angoli si aveva un picco nell’intensità degli
elettroni diffusi, in accordo con la condizione di interferenza costruttiva tra le “onde elettroniche”
riflesse da diversi piani reticolari, in maniera identica a quello che accade con i raggi X.
Principio di indeterminazione di Heisenberg (1927)
Tale legge pone un limite invalicabile alla possibilità di conoscenza umana,
riconoscendo l’impossibilità teorica di determinare contemporaneamente e con
precisione arbitraria due parametri fisici importanti di una particella quali sono la
posizione spaziale e il momento.
Il prodotto tra l’incertezza ∆x della misura della posizione x di una particella, e
l’incertezza ∆(mv) della misura della sua quantità di moto non può essere inferiore ad
una quantità minima, pari a h/2π
π
W. Heisenberg
(1901-1976)
Nobel 1932
∆x ⋅ ∆ (mv ) ≥
h
h = 6,626·10-34 J·s (cost. di Planck)
2π
(un modello atomico in cui l’elettrone compie orbite ben determinate intorno al nucleo
perde ogni significato scientifico)
nessun limite apprezzabile alla possibilità di misurare posizione e velocità di una particella
macroscopica (es. un pallone da calcio)
m=500 g
∆x= 10-6 m
h
6,626 ⋅10 −34 ( J ⋅ s )
∆v ≥
=
= 2,1 ⋅10 − 28 (m / s )
−6
2πm∆x 2π ⋅ 0.500(kg ) ⋅10 (m )
limiti alla possibilità di misurare posizione e velocità di una particella microscopica
melettrone=9,1·10-31 kg
∆x= 10-12 m
h
6,626 ⋅ 10 −34 ( J ⋅ s )
∆v ≥
=
= 1,16·108 (m / s )
− 31
−12
2πm∆x 2π ⋅ 9,1 ⋅ 10 (kg ) ⋅ 10 (m )
Principio di Indeterminazione di Heisemberg
È possibile conoscere con
precisione arbitraria la
posizione di una particella
È possibile conoscere
con precisione arbitraria
la sua velocità
Non è possibile conoscere simultaneamente
queste variabili con precisione qualsiasi..
h
∆x ⋅ ∆(mv ) ≥
2π
Modello atomico ondulatorio
Equazione d’onda di Schrödinger
ΗΨ = ΕΨ
Η
Ψ
Ε
operatore caratteristico del sistema atomico
E. Schrödinger
autofunzione (descrive l’elettrone dal punto di vista
ondulatorio: ψ 2(x,y,z) rappresenta la probabilità che
l’elettrone si trovi nel punto di coordinate x,y,z)
(1887-1961)
Nobel 1933
autovalore (energia dell’elettrone)
Tra le soluzioni dell’equazione di Schrödinger, le funzioni d’onda Ψ fisicamente
accettabili devono soddisfare particolari condizioni al contorno imposte dalla natura
del sistema:
1) finite, continue e ad un solo valore in tutto lo spazio
2)
tendere a zero a distanza infinita dal nucleo
3)
normalizzate
Le condizioni al contorno imposte fanno sì che ognuna delle infinite funzioni d’onda Ψ che
rappresentano le soluzioni dell’equazione d’onda, dette orbitali atomici, viene ad essere
caratterizzata da quattro numeri quantici:
n=1, 2, 3, … numero quantico principale
l=0, 1, … (n-1) numero quantico secondario
m =0, ±1, … ±l numero quantico magnetico
ms=±
±1/2 numero quantico magnetico di spin
Ψnllm
Εnllm
Modello atomico ondulatorio
Equazione d’onda di Schrödinger
ΗΨ = Ε·Ψ
Ψ
La funzione d’onda Ψ descrive un’onda stazionaria
onda stazionaria
2πr = nλ = n
h
h
⇒ mvr = n
mv
2π
h 2 ∂ 2ψ ∂ 2ψ ∂ 2ψ
− 2 ⋅ 2 + 2 + 2
8π m ∂x
∂y
∂z
+ V ⋅ψ = E ⋅ψ
Modello atomico ondulatorio
Significato fisico dei numeri quantici orbitalici
Ψnllm
n
l
Definisce lo strato e da esso dipende l’energia dell’orbitale
m
Definisce l’orientazione nello spazio degli orbitali. Orbitali
col medesimo m sono degeneri (cioè stessa energia)
Definisce il livello, e quindi la forma dell’orbitale. Da esso
dipende (in piccola misura) l’energia dell’orbitale
ms = numero quantico magnetico di spin
Modello atomico ondulatorio
Significato fisico dei numeri quantici orbitalici
Equazione di Dirac:
Descrive il
comportamento di
particelle relativistiche
P.A M. Dirac
(1902-1984)
Nobel 1933
La teoria quantistica del moto dell'elettrone lo indusse a postulare
nel 1928 l'esistenza di una particella identica all'elettrone in ogni
aspetto tranne che nella carica, avendo l'elettrone carica negativa e
questa ipotetica particella, invece, carica positiva. La teoria di Dirac
venne confermata nel 1932, quando il fisico statunitense Carl David
Anderson scoprì il positrone.
L’elettrone ha un
momento angolare
intrinseco : spin
n=1, 2, 3, …
l=0, 1, … (n-1)
m =0, ±1, … ±l
Orbitali atomici e numeri quantici
n
l m
1
0
0
Ψnlm
n
l m
1s
4
0
0
Ψnlm
y
4s
x
1s
z
2
0
0
2
1
-1
2
1
0
2
1
+1
2s
2p
4
1
-1
4
1
0
4
1
+1
4
2
-2
x
4
3
0
0
3
1
-1
3
1
0
3
1
+1
3
2
-2
3
2
-1
3
2
0
3
2
+1
3
2
+2
y
4p
3s
3p
3d
2
-1
4
2
0
4
2
+1
4
2
+2
4
4
4
4
3
3
3
3
-3
-2
-1
0
4
3
+1
4
4
3
3
+2
+3
z
2s
4d
y
2py
4f
x
2px
z
2pz
Forme degli orbitali
L’orbitale viene rappresentato
graficamente in modo tale che
nel suo volume vi sia una certa
probabilità (90%, 95% oppure
99%) di trovare l’elettrone.
Sulla superficie dell’orbitale la
probabilità di trovare
l’elettrone è costante
Il segno dell’orbitale
rappresenta il segno della
funzione d’onda Ψ.
L’orbitale 1s
La funzione ψ1s dipende solo
dal raggio r ⇒ l’orbitale 1s è
sferosimmetrico
consideriamo l’orbitale 1s come
una sfera all’interno della quale
la
probabilità
di
trovare
l’elettrone è pari al 95%
probabilità
di
trovare
l’elettrone in un guscio
sferico di volume dr a
distanza r dal nucleo ⇒
probabilità radiale 4πr2ψ2
Orbitali atomici
Energia degli orbitali atomici
E
…
…
4s
4p
4d
3s
3p
3d
2s
2p
4f
··· ··· ···
…
4p
3d
4s
3p
3s
2p
1s
2s
1s
1s < 2s = 2p < 3s = 3p = 3d <
< 4s = 4p = 4d =4f < 5s = 5p …
Livelli energetici in ordine crescente di energia
Energia dei livelli
E
Atomi polielettronici
…
Atomi idrogenoidi
1s
2s
3s
4s
5s
6s
7s
2p
3p
4p
5p
6p
7p
3d
4d
5d
6d
…
4f
5f …
6f … …
… … …
Confronto fra la teoria di Bohr e teoria ondulatoria
teoria di Bohr
teoria ondulatoria
meccanica Newtoniana
deterministica
meccanica quantistica, concetto
probabilità
e
principio
indeterminazione di Heisenberg
particella puntiforme dotata di
carica negativa
particella dotata di massa a cui è
associata un’onda
orbita: traiettoria definita
seguita dall’elettrone a cui
corrisponde un definito valore di
energia
orbitale: funzione matematica ψ che
descrive l’onda associata all’elettrone
a cui corrisponde un definito valore di
energia
raggio dell’orbita
probabilità di trovare l’elettrone in un
punto dello spazio dipende da ψ2
r0 = 0,53 Å
raggio della prima orbita
dell’atomo di idrogeno
distanza dal nucleo a cui è massima la
probabilità di trovare l’elettrone in un
elemento di volume infinitesimo
nell’atomo di idrogeno
numeri
quantici
parametri fisici
(ad es. forma dell’orbita)
valori dei coefficienti della funzione
d’onda
energia
E = -1/n2 · E0
E = -1/n2 · E0
autovalore della funzione d’onda
basi teoriche
elettrone
localizzazione
dell’elettrone
di
di
“Evoluzione” della teoria atomica
“aspettando” una nuova teoria atomica
?
Principio di esclusione di Pauli. Regola di Hund
Principio di esclusione di Pauli
In uno stesso atomo non possono esistere due elettroni caratterizzati
dalla stessa quaterna di numeri quantici n l m ms.
Se due elettroni sono descritti dal medesimo orbitale, essi devono
possedere diverso numero quantico di spin (spin opposto) ⇒ un orbitale può
contenere al massimo due elettroni
ms = +1/2
orbitale di numeri quantici n, l, m
ms = -1/2
l’attrazione fra gli opposti momenti magnetici di spin compensa la repulsione elettrostatica
Regola di Hund (principio di massima molteplicità)
Nel riempimento di orbitali degeneri (con la medesima energia), gli
elettroni ne occupano il maggior numero possibile disponendosi a spin
parallelo
orbitali di numeri quantici
n, l,
m1 m2 m3
la repulsione è minore nel caso di 2 elettroni in due orbitali con spin paralleli
Configurazione elettronica
2p
2s
1s
m=0
m = -1, 0, +1
n=1
l=0
1 elettrone
1s1
n=2
l=1
3 elettroni
2p3
4d7
n=4
l=2
7 elettroni
5f12
n=5
l=3
12 elettroni
m=0
Il principio dell’Aufbau
Aufbau = costruzione
Si possono “costruire” idealmente gli atomi di tutti gli elementi:
si parte dall’idrogeno
si procede in ordine di numero atomico crescente
si aggiunge un protone nel nucleo
si aggiunge un elettrone nell’orbitale a più bassa energia disponibile rispettando il
principio di Pauli e la regola di Hund
si sistemano sulla stessa riga gli elementi con lo stesso numero quantico
principale n (stesso livello)
gli elementi che presentano elettroni nel livello 3d vanno sistemati su una riga tra
gli elementi che riempiono l’orbitale 4s e quelli che riempiono gli orbitali 4p
gli elementi che presentano elettroni nei livelli 4d, 5d e 6d vanno sistemati su altre
tre righe in corrispondenza degli elementi che presentano elettroni nel livello 3d
gli elementi che riempiono gli orbitali 4f e 5f vanno sistemati su due righe a parte
Il principio dell’Aufbau
1s
2s
3s
4s
5s
6s
7s
1
H
1s1
4
Li
2s1
11
Na
3s1
19
K
4s1
Be
2s2
12
Mg
3s2
20
Ca
4s2
21
Sc
22
23
Ti
24
V
Cr
25
Mn
2
3d
4d
5d
6d
…
26
Fe
He
1s2
4f
5f …
6f … …
… … …
27
Co
28
Ni
5
6
B
7
C
8
N
9
O
10
F
Ne
2s22p1 2s22p2 2s22p3 2s22p4 2s22p5 2s22p6
13
Al
14
Si
15
P
16
S
17
Cl
18
Ar
3s23p1 3s23p2 3s23p3 3s23p4 3s23p5 3s23p6
29
Cu
30
Zn
31
Ga
32
Ge
33
As
34
Se
35
Br
36
Kr
3d14s2 3d24s2 3d34s2 3d54s1 3d54s2 3d64s2 3d74s2 3d84s2 3d104s1 3d104s2 4s24p1 4s24p2 4s24p3 4s24p4 4s24p5 4s24p6
E
…
3
2p
3p
4p
5p
6p
7p
…
4p
3d
4s
3p
3s
2p
2s
1s
Il principio dell’Aufbau: la tavola periodica
1s
2s
3s
4s
5s
6s
7s
1
H
1s1
3
4
Li
2s1
11
Na
3s1
19
K
4s1
37
Rb
5s1
55
Cs
6s1
87
Fr
7s1
58
Ce
Be
2s2
12
Mg
3s2
20
21
Ca
4s2
38
22
Sc
Ti
23
24
V
2p
3p
4p
5p
6p
7p
25
Cr
3d
4d
5d
6d
…
26
Mn
2
He
1s2
4f
5f …
6f … …
… … …
27
Fe
Co
28
Ni
5
6
B
7
C
8
N
9
O
10
F
Ne
2s22p1
2s22p2
2s22p3
2s22p4
2s22p5
2s22p6
13
14
15
16
17
18
Al
Si
P
S
Cl
Ar
3s23p1 3s23p2 3s23p3 3s23p4 3s23p5 3s23p6
29
30
Cu
31
Zn
Ga
32
Ge
33
34
As
35
Se
36
Br
Kr
3d14s2 3d24s2 3d34s2 3d54s1 3d54s2 3d64s2 3d74s2 3d84s2 3d104s1 3d104s2 4s24p1 4s24p2 4s24p3 4s24p4 4s24p5 4s24p6
39
Sr
40
Y
Zr
41
42
Nb
43
Mo
44
Tc
45
Ru
Rh
46
Pd
47
48
Ag
49
Cd
In
50
Sn
51
52
Sb
53
Te
54
I
Xe
5s2 4d15s2 4d25s2 4d45s1 4d55s1 4d55s2 4d75s1 4d85s1 4d105s04d105s1 4d105s2 5s25p1 5s25p2 5s25p3 5s25p4 5s25p5 5s25p6
56
57
Ba
72
La
Hf
73
74
Ta
75
W
76
Re
77
Os
Ir
78
Pt
79
80
Au
81
Hg
Tl
82
Pb
83
84
Bi
85
Po
86
At
Rn
6s2 5d16s2 5d26s2 5d36s2 5d46s2 5d56s2 5d66s2 5d76s2 5d96s1 5d106s15d106s2 6s26p1 6s26p2 6s26p3 6s26p4 6s26p5 6s26p6
88
89
RA
7s2
Ac
6d17s2
59
Pr
60
Nd
61
Pm
62
Sm
63
Eu
64
Gd
65
Tb
66
Dy
67
Ho
68
Er
69
Tm
70
Yb
71
Lu
4f15d16s2 4f25d16s2 4f35d16s2 4f45d16s2 4f55d16s2 4f65d16s2 4f75d16s2 4f85d16s2 4f95d16s2 4f105d16s2 4f115d16s2 4f125d16s2 4f135d16s2 4f145d16s2
90
Th
91
Pa
92
U
93
Np
6d27s2 5f25d17s2 5f35d17s2 5f45d17s2
94
Pu
5f67s2
95
Am
5f77s2
96
Cm
97
Bk
98
Cf
5f76d17s2 5f86d17s2 5f107s2
99
Es
5f117s2
100
Fm
5f127s2
101
Md
5f137s2
102
No
103
Lw
5f147s2 5f146d17s2
La tabella periodica degli elementi
blocco s
nsX
1
2
blocco d
(n-1)dXns2
3
4
5
6
7
8
blocco p
ns2npX
9
10 11 12
13 14 15 16 17
18
IIIA IVA VA VIA VIIA
0
Gruppo
Periodo
IA IIA
1
H
2
Li Be
IIIB IVB VB VIB VIB
VIIIB
IB IIB
He
B
3 Na Mg
C
N O
Al Si P
F
Ne
S Cl
Ar
K Ca
Sc Ti V Cr Mn Fe Co Ni Cu Zn
Ga Ge As Se Br
Kr
5 Rb Sr
Y Zr Nb Mo Tc Ru Rh Pd Ag Cd
In Sn Sb Te I
Xe
6
Cs Ba
La Hf Ta W Re Os Ir Pt Au Hg
Tl Pb Bi Po At
Rn
7
Fr Ra
Ac
4
Gruppo degli alogeni
Gruppo dei calcogeni
Gruppo dei metalli
alcalini
Gruppo dei metalli
alcalino-terrosi
Gruppo dell’azoto
6
Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu
7
Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr
Gas nobili
blocco f
(n-2)fX(n-1)d1s2
Elementi tipici
Metalli di transizione
Elementi di transizione interna
Gruppo del carbonio
Gruppo degli el. terrosi
Serie dei lantanidi
(terre rare)
Serie degli attinidi
La Tavola periodica degli elementi,storicamente, nasce nel
1869::
1869
Nel 1869 il chimico Mendeleev (russo)
trovò che ordinando gli elementi in ordine
di peso atomico e disponendoli in file
orizzontali una sopra l'altra, gli elementi
di ogni colonna avevano proprietà simili.
Mendeleev, Dmitri Ivanovitch
1834 - 1907
Tale disposizione tabulare degli elementi è nota come tavola periodica
Proprietà periodiche degli elementi
Raggio atomico
raggio atomico ⇒ si ricava dalla distanza fra
due atomi adiacenti nella molecola dell’elemento
r
Il raggio atomico
diminuisce lungo un
periodo e aumenta
lungo un gruppo.
Effetto dello schermo
degli elettroni interni
Effetto dell’azione attrattiva della carica nucleare
Proprietà periodiche degli elementi
Raggio ionico
raggio ionico ⇒ si ricava dallo ione (positivo o negativo)
formato dall’atomo cedendo o acquistando elettroni
r (Na+) < r (Na) ⇒ maggiore carica nucleare positiva, aumenta
l’attrazione esercitata dai protoni
r (O2-) > r (O) ⇒ maggiore carica negativa, aumenta la
repulsione tra gli elettroni
Proprietà periodiche degli elementi
Raggio ionico
Raggi ionici
Sono riferiti alla regione sferica attorno al nucleo dello ione entro la quale è più
probabile trovare l'elettrone. La definizione è in qualche modo arbitraria come per i
raggi atomici (es. distanze tra i nuclei dei cristalli, diffrazione ai raggi X).
Un catione è più piccolo del corrispettivo atomo neutro perché ha perso gli
elettroni di valenza o parte di essi. Rcatione < Ratomo
Al contrario un anione è più grande del
corrispettivo atomo neutro perché ha
acquistato degli elettroni. Ranione > Ratomo
Proprietà periodiche degli elementi
Raggio ionico
In breve sui raggi ionici potremmo dire che:
Proprietà periodiche degli elementi
Energia di ionizzazione. Affinità elettronica.
EI
AE
EI
AE
Energia ionizzazione (E.I.):
Affinità elettronica (A.E.):
Energia
necessaria
ad
allontanare una mole di elettroni
da una mole di atomi gassosi
con la formazione di una mole di
ioni positivi gassosi
energia rilasciata da una mole di
atomi gassosi quando acquista
una mole di elettroni dando luogo
alla formazione di una mole di
ioni negativi gassosi
A(g) → A+(g) + e-
A(g) + e- → A -(g)
È l’energia di prima ionizzazione.
L’energia di una successiva
ionizzazione è sempre maggiore di
quella della ionizzazione precedente.
Energia di (prima) ionizzazione in funzione del numero atomico Z
L’energia di
ionizzazione
aumenta lungo un
periodo e
diminuisce lungo
un gruppo.
Affinità elettronica in funzione del numero atomico Z
L’affinità elettronica
aumenta lungo un
periodo e diminuisce
lungo un gruppo
N
Primi tre periodi
Proprietà periodiche degli elementi
Energia di ionizzazione e Affinità elettronica: Metalli e non metalli
E.I.
A.E.
E.I.
A.E.
METALLI: elementi con bassa E.I. e bassa A.E.
Perdono facilmente un elettrone
NON METALLI: elementi con alta E.I. e alta A.E.
Acquistano facilmente un elettrone
Proprietà periodiche degli elementi
Elettronegatività
Elettronegatività
Elettronegatività
È la tendenza di un atomo ad
attrarre gli elettroni di
legame
Numero di ossidazione
È la carica che resta su un
atomo quando si assegnano
all’atomo più elettronegativo i
doppietti di legame.
Sarà affrontato nelle prossime lezioni.….
lezioni….
Altre proprietà periodiche:
caratteristiche acide e basiche degli ossidi degli elementi
Saranno affrontate nelle prossime lezioni.….
Elettronegatività,
χ
è la misura dell’abilità di un atomo, in una
molecola, ad attrarre gli elettroni verso di
esso.
Concetto proposto (1932) da
Linus Pauling
L'elettronegatività è un concetto molto utile
ed importante in chimica, in quanto consente
di fare diverse considerazioni sulla struttura,
le proprietà e la reattività delle molecole.
Linus Carl Pauling (1901-1994)
(Chimico statunitense)
Nobel per la Chimica 1954
Nobel per la Pace
1962
Non confondere l’elettronegatività con
l’affinità per l’elettrone che è un dato
relativo all’atomo isolato.
Pauling fu il primo ad applicare la meccanica
quantistica per determinare la struttura delle
molecole e la natura dei legami.
Elettronegatività, χ (Scala di Pauling)
Per poter disporre di valori di elettronegatività confrontabili per diversi atomi,
si è stabilito, per convenzione, di considerare come valore di elettronegatività
di un atomo quello che tale atomo assume nel legame con l’atomo di idrogeno.
aumenta
diminuisce
MINIMO
MASSIMO
RIFERIMENTO
L'elettronegatività è, quindi, una proprietà periodica
degli elementi, proporzionale all'affinità elettronica
e all’energia di ionizzazione. Essa tende a diminuire
all'interno di un gruppo procedendo dall'alto in
basso, e all'interno di un periodo procedendo da
destra a sinistra.
Chimica
(A.A. 2011/2012, 6 CFU)
• Il legame chimico. Tipi di legame e proprietà generali.
• Il legame ionico (cenni).
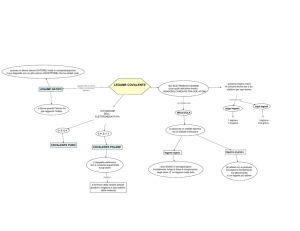
• Il legame covalente. Teoria del legame di valenza
(Ibridazione. Formule di struttura e rappresentazioni
di Lewis. Formule di risonanza. Il principio di elettroneutralità)
• Esercitazione alla lavagna (NO SLIDE)
Il legame chimico
I gas nobili:
• sono specie monoatomiche
• sono particolarmente stabili
• non formano composti
• hanno alta E.I. e A.E.
Gli orbitali s e p dell’ultimo livello sono completamente occupati con 8 elettroni*
ottetto completo sull’ultimo livello ⇔ configurazione stabile
tendenza degli atomi a raggiungere l’ottetto ⇒ formazione del legame chimico
*Ad eccezione dell’elio che completa lo strato esterno con due elettroni.
Il legame chimico
“Fra due atomi si forma un legame chimico quando le forze
agenti fra di essi danno luogo ad un aggregato abbastanza
stabile da essere rivelato”. (Linus Pauling, premio Nobel)
I legami tra atomi nascono per interazione tra gli elettroni
dell’ultimo strato (elettroni di valenza) e si suddividono in tre
tipi in funzione della natura di tale interazione.
Gli elettroni di valenza sono quelli legati
meno fortemente, quindi con un contenuto
di energia più alto, più facilmente
allontanabili dall’atomo.
Il legame chimico
Tipi di legame e proprietà generali
I legami tra atomi nascono per interazione tra gli elettroni dell’ultimo
strato (elettroni di valenza) e si suddividono in tre tipi in funzione
della natura di tale interazione.
LEGAME IONICO
Dovuto all’attrazione
elettrostatica fra ioni
che si formano per
acquisto o cessione di
elettroni tra due o più
atomi.
CsF
F2
LEGAME COVALENTE
Dovuto
a
coppie
di
elettroni condivise tra due
o più atomi.
Cs
LEGAME METALLICO
Coinvolge tutti gli elettroni dello strato di valenza degli atomi, che formano
strutture solide a temperatura ambiente (eccetto Hg).
Non è possibile fare una distinzione netta fra i tipi di legame poiché le
proprietà degli elementi variano gradualmente lungo la tavola periodica.
Il legame ionico
E’ un legame di natura elettrostatica. Si instaura fra elementi dei primi gruppi (m.
alcalini) caratterizzati da bassa energia di ionizzazione ed elementi degli ultimi gruppi
(alogeni) caratterizzati da alta affinità elettronica.
Gli elementi si trovano nel composto come ioni positivi (cationi) e negativi (anioni).
Ma…
…la più piccola energia di ionizzazione (Cs = 375,7 kJ/mol) è maggiore della più grande
affinità elettronica (F = 327 kJ/mol) ⇔ l’energia liberata nella formazione dell’anione
non è sufficiente a togliere un elettrone all’atomo che deve formare il catione.
E allora?
Vi sono altri fattori energetici in gioco.
ENERGIA RETICOLARE: energia guadagnata
nella formazione di una struttura costituita da un
gran numero di cationi e anioni.
RETICOLO CRISTALLINO: struttura simmetrica
e ordinata nello spazio in cui si alternano cationi
e anioni. Struttura rigida.
Proprietà fisiche di composti ionici:
Solidi cristallini
Elevata Tf
Isolanti allo stato solido
Buona conducibilità elettrica allo stato fuso o in soluzione
Il legame ionico
numero di coordinazione:
• numero di ioni che circondano uno ione centrale con carica opposta
• dipende dai raggi di catione e anione, in particolare dal rapporto
rcatione/ranione
• deve tener conto della stechiometria del composto
NaCl
n° coord. Na = 6
n° coord. Cl = 6
CaCl2
n° coord. Ca = 6
n° coord. Cl = 3
Esistono anche composti ionici formati da ioni poliatomici:
NaNO3
NH4Cl
Il legame covalente
Il legame covalente si instaura fra elementi aventi piccola (o nulla)
differenza di elettronegatività e spiega l’esistenza delle molecole e
delle macromolecole.
Responsabili della formazione del legame sono coppie di elettroni
condivise da due nuclei che si trovano nella zona dello spazio compresa
tra i nuclei stessi.
−
+
+
Il legame covalente
Si instaura fra elementi dei gruppi centrali che hanno valori di E.I. e
A.E. troppo bassi per poter formare ioni e quindi legami ionici.
Si instaura fra atomi di elementi diversi o uguali (H2, O2, HCl, H2O, …).
Gli elettroni interessati alla formazione del legame non vengono ceduti o
acquistati, ma condivisi. Questi elettroni sono localizzati* nella zona fra
i nuclei degli atomi coinvolti nel legame.
Legame σ: gli elettroni di legame si trovano lungo la congiungente i nuclei.
Legame π: gli elettroni di legame si trovano fuori dalla congiungente i nuclei. Il legame π
è meno forte del legame σ.
*La
probabilità di trovare gli elettroni di legame è massima nello spazio compreso fra i
due nuclei.
Grafico distanza-energia
Forze attrattive: nucleo-elettroni.
Forze repulsive: nucleo-nucleo e
elettrone-elettrone.
Distanza di legame: distanza a cui l’energia del sistema è minima.
Energia di legame: energia che si sviluppa quando si forma il legame = energia
necessaria a rompere il legame = energia di dissociazione.
Il legame covalente
Teoria del legame di valenza
La teoria del legame di valenza descrive la formazione del
legame con la sovrapposizione degli orbitali atomici dello
strato più esterno (orbitali di valenza) che “ospitano” gli
elettroni partecipanti al legame.
bisogna sovrapporre orbitali atomici con lo stesso segno contenenti ciascuno 1
elettrone
gli elettroni si dispongono con spin antiparallelo formando un doppietto di legame
eventuali altre coppie di elettroni che non intervengono nel legame rimangono
intorno al proprio atomo = doppietti solitari
se un atomo dispone di un doppietto solitario e l’altro di un orbitale vuoto, si ottiene
un legame dativo
“Formule” di Lewis:
Rappresentazioni (Notazioni) di Lewis:
Gilbert N. Lewis (1875-1946)
si rappresentano gli elettroni di valenza
chimico statunitense
un singolo elettrone viene rappresentato con un punto
un doppietto di legame viene rappresentato con un trattino che congiunge i due
atomi
un doppietto solitario su un atomo viene rappresentato con un trattino (oppure con
un punto per ciascun elettrone)
_
O:
:
C:
H: 1s
H.
O: 2s2 2p4
Ca: 3s2
Ca :
_
C: 2s2 2p2
_
:
: Cl .
Cl: 3s2 3p5
Il legame covalente
Teoria del legame di valenza: H2
E
Atomo H: 1s
1s
repulsione
Molecola H2
0
1s
r0
r
1s
E0
_
+
attrazione
+
_
Forze attrattive: nucleo-elettroni.
Forze repulsive: nucleo-nucleo e elettrone-elettrone
H H
notazione di Lewis
Legame semplice
Il legame semplice è sempre di tipo σ
Ha simmetria cilindrica intorno all’asse congiungente i nuclei
Cl: 3s2 3p5
N.B.: dopo la formazione del legame ciascun atomo raggiunge l’ottetto
Legame doppio
Il legame doppio è costituito da un legame σ e da un legame π.
Il legame doppio è più forte di un legame semplice.
Occorrono due
sull’ossigeno
elettroni
per
completare
l’ottetto
Legame triplo
Il legame triplo è costituito da un legame σ e da due legami π.
Il legame triplo è più forte di un legame semplice o doppio.
Occorrono tre elettroni per
completare l’ottetto sull’azoto
Legame covalente polare. Molecole biatomiche eteronucleari
Legame covalente polare. Molecole biatomiche eteronucleari
La differenza di elettronegatività tra i due atomi determina una distribuzione
non simmetrica di densità elettronica:
⇒ gli elettroni sono attratti maggiormente verso l’elemento più elettronegativo
⇒ nella molecola il baricentro delle cariche negative non coincide più con quello delle
cariche positive
⇒ la molecola è polare e possiede un momento di dipolo
µ=q·d
q = carica
d = distanza di legame
⇒ il legame si definisce covalente polare
dipolo = sistema di due cariche
elettriche puntiformi q uguali e di
segno opposto, poste a distanza d.
Il valore del momento di dipolo determina la % di carattere ionico di un legame
⇒ momento di dipolo alto = % carattere ionico maggiore
Legame covalente polare. Molecole biatomiche eteronucleari.
Momento di dipolo
Gli elettroni non si trovano più al centro fra i due atomi, ma sono
spostati più verso l’atomo a maggiore elettronegatività su cui si forma
una parziale carica negativa (δ–). L’altro atomo acquisisce una
parziale carica positiva (δ+).
Elettronegatività e Legame covalente polare
L’elettronegatività è la tendenza di un atomo ad attrarre gli elettroni di legame.
Il grado di polarità del legame è correlato con la
differenza di elettronegatività dei due atomi
impegnati nel legame.
Dalla differenza di elettronegatività dei due atomi
impegnati in un legame è possibile risalire alla % di
carattere ionico del legame.
Elettronegatività e Legame covalente polare
Tanto maggiore è la differenza
di elettronegatività fra due
atomi, tanto più è polarizzato il
legame che li unisce.
Il legame covalente
Teoria dell’ibridazione
y
Atomo C: (He) 2s22p2
2py
2s
2p
x
2s
Atomo H: 1s
1s
Molecola CH2
H
C
H
“NON ESISTE!”
ovvero esiste se stabilizzato con ZnI2
1s
2px
z
2pz
Il legame covalente
Teoria dell’ibridazione
L’efficacia di un legame è proporzionale alla entità di
sovrapposizione degli orbitali di valenza
La stabilità di una molecola è legata alla minimizzazione
delle repulsioni tra i doppietti elettronici (teoria VSEPR)
IBRIDAZIONE rimescolamento di orbitali che permette
IBRIDAZIONE:
all’atomo di formare legami più efficaci attraverso:
• una più estesa sovrapposizione di orbitali
• un’ottimale minimizzazione delle repulsioni fra i doppietti
Il legame covalente
Teoria dell’ibridazione (o ibridizzazione)
IBRIDAZIONE
operazione matematica sulle funzioni d’onda orbitaliche
combinazione lineare di funzioni d’onda opportune* di un atomo; il
peso** di ciascuna funzione d’onda è indicato dal suo coefficiente
consente di ottenere un numero di nuovi orbitali pari a quello di
partenza
i nuovi orbitali sono detti orbitali ibridi
gli orbitali ibridi sono isoenergetici (cioè stessa energia). La somma
delle energie degli orbitali atomici è uguale alla somma delle energie dei
nuovi orbitali ibridi
gli elettroni si ridistribuiscono negli orbitali ibridi in base alla regola di
Pauli e al principio di Hund
*quelle relative ad orbitali esterni con contenuto di energia simile
**contributo della funzione d’onda alla descrizione della molecola
Il legame covalente
Teoria del legame di valenza: CH4
y
C: (He) 2s22p2
C*: (He) 2s12p3
Ibridazione sp3
2s
2p
x
2p
2s
sp3
z
Atomo H: 1s
1s
1s
H
H
H
Molecola CH4
C
H
H
Un angolo di legame
di 109,5°
L’angolo di legame ideale in un tetraedro
Quando una molecola ha la forma di un poligono o di un poliedro regolari, i suoi
angoli di legame (ideali) sono definiti in modo inequivocabile.
Le molecole tetraedriche come ad esempio il metano (CH4),
hanno angoli di 109,5° (figura accanto). Il valore di 109,5° si
ricava dall'espressione 2 arcosen (2/3 ) deducibile dalla
figura di sotto applicando il teorema di Pitagora e la
definizione di seno:
109,5°
Si prenda un cubo di lato unitario si iscriva
in esso un tetraedro ……….
2
2
α
sen = 2 =
3
3
2
2
⇒
α
2
= arcosen
2
3
α = 2 arcosen (2/3 ) = 109° 28' = 109,47° ≅ 109,5°
L’ibridazione sp3 (tetraedrica)
Ψsp3 = c1Ψ2s+ c2Ψ2px + c3 Ψ2py+ c4 Ψ2pz
L’ibridazione sp3 deriva dal mescolamento, e
successiva equipartizione dell’energia, di un
orbitale s e di 3 orbitali p dello stesso
atomo; i quattro orbitali ibridi formano fra
loro angoli di 109,5°e sono perciò diretti
verso i vertici di un tetraedro di cui il nucleo
dell’atomo occupa il centro.
L’ibridazione sp2 (trigonale planare)
Ψsp2 = c1Ψ2s+ c2Ψ2px + c3Ψ2py
L’ibridazione sp2 deriva dal mescolamento, e
successiva equipartizione dell’energia, di un
orbitale s e di 2 orbitali p dello stesso
atomo; i tre orbitali ibridi formano fra loro
angoli di 120° e sono perciò diretti verso i
vertici di un triangolo equilatero di cui il
nucleo dell’atomo occupa il centro.
L’ibridazione sp2 (trigonale planare)
I tre orbitali ibridi che si
ottengono, equivalenti tra loro
(e tre volte degeneri), sono
disposti nel piano dei due p
usati per l’ibridazione e
diretti ai vertici di un
triangolo equilatero, formando
tra loro, quindi, angoli di 120°
L’orbitale atomico puro p
non utilizzato
nell’ibridazione, che è
perpendicolare al piano dei
due che sono stati
mescolati con l’orbitale s,
conserva questa
perpendicolarità e forma
con ciascuno dei tre ibridi
un angolo di 90°.
L’ibridazione sp (lineare)
Ψsp = c1Ψ2s+ c2Ψ2px
L’ibridazione sp deriva dal mescolamento, e
successiva equipartizione dell’energia, di un
orbitale s e di un orbitale p dello stesso
atomo; i due orbitali ibridi formano fra loro
angoli di 180° e sono perciò allineati in
posizione simmetrica rispetto al nucleo
dell’atomo.
L’ibridazione sp (lineare)
I due orbitali ibridi che si
ottengono, equivalenti tra
loro e, ovviamente, due
volte
degeneri,
sono
disposti
lungo
l’asse
dell’orbitale p usato e
formano tra loro
un angolo di 180°
I due orbitali atomici
puri p, perpendicolari a
quello utilizzato
nell’ibridazione,
conservano questa
perpendicolarità e
formano con i due ibridi
angoli di 90°.
L’ibridazione sp3d e sp3d2
sp3d
sp3d2
Bipiramidale trigonale
ottaedrica
Oltre alle ibridazioni sp3d e sp3d2 esistono anche le ibridazioni:
sp2d ⇒ quadrato planare
sd3 ⇒ tetraedrica (con orbitali d)
dsp3⇒ piramidale a base quadrata
Formule di struttura
[AXxYy]z
A
atomo centrale
X
qualsiasi atomo (o gruppo) monovalente (H, F, Cl, Br, I...)
x numero di atomi di tipo X
Y
qualsiasi atomo (o gruppo) bivalente (O, S...)
y numero di atomi di tipo Y
z eventuale carica ionica presa con il suo segno
N+x−z
dd =
2
N = gli elettroni di valenza della atomo centrale A
dd = doppietti direzionati (o NUMERO STERICO)
Il numero di doppietti direzionati indica il tipo di ibridazione
Formule di struttura
N+x−z
dd =
2
Numero di doppietti direzionati
N = gli elettroni di valenza della atomo centrale A
Ibridazione dell’atomo centrale
dd = 2
sp lineare
dd = 3
sp2 trigonale planare
dd = 4
sp3 tetraedrica
dd = 5
sp3d bipiramidale-trigonale
dd = 6
sp3d2 ottaedrica
Formule di struttura
Doppietti direzionati
Teoria VSEPR
(teoria della repulsione delle
coppie
elettroniche
di
valenza)
Si considerano doppietti direzionati i doppietti di
legame σ e i doppietti solitari intorno all’atomo
centrale.
I doppietti direzionati si dispongono in maniera tale
che sia minima la repulsione fra di essi.
Il numero di doppietti direzionati sull’atomo centrale indica il tipo di ibridazione e la
struttura dello scheletro della molecola.
Per determinare la geometria della molecola bisogna considerare l’atomo centrale.
Quando sono presenti doppietti solitari sull’atomo centrale la geometria si ottiene
considerando i doppietti di legame σ.
H
H
C
H
N
H
O
H
H
H
H
H
Metano CH4 : 4dσ
σ
dσ
σ = doppietti di legame σ
Ammoniaca NH3 : 3dσ
σ + 1ds
ds = doppietti di solitari
Acqua H2O : 2dσ
σ + 2ds
Formule di struttura: calcolo dei doppietti
Consideriamo un atomo A avente N elettroni di valenza circondato dagli atomi o gruppi X e Y
X = atomo (o gruppo) monovalente X·
forma solo un legame σ
Y = atomo (o gruppo) bivalente Y:
forma un legame σ e un legame π
z = carica (positiva, negativa, nulla)
[AXxYy]z
doppietti di legame σ di A
doppietti solitari di A
doppietti direzionati di A
doppietti totali
dσ = x + y
N − x − 2y − z
2
N+x−z
dd = ds + dσ =
2
ds =
dt =
(n° elettroni di valenza totali di A, X, Y) − (carica z)
2
Vediamo un po’ in dettaglio il modello VSEPR :
L'acronimo VSEPR abbrevia l'espressione inglese Valence Shell Electron Pair
Repulsion, cioè repulsione delle coppie elettroniche nel guscio (nello strato) di valenza;
tale repulsione CONSENTE DI FARE IPOTESI SULLA GEOMETRIA FINALE DELLA
MOLECOLA.
I principi fondamentali della teoria VSEPR sono:
la disposizione degli atomi in una molecola dipende dal numero totale di
coppie elettroniche di valenza che circondano l’atomo centrale;
le coppie elettroniche, avendo uguale segno, si respingono e si collocano
alla maggiore distanza possibile le une dalle altre.
doppietto solitario (ds)
doppietto solitario (ds)
>
doppietto di legame (dσ
σ)
doppietto solitario (ds)
doppietto di legame (dσ
σ)
>
doppietto di legame (dσ
σ)
Se non vi sono doppietti solitari la geometria della molecola coincide
con quella dello scheletro (cioè è uguale a quella derivante della
distribuzione elettronica ≡ ibridazione).
Se vi sono doppietti solitari la geometria della molecola si può
prevedere mediante il modello VSEPR:
La tabella del modello VSEPR :
Doppietti
direzionati
(dd)
Idridazione
(distribuione elettronica
≡ scheletro )
dσ
σ
ds
Geometria
molecolare
2
sp, lineare
2
0
Lineare
CO2, BeCl2,
HCN
3
sp2, trigonale planare
3
0
Trigonale planare
BH3, BF3,
BCl3, SO3,
NO3-,AlCl3
3
sp2, trigonale planare
2
1
Piegata
(Angolare)
SO2, O3,
SnCl2, NOCl
4
sp3, tetraedrica
4
0
tetraedrica
CH4,
NH4+,SiCl4,
BF4-
Ad esempio:
La tabella del modello VSEPR :
Doppietti
direzionati
(dd)
Idridazione
(distribuione elettronica
≡ scheletro )
dσ
σ
ds
Geometria
molecolare
4
sp3, tetraedrica
3
1
Trigonale piramidale
NH3, PH3,
AsH3,
PCl3,H3O+
4
sp3, tetraedrica
2
2
Piegata
(Angolare)
H2O, H2S,
SCl2,ClO2-
5
sp3d, Bipiramidale
trigonale
5
0
Bipiramidale trigonale
Ad esempio:
PCl5, PF5,
SiF5–, SOF4
IO2F3
La tabella del modello VSEPR :
Doppietti
direzionati
(dd)
Idridazione
(distribuione elettronica
≡ scheletro )
dσ
σ
ds
Geometria
molecolare
5
sp3d, Bipiramidale
trigonale
4
1
Ad altalena o sella o
tetraedro distorto
5
sp3d, Bipiramidale
trigonale
3
2
Forma a T
5
sp3d, Bipiramidale
trigonale
2
3
Lineare
Ad esempio:
SF4, BrF4+
IF4+
ClF3
ICl2-, I3-
La tabella del modello VSEPR :
Doppietti
direzionati
(dd)
Idridazione
(distribuione elettronica
≡ scheletro )
dσ
σ
ds
Geometria
molecolare
6
sp3d2,
ottaedrica
6
0
Ottaedrica
6
sp3d2,
ottaedrica
5
1
Piramidale quadrata
6
sp3d2,
ottaedrica
4
2
Planare quadrata
Si potrebbe continuare ……..
Ad esempio:
SF6, AlF63–,
SiF62–, PF6–,
IF6+
BrF5
ICl4-, IF4-
Formule di struttura:
Principio di elettroneutralità di Pauling
“una molecola è tanto più stabile quanto minore
è la separazione di carica”
Per abbassare la separazione di carica è
possibile scrivere delle formule di struttura in
cui le posizioni dei nuclei rimangono immutate, e
varia la distribuzione degli elettroni.
Formule di struttura:
risonanza (o mesomeria)
Le formule di struttura in cui le posizioni dei nuclei
rimangono immutate, e varia la distribuzione degli
elettroni si dicono:
“formule di risonanza”
la molecola è descritta come l’insieme (ibrido) di
tutte le possibili formule di risonanza e la sua
energia è minore dell’energia di ciascuna possibile
formula di risonanza.
CALCOLO DEI DOPPIETTI e CARICA FORMALE
In conclusione avendo la specie chimica (molecola, catione o anione poliatomico)
di formula generale:
[AXxYy]z
1. individuare l’atomo centrale A a cui sono legati gli altri atomi;
2. definire lo scheletro della molecola o ione individuando (calcolando)
l’ibridazione di A e definire la struttura dello scheletro della molecola.
3. costruire i legami σ tra A e gli altri atomi;
4. individuare la presenza di doppietti solitari su A (ipotizzare la geometria)
5. Calcolare i doppietti totali, sottrarre quelli già assegnati e completare la
configurazione di tutti gli atomi sistemando i restanti doppietti. Fare
attenzione a rispettare la regola dell’ottetto per il 2° periodo; fanno
eccezione: l’idrogeno ⇒ può formare solo un legame (max. 2 elettroni); gli
elementi di transizione ⇒ possono avere fino a 18 elettroni nei livelli (n1)d ns np; gli elementi dal 3° periodo in poi ⇒ hanno a disposizione il livello
d (si dice che espandono l’ottetto).
6. Per ogni atomo della specie chimica deve essere calcolare la carica
formale:
carica
= (elettroni di valenza) - (elettroni dei doppietti solitari) - (n° di legami σ o π )
formale
7. Scrivere le formule di risonanza più rappresentative (cioè con maggior
peso) tenendo conto della regola dell’ottetto.
Dal libro di testo (Nobile-Mastrorilli)
rispondere agli esercizi N. 1, 2, 3 e 4
pag. 181-182.
Chimica
(A.A. 2010/2011, 6CFU)
•Numero di ossidazione
•Nomenclatura IUPAC e classica
NUMERO DI OSSIDAZIONE (n.o.):
“Numero positivo o negativo che viene attribuito a un elemento
in un composto dopo che gli elettroni che lo legano agli atomi
che lo coordinano sono stati assegnati agli elementi più
elettronegativi”.
Il valore del numero di ossidazione di un elemento in un composto si
ottiene dalla formula di struttura sommando algebricamente:
1) Il numero di elettroni che l’atomo considerato mette in comune con gli
atomi più elettronegativi, preso col segno positivo.
2) Le cariche formali presenti sull’elemento considerato, prese con il
proprio segno.
3) Il numero di elettroni messi in comune con atomi meno
elettronegativi, preso con il segno negativo.
4) Non si tiene conto degli elettroni messi a comune fra atomi uguali.
X n.o.
Ricordiamo che….
Elettronegatività, χ (Scala di Pauling)
aumenta
diminuisce
MINIMO
RIFERIMENTO
MASSIMO
Numero di ossidazione (n.o.):
esempio dell’acido solforico
O
O
etc..
O
S
O
O
O
H
H
O
O
H
S
n.o. di S = +6
perché mette a comune 6
elettroni con un atomo più
elettronegativo (l’ossigeno)
H
n.o. di S = +6
perché mette a comune 5
elettroni con un atomo più
elettronegativo (l’ossigeno)
inoltre va aggiunta la carica
formale +1, quindi(5+1)= +6
PURCHÈ LA FORMULA DI STRUTTURA SIA CORRETTA QUALUNQUE
FORMULA DI RISONANZA SCELTA CI DÀ SEMPRE LO STESSO NUMERO
DI OSSIDAZIONE PER L’ATOMO PRESO IN ESAME (NELL’ESEMPIO LO
ZOLFO).
_
_
H
N
O
_
O
_
O_
_
_
N
_
O_
O
_
O
_
_
H
_
Altri esempi:
_
O
H
_
C
O
_
C
_
_
_
O
H
_
O
_
_
O
_
_
_
C
O
O
_
O
_
_
H
_
O
_
_
_
_
L’azoto nell’acido nitrico ha un n.o. pari a +5
perché mette a comune 4 elettroni con un atomo più elettronegativo
(l’ossigeno) inoltre va aggiunta la carica formale (+1), quindi (4+1) = +5
Il carbonio nell’anione bicarbonato ha n.o. pari a +4
Tuttavia non è necessario conoscere tutte le formule di struttura per
calcolare il numero di ossidazione…………..
È anche possibile ricavare il numero di ossidazione di un elemento
dalla formula molecolare, facendo ricorso alle seguenti otto regole:
a)
Allo stato elementare (non combinato):
1) Il numero di ossidazione di qualunque elemento è zero (N2, O2, P4, S8…)
b)
Nei composti:
2) Il n.o. dell’idrogeno è +1, eccetto che negli idruri metallici, nei quali è –1;
3) Il n.o. dei metalli alcalini è sempre +1;
4) Il n.o. dei metalli alcalino terrosi, dello zinco (Zn) e del cadmio (Cd) è sempre +2;
5) Il n.o. del boro (B) e dell’alluminio (Al), i primi due elementi del terzo gruppo, è
sempre +3;
6) Il n.o. dell’ossigeno è –2, eccetto che nei perossidi nei quali è –1 (ad esempio H2O2
perossido di idrogeno), e nel composto OF2 in cui è +2; il n.o. dello zolfo (S) è –2
nei solfuri (S2-) e –2/n nei polisolfuri (Sn2-) ;
7) Il n.o. del fluoro (F) è sempre –1. Questo stato di ossidazione può essere
assegnato anche agli altri alogeni quando essi sono in composti non ossigenati; nei
composti privi di ossigeno ma con più di un alogeno sarà assegnato stato di
ossidazione –1 a quello scritto per ultimo (più elettronegativo);
8) La somma dei n.o. di tutti gli elementi in un composto neutro deve essere zero,
mentre in uno ione poliatomico deve essere uguale alla sua carica.
Esercizio
HCl
H = +1
Cl = -1
CaH2
Ca = +2 H = -1
NaBr
Na = +1 Br = -1
AlF3
F = -1
Al = +3
K2O
K = +1
O = -2
Na2S2
Na = +1 S = -2/2 = -1 disolfuro
SO2
O = -2
S = +4
H3PO2
H = +1
O = -2
PO43-
O = -2
P = -[(-2)·4 + 3] = +5
Ca3(PO4)2
Ca = +2 O = -2
P = +5
LiIO4
Li = +1
I = -[(-2)·4 + 1] = +7
BrCl3
Cl = -1 più elettronegativo
PF6-
F = -1
P = +5
H2O2
H = +1
O = -1 c’è un legame O-O
O = -2
P = -[(-2)·2 + 3] = +1
Br = +3
Studiare l’esercizio a pag. 163 del libro di testo
Esercizio. Calcolare il numero di ossidazione delle seguenti specie chimiche:
… svolgere l’esercizio n. 5 a pag. 183 del libro di testo
NOMENCLATURA
formula minima
“indica, con numeri interi più piccoli possibili, i rapporti
con cui gli atomi si legano tra loro in un composto”
formula molecolare
“indica l’esatto numero di atomi che si legano tra loro
in un composto”
formula di struttura
“indica le posizioni steriche relative degli atomi che si
legano tra loro in un composto”
NOMENCLATURA RAZIONALE (IUPAC)
NOMENCLATURA
NOMENCLATURA D’USO ( O CORRENTE)
La nomenclatura chimica moderna utilizza le regole redatte* sin dal 1970
dall’Unione Internazionale di Chimica Pura e Applicata (IUPAC) che
prescindono dalle conoscenze delle proprietà degli elementi e sono, perciò,
facilmente acquisibili anche dai non addetti ai lavori.
* Periodicamente seguono degli aggiornamenti
REGOLE IUPAC
nomenclatura sistematica
I nternational
U nion of
P ure and
A pplied
C hemistry
Unione
Internazionale
di
Chimica Pura e Applicata
(IUPAC)
presso tale organismo sono permanentemente insediate due
commissioni incaricate di redigere le regole di nomenclatura
rispettivamente per la Chimica inorganica e per la Chimica organica.
CARATTERISTICHE
DELLA NOMENCLATURA IUPAC
È un sistema nel quale ogni composto ha un suo nome.
Seguendo le regole, chiunque assegna il medesimo
nome a un dato composto.
Viceversa, dato il nome di un composto, ognuno è
in grado di scrivere (disegnare) il composto.
FORMULA
(STRUTTURA)
IUPAC
NOME
NOMENCLATURA
ELEMENTI POLIATOMICI
SIMBOLO
NOME IUPAC
NOME CORRENTE
O
(mono)ossigeno
ossigeno monoatomico
O2
diossigeno
ossigeno
O3
triossigeno
ozono
F2
difluoro
fluoro
P4
tetrafosforo
fosforo bianco
S8
ottazolfo
zolfo-λ
NOMENCLATURA
Un’altra premessa è l’uso della radice dei nomi degli elementi da usare nella formula dei
relativi composti.
Tale radice si ricava generalmente togliendo la “o” finale, o la “io” finale oppure, per
terminazioni differenti, lasciando il nome dell’elemento tal quale. Per esempio:
Elemento
Radice
Si usa ad
esempio in:
Ferro
ferr-
Ossido ferroso
Iodio
iod-
Iodato, ioduro
Rame
rame-
Ossido rameico
Le più importanti eccezioni a queste regole sono:
Elemento
Radice
Esempio
Azoto
Nitr-
Nitrito, Nitrato
Zolfo
Solfor-, solf-
Acido solforico, solfato
Fosforo
Fosfor-, fosf
Acido fosforico, fosfato
Arsenico
Arseni-, arsen-
Arseniato, acido arsenico
Manganese
Mangan-
Ossido manganoso
Stagno
Stann-
Idrato stannoso
Oro
Aur-
Cloruro Aurico
Premessa: COMPOSTI BINARI
AmB n
Un composto binario è un composto formato da due soli elementi.
I composti binari, costituiti cioè solo da due elementi, si scrivono
indicando a sinistra l’elemento che precede l’altro nella serie:
M
B
III A
Si C
IVA
Sb As P N
VA
H
Te Se S
VIA
At I Br Cl
O
F
VIIA
L’ordine è quello dei gruppi dal III A al VII A e dal basso verso l’alto
con le eccezioni di H e O. Con il simbolo generico M si indica un
qualunque metallo.
I composti binari fra un metallo e un non-metallo sono solitamente
ionici. Sono invece molecolari i composti binari formati fra due nonmetalli. L’elemento che compare per primo nella sopraindicata serie
è scritto per primo nella formula e secondo nel nome.
NOMENCLATURA
COMPOSTI BINARI
AmB n
I composti binari si scrivono indicando a sinistra l’elemento che precede nella serie:
M, B, Si, C, Sb, As, P, N, H, Te, Se, S, At, I, Br, Cl, O, F
Dove M è un qualunque metallo.
•
Secondo la nomenclatura IUPAC:
pref-B-uro-di pref-A
Esempi: NaCl, GaAs, PbI2, FeCl3, Hg2Cl2, OF2, PI3, Fe2S3, PH3, NH3, AsH3.
•
Secondo la nomenclatura d’uso (classica):
B-uro A-suff
Dove –suff rappresenta un suffisso che dipende dalle proprietà dell’elemento A e dal suo
stato di ossidazione nel composto.
Se A è un elemento a stato di ossidazione fisso, si usa il suffisso –ico. Alternativamente si
può usare la dizione B-uro di A, che indica univocamente un composto di ben determinata
stechiometria.
Esempi: NaCl, K3P, Na2S, ZnI2, CdCl2.
Se A è un elemento che esibisce due stati di ossidazione, la nomenclatura classica attribuisce
ai suoi composti binari il suffisso
-ico quando A è nel suo alto stato di ossidazione
-oso quando A è nel suo basso stato di ossidazione
Esempi:FeI2, FeBr3, Hg2Cl2, HgCl2, CuS, Cu2S, SnCl2, SnCl4.
NOMENCLATURA
Caso di due stati di ossidazione
-ico -oso
Altri esempi,COMPOSTI BINARI AmBn
IUPAC: pref-B-uro di pref-A
•
•
•
•
•
NaCl: cloruro di sodio
FeCl2: dicloruro di ferro
FeCl3 : tricloruro di ferro
As2S3: trisolfuro di diarsenico
Hg2Cl2: dicloruro di dimercurio
Altri esempi, COMPOSTI BINARI AmBn
TRADIZIONALE (CLASSICA):
B-uro di A (se A ha un solo numero di ossidazione)
B-uro A-oso (riferito al numero di ossidazione più basso di A)
B-uro A-ico (riferito al numero di ossidazione più alto di A)
•NaCl
cloruro di sodio
•CaBr2
bromuro di calcio
•FeCl2
cloruro ferroso
•FeCl3
cloruro ferrico
•Cu2S
solfuro rameoso
•CuS
solfuro rameico
•Hg2Cl2
cloruro mercuroso (calomelano)
•HgCl2
cloruro mercurico
NOMENCLATURA
COMPOSTI BINARI DELL’IDROGENO:
La nomenclatura classica
Calcogenuri d’idrogeno
Alogenuri d’idrogeno
HnX
acido X-idrico
ove X elemento VI e VII gruppo
Esempi: H2S, H2Se, HF, HCl, HBr, HI
Idruri:
AHn
ove X elemento dei restanti gruppi
Esempi: CaH2, CH4, SiH4, AsH3, PH3, NH3
Detti anche idracidi
per distinguerli
dagli ossiacidi
Nomenclatura tradizionale: IDRACIDI
Per il momento definiamo acido (secondo Arrhenius) un composto che
produce ioni H+ ed un anione quando viene sciolto in acqua:
Ad esempio
HCl
in acqua dà H+ e Cl-
Gli alogeni e lo zolfo formano (nei loro n.o. negativi) acidi binari con
l’H. Si indicano col suffisso –IDRICO (essi fanno comunque parte di una
classe più vasta, detta dei composti binari, il cui nome sistematico
IUPAC si ottiene con le regole viste prima)
HF
HCl
H2S
HBr
HI
HCN
acido
acido
acido
acido
acido
acido
fluoridrico (fluoruro di idrogeno)
cloridrico (cloruro di idrogeno)
solfidrico (solfuro di diidrogeno)
bromidrico (bromuro di idrogeno)
iodidrico (ioduro di idrogeno)
cianidrico (cianuro di idrogeno)
Premessa, COMPOSTI BINARI DELL’OSSIGENO:
Sia i metalli che i non metalli formano, nei loro numeri di ossidazione
positivi, composti binari con l’ossigeno
COMPOSTI
BINARI
DELL’OSSIGENO
XmOn
METALLO
+
OSSIGENO
Nomenclatura
tradizionale:OSSIDO
BASICO (OSSIDO)
NON METALLO
+
OSSIGENO
Nomenclatura
tradizionale:OSSIDO
ACIDO (ANIDRIDE)
La nomenclatura IUPAC non fa distinzione tra ossido basico e ossido acido.
NOMENCLATURA
COMPOSTI BINARI DELL’OSSIGENO:
Nomenclatura IUPAC
I composti binari dell’ossigeno sono tutti del tipo
XmOn
Pref-ossido di pref-X
Unica eccezione OF2 (difluoruro di ossigeno)
Esempi: Li2O, Na2O, Na2O2, CaO, Al2O3
Al2O3
triossido di dialluminio
È necessario specificare il prefisso mono- quando esistono diversi ossidi
dello stesso elemento.
(ad esempio: FeO, Fe2O3, SnO, SnO2, CO, CO2)
NOMENCLATURA
COMPOSTI BINARI DELL’OSSIGENO
XmOn
Nomenclatura classica (corrente)
La nomenclatura classica divide gli ossidi in base al loro carattere acido, basico o anfotero:
XmOn con carattere acido
Anidridi
XmOn con carattere basico o anfotero
Ossidi
Se X può esibire solo due stati di ossidazione si tiene conto della stechiometria mediante l’uso del suffisso
suffisso -ico
(alto)
suffisso -oso
(basso)
Quattro stati di ossidazione combinazione di prefissi e suffissi, partendo dal suffisso che indica lo stato di
ossidazione massimo
Esempi:Cl2O, Cl2O3, Cl2O5, Cl2O7
per—ico
-ico
-oso
ipo--oso
(massimo)
(minimo)
Premessa, PRODOTTI DI IDRATAZIONE DI OSSIDI BASICI:
IDROSSIDI (BASI)
Per il momento definiamo base (secondo Arrhenius) un composto che
produce ioni OH- ed un catione metallico quando viene sciolto in acqua:
Ad esempio
NaOH
in acqua dà Na+ e OH-
Gli idrossidi (le basi) derivano formalmente dalla reazione di ossidi basici (ossidi
metallici) con acqua (idratazione):
K2O + H2O → 2 KOH
Sono costituiti dallo ione METALLICO positivo Mn+ e da n IONI OSSIDRILI
OH-.
ossidi basici
MO
Idratazione
idrossidi
M(OH)
NOMENCLATURA
Prodotti di idratazione di ossidi basici: IDROSSIDI
M(OH)n
Nomenclatura IUPAC
Pref-idrossido di M
Esempi: NaOH, Ca(OH)2, Fe(OH)2, Fe(OH)3
La NOMENCLATURA CLASSICA utilizza, come per i composti binari, i suffissi –ico, –oso
Esempi: Fe(OH)2, Fe(OH)3, CuOH, Cu(OH)2
Confronto:
Tralasciando gli acidi di origine organica, gli acidi inorganici si dividono
in due categorie:
ACIDI
IDRACIDI
OSSOACIDI
ANIDRIDI
I prodotti di idratazione degli ossidi acidi (delle anidridi)
NOMENCLATURA
Prodotti di idratazione di ossidi acidi: OSSOACIDI
H j XkO l
dove X= metallo in alto stato di ossidazione oppure un non metallo
Nomenclatura IUPAC: È piuttosto elaborata e il termine “acido” è ammesso solo
per specie chimiche in soluzione.
Esempi:l’acido solforico H2SO4 dovremmo chiamarlo tetraossosolfato di
diidrogeno oppure solfato(VI) di diidrogeno mentre l’acido nitrico (HNO3)
diventa triossonitrato di idrogeno oppure nitrato (V) di idrogeno.
Tuttavia, la tradizione di individuare come acidi anche le specie pure e così
radicata tra i chimici, che la IUPAC considera tali denominazioni ancora
accettabili. Noi, quindi, useremo soltanto la nomenclatura classica.
Nomenclatura classica
Nella costruzione del nome dell’acido bisogna tener conto del numero di
ossidazione di X, di quante volte X è contenuto nella formula, del grado di
idratazione dell’acido e della presenza di eventuali gruppi perossidici (O-O).
NOMENCLATURA:
OSSOACIDI
H j XkO l
Per specificare lo stato dell’elemento X
• suffisso –ico se X forma un solo ossoacido
• suffissi -oso –ico se X forma due ossoacidi
• se X forma quattro ossoacidi usare combinazione di prefissi e suffissi:
per—ico
-ico
-oso
ipo--oso
(massimo)
(minimo)
Per specificare il grado di idratazione usare il prefisso:
ortometa-
(più alto stato di idratazione)
(più basso stato di idratazione)
Per specificare il numero di atomi X usare il prefisso:
mono-(generalmente si omette), di-, tri-, tetra-, penta-, ecc.
NOMENCLATURA:
OSSOACIDI
H j XkO l
Tutti gli acidi contrassegnati con un asterisco (*) non sono stabili, ma il loro
nome serve nella nomenclatura dei loro sali.
Nomenclatura: acidi ossigenati o ossoacidi HjXkOl
HClO
HClO2
HClO3
HClO4
(+1)
(+3)
(+5)
(+7)
acido
acido
acido
acido
ipocloroso
cloroso
clorico
perclorico
SO2 + H2O → H2SO3
SO3 + H2O → H2SO4
H2SO5
H2S2O8
H2S2O7
H2S2O3
H2SxO6
N2O3 + H2O → 2 HNO2 (+3)
N2O5 + H2O → 2 HNO3 (+5)
acido nitroso
acido nitrico
HBO2
H3BO3
H2CrO4
H2Cr2O7
H2MnO4
HMnO4
(+4)
(+6)
(+6)
(+6)
(+6)
(+2)
(+10/x)
acido
acido
acido
acido
acido
acido
acido
acido
acido
acido
acido
acido
acido
metaborico
(orto)borico
cromico
dicromico
manganico
permanganico
solforoso
solforico
perossomonosolforico
perossodisolforico
disolforico
tiosolforico
x-tionico
Nomenclatura: acidi ossigenati o ossoacidi HjXkOl
acido ipofosforoso
H
H
_
_
O
P
O
_
_
H
_
_
H3PO2 (+1)
O
H3PO3 (+3)
_
_O
P
_
_ H
O
acido fosforoso
H
_
_
O
H
H
_
O
_
P
_
acido (orto)fosforico
O
_
P2O5 + 3 H2O → 2 H3PO4 (+5)
H
_
_
O
_
P
O_
P2O5 + 1 H2O → 2 HPO3
(+5)
acido metafosforico
_
_O
H
H3PO5 (+5)
P2O5 + 2 H2O → H4P2O7
(+5)
acido perossofosforico
acido difosforico o pirofosforico
_
_O
H
Nomenclatura: cationi
Prefissi
cationi metallici [A]n+:
ione A
ione A-ico
⇒ A ha un unico n°di ox
ione A-ico
ione A-oso
⇒ A ha alto n°ox
⇒ A ha basso n°ox
cationi formati da H+ (idrogenione) con elementi dei gr. VA VIA VIIA:
ione A-onio
ione rameoso o ione rame(I) Cu+
ione rameico o ione rame (II) Cu2+
ione sodio Na+
ammonio NH4+
fosfonio PH4+
solfonio H3S+
iodonio H2I+
ossonio H3O+
Prefissi
Nomenclatura: anioni
anioni di elementi degli ultimi gruppi [X]n-:
ione X-uro
anioni derivanti dai corrispondenti ossoacidi [XOm]n-:
acido per-X-ico
acido X-ico
acido X-oso
acido ipo-X-oso
⇒ ione per-X-ato
⇒ ione
X-ato
⇒ ione
X-ito
⇒ ione ipo-X-ito
⇒ X ha
⇒ X ha
⇒ X ha
⇒ X ha
massimo n° ox
alto n° ox; X ha unico n° di ox
basso n° ox
minimo n° ox
NOMENCLATURA
I
SALI
I sali derivano formalmente dalla sostituzione di uno o più atomi d’idrogeno di un
acido con atomi di metallo o con cationi poliatomici; oppure derivano dalla
sostituzione di uno o più gruppi OH di un idrossido con anioni ottenuti da acidi
per eliminazione di tutti gli atomi d’idrogeno (protoni acidi)
I sali in altri termini derivano dalla combinazione di uno o più cationi (mono o
poliatomici) con uno o più anioni (mono o poliatomici)
CATIONI POLIATOMICI
I più comuni cationi poliatomici derivano dall’addizione di un protone su un
composto binario dell’idrogeno con un elemento del VA,VIA,VIIA. Il nome di tali
cationi si ottiene aggiungendo il suffisso –onio alla radice del nome dell’elemento
ESEMPI: NH4+, PH4+, H3S+, H2I+ .
NOMENCLATURA
I
SALI SEMPLICI
I sali semplici sono prodotti dalla sostituzione di tutti gli idrogeni acidi di una
molecola. Il nome dei sali semplici si ottiene dal nome dell’acido da cui il sale
formalmente deriva, sostituendo i suffissi che caratterizzavano l’acido, come di
seguito indicato:
ACIDO
per--ico
-ico
-oso
ipo--oso
SALE
per--ato
-ato
-ito
ipo--ito
(massimo)
(minimo)
A tale termine segue la specificazione del catione (mono o poliatomico) che ha
sostituito gli atomi di idrogeno ( preceduti eventualmente da prefissi che ne indichino
il numero).
Il nome completo del sale tiene conto anche del grado d’idratazione dell’acido
utilizzando i prefissi orto-(omittibile) o meta- (necessario)
ESEMPI: NaNO2, Ca(NO3)2, (PH4)2S2O7, KMnO4
NOMENCLATURA: I
SALI SEMPLICI
NOMENCLATURA
I SALI ACIDI
I sali acidi si ottengono per parziale sostituzione di alcuni atomi d’idrogeno da un acido poliprotico.
Secondo la NOMENCLATURA IUPAC è necessario utilizzare la seguente dicitura:
Pref-idrogeno-anione di catione
La NOMENCLATURA CLASSICA fa invece seguire al nome dell’ANIONE l’aggettivo
Anione pref-acido di catione
Dove il pref- indica il numero di atomi d’idrogeno acidi ancora presenti nell’anione del sale, oppure si
riferisce al numero di atomi di idrogeno sostituiti, indicandoli con l’aggettivo:
Anione pref-basico di catione
dove il pref- indica il numero di atomi di idrogeno acidi sostituiti nel sale.
Per l’unico sale acido di un acido diprotico MHXOy, la nomenclatura classica può usare anche il nome:
bi-anione di catione
ESEMPI: NaHCO3, NH4HSO4, NaH2PO3, NaH2PO4, Li2HPO4, Ca(H2PO4)2.
NOMENCLATURA: I SALI ACIDI
Nomenclatura: sali acidi
_
_
O
H
H
P
_
_ H
O
H3PO2 → H2PO2-
Ipofosfito
H3PO3 → H2PO3-
idrogenofosfito
_
_
O
P
_
_O
O
HPO32-
H
_
_
H
H
fosfito
_
_
O
O
_
_O
H
_
_
P
H3PO4 → H2PO4-
H
diidrogenofosfato
HPO42-
idrogenofosfato
PO43-
fosfato
_
_
O
P
_
H
_
O
_
O_
_
_O
H
HPO3 →
PO3-
metafosfato
NOMENCLATURA
I COMPLESSI ( O COMPOSTI DI COORDINAZIONE)
[MLn]z
Ove z è l’eventuale carica (essi possono essere neutri , cationici o anionici)
L è un singolo atomo o un gruppi di atomi (molecola) ed è detto Legante (esso può essere neutro o
anionico)
n è il numero di coordinazione
Prefissi per i leganti:
se anionici cambiare il suffisso –uro –ico con –o
Se neutri non cambiano nome. ECCEZIONI: H2O, NH3, CO, NO
Esempi di complessi cationici o neutri: [Cu(NH3)4]2+, Ni(CO)4, [Cu(H2O)6]2+
Pref-L-atomo centrale (n.o. in cifre romane)
Esempi di complessi anionici:
Pref-L-atomo centrale-ato (n.o. in cifre romane)
NOMENCLATURA: I COMPLESSI [MLn]z
Leganti
Acidi organici (da conoscere)
• Acido acetico: CH3COOH
• Acido formico: HCOOH
• Acido ossalico: H2C2O4
• acido benzoico: C6H5COOH
Sali (per esempio del sodio)
• Acetato di sodio: CH3COONa
• Formiato di sodio: HCOONa
• Ossalato acido di sodio: NaHC2O4
• Ossalato di sodio: Na2C2O4
• Benzoato di sodio: C6H5COONa
Basi organiche (Azotate)
NOMENCLATURA : UN UTILE SCHEMA PER IL NOSTRO CORSO
Elementi
Metallo
Non-Metallo
+ Ossigeno
+ Ossigeno
Ipo---oso
---oso
Ossido Basico----
---oso
Ossido Acido o Anidride----
---ico
+ Acqua
---ico
Per---ico
+ Acqua
Ipo---oso
---oso
Acido (Ossoacido)----
Idrossido
---ico
Per---ico
Binario (---uro)
Sale----
Ipo---ito
---ito
Ternario
---ato
Per---ato
Esercizio
Esercizi
Dal libro di testo (Nobile-Mastrorilli)
rispondere agli esercizi N. 1, 2, 3 e 4
pag. 197-198.
Chimica
(A.A. 2011/2012, 6CFU)
• Legame covelente secondo la Teoria dell’orbitale
molecolare. LCAO.
(Molecole biatomiche omonucleari: H2 , F2 ,O2)
• Il legame metallico.
(Conduttori, isolanti e semiconduttori elettrici. Drogaggio)
• Forze di legame intermolecolari
(Forze di van der Waals. Forze di London.
Legame idrogeno. Interazioni tra ioni e dipoli)
Il legame covalente
Teoria dell’orbitale molecolare: M.O.
Nella teoria M.O. si applica lo studio ondulatorio al sistema costituito da tutti i nuclei e tutti gli
elettroni. Alla descrizione delle molecole concorrono, in principio, TUTTI GLI ELETTRONI e non
solo quelli di valenza spaiati.
ΗΨ = ΕΨ
Η
Ψ
Ε
operatore caratteristico del sistema molecolare
autofunzione molecolare (descrive il moto dell’elettrone
nella molecola: ψ 2 dV rappresenta la probabilità che
l’elettrone si trovi nell’infinitesimo elemento di volume
dV intorno al punto di coordinate x,y,z)
autovalore molecolare (enenrgia dell’elettrone
nella molecola)
Tra le soluzioni dell’equazione di Schrödinger, le funzioni d’onda Ψ fisicamente accettabili devono
soddisfare particolari condizioni al contorno imposte dalla natura del sistema:
1)
2)
3)
finite, continue e ad un solo valore in tutto lo spazio
tendere a zero a distanza infinita dai nuclei
normalizzate
Le funzioni d’onda molecolari ψ , descrivono gli elettroni che risentono della presenza di più
nuclei (elettroni di sistemi molecolari) e sono dette orbitali molecolari.
L’equazione di Schrödinger applicata ai sistemi polinucleari non è risolvibile direttamente: le funzioni
d’onda molecolari si ricavano, nell’approssimazione più semplice della teoria, mediante il metodo della
combinazione lineare degli orbitali atomici (LCAO).
Il legame covalente
Teoria dell’orbitale molecolare. Metodo LCAO
Regole di combinazione degli orbitali atomici
1
si possono combinare solo orbitali atomici che posseggono energie non
troppo diverse tra loro
2
le superfici di inviluppo degli orbitali atomici devono sovrapporsi il più
possibile (criterio della massima sovrapposizione)
3
si possono combinare orbitali atomici che posseggono la stessa simmetria
rispetto all’asse di legame
Il legame covalente
Teoria dell’orbitale molecolare. Metodo LCAO
orbitali di tipo σs
orbitali di tipo σp
Il pedice indica il
tipo di OA da cui
derivano
orbitali di tipo πp
Molecola di H2
• Ciascun atomo di H presenta un unico orbitale atomico 1s.
• Gli orbitali atomici di partenza hanno uguale energia e uguale
simmetria, quindi è possibile applicare il metodo LCAO.
• Dalla combinazione dei due orbitali atomici 1s relativi ai due atomi
otterremo due orbitali molecolari di tipo σ.
• Un o.m. è di legame, l’altro è di antilegame.
orbitali atomici 1s
orbitali molecolari σs
Molecola di H2
Dopo aver ottenuto gli orbitali molecolari, possiamo costruire il diagramma
energetico o di correlazione per la molecola H2.
Nel diagramma sono indicati gli orbitali atomici di partenza e gli orbitali
molecolari ottenuti.
Gli o.m. vanno riempiti con tutti gli elettroni della molecola, rispettando il
principio di Pauli e la regola di Hund.
diagramma di correlazione per la molecola di H2
Molecola di H2
La configurazione elettronica della molecola H2 viene ricavata in analogia alle
configurazioni elettroniche degli elementi. Si indica per ciascun orbitale
molecolare il numero di elettroni in esso contenuti.
H2: (σ
σ1s)2
Dalla configurazione elettronica si calcola l’ordine di legame:
ordine di legame =
(n° el. negli orb. di legame) − (n° el. negli orb. di antilegame )
2
Per la molecola H2 l’ordine di legame è 1.
Ordine di legame Una specie chimica esiste se gli elettroni che occupano
orbitali leganti sono in numero maggiore degli elettroni
che occupano orbitali antileganti
OL =
n° e- leganti – n°e- antileganti
2
σ∗1s
1s
σ∗1s
1s
He2
σ∗1s
+
1s
OL = 1/2
H2−
1s
σ1s
OL = 1/2
1s
σ1s
σ∗1s
H2+
1s
σ1s
1s
OL = 0 la specie non esiste
OL = 1/2
He2
1s
σ1s
OL = 0
Il legame covalente
LCAO. Molecole biatomiche omonucleari tra atomi del II periodo
_
F2
σ∗2px
π∗2pv π∗2pz
F
E
y
2px 2py 2pz
F
_
+
2pz 2py 2px
y
_
x
+
+ _
π2pv π2pz
_
σ2px
σ∗2s
+
_
z
2s
x
_
_
+
2s
+
+
z
y
_
+
_
x
z
+
_
+
y
x
z
+
σ2s
[1s21s2 (σ
σ2s)2 (σ∗
σ∗2s)
σ2px)2(π
π2py2pz)4 (π∗
π∗2p
π∗2p
σ∗ 2 (σ
π∗ y)2 (π∗
π∗ z)2]
ordine di legame: 1
y
1s
1s
1s
1s
y
+
z
x
orbitali atomici
z
orbitali molecolari
orbitali atomici
x
+
Il legame covalente
LCAO. Molecole biatomiche omonucleari tra atomi del II periodo
_
O2
σ∗2px
π∗2pv π∗2pz
O
E
y
2px 2py 2pz
O
_
+
2pz 2py 2px
y
_
x
+
+ _
π2pv π2pz
_
σ2px
σ∗2s
+
_
z
2s
x
_
_
+
2s
+
+
z
y
_
+
_
x
z
+
_
+
y
z
x
+
σ2s
[1s21s2 (σσ2s)2 (σ∗
σ∗2s)
σ2px)2(π
π2py2pz)4 (π∗
π∗2p
π∗2p
σ∗ 2 (σ
π∗ y)1 (π∗
π∗ z)1]
ordine di legame: 2
y
z
1s
1s
1s
x
orbitali atomici
1s
y
+
z
orbitali molecolari
orbitali atomici
x
+
Diamagnetismo e paramagnetismo
F2
O2
σ2px*
σ2px*
π2py*
π2pz*
π2py*
π2pz*
π2py
π2pz
π2py
π2pz
σ2px
σ2px
σ2s*
σ2s*
σ2s
σ2s
orbitali di non legame
1s
1s
orbitali di non legame
1s
1s
Gli esperimenti mostrano che l’ossigeno (O2) è paramagnetico
La molecola dell’ossigeno viene
attratta da un campo magnetico:
quindi è paramagnetica (ha uno o
più elettroni spaiati)
In generale per
identificare il
comportamento
paramagnetico di una
molecola (quanti elettroni
spaiati essa possiede )
si utilizza la
Bilancia di Gouy
I legami chimici
Legame ionico
Legami forti
Legami
Legame covalente
Legame metallico
Legami deboli
Sono i prossimi da studiare
Il legame metallico
Introduzione: Caratteristiche dei metalli
I metalli presentano alcune caratteristiche peculiari:
• buona conducibilità termica e elettrica;
• bassa energia di ionizzazione (facilità a perdere gli elettroni di valenza);
• opacità e potere riflettente;
• duttilità e malleabilità (non presenti nei solidi ionici);
• alto numero di coordinazione non spiegabile con la formazione di singoli legami
atomici
⇒ mobilità degli elettroni
Il legame metallico
Introduzione: Caratteristiche dei metalli
Modello di Lorentz (1905):
i metalli sono costituiti da un reticolo cristallino di cationi immersi in un mare
di elettroni liberi di muoversi (= delocalizzati) in tutto il cristallo.
⇒ nei metalli non vi sono legami direzionati
Reticolo metallico prima
e dopo la deformazione:
Reticolo ionico prima e
dopo la deformazione:
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
+
–
+
–
+
–
+
–
+
+
–
+
–
+
–
+
–
–
+
–
+
–
+
–
+
+
–
+
–
+
–
+
–
+
+
+ + + +
+ + + +
+
+
+
+
+
+
+
+
+
+
+
+
+ + + +
+ + + +
+
+
–
+
–
+
–
+
–
+
+
–
+
–
+
–
+
–
repulsione!
–
+
–
+
–
+
–
+
+
–
+
–
+
–
+
–
Il legame nei metalli è di natura diversa rispetto al legame ionico o covalente.
La teoria del legame di valenza non permette di spiegare la formazione del legame metallico. L’uso
della teoria degli orbitali molecolari invece consente di spiegare le proprietà di questi composti.
Il legame metallico
Teoria delle bande
Un cristallo metallico è costituito da un numero enorme di atomi (e quindi di elettroni).
La combinazione lineare di N orbitali atomici degli strati di valenza di un metallo porta alla
formazione di N orbitali molecolari, dove N è un numero molto grande.
All’aumentare di N la distanza tra livelli
energetici adiacenti diminuisce, quindi la
differenza di energia tra un orbitale molecolare
e l’altro diventa sempre più piccola. Si passa
quindi da un numero discreto di livelli energetici
a un “continuo” che prende il nome di banda di
energia.
N orbitali atomici
degeneri
Gli N orbitali molecolari estesi a tutto il cristallo a cui è associata la banda di
energia rendono conto della delocalizzazione degli elettroni.
Per far passare un elettrone da un livello ad un altro superiore vuoto sarà quindi
necessaria una piccola quantità di energia. Questo spiega la mobilità degli elettroni
nei metalli.
Legame metallico - La teoria delle bande
Costruzione di un reticolo metallico degli elementi del gruppo I
configurazione elettronica esterna: ns1
Li6
Li2
σ2s*
∆Etot
∆Etot
σ2s
LiN
Li22
∆Etot
σ2s* o.m. di antilegame
∆Etot
σ2s o.m. di legame
Legame metallico - La teoria delle bande
Costruzione di un reticolo metallico degli elementi del gruppo I
configurazione elettronica esterna: ns1
N elettroni
N/2 livelli energetici
occupati
N atomi di Li
N orbitali molecolari
LiN
N/2 orbitali vuoti
∆Etot
BANDA DI VALENZA
N/2 orbitali occupati
Gli elettroni possono essere
promossi
da
un
livello
energetico occupato ad uno
libero con una modesta spesa
di energia.
energia termica
conducibilità termica e elettrica
energia elettrica
Legame metallico - La teoria delle bande
Costruzione di un reticolo metallico degli elementi del gruppo II
configurazione elettronica esterna: ns2
2N elettroni
N atomi di Ca
N livelli energetici occupati
N orbitali molecolari
3N orbitali vuoti (derivanti dagli O.A. p)
zona di sovrapposizione
N orbitali occupati (derivanti dagli O.A. s)
Gli elettroni possono essere
promossi dalla banda di
valenza
alla
banda
di
conduzione con una modesta
spesa di energia.
energia termica
conducibilità termica e elettrica
energia elettrica
Legame metallico - La teoria delle bande
Costruzione di un reticolo metallico degli elementi del gruppo IV
4N elettroni
N atomi di C
conf. el. est. ns2
np2
2N livelli energetici occupati
4N orbitali molecolari
2N orbitali vuoti
2N orbitali occupati
La banda di valenza e la banda di conduzione sono separate da un gap di
energia la cui entità dipende dal tipo di elemento. Il gap diminuisce scendendo
lungo il gruppo.
Legame metallico - La teoria delle bande
Costruzione di un reticolo metallico degli elementi del gruppo IV
stagno e piombo
ISOLANTE
CONDUTTORI
SEMICONDUTTORI
La conducibilità elettrica aumenta all’aumentare della temperatura.
L’energia termica consente di superare il gap di energia per un numero
maggiore di elettroni.
Legame metallico - La teoria delle bande
Drogaggio dei semiconduttori
La conducibilità elettrica di un semiconduttore può essere aumentata
modificando la struttura del cristallo ⇒ drogaggio
Si aggiungono al cristallo (allo stato fuso o solido) piccole quantità (1
atomo su 1010) di un altro elemento (drogante) che si distribuiscono
uniformemente nel reticolo del semiconduttore.
La struttura delle bande del semiconduttore non risulta in tal modo
alterata.
Il drogante è in genere un elemento con un elettrone di valenza in
meno o in più rispetto al semiconduttore.
Legame metallico - La teoria delle bande
Drogaggio di tipo p dei semiconduttori
Consideriamo un cristallo di silicio (IV gruppo) drogato con
gallio (III gruppo) che ha un elettrone in meno.
Con la sostituzione di alcuni atomi di Si con atomi di Ga
alcuni livelli energetici nella banda di valenza del Si
risultano vuoti. I livelli vuoti si trovano all’estremità
superiore della banda di valenza, e possono essere
occupati da elettroni della banda di valenza.
Energy gap
Energy gap
Silicio
livelli energetici vuoti
Silicio drogato con gallio
Legame metallico - La teoria delle bande
Drogaggio di tipo p dei semiconduttori
Gli elettroni che si spostano sui livelli vuoti
creano delle lacune nella banda di valenza.
Tali lacune costituiscono dei livelli energetici
vuoti che possono essere occupati da altri
elettroni che si “muovono” da livelli
energetici inferiori per esempio sotto
l’azione di un campo elettrico.
livelli vuoti
Drogaggio di tipo p (positivo) ⇒
presenza di lacune di elettroni nella
banda di valenza⇒
⇒ movimento di cariche
positive ⇒ conducibilità elettrica
Legame metallico - La teoria delle bande
Drogaggio di tipo n dei semiconduttori
Consideriamo un cristallo di silicio (IV gruppo) drogato
con arsenico (VI gruppo) che ha un elettrone in più.
Con la sostituzione di alcuni atomi di Si con atomi di As
alcuni livelli energetici nella banda di conduzione del Si
vengono occupati dagli elettroni dell’As. I livelli occupati
si trovano all’estremità inferiore della banda di
conduzione.
Energy gap
livelli energetici occupati
Silicio
Energy gap
Silicio drogato con arsenico
Legame metallico - La teoria delle bande
Drogaggio di tipo n dei semiconduttori
Gli elettroni presenti sui livelli occupati possono “muoversi” verso i livelli energetici
vuoti della banda di conduzione per esempio sotto l’azione di un campo elettrico.
livelli occupati
Drogaggio di tipo n (negativo) ⇒ presenza di
elettroni nella banda di conducibilità ⇒
movimento di cariche negative ⇒ conducibilità
elettrica
Esistono semiconduttori
costituiti da composti 1:1 di
elementi di III e V gruppo,
come ad esempio GaAs.
Forze secondarie di legame
Forze di Van der Waals e Forze di London
Le forze secondarie di legame sono di tipo intermolecolare.
Esse sono essenzialmente dei legami deboli (0,01-15
kcal/mol), responsabili dell’esistenza della materia in fasi
condensate. Le principali forze secondarie di legame sono
di tipo:
Ione-Dipolo
Dipolo-Dipolo (L. idrogeno)
Forze di Van der Waals
Dipolo-Dipolo indotto
Dipolo indotto- Dipolo indotto
Forze di London
Forze di legame intermolecolari
Interazioni ione-dipolo
Interazione elettrostatica tra uno ione e una molecola dipolare
_
δ+
H
Na+
Cl-
δ-
_
Esempio: un cristallo di NaCl sciolto in acqua
NaCl(s) + H2O(l) → Na+(aq) + Cl-(aq)
O
δ+
H
Le molecole di acqua,
dipolari, vengono orientate
dal campo elettrico creato
dallo
ione.
Il
campo
elettrico è
tanto più
elevato quanto maggiore è
la carica dello ione e quanto
minore è il suo raggio.
La solubilità delle sostanze saline in acqua (o in liquidi polari in genere) è dovuta
alla solvatazione degli ioni.
Ogni ione viene circondato da un certo numero di molecole di acqua che si
orientano ⇒ ad ogni interazione ione-molecola di acqua è associata una certa
quantità di energia elettrostatica ⇒ la somma delle energie per un gran numero
di interazioni è tale da vincere l’energia reticolare ⇒ il sale si dissolve in acqua.
Forze di legame intermolecolari
Interazioni Dipolo-Dipolo
Interazione elettrostatica tra molecole dipolari (uguali o diverse).
Le molecole si orientano in modo
che la parte positiva del dipolo
di una molecola sia prossima alla
parte negativa del dipolo di
un’altra molecola.
Forze di legame intermolecolari
Legame idrogeno
Il legame idrogeno è un tipo di interazione dipolo-dipolo
particolarmente forte (fino a ~30 di kJ/mol). Si realizza quando un
atomo di idrogeno è legato ad un atomo molto elettronegativo (azoto,
ossigeno, fluoro).
HF
Forze di legame intermolecolari
Legame idrogeno
Le temperature di fusione e di ebollizione di H2O, HF, NH3 sono più alti
rispetto a quelli degli idruri omologhi a causa della formazione del legame
idrogeno. E’ necessario fornire più energia per il passaggio di stato poiché
bisogna rompere anche i legami idrogeno.
°C
Andamento delle temp. di fusione per
serie di molecole omologhe
+100
°C
H2O
+100
Andamento delle temp. di ebollizione
per serie di molecole omologhe
HF
H2O
0
0
NH3
H2Te
H2Se
NH3
HI
H2S
HF
HCl
-100
PH3
GeH4
SiH4
AsH3
CH4
SiH4
CH4
SnH4
GeH4
-200
AsH3
HCl
SbH3
PH3
H2Se
HBr
HBr
-100
H2S
-200
H2Te
SbH3
HI
SnH4
Forze di legame intermolecolari
Legame idrogeno
A causa della formazione dei legami idrogeno fra le molecole di acqua allo
stato solido, si forma una struttura “aperta” con una densità minore rispetto
all’acqua allo stato liquido.
Allo stato liquido infatti i legami idrogeno vengono continuamente rotti e
riformati fra molecole diverse a causa dei moti molecolari; allo stato solido
invece le molecole sono “ferme” e i legami idrogeno non vengono rotti.
Le straordinarie proprietà dell'acqua sono dovute alla
specificità del legame ad idrogeno:
Acqua liquida
Acqua solida
(ghiaccio)
Struttura “aperta” con una densità minore rispetto all’acqua liquida.
Legame idrogeno e DNA
Il legame ad idrogeno è alla base del codice genetico
Le basi azotate dei nucleotidi
sono legate fra loro
attraverso legami a idrogeno
In questo modo si forma la
doppia elica del DNA
Forze di legame intermolecolari
Interazioni dipolo-dipolo indotto
Interazione elettrostatica tra una molecola dipolare e un dipolo indotto
Il campo elettrico generato da molecole polari può indurre la formazione di un
dipolo in sostanze apolari facilmente polarizzabili.
Forze di legame intermolecolari
Forze di London: interazioni dipolo indotto-dipolo indotto
Le molecole apolari possono generare dei dipoli a
causa di variazioni “istantanee” di densità
elettronica attorno ai nuclei. Tali dipoli “istantanei”
creano campi elettrici che possono indurre la
formazione di dipoli nelle molecole vicine.
L’interazione è tanto maggiore quanto più
polarizzabile è la molecola.
Polarizzabilità = tendenza a “deformare” il volume, la nuvola elettronica
Le interazioni dipolo indotto-dipolo indotto
sono alla base della formazione degli stati
condensati di molecole apolari.
Nel caso degli alogeni (molecole biatomiche)
la polarizzabilità aumenta scendendo lungo
il gruppo all’aumentare del volume atomico e
quindi della nuvola elettronica.
Lo iodio è solido
a temperatura ambiente
Chimica
(A.A. 2011/2012, 6CFU)
Le reazioni chimiche (I parte):
Reazioni acido-base ovvero reazioni di non ossidoriduzione e loro
bilanciamento
Reagente limitante
Esercitazione
Esercizi: calcoli stechiometrici sulle reazioni acido-base.
La resa (il rendimento) di una reazione chimica: definizione,
esempi ed esercizi.
Le reazioni chimiche (II parte):
Introduzione alle
reazioni di ossidoriduzione (RedOx)
Esercitazione (bilanciamento
(bilanciamento RedOx
RedOx,, equivalenti chimici)
chimici)
alla lavagna (No
(No slide !)
Cos’è una reazione chimica?
Una reazione chimica è il processo mediante il
quale uno o più composti reagiscono tra loro per
produrre uno o più composti diversi da quelli di
partenza.
Lavoisier ci ricorda che la materia non si crea
né si distrugge ma si trasforma.
Una
reazione
chimica
è,
quindi,
una
trasformazione della materia.
trasformaz
ione
reagenti → prodotti
trasformaz
ione
reagenti
→ prodotti
2 HgO(s)
→ 2 Hg(l)
+ O2(g )
trasformaz
ione
reagenti
→ prodotti
Li(s)
+ H2O(l)
→ 2LiOH(aq)
+ H2(g)
Le reazioni chimiche
Lo studio delle reazioni è la parte centrale della disciplina, la chimica, che si
occupa delle trasformazioni della materia e che deve individuare quali proprietà
devono possedere due composti per poter reagire tra loro e trasformarsi in
sostanze diverse.
Ogni reazione chimica, quindi, comporta la rottura di alcuni legami e la formazione
di nuovi legami chimici, ed avviene spontaneamente se ad essa corrisponde una
diminuzione dell’energia libera (∆
∆G) delle specie di partenza. Ogni reazione è
caratterizzata da dati termodinamici che consentono di determinare se e quanto
la reazione può avvenire, e da dati cinetici che consentono di determinare la
velocità con cui essa avviene.
Più in generale, una reazione chimica è il processo mediante il quale due (o più)
composti, detti reagenti reagiscono tra loro per produrre uno (o più) composti
diversi, detti prodotti di reazione.
Indicando con A e B due reagenti e con C e D i prodotti, la generica reazione
può essere descritta dall’equazione chimica:
A + B → C + D
Le reazioni chimiche
Una reazione deve rispettare la legge della conservazione delle masse di
Lavoisier e, perciò, l’equazione che la rappresenta deve essere bilanciata;
per bilanciarla occorre dotare ciascuna specie di opportuni coefficienti,
detti stechiometrici, che rendano il numero degli atomi di ciascun elemento
presenti a sinistra uguale a quello che, dello stesso elemento, sono presenti
a destra. Indicando con a, b, c, d i coefficienti stechiometrici dei
reagenti e prodotti, l’equazione bilanciata diventa:
aA + bB → cC + dD
e indica che:
a moli di A reagiscono con b moli di B per dare c moli di C e d moli di D.
Le reazioni chimiche
Se il processo non porta al consumo di tutta la quantità di almeno uno
dei reagenti, la reazione raggiunge uno stato di equilibrio in cui sono
presenti sia A e B che C e D: in questo caso, per separarli si usa una
doppia freccia, come mostra la seguente:
aA + bB
←
→
cC + dD
La doppia freccia sta a indicare che l’equilibrio può essere raggiunto
sia ponendo a reagire A e B, che producono C e D, fino al
raggiungimento dell’equilibrio, sia facendo reagire C e D che
producono A e B. Per una reazione di questo tipo, reagenti e prodotti
sarebbero indistinguibili: si conviene, tuttavia, di indicare sempre
come reagenti i composti a sinistra della doppia freccia e come
prodotti quelli a destra.
Le reazioni chimiche
Un’equazione chimica, per essere completa, deve riportare lo stato di
ciascun reagente e prodotto indicando: un solido con (s), un liquido con
(l ), un gas o vapore con (g), un composto in soluzione, di solito acquosa,
con (aq); ciò spesso viene omesso perché si ritiene che sia noto al
lettore.
Na2CO3(s)
NaO(s) + CO2(g)
Esempi:
(NH4)2CO3(s)
NH3(g) + CO2(g) +H2O(l)
3 Ca(OH)2(aq) + 2 H3PO4(aq)
Ca3(PO4)2(s) + 6 H2O(l)
oppure, se in una reazione si forma un precipitato (un solido insolubile) si pone
il segno
a destra della relativa formula; analogamente se si sviluppa un gas si pone
il segno
, ad esempio:
+
Ag + Cl
-
Zn + 2 H+
AgCl
Zn2+ + H2
Classificazione delle reazioni
NON ESISTE UNA CLASSIFICAZIONE UNIVOCA. Spesso
si fa riferimento ad una classificazione tradizionale basata su
come vengono riordinati atomi o gruppi di atomi. Essa
comprende 5 tipi di reazione:
1) Reazioni di combinazione
Due sostanze si combinano per dare una terza sostanza
2 Na (s) + Cl2 (g)
CaO (s) + SO2 (g)
→ 2 NaCl (s)
→ CaSO3 (s)
2) Reazioni di decomposizione
Una sostanza reagisce dando due o più sostanze
2 HgO (s)
→ 2 Hg (l) + O2 (g)
3) Reazioni di spostamento
Un elemento reagisce con un composto spostando da esso
un altro elemento
Fe (s) + CuSO4 (s)
Zn (s) + 2 HCl (aq)
→ Cu(s) + FeSO4 (s)
→ H2 (g) + ZnCl2 (aq)
4) Reazioni di metatesi o doppio scambio
Comporta lo scambio di parti tra due reagenti
KI (aq) + AgNO3 (aq)
→
KNO3 (aq) + AgI (s)
5) Reazioni di combustione
Sono particolari reazioni di combinazione implicanti O2
CH4 (g) + 2O2 (g)
→
CO2 (g) + 2 H2O (g)
Un’altra classificazione è quella basata su due grandi categorie:
reazioni di ossidoriduzione e reazioni di non ossidoriduzione
Le reazioni chimiche
Le reazioni possono, quindi, dividersi in DUE GRANDI CLASSI:
a) Reazioni di ossidoriduzione;
ossidoriduzione nelle quali alcune specie atomiche variano il
numero di ossidazione. Ad esempio:
(0)
(+1)
Zn(s) + H2SO4(aq)
(+2)
(o)
ZnSO4(aq) + H2(g)
Le combustioni formalmente è come se fossero delle reazioni di ossidoriduzione:
(0)
(-1)
(+4)
(-2)
C6H6(l) + 15 O2(g)
2
6 CO2(g) + 3 H2O(g)
b) Reazioni di non ossidoriduzione; nelle quali nessuna specie atomica varia il
numero di ossidazione. In queste si ha soltanto scambio di specie atomiche
fra i reagenti. Le reazioni acido-base fanno parte di questo
raggruppamento:
3 Ca(OH)2(aq) + 2 H3PO4(aq)
Ca3(PO4)2(s) + 6 H2O(l)
Le reazioni chimiche: acidi e basi
secondo Arrhenius
La più semplice, e limitata, tra le definizioni di acido e di base è quella di
Arrhenius, per la quale una specie chimica è:
Arrhenius
• un acido se in soluzione acquosa si dissocia fornendo uno o più ioni idrogeno
(protoni); un acido è monoprotico (o monovalente o monobasico) quando fornisce
un solo ione H+ e poliprotico (o polivalente o polibasico) quando ne dà più di uno.
• una base se in soluzione acquosa si dissocia fornendo uno o più ioni idrossido
OH– (ossidrile); una base è monoossidrilica (o monovalente o monoacida) quando
fornisce un solo ione OH– e poliossidrilica (o polivalente o poliacida) quando ne
dà più di uno.
ACIDI SECONDO
ARRHENIUS: Tutte le specie chimiche che in soluzione cedono ioni H+.
BASI SECONDO
ARRHENIUS: Tutte le specie chimiche che in soluzione cedono ioni OH–.
Elettroliti forti e deboli
I sali, gli acidi e le basi si trovano dissociati in soluzione acquosa.
Per questo motivo vengono anche chiamati elettroliti.
I sali solubili si dissociano in soluzione acquosa dando luogo ai
rispettivi ioni positivi e negativi da cui sono formati. Poiché i sali
sono completamente dissociati in soluzione acquosa, essi sono
elettroliti forti.
Gli acidi e le basi possono essere elettroliti forti oppure deboli.
In una reazione si scrivono in forma indissociata gli elettroliti
deboli, le specie non solubili e i non elettroliti. Tutte le altre specie
possono anche essere scritte nella forma dissociata.
Le reazioni chimiche: acidi e basi
Il loro bilanciamento:
Bilanciare per primi gli atomi di metallo e non metallo nelle
formule (generalmente è meglio scegliere il prodotto) con il
maggior numero di atomi.
Bilanciare per ultimi gli elementi (quasi sempre idrogeno e
ossigeno) presenti in più formule.
Se si ottengono numeri frazionari, eliminarli moltiplicando tutti
i coefficienti per un opportuno fattore.
Bilanciamento
3 Ca(OH)2 + 2H3PO4→ Ca3(PO4)2 + 6 H2O
Al2O3 + 6 HClO4 → 2 Al(ClO4)3 + 3 H2O
As2S3 + 3 H2SO4 → As2(SO4)3 + 3 H2S
Esercizi sul bilanciamento delle reazioni di non ossidoriduzione
[R. 1 , 1, 3]
[R. 1, 3, 2]
[R 4, 1, 1, 6, 1]
Esercizi sul bilanciamento delle reazioni di non ossidoriduzione
Esercizi sul bilanciamento delle reazioni di non ossidoriduzione
Dal libro Nobile-Mastrorilli, per il bilanciamento delle reazioni di non
ossidoriduzione (e quindi acido-base) si svolgano solo gli esercizi n.1, 2 e 9
di pag. 252-253 e pag.255:
n.1
n.2
n.9
Non svolgere gli esercizi dal n.3 al n.8!!!
perché richiedono conoscenze che non siete ancora in grado di capire
del tutto e potrebbero, quindi, confondervi.
Prodotto con il maggior numero di atomi (13 atomi), quindi per la regola
(“Bilanciare per primi gli atomi di metallo e non metallo nelle formule con il
maggior numero di atomi”):
3
2
Bilanciare per ultimi gli elementi presenti in più formule (in questo
caso cloro, azoto,idrogeno e ossigeno).
Per il cloro deve essere:
3
2
6
2
6
Per l’azoto deve dunque essere:
3
2
L’ossigeno è già bilanciato, usiamo l’idrogeno con verifica del bilanciamento:
2x3 + 2x4x2+2= 24 idrogeni a sinistra
6x4 = 24 idrogeni a destra
La reazione è bilanciata
Il bilanciamento delle reazioni chimiche può sempre realizzarsi mediante un
metodo algebrico (ovvero un metodo prettamente matematico!).
A scanso di equivoci diciamo subito che il cosiddetto metodo algebrico di
bilanciamento è una tecnica generale, cioè applicabile a qualsiasi reazione
chimica senza bisogno di riconoscerne la tipologia, con però il grosso difetto
di trascurare completamente l'aspetto chimico delle reazioni (in particolar
modo per le reazioni di ossidoriduzione), in quanto alla soluzione si perviene
algebricamente, ossia convertendo la reazione in un sistema di equazioni in
base a due principi di conservazione:
Conservazione delle specie atomiche: il numero globale di atomi di ciascun
elemento presente nei reagenti è necessariamente uguale a quello globale
dello stesso elemento dalla parte dei prodotti. In altre parole nelle
reazioni chimiche gli atomi non si distruggono, ma si riorganizzano.
Conservazione della carica globale: la somma algebrica di tutte le cariche
lato reagenti è necessariamente uguale alla somma algebrica delle cariche
lato prodotti. Ovvero in una qualsiasi reazione chimica la carica si
conserva.
Vediamo il caso della reazione precedente:
a
b
c
d
e
La reazione non presenta carica basta applicare la conservazione delle specie
atomiche e siano a, b, c, d , e i coefficienti stechiometrici:
Conservazione di
Mn
Conservazione di
Cl
Conservazione di
N
Conservazione di
H
Conservazione di
P
Conservazione di
O
a = 3d
2a = e
b + 2c = e
3b + 9c = 4e
c = 2d
4c = 8d
a = 3d
2a = e
b + 2c = e
3b + 9c = 4e
c = 2d
Questo è un caso semplice 6 equazioni in 5 incognite, ma due equazioni sono ridondanti!
Di solito si hanno sistemi in cui l’equazioni sono più delle incognite…...oppure le incognite
sono più dell’equazioni!!! Quindi, bisogna sempre scegliere per un’incognita un valore
arbitrario di partenza!!!
Cerchiamo, per
rispetto a d
a = 3d
2a = e
b + 2c = e
3b + 9c = 4e
c = 2d
esempio,
a = 3d
2 ⋅ (3d) = e
b + 2 ⋅ (2d) = e
3b + 9c = 4e
c = 2d
a = 3d
e = 6d
b + 4d = 6d
3b + 9c = 4e
c = 2d
di
esplicitare
ogni
incognita
a = 3d
e = 6d
b + 4d = e
3b + 9c = 4e
c = 2d
a = 3d
e = 6d
b = 2d
c = 2d
a
b
c
d
e
Adesso ponendo per d un valore di 1 otterremo :
a =3
b=2
c=2
d =1
a = 3d
b = 2d
e = 6d
c = 2d
3
2
e=6
2
1
6
COME
VOLEVASI
DIMOSTRARE:
IL
METODO
ALGEBRICO
DI
BILANCIAMENTO È DAVVERO UNA TECNICA GENERALE, MA TROPPO
LABORIOSA E
CON IL GROSSO DIFETTO DI TRASCURARE
COMPLETAMENTE L'ASPETTO CHIMICO DELLE REAZIONI.
Stechiometria: dal greco
στοιχειον µετρον =
elemento misura
Calcolo dei rapporti ponderali esistenti, fra
elementi e composti,
nelle reazioni
chimiche.
La stechiometria è, quindi, il ramo della
chimica che si occupa delle relazioni
quantitative fra i reagenti e i prodotti di
una reazione.
Le reazioni chimiche: reagente limitante
Quando le quantità (moli) dei reagenti stanno tra di loro in un
rapporto uguale a quello espresso dai loro coefficienti si dice che sono
in rapporto stechiometrico: se la reazione è completamente spostata
verso destra (→), esse reagiscono completamente e nel sistema finale
sono presenti solo i prodotti (secondo i rapporti stechiometrici dei
prodotti).
Se invece le quantità sono in un rapporto diverso da quello dei
coefficienti stechiometrici, per esempio per la generica reazione:
a A+bB→cC+d D
Se uno dei due reagenti è disponibile in quantità insufficienti rispetto
al rapporto molare (stechiometrico) indicato dall’equazione chimica si
dice che è in difetto. È detto anche reagente limitante. L’altro reagente
(in eccesso) reagisce solo nella quantità permessa dal reagente in
difetto. Nel sistema finale sono presenti i prodotti della reazione e il
reagente in eccesso: per ottenere la quantità di ciascuno, il calcolo deve
essere impostato con riferimento a quello del reagente in difetto.
Esercizio (il caso più semplice):
stechiometrico tra i reagenti è 1:1
il
rapporto
3,65 g di acido cloridrico reagiscono con 11,2 g di idrossido potassico
secondo la seguente reazione:
HCl (aq) + KOH(aq) → KCl (s) + H 2O(l)
Calcolare quanti grammi di KCl vengono prodotti e dire qual è il reagente in
eccesso.
Svolgimento
Calcoliamo, innanzitutto, le moli di HCl e KOH:
n HCl
n KOH
m HCl
3,65 g
=
=
= 0,1 mol
PM HCl 36,5 (g/mol)
m KOH
11,2 g
=
=
= 0,2 mol
PM KOH 56,0 (g/mol)
HCl + KOH
→
KCl
+ H2O
Moli
iniziali
0,1
0,2
-
-
Moli
consumate
0,1
0,1
-
-
Moli
prodotte
-
-
0,1
0,1
Totale
--
0,1
0,1
0,1
I grammi di KCl prodotti sono pari a
m KCl = n KCl ⋅ PM KCl
g
= 0,1 mol ⋅ 74,5 (
) = 7,45 g
mol
il reagente in eccesso è l’idrossido di potassio e la sua entità è pari a 0,1 moli.
Esercizio (più “impegnativo”)
10 g di acido solforico reagiscono con 10 g di idrossido di alluminio secondo
la seguente reazione (da bilanciare):
H 2SO4 (aq) + Al(OH) 3(s) → Al 2 (SO4 )3(s) + H 2O(l)
Calcolare quanti grammi di Al2(SO4)3 vengono prodotti e dire qual è il
reagente in eccesso.
Svolgimento
Bilanciare, innanzitutto, la reazione
3 H 2SO 4 (aq)
+2 Al(OH)3(s) → Al2 (SO 4 ) 3(s) + 6 H 2O (l)
Calcoliamo le moli dei reagenti:
m H 2SO 4
10,0 g
n H 2SO 4 =
=
= 0,102 mol
PM H 2SO 4 98,073 (g/mol)
m Al(OH)3
10,0 g
n Al(OH)3 =
=
= 0,128 mol
PM Al(OH)3 78,003 (g/mol)
3 H2SO4
+ 2 Al(OH)3 → Al2(SO4)3
Moli
iniziali
0,102
0,128
Moli
consumate
?
?
n H 2 SO 4 : n Al(OH)3 = 3 : 2
n H 2 SO 4 =
n Al(OH)3
n Al(OH)3
-
n H 2 SO 4
+ 6 H2O
-
3
= ⋅ n Al(OH)3
2
3
⋅ 0,128 = 0,192 mol > 0,102 mol
2
2
= ⋅ n H 2SO 4
3
2
= ⋅ 0,102 mol = 0,068 mol < 0,128 mol
3
L’acido solforico è
il reagente limitante
L’idrossido di alluminio è
il reagente in eccesso
3 H2SO4
+ 2 Al(OH)3 → Al2(SO4)3
+ 6 H2O
Moli
iniziali
0,102
0,128
Moli
consumate
0,102
0,068
-
-
Moli
formate
-
-
?
?
n H 2 SO 4 : n Al 2 (SO 4 ) 3 = 3 : 1
n Al2 (SO 4 )3
1
1
= ⋅ n H 2SO 4 = ⋅ 0,102 mol = 0,034 mol
3
3
Oppure si giunge al medesimo risultato
n Al(OH)3 : n Al 2 (SO 4 ) 3 = 2 : 1
n Al2 (SO 4 )3
1
1
= ⋅ n Al(OH)3 = ⋅ 0,068 mol = 0,034 mol
2
2
3 H2SO4
+ 2 Al(OH)3 → Al2(SO4)3
+ 6 H2O
Moli
iniziali
0,102
0,128
Moli
consumate
0,102
0,068
-
-
Moli
formate
-
-
0,034
0,204
Totale
-
0,060
0,034
0,204
m Al 2 (SO 4 ) 3 = n Al 2 (SO 4 ) 3 ⋅ PM Al 2 (SO 4 ) 3
= 11,63 g
Verificate da soli la legge di Lavoisier
g
= 0,034 mol ⋅ 342,136
=
mol
ESERCIZI: calcoli stechiometrici sulle REAZIONI ACIDO-BASE
1) 10 g di acido solforico reagiscono con 10 g di idrossido ferrico
secondo la seguente reazione (da bilanciare):
H2SO4(aq)+ Fe(OH)3(s) → Fe2(SO4)3(s) + H2O(l)
Calcolare quanti grammi di Fe2(SO4)3 vengono prodotti e dire qual è il
reagente in eccesso. [Risultato 13,596 g; Fe(OH)3]
2) 100 g di acido ortofosforico reagiscono con 100 g di idrossido
stannoso secondo la seguente reazione (da bilanciare):
H3PO4(aq)+ Sn(OH)2(s) → Sn3(PO4)2(s) + H2O(l)
Calcolare quanti grammi di Sn3(PO4)2 vengono prodotti e dire qual è il
reagente in eccesso.[Risultato 119,22 g; H3PO4]
ESERCIZI: calcoli stechiometrici sulle REAZIONI ACIDO-BASE
3) 20 g di acido solfidrico reagiscono con 15 g di idrossido di alluminio
secondo la seguente reazione (da bilanciare):
H2S (aq)+ Al(OH)3(s) → Al2S3(s) + H2O(l)
Calcolare quanti grammi di Al2S3 vengono prodotti e dire qual è il
reagente in eccesso. [Risultato 14,49 g; H2S]
4) L’idrossido di bario e l’acido solforico reagiscono secondo la
seguente reazione (da bilanciare):
H2SO4(aq) + Ba(OH)2(s) → BaSO4(s) + H2O(l)
Calcolare i grammi di idrossido di bario ed i grammi di acido solforico
che bisogna far reagire per ottenere 100 g di solfato di bario. [Risultato:
42,02 g di H2SO4 e 74,41 di Ba(OH)2]
ESERCIZI: calcoli stechiometrici sulle REAZIONI ACIDO-BASE
5) L’acido nitrico e l’idrossido ferrico reagiscono secondo la seguente
reazione (da bilanciare):
HNO3(aq)+ Fe(OH)3(s) → Fe(NO3)3(s) + H2O(l)
Calcolare i grammi di idrossido ferrico ed i grammi di acido nitrico che
bisogna far reagire per ottenere 100 g di nitrato ferrico. [Risultato:
76,160 g di HNO3 e 44,186 di Fe(OH)3]
ESERCIZI: calcoli stechiometrici sulle REAZIONI ACIDO-BASE
6)
7)
8)
9)
R. 32,7 g
R. 140 g
10)
11)
Data la reazione (da bilanciare)
BaCl2 + H2SO4 → BaSO4 + HCl
calcolare quanti grammi di solfato di bario (BaSO4) si formano facendo reagire 500 g
di cloruro di bario (BaCl2) con 100 g di acido solforico (H2SO4). Calcolare inoltre
quale dei due reagenti non reagisce completamente ed in che quantità si trova al
termine della reazione.
R. 238,0g di BaSO4, 287,7g di BaCl2
La resa (il rendimento) di una reazione chimica
a A + b B → c C + d D
+ Sottoprodotti (prodotti indesiderati)
Non sempre una reazione chimica produce la quantità di prodotti
attesa sulla base delle relazioni stechiometriche.
Questo può succedere per varie ragioni:
• ci sono reazioni collaterali, vale a dire dagli stessi reagenti si
possono formare anche altri prodotti (sottoprodotti);
• non è possibile isolare tutto il prodotto dall'ambiente di reazione …..
La resa (il rendimento) di una reazione chimica
a A + b B → c C + d D
Resa teorica = resa stechiometrica = la
quantità calcolata di un prodotto in una
reazione chimica;
Resa sperimentale (reale) = la quantità di un
prodotto ottenuto in pratica dalla reazione;
Resa percentuale (η) =
(resa sperimentale/resa teorica)•100
La resa (il rendimento) di una reazione chimica
Data la generica reazione chimica:
a A + b B → c C + d D
si definisce, ad esempio, resa percentuale della reazione chimica in termini di
prodotto C rispetto al reagente A l’espressione:
n C,f
η = ∗ ⋅100
nC
nC,f = numero di moli di C che si sono effettivamente formate alla fine della
reazione.
n*C = numero di moli di C che si formerebbero se tutto il reagente A si
trasformasse completamente.
oppure
mC,f
η = ∗ ⋅100
mC
mC,f = massa di C che si è effettivamente formata alla fine della reazione.
m*C = massa di C che si formerebbe se tutto il reagente A si trasformasse
completamente.
Esempio. Calcolare la resa della reazione:
CaCO3 → CaO + CO 2
sapendo che da 300 g di CaCO3 si sono ottenuti
effettivamente 135 g di CaO.
Svolgimento
n CaCO3 =
n CaO
m CaCO3
PM CaCO3
=
300 g
= 3,0 mol ≡ n *CaO (moli teoriche)
100 (g/mol)
m CaO
135 g
=
=
= 2,41 mol ≡ n CaO, f (moli effettive)
PM CaO 56,0 (g/mol)
n CaO, f
2,41
η = ∗ ⋅100 = ⋅100 = 80,3 %
n CaO
3
Esempio. Milioni di tonnellate di urea CO(NH2)2 vengono ogni anno
prodotte ed utilizzate come fertilizzante. La reazione usata è
2 NH3 + CO2 →
CO(NH2 ) 2 + H 2 O
Sperimentalmente si trova che operando in eccesso di ammoniaca si
formano 47,7 g di urea per mole di CO2 reagita, qual è la resa
percentuale in questa reazione?
Svolgimento
n CO 2 = 1,0 mol ≡ n *CO(NH 2 ) 2 (moli teoriche)
n CO(NH 2 ) 2 =
m CO(NH 2 ) 2
PM CO(NH 2 ) 2
=
47,7 g
≅ 0,7943 mol ≡ n CO(NH 2 ) 2 (moli effettive)
60,0553 (g/mol)
n CO(NH ) , f
0,7943
η= ∗
⋅100 =
n CO(NH )
1,0
2 2
2 2
⋅100 = 79,43 %
Se la resa percentuale fosse stata 87,50 %, che massa di CO2
assieme ad un eccesso di NH3 si sarebbe dovuto usare per
ottenere 50,0 di CO(NH2)2?
Svolgimento
n CO(NH ) , f
η = 87,50 % = ∗
⋅100
n CO(NH )
2 2
2 2
n CO(NH ) , f (moli
2 2
effettive)
=
m CO(NH2 ) 2
PM CO(NH2 )2
50,0 g
=
≅ 0,8326 mol
60,0553 (g/mol)
Quindi le moli teoriche
∗
n CO(NH )
2 2
=
n CO(NH ) , f
2 2
87,50
0,8326 mol
⋅100 =
⋅100 = 0,9515 mol
87,50
n CO 2 : n *CO(NH2 ) 2 = 1 : 1 ⇒ n CO 2 = 0,9515 mol
⇒ m CO 2 = n CO 2 ⋅ PM CO 2 = 0,9515 mol ⋅ 44,0095
g
≅ 41,875 g
mol
ESERCIZI: calcolo della resa
1) La reazione di 15,0 g di C4H10O, 22,4 g di NaBr e 32,7 di di H2SO4
produce 17,1 g di C4H9Br secondo la reazione:
C4H10O + NaBr + H2SO4 → C4H9Br + NaHSO4 + H2O
quale è la resa percentuale di questa reazione? [Risultato 61,7 %]
2) Quanti grammi di C2H4O2 bisogna far reagire con un eccesso di
PCl3 per preparare 75 g di C2H3OCl se la seguente reazione (da
bilanciare):
C2H4O2 + PCl3 → C2H3OCl + H3PO4
ha una resa percentuale del 78,2%.[Risultato 73,4 g di C2H4O2]
ESERCIZI: calcolo della resa
3) La calce Ca(OH)2 (ovvero l’idrossido di calcio) può essere utilizzata
per neutralizzare l’acido di una perdita. Un campione di 5,57 g di
calce reagisce con un eccesso di acido cloridrico HCl; si formano 7,25
g di cloruro di calcio CaCl2 secondo la reazione:
Ca(OH)2 +2 HCl→ CaCl2 + 2 H2O
quale è la resa percentuale di questo esperimento? [Risultato 86,9%]
Reazioni di ossidoriduzione. Ossidanti e riducenti
In una reazione di ossidoriduzione alcuni elementi nei composti cambiano stato
di ossidazione passando dai reagenti ai prodotti.
La variazione dello stato di ossidazione è legata alla cessione o all’acquisto di elettroni.
Un elemento (e il composto che lo contiene) si riduce se il suo n° di ossidazione
diminuisce passando da reagenti a prodotti.
Un elemento (e il composto che lo contiene) si ossida se il suo n° di ossidazione
aumenta passando da reagenti a prodotti.
Ma gli elettroni non esistono liberi e possono essere solo scambiati fra due specie.
Quindi nella stessa reazione vi devono essere almeno due specie che cambiano stato di
ossidazione: una si ossiderà cedendo elettroni all’altra che quindi si ridurrà.
La specie che cede elettroni ossidandosi è detta (agente) riducente.
La specie che acquista elettroni riducendosi è detta (agente) ossidante.
e−
Aox
+
Brid
coppia redox A
Arid
+
coppia redox B
Box
REAZIONE DI OSSIDORIDUZIONE
Composto A ossidato
(agente ossidante)
Composto B ridotto
(agente riducente)
e-
B
e-
+
A
A è ridotto,
acquista elettroni
B è ossidato,
perde elettroni
B
Composto B ossidato
+
A
ee-
Composto A ridotto
Reazioni di ossidoriduzione
0
+1
+2
0
Zn(s) + 2 HCl(aq) → ZnCl2(aq) + H2(g)
Zn si ossida a Zn2+ ⇒ Zn agente riducente
Zn/Zn2+ ⇒ coppia redox
H+ si riduce a H2 ⇒ HCl agente ossidante
H+/H2 ⇒ coppia redox
2+
Zn (s) → Zn (aq)
+ 2e −
+
2H (aq)
+ 2e − → H 2(g)
Forza di un ossidante/riducente: maggiore o minore
tendenza a acquistare/cedere gli elettroni.
Bilanciamento delle reazioni di ossidoriduzione
Il numero totale di elettroni acquistati dall’ossidante deve essere
uguale a quello di elettroni ceduti dal riducente.
Per bilanciare la reazione, bisogna:
• individuare gli elementi che presentano variazione di stato di ossidazione,
e, quindi, le due coppie redox;
• calcolare il numero di elettroni acquistati o ceduti da ciascuna coppia dalla
differenza degli stati di ossidazione della forma ossidata e di quella ridotta;
• trovare il minimo comune multiplo (m.c.m.) tra gli elettroni ceduti e quelli
acquistati per ottenere il numero di elettroni totale in gioco nella reazione;
• dividere il m.c.m. per il numero di elettroni in gioco in ciascuna coppia e
assegnare il quoziente ottenuto come coefficiente stechiometrico alla forma
ossidata e ridotta della coppia.
Dopo aver bilanciato in questo modo l’ossidante e il riducente e le corrispondenti
forme ridotte e ossidate, il bilanciamento prosegue attraverso un’attenta
osservazione dell’equazione e delle regole stabilite per le reazioni acido-base.
Metodo schematico*
KMnO4(aq)M+K2S(aq)M+ HClO4(aq)M→Mn(ClO4)2(aq)+ SO2(g) + KClO4(aq)M+MH2O(l)
\
Mn(+7)M+M5 e−M →MMn(+2)
S(−2)M→MS(+4)M+M6 e−
×6
×5
6 KMnO4 + 5 K2S +28HClO4(aq)→ 6 Mn(ClO4)2(aq)+ 5 SO2+16 KClO4+14 H2O(l)
* Vedremo che questo metodo è il più utile solo per le
reazioni che non avvengono in soluzione, cioè tutte quelle
reazioni che non avvengono nella fase acquosa ma allo stato
solido o fuso.
In forma ionica:
MnO4−(aq)M+MS2−(aq)M+MH+(aq)M →MMn2+(aq)M+MSO2(g)M+MH2O(l)
Mn(+7)M+M5 e−M →MMn(+2)
×6
×5
S(−2)M→MS(+4)M+M6 e−
6 MnO4- + 5 S2- + 28 H+→ 6 Mn2++ 5 SO2+14 H2O(l)
Sbilanciamento di carica:
- 16
+12
28
Metodo ionico-elettronico
Il metodo ionico-elettronico, utilizzabile per reazioni che avvengono in soluzione
acquosa, richiede che:
si divida la reazione, ma non in maniera schematica, nelle due semi-reazioni di
ossidazione e di riduzione, bilanciando, se necessario, il numero di atomi dell’elemento
che cambia stato di ossidazione;
si scrivano dalla parte della forma ossidata un numero di elettroni pari alla differenza
degli stati di ossidazione della forme ossidata e ridotta;
si bilanci ciascuna delle semireazioni usando per il bilanciamento della carica ioni H+, se
la reazione viene condotta in ambiente acido, ioni OH-, se la reazione è in ambiente
basico, e si aggiungano le molecole di acqua necessarie al bilanciamento degli atomi di
idrogeno e di ossigeno;
si calcoli il m.c.m. del numero di elettroni acquistati e ceduti nelle due coppie;
si moltiplichino tutte le specie che compaiono in ciascuna delle due semireazioni
bilanciate per il quoziente tra il m.c.m. ed il numero di elettroni in gioco in nella semireazione;
si sommino membro a membro le due semi-reazioni, semplificando i termini simili.
MnO4
−
(aq)
M+MS2−
(aq)M
H+
→MMn2+(aq)M+MSO2(g)
Ambiente
Acido
MnO4−(aq)M+M5 e−M+M8 H+(aq)M →MMn2+(aq)M+M4 H2O(l)
S2−(aq)M+M2 H2O(l)M →MSO2(g)M+M6 e−M+M4 H+(aq)
×6
×5
6 MnO4−(aq)M+M30 e−M+M48 H+(aq)M→M6 Mn2+(aq)M+M24 H2O(l)
5 S2−(aq)M+M10 H2O(l)M→M5 SO2(g)M+M30 e−M+M20 H+(aq)
___________________________________________________
6 MnO4−(aq)M+M5 S2−(aq)M+M28 H+(aq)M→M6 Mn2+(aq)M+5 SO2(g)M+14 H2O(l)
Un altro Esempio
Cu(s)+ HNO3(aq) → Cu(NO3)2(aq) + NO(g) + H2O(l)
Con il metodo schematico:
Cu(0) → Cu(+2) + 2 e− | × 3
N(+5) + 3 e− → N(+2) | × 2
3 Cu(s)+ 2 HNO3(aq)+ 6 HNO3 → 3 Cu(NO3)2(aq)+2 NO(g)+ 4 H2O(l)
3 Cu(s)+8 HNO3(aq) →3 Cu(NO3)2(aq)+2 NO(g)+ 4 H2O(l)
In forma ionica:
H+
Cu(s)+ NO3-(aq) → Cu2+(aq) + NO(g)
Cu(0) → Cu(+2) + 2 e− | × 3
N(+5) + 3 e− → N(+2) | × 2
m.c.m. = 6
3 Cu(s)+ 2 NO3-(aq)+ 8 H+
→ 3 Cu2+(aq)+2 NO(g)+ 4 H2O(l)
Con il metodo ionico-elettronico:
m.c.m. = 6
Cu(s) → Cu+2 + 2 e−
×3
NO3-(aq) + 4 H+ + 3 e− → NO(g) + 2 H2O(l) × 2
___________________________________________
3 Cu(s)+ 2 NO3-(aq) + 8 H+→ 3 Cu2+(aq) + 2 NO(g) + 4 H2O(l)
Adesso tanti e tanti esempi di bilanciamento
ed esercizi stechiometrici correlati:
Esercitazione alla lavagna (NO SLIDE!) perché
è didatticamente più utile per il vostro
apprendimento (NON DISTRAETEVI!!)
Studiate gli esempi svolti al cap. 8 del
libro Nobile-Mastrorilli.
Esercizi
sul
bilanciamento
delle
reazioni di ossidoriduzione (RedOx) e
sugli esercizi stechiometrici correlati.
Dal libro Nobile-Mastrorilli, per il bilanciamento
delle reazioni di ossidoriduzione (RedOx) bisogna
esser in grado di svolgere gli esercizi e i
problemi:
N. 10, 11, 12, 13, 14, 15, 16,
20, 21, 22, 23, 24, 39, 40, 41,
42, 43, 44, 45, 47, 49, 51, 52,
53, 54, 55, 56. Pag. 255-264.