Verifica di fisica sul primo principio della termodinamica
– Classe 4E – 19 novembre 2014
Durata: 55 minuti. Soglia sufficienza: 60 pt. Punteggio massimo: 100 pt.
Es. 1 Considera un quantità pari a n = (10.0/8.314)mol di gas perfetto monoatomico alla
pressione pA = 15.0 bar all’interno di un cilindro chiuso da un pistone. Il cilindro è immerso in
una miscela di acqua e ghiaccio che mantiene costante la temperatura a 273 K. Assorbendo calore
dalla miscela di acqua e ghiaccio il gas si espande isotermicamente fino a raggiungere un volume
finale VF triplo di quello iniziale. Determina:
À il volume e la pressione finale del gas;
Á il lavoro compiuto sull’ambiente, il calore assorbito dal gas e la variazione di energia interna del
gas;
 la massa di ghiaccio che si è formata durante la trasformazione.
[Punti 20]
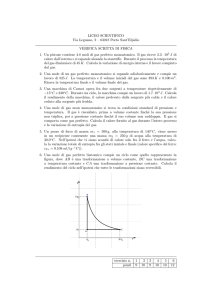
Es. 2 Considera n = (10.00/8.314)mol di gas perfetto monoatomico sottoposte alla trasformazione
quasi-statica (ABCA) riportata in figura. Sapendo che TB = 1600 K e pA = 2.000 bar determina:
p
B
>
>
4pA
pA
C
>
À il volume VA e la temperatura negli stati
A e C;
Á il calore assorbito nei tratti AB, BC, CA;
 il lavoro complessivo L e il calore Q
assorbito dal sistema in un ciclo completo.
A
VA
3VA
V
[Punti 36]
Es. 3 Si dimostri (giustificando adeguatamente i passaggi) che quando n moli di gas subiscono una
trasformazione adiabatica quasistatica dalla temperatura T1 alla temperatura T2 , sull’ambiente
viene compiuto un lavoro pari a:
L = nCV (T1 − T2 ). [Punti 16]
1→2
Es. 4 Considera n = (4.00/8.314)mol di gas perfetto monoatomico alla temperatura TA = 200 K
e pressione pA = 4.00 bar, racchiuse in un cilindro chiuso da un pistone. Il gas viene inizialmente
scaldato a volume costante portandolo alla pressione pB = 12.0 bar e poi riportato alla pressione
iniziale (stato C ) con una espansione adiabatica. Determina:
À temperatura e volume del gas negli stati B e C;
Á il lavoro L svolto dal gas e il calore assorbito Q nella trasformazione (ABC).
[Punti 28]
N.B. Si ricorda che: il calore latente di fusione dell’acqua è Lf = 335 × 103 J kg−1 , la costante
dei gas perfetti è R = 8.314 J mol−1 K−1 .