RISCHI E PRECAUZIONI
Per la manipolazione delle sostanze: cloruro di bario e nitrato di argento e solfo cianuro di potassio
è opportuno consultare la scheda di sicurezza e bisogna evitare la dispersione e l’inalazione delle
polveri . Per il nitrato di argento bisogna evitare il contatto risulta corrosivo, inoltre reagisce con la
luce e la soluzione và preparata in un contenitore di vetro scuro. L’acido cloridrico conc è corrosivo
preparare le soluzioni diluite sotto cappa evitare l’inalazione dei fumi e il contatto con la pelle, la
soluzione di ioduro e bromuro di sodio risultano nocive nella preparazione delle soluzione evitare la
dispersione e l’inalazione delle polveri
Per le reazione del cloruro ferrico e ferroso con idrossido di ammonio e idrossido di sodio, evitare il
contatto con i sali di ferro sono corrosivi, utilizzare la soluzione di ammoniaca solo sotto cappa
sviluppa vapori nocivi e irritanti
Durante l’esecuzione delle prove di gruppo si utilizzano fiamme libere evitare la presenza di
sostanze infiammabili sui banconi.
Nel riscaldamento in provetta del tiosolfato e del saccarosio, la pinza va sistemata nella parte alta
della provetta altrimenti può bruciare (pinze in legno), utilizzare occhialini, e legare i capelli dietro
la nuca.
Nella combustione del magnesio si forma l’ossido di magnesio che si deposita anche sui banconi,
alla fine dell’esperienza bisogna pulire
MATERIALE SOSTANZE E RISCHI
STRUMENTI E MATERIALE
SOSTANZE
Esperienza dimostrativa: carbonato di calcio con Soluzione di cloruro di bario 5%, carbonato di
calcio, acido cloridrico 1 M, nitrato di Argento
acido cloridrico, nitrato di Argento con cloruro,
1%, ioduro, cloruro, bromuro e solfato di sodio,
ioduro e bromuro di sodio, solfato di sodio con
cloruro di bario…………….e tutte quelle del ferro soluzione di idrossido di ammonio 1 M, cloruro
MATERIALE: Provette varie, portaprovette, beuta ferrico e ferroso 0,5 M, soluzione di
con tappo, contagocce
solfocianuro di potassio 0,1 M e di ferrocianuro
Esperienze di gruppo: tiosolfato di sodio ,
di potassio 0,1 M, Magnesio, tiosolfato di sodio
saccarosio due provette una pinza in legno e un
saccarosio
portaprovette per gruppo
Sintesi ossido di magnesio:1 pinza di acciaio,
occhialini per gruppo.
SISTEMAZIONE MATERIALE E STRUMENTI: Recuperare i prodotti di reazione, cloruri
ioduri e bromuri, poi separatamente solfato di bario, idrossidi di ferro, e ancora separatamente i
due sali blu, e rosso di ferro. Lavare la vetreria con qualche goccia di detersivo molta acqua di
rubinetto e alla fine con poca acqua distillata. La provetta con saccarosio bruciato non è possibile
lavarla quindi va eliminata nella raccolta del vetro, la provetta con tiosolfato, fondere il tiosolfato,
recuperare, e lavare le provette con acqua calda. Pulire accuratamente la superficie dei banconi dai
residui di ossido di magnesio.
Esperienze per il laboratorio di chimica Mannarino
Esperienze per il laboratorio di chimica Mannarino
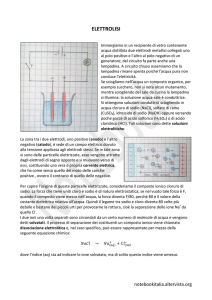
TRASFORMAZIONI CHIMICHE
Esperienze dimostrative: combustione della carta, decomposizione del carbonato di calcio con
acido cloridrico, , reazione in soluzione di cloruro, ioduro, bromuro di sodio con nitrato di
Argento, e di solfato di sodio con cloruro di bario, reazioni del cloruro ferrico e ferroso con
idrossido di ammonio 1 M e idrossido di sodio, reazioni del cloruro ferrico con ferrocianuro di
potassio 0,1 M e con solfocianuro di potassio 0,1 M
trasformazione chimica, trasformazione fisica (riscaldamento del tiosolfato di sodio,
riscaldamento del saccarosio); trasformazione chimica di sintesi magnesio più ossigeno