La sintesi degli acidi grassi avviene
essenzialmente
nel fegato e negli adipociti
e in misura minore in cellule specializzate, quali le
ghiandole mammarie durante l’allattamento.
La biosintesi degli acidi grassi viene indicata
come
sintesi de novo o ex novo per distinguerla dalla
sintesi per allungamento che si può avere nel
mitocondrio come reversal della b-ossidazione.
La via di sintesi è nettamente distinta da quella
degradativa (b-ossidazione)
•La sintesi si realizza nel citosol (mentre l’ossidazione nei mitocondri)
•Nella sintesi gli intermedi sono legati come tioesteri alla proteina
trasportatrici di gruppi acilici (ACP) (nell’ossidazione i tioesteri attivi sono
derivati del CoA)
•Una proteina multifunzionale formata da due catene identiche polipeptidiche
catalizza gran parte delle reazioni biosintetiche (enzimi distinti catalizzano le
reazioni di ossidazione).
•Sia la sintesi che la degradazione procedono per cicli che riguardano
frammenti bicarboniosi; la sintesi richiede un substrato a 3 atomi di carbonio,
il malonil-CoA, che trasferisce unità bicarboniose alla catena nascente con
liberazione di CO2 (l’ossidazione produce un frammento a due atomi di
carbonio, l’aceti-CoA).
•Il potere riducente per la sintesi proviene dal NADPH (mentre per
l’ossidazione dipinde dal NAD+ e dal ETF)
Localizzazione
Ossidazione
Sintesi
Mitocondri
Citosol
Trasportatore di CoA
Acili
Proteina trasportatore di acili
Unità
carboniose
C2
C2
Accettore
/donatore
CoA(C2)
Malonil-CoA (C3, la reazione libera
CO2)
Cofattori
ossido-riduttivi
mobili
NAD+ ETF
NADPH
Organizzazione
degli enzimi
Enzimi
separati
Enzima multifunzionale
La sintesi degli acidi grassi può essere suddivisa
in tre stadi:
1.Nel
primo
l’acetil-CoA
mitocondriale
è
trasportato nel citosol, poi la carbossilazione
genera malonil-CoA, substrato delle reazioni di
allungamento della catena acilica.
2.La carbossilazione dell’acetil-CoA è la reazione
regolata della sintesi degli acidi grassi.
3.L’acido grasso-sintetasi fa procedere
costruzione della catena acilica.
la
La sintesi degli acidi grassi nel citosol richiede acetil-CoA.
Procede per aggiunta di unità bicarboniose fornite dal
malonil-CoA che a sua volta deriva dall’acetil-CoA.
L’acetil-CoA proviene dai mitocondri ove è prodotto, dal
metabolismo dei carboidrati, in normali condizioni di
nutrizione.
L’acetil CoA condensa con l’ossalacetato per dare citrato,
attraverso l’enzima citrato sintasi.
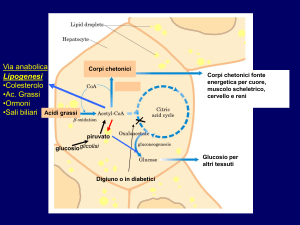
ORIGINE DELL'ACETIL-CoA UTILIZZATO PER LA
SINTESI DEGLI ACIDI GRASSI
L' acetil-CoA è formato nel mitocondrio ad opera di
due soli processi:
1) decarbossilazione ossidativa dell'acido piruvico
( catalizzata dalla PDH)
2) beta-ossidazione degli acidi grassi
La prima via è quella che permette alle molecole
carboniose derivanti da glucosio ed aminoacidi di
essere convertiti in acidi grassi.
Per poter essere utilizzato nella sintesi degli acidi
grassi l'acetil-CoA lascia il mitocondrio ultizzando il
sistema di trasporto degli acidi tricarbossilici:
Matrice mitocondriale
citosol
La decarbossilazione ossidativa del malato ad opera dell'
enzima malico genera NADPH necessario per la sintesi degli
acidi grassi
PERCHÉ IL CITRATO PRENDE UNA STRADA INVECE CHE
UN’ALTRA?
Bisogna considerare due enzimi:
•isocitrato deidrogenasi
•il carrier dei tricarbossilici o carrier del citrato
Quest’ultimo ha per il citrato una Km più elevata di quella
dell’isocitrato deidrogenasi.
Il citrato viene di norma risucchiato nel ciclo di Krebs.
Però a bassa concentrazione di ADP aumenta la Km
dell’isocitrato deidrogenasi per il citrato e supera la Km
del carrier del citrato: il citrato viene così di preferenza
trasportato fuori del mitocondrio, perché l’affinità del
carrier si trova ad essere maggiore dell’enzima del ciclo di
Krebs.
FUORI DEL MITOCONDRIO :
il citrato viene convertito ad
ossalacetato e acetil CoA
per mezzo dell’enzima citrato liasi.
Il citrato è la molecola che trasporta nel citosol l’acetilCoA necessario per la sintesi degli acidi grassi, non
potendo questo passare direttamente attraverso la
membrana mitocondriale interna.
L’ossalacetato viene convertito in malato dalla
malato deidrogenasi citoplasmatica.
Questa reazione serve a riformare il NAD+ necessario alla
glicolisi, quando l’organismo converte l’eccesso di
carboidrati in acidi grassi.
NEL CITOSOL
1° reazione:
citrato liasi
CITRATO + CoA + ATP
ossalacetato
Malato
deidrogenasi
citoplasmatica
MALATO
ACETIL-CoA + ADP + Pi
Destino
dell’ossalacetato
e del malato
Nella ghiandola mammaria il malato rientra nel mitocondrio e ridà
ossalacetato.
Nel fegato, invece il malato citoplasmatico forma il piruvato per
mezzo dell’enzima malico. Si forma NADPH , necessario per la sintesi
degli acidi grassi come equivalente riducente. Una seconda via per
ottenere NADPH è il ciclo dei pentosi.
Da malato e
piruvato si forma
di nuovo
ossalacetato che
condensando con
l’acetil-CoA forma
di nuovo citrato
che esce di nuovo
dal mitocondrio a
dare malato e di
nuovo piruvato.
Il risultato è che molte molecole di acetil-CoA, provenienti
dal glucosio possono formare molte molecole di acido
grasso senza richiedere nuovo ossalacetato.
Ricapitoliamo:
Il primo evento nella biosintesi degli acidi grassi è
rappresentato quindi dalla fuoriuscita del citrato dal
mitocondrio.
Il citrato, una volta fuori del mitocondrio, può fare tre
cose:
Inibire insieme all’ATP la fosfofruttochinasi della
glicolisi, in modo da limitare la produzione di acetil-CoA
da glucosio.
Formare l’acetil-CoA citoplasmatico che serve per la
biosintesi degli acidi grassi.
Attivare l’acetil-CoA carbossilasi per formare malonilCoA. Questa reazione è importante in quanto il malonil-
CoA è il donatore delle unità bicarboniose per la biosintesi
degli acidi grassi.
REAZIONI DELLA SINTESI DEGLI ACIDI GRASSI
La sintesi del malonil-CoA è il committed step nella sintesi
degli acidi grassi.
L’acetil-CoA subisce una carbossilazione
La reazione è catalizzata dalla acetil-CoA carbossilasi (ACC): richiede
il coenzima biotina per il trasferimento della CO2.
Procede in due fasi:
•Attivazione ATP-dipendente dell’HCO3•Trasferimento della CO2 attivata all’acetil-CoA
CARBOSSIBIOTINA
MALONIL CoA
acetil-CoA carbossilasi
L’ACC È UN IMPORTANTE SITO DI CONTROLLO DELLA
BIOSINTESI DEGLI ACIDI GRASSI.
Può esistere in una forma polimerica detta “filamentosa”
che è la forma attiva e dipende dalla presenza del citrato
In una forma monomerica inattiva che si ha in presenza
di acidi grassi ed in assenza di citrato.
È controllato anche da un meccanismo di
fosforilazione/defosforilazione cAMP dipendente.
La forma fosforilata è inattiva.
Il glucagone induce la fosforilazione e l’inattivazione nel
fegato; l’adrenalina fa lo stesso negli adipociti.
L’insulina ha effetto opposto.
Una volta formato il malonil-CoA può iniziare la sintesi
degli acidi grassi.
LA VIA METABOLICA RICHIEDE L’INTERVENTO DI BEN
SETTE REAZIONI ENZIMATICHE
di cui è responsabile un solo complesso enzimatico:
L’ACIDO GRASSO SINTASI
È una proteina dimerica di 480 kDa, che ha due unità
Uguali di 240 kDa orientate in modo opposto l’una
rispetto all’altra.
Ogni subunità ha sette diversi siti catalitici.
STRUTTURA DELL'ACIDO GRASSO SINTASI
L'acido grasso sintasi è un enzima polifunzionale, formato da
due catene polipeptidiche identiche.
Perché un complesso multienzimatico ?
L’associazione di enzimi che catalizzano reazioni
sequenziali all’interno di una via metabolica è
notevolmente vantaggioso:
Permette di veicolare i reagenti e prodotti fra i siti
attivi senza venire in contatto con il solvente.
Ciò velocizza la via metabolica e protegge gli
intermedi instabili.
Inoltre consente di regolare l’espressione di un solo
gene codificante per quella struttura enzimatica.
CARICAMENTO
I primi due enzimi che intervengono sono:
l’acetil-CoA-ACP transferasi (AT)
malonil-CoA –ACP transferasi (MT)
transferasi
transferasi
La proteina trasportatrice di acili (ACP) consta di:
-una parte proteica
-una parte prostetica, che corrisponde alla fosfopanteteina, che deriva
dal CoA.
-Il fosfato della fosfopanteteina si lega al residuo di serina-36 della proteina.
Qui si legano gli
intermedi della
sintesi degli acidi
grassi,
dando luogo a
composti acilici
attivati, sottoforma
di tioesteri.
Il gruppo –SH (tiolico) all’estremità della fosfopanteteina
è quello che lega gli intermedi della biosintesi degli acidi
grassi.
L’-SH è il sito di acilazione dell’ACP, che dà luogo ad
intermedi attivati tioesteri.
Segue la reazione di :
CONDENSAZIONE
La chetoacil-ATP sintetasi,
detta anche enzima condensante
accetta il gruppo acetile dell’acil-ACP, e lo trasferisce al
malonil-ACP con liberazione di CO2
formando aceto-acetil-ACP
RIDUZIONE
Un gruppo chetonico è ridotto a gruppo alcolicoad opera della
b-chetoacil-ACP reduttasi
DEIDRATAZIONE
L’enzima b-D-idrossiacil deidratasi rimuove una molecola d’acqua
con formazione di un doppio legame.
RIDUZIONE
Enoil-ACP-reduttasi NADPH-dip
Si forma un acil-ACP a quattro atomi di carbonio:
butirril-ACP; il butirrato viene trasferito dall’ACP
all’enzima condensante e sull’ACP reso libero si
lega un altro malonato. Il ciclo riprende con il
legame del butirrato al malonato, con perdita
della CO2, come nel primo ciclo; ora il butirrato
sostituisce l’acetato.
La sintesi procede per ripetizione del processo a partire dallo stato di
condensazione;
L’acil-ACP, ovvero il butirril-ACP, sostituisce l’acetil-ACP ed una nuova
molecola di malonil-CoA entra in ciascun ciclo.
Mentre nel primo ciclo l’acetil-CoA fornisce l’unità bicarboniosa che
corrisponde all’ultimo e penultimo atomo di carbonio della molecola
in formazione, nei cicli successivi il malonil-CoA fornisce l’unità
bicarboniosa terminale.
I cicli sintetici continuano fino al gruppo C16-palmitoile.
Il palmitoil-ACP è poi substrato di una tiolasi
che lo stacca dall’ACP, mediante attività idrolitica
Sintesi del palmitato
ALLUNGAMENTO E DESATURAZIONE DEGLI ACIDI
GRASSI
ALLUNGAMENTO DELL'ACIDO PALMITICO (C 16):
1) nel mitocondrio, l'allungamento ha inizio con la reazione
tiolasica:
palmitoil-CoA + acetil-CoA ------------> b-chetostearoilCoA + HS-CoA
seguita dalle reazioni catalizzate dalla idrossiacil-CoA
deidrogenasi, enoil-CoA deidratasi ed enoil-CoA reduttasi.
2) nel reticolo endoplasmico, l'allungamento avviene per
addizione di unità C2 in forma di malonyl-CoA.
In entrambi
NADPH.
i
casi
viene
utilizzato
esclusivamente
REGOLAZIONE DELLA SINTESI DEGLI ACIDI
GRASSI
La sintesi degli acidi grassi è controllata in primo luogo
dall'equilibrio esistente tra la forma monomerica dell'ACC
(inattiva) e la forma polimerica (attiva) Il citrato, attivatore
allosterico, sposta l'equilibrio verso la forma polimerica
attiva;mentre gli acil-CoA a lunga catena spostano l'equilibrio
verso i monomeri inattivi.
La fosforilazione dell'ACC modula l'attivazione da parte
del citrato e l'inibizione da parte dell' acil-CoA.
Il glucagone e l'adrenalina aumentano
l'attività della PKA che fosforila alcuni residui
di serina dell'ACC.
Il risultato è una diminuzione dell'attività
enzimatica.
L'insulina, invece fa aumentare l'attività
dell'enzima.
Gli enzimi DESATURASI catalizzano la formazione dei doppi legami
all’interno della catena carboniosa degli acidi grassi.
Le cellule animali contengono enzimi in grado di desaturare solo fino
alla posizione 9 a partire dal gruppo carbossilico dell’acido grasso.
Solo le piante sono in grado di andare oltre con l’insaturazione.
DESATURAZIONE:
Negli animali superiori è possibile la desaturazione di un acido
grasso a livello del reticolo endoplasmico come nel caso della
stearoil-desaturasi.
Gli acidi grassi insaturi così ottenuti possono essere
successivamente allungati. Dall'acido grasso essenziale
linoleico (D9,12- 18:2) si ottiene del reticolo endoplasmico
l'acido arachidonico ( D4,8,11,14 - 20:4)
L’ORGANISMO ANIMALE NON RIESCE A SINTETIZZARE ALCUNI ACIDI
GRASSI, DETTI:
Acido linoleico
CH3 (CH2)4 CH
CH CH2 CH
Acido a-linolenico
CH3 CH2 CH
CH CH2 CH
CH (CH2)7COO
H
CH CH2 CH
CH (CH2)7 COOH
L’essenzialità risiede nel fatto che l’organismo non riesce
ad inserire insaturazioni ossia doppi legami in determinate
posizioni ω3 ed ω6. ( questa denominazione prende come
riferimento il metile alla testa dell’acido grasso.)
Essi sono i capostipiti dagli acidi grassi delle serie:
•Linoleica
•Linolenica
La classificazione con il simbolo “ω“ indica la posizione del doppio
legame a partire dal metile in testa.
Derivano dall’acido arachidonico,
presente nel foglietto interno della
membrana cellulare, all’interno di
lipidi complessi, i fosfolipidi.
Esso viene liberato per azione di una
fosfolipasi A2.
Derivano dagli acidi grassi
insaturi a lunga catena e
funzionano come molecole
regolatrici di numerosi
processi nell’organismo.
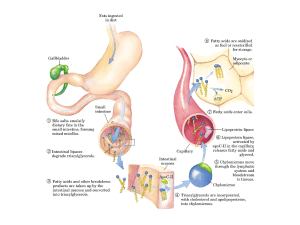
SINTESI DEI TRIGLICERIDI
• Sintesi ex-novo
• Acilazione di mono e di-gliceridi
ORIGINE AC. GRASSI
1) DALLE LIPOPROTEINE
- VLDL, Chilomicroni (LPL)ac.grassi +
monogliceride (monogliceride lipasi)
glicerolo+ac.glicerico
- VLDL LDL; chilomicroni HDL
2)
IDROLISI TG ADIPOCITARI
3) SINTESI EX-NOVO
ORIGINE DEL GLICEROLO-3P
-Catabolismo glucidico:1) ox. a CO2 x energia;
2) shunt pentosoP x NADPH; 3) sintesi
ac.grassi; 4)formazione del glicerolo-3P da
DHAP (diidrossiacetone fosfato)
- Attività della glicerolo kinasi molto bassa
SINTESI DEI TRIGLICERIDI
I trigliceridi ed i fosfolipidi ed i fosfolipidi
neutri (fosfatidilcolina, etanolammina) sono
sintetizzati attraverso una via comune.
La prima parte è schematizzata in figura
Il diidrossiacetone fosfato (DHAP)
provienente dalla glicolisi, viene
dapprima
ridotto
a
glicerolo-3fosfato.
Quest’ultimo serve da scheletro per le
successive acilazioni con molecole di
acil-CoA grazie a due differenti aciltrasferasi.
Si ottiene così l’acido fosfatidico.
Il passo successivo è la
defosforilazione dell’acido
fosfatidico
Si ottiene
1,2- Diacilglicerolo
Che può essere direttamente
acilato a formare il
triacilglicerolo
SINTESI DEI TRIGLICERIDI
Una molecola di glicerolo-3fosfato viene incorporata nel CDPdiacilglicerolo con spiazzamento
del CMP
Fosfatidilglicerolofosfato
Quindi una fosfatasi catalizza la
formazione del fosfatidilglicerolo.
Fosfatidilglicerolo
Segue lo spiazzamento del
glicerolo da parte del
fosfatidilglicerolo
Difosfatidilglicerolo (Cardiolipina)
STRUTTURA DEI FOSFOLIPIDI
Fosfatidilcolina
Fosfatidiletanolamina
Fosfatidilserina
Fosfatidilinositolo
Fosfatidilglicerolo
Difosfatidilglicerolo (Cardiolipina)
C5) SINTESI
TRIGLICERIDI
Sintesi di glicerolo-3P
da glicerolo o DHAP
L’1,2 diacilglicerolo può anche reagire con:
CDP-colina
CDP-etanolammina
fosfatidiletanolammina
fosfatidilcolina
Fosfolipidi neutri
La CDP-colina si forma dalla fosforilazione della colina via colina cinasi seguita
dalla condensazione con CTP via CTP :fosfocolina citidiltrasferasi.
LE FOSFOLIPASI
PLASMALOGENI
• I plasmalogeni sono una sottoclasse di
glicerofosfolipidi che presentano un gruppo
alchilico legato con un legame etere al C-1 del
glicerolo. I plasmalogeni sono i lipidi più
abbondanti nelle membrane mitocondriali e sono
anche presenti in considerevoli quantità nel
tessuto nervoso e muscolare ( basti pensare che
nel cuore i plasmalogeni rappresentano circa il
50% dei fosfolipidi totali).
PLASMALOGENI
• La funzione di tali molecole sembrerebbe quella
di proteggere dallo stress ossidativo, i tessuti
che presentano un notevole metabolismo
aerobio, dato che sono molto resistenti alla
degradazione ossidativa. Ciò è assai importante
soprattutto per il fatto che nella maggior parte
delle membrane, i fosfolipidi si rinnovano in
continuazione,
processo
questo
che
è
particolarmente evidente in risposta a danni
ossidativi che si instaurano soprattutto nel corso
di reazioni infiammatorie.
SFINGOLIPIDI
• Gli sfingolipidi sono un gruppo eterogeneo di
lipidi polari ed anfipatici. La loro struttura
centrale presenta un ammino-alcool a catena
lunga, la sfingosina, che viene sintetizzata
mediante condensazione e decarbossilazione
ossidativa della serina con il palmitato.
In tutti gli sfingolipidi, un acido grasso a catena
lunga è unito al gruppo aminico della sfingosina
mediante un legame amidico.
SFINGOLIPIDI
• La sintesi dell’unità di sfingosina degli
sfingolipidi prevede la condensazione del
palmitoil CoA con la serina, reazione questa in
cui il carbonio 1 della serina viene perso come
biossido di carbonio; il prodotto di tale
reazione viene poi convertito attraverso
diverse tappe a sfingosina, la quale viene
successivamente N-acilata per generare il
ceramide ( N-acilsfingosina).
• Il ceramide rappresenta a sua volta il
precursore e lo scheletro strutturale della
sfingomielina e degli glicosfingolipidi.
SFINGOMIELINA
• La sfingomielina è uno sfingolipide
presente
nelle
membrane
plasmatiche e nelle membrane degli
organuli subcellulari, del reticolo
endoplasmatico e dei mitocondri.
• La sfingomielina è l’unico sfingolipide
che contiene un gruppo fosforico, e
rappresenta
il
fosfolipide
più
abbondante nella guaina mielinica
dei nervi.
SFINGOMIELINA
• Durante la sua sintesi, una unità di
fosfocolina è trasferita sul gruppo
ossidrilico terminale della sfingosina. La
composizione
in
acidi
grassi
della
sfingomielina può variare, anche se sono
molto comuni acidi grassi a catena lunga
come
• –l’acido lignocerico ( C-24:0)
• -l’acido cerebronico ( 2-idrossilignocerico)
• -l’acido nervonico ( C-24:1)
GLICOLIPIDI
• I glicolipidi, o glicosfingolipidi, sono
sfingolipidi che contengono unità
saccaridiche legate covalentemente.
• Essi possono essere classificati in
quattro gruppi diversi:
• -i cerebrosidi
• -i sulfatidi
• -i globosidi
• -i gangliosidi.
GLICOLIPIDI
• In tutte queste classi, la testa polare,
che comprende le unità saccaridi che,
è unità al ceramide attraverso un
legame glicosidico con il gruppo
ossidrilico terminale della sfingosina.
• I più semplici fra i glicosfingolipidi
sono il glucoe il galatto-cerebrosidi
(glucosil e galattosil ceramidi), che
presentano
un
monosaccaride
attaccato alla sfingosina.
GLICOLIPIDI
• I sulfatidi si formano in seguito all’aggiunta di un
gruppo solfato da parte del donatore 3’fosfoadenosina-5’-fosfosolfato Se la porzione
saccaridica di un cerebro side contiene due o più
monosaccaridi ed almeno un unità di N-acetil
galattosamina, allora il glicosfingolipide appartiene
alla classe dei globosidi.
• Infine, i glicolipidi la cui catena oligosaccaridica
contiene l’acido sialico, sono chiamati gangliosidi.
Malattie genetiche associate al metabolismo degli sfingolipidi:
sfingolipidosi
Gli sfingolipidi sono normalmente degradati dai lisosomi nelle
cellule fagocitarie del SISTEMA RETICOLO ENDOTELIALE (fegato,
milza midollo osseo)
Durante il periodo neonatale il turn-over dei gangliosidi nel SNC è
molto elevato ed essi sono rapidamente degradati e risintetizzati.
Quando a causa di errori genetici l’attività di un enzima idrolitico è
ridotta, il substrato a monte della reazione coinvolta si accumula e
si deposita nei tessuti responsabili del catabolismo di quel lipide,
causando danni tissutali notevoli (ritardo mentale, cecità,
ingrossamento del fegato e della milza, ecc.)
Alcune di queste patologie (con i lipidi coinvolti) sono:
•Malattia di Gaucher (sfingomielina)
•Malattia di Tay-Sachs (glucocerebroside)
•Malattia di Fabry (ceramide triesoside)
•Malattia di Niemann-Pick (sfingomielina)
SINTESI DEL CERAMIDE
La 3-chetosfinganina sintetasi
necessita
del
piridossalfosfato,coenzima
derivato dalla vitamina B6
(piridossale,piridossolo,piridos
samina).
SINTESI DELLA SFINGOMIELINA
SINTESI DEL CERAMIDE
La 3-chetosfinganina sintetasi
necessita
del
piridossalfosfato,coenzima
derivato dalla vitamina B6
(piridossale,piridossolo,piridos
samina).
SINTESI DELLA SFINGOMIELINA
SINTESI DEI SOLFATIDI
ASPETTI CLINICI
La sindrome da stress respiratorio è causa di morte prematura nel neonato.
E' dovuta ad insufficente produzione a livello polmonare della dipalmitoillecitina, tensioattivo necessario per il normale rilasciamento degli alveoli
polmonari.
La maturazione del polmone fetale può essere dedotta dalla determinazione
nel liquido amniotico del rapporto dipalmitoil-lecitina/sfingomielina: per
valori inferiori a 2 si ha rischio di sindrome da stress respiratorio.
Malattie genetiche associate al metabolismo degli sfingolipidi: sfingolipidosi.
• La funzione del DPCC è quella di diminuire la
tensione superficiale del sottile strato acquoso
nei polmoni, facilitando l’apertura degli alveoli
durante l’inspirazione. La carenza di questo
surfactante causa il collasso dei polmoni durante
l’espirazione con conseguente insufficienza
respiratoria.
• La maturazione del polmone fetale può essere
dedotta dalla determinazione nel liquido
amniotico
del
rapporto
dipalmitoillecitina/sfingomielina: per valori inferiori a 2 si
ha rischio di sindrome da stress respiratorio.
PATOLOGIE DA FOSFOLIPIDI: LA SINDROME DA
INSUFFICIENZA RESPIRATORIA ACUTA ( ARDS)
• I polmoni dei neonati prematuri non
presentano un numero adeguato di cellule
epiteliali di tipo II per sintetizzare quantità
sufficienti
del
fosfolipide
dipalmitoilfosfatidilcolina ( DPPC). Tale
fosfolipide costituisce da solo oltre l’80%
dei fosfolipidi totali disposti a formare uno
strato extracellulare che riveste gli alveoli
dei polmoni normali.