42527 MEDICINA GENETICA - C.I. (09/10)
Canale B
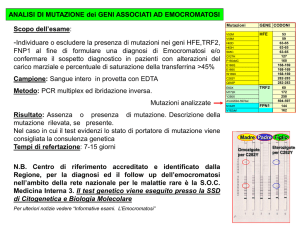
EMOCROMATOSI
Vincenzo Stanghellini (016074)
051.636-4101
[email protected]
OMEOSTASI DEL Fe IN CONDIZIONI NORMALI
Eritrociti circolanti
1500-2500 mg
Emolisi
(monociti/macrofagi):
20 mg/die
Assorbimento
(intestino)
1-2 mg/die
Eritropoiesi
(midollo osseo)
20 mg/die
Pool plasmatico
4 mg
Deposito corporeo totale
macrofagi tessutali, epatociti : 4g
(fegato: 300mg –1g)
Eliminazione
(intestino)
1-2 mg/die
OMEOSTASI DEL Fe IN CONDIZIONI NORMALI
•
ASSORBIMENTO:
assorbimento intestinale regolato da ipo- o
ipersideremia
•
ESCREZIONE:
non correlato alla sideremia (desquamazione
entereociti, emorragie, mestruazioni, gravidanza)
SITI CHIAVE DEL METABOLISMO DEL Fe
ENTEROCITA DEL VILLO E DELLA CRIPTA DUODENALE
DcytB:
citocromo B duodenale
(Fe-reduttasi: ferrico Fe3+ ferroso Fe2+)
DMT1:
trasportatore metallico divalente 1
Efestina: Fe-ossidasi (ossida il Fe2+ a Fe3+)
Ferroportina: Fe-transporter
SITI CHIAVE DEL METABOLISMO DEL Fe
ENTEROCITA DEL VILLO DUODENALE
Versante luminale
• DcytB1 (ferric reductase) riduce Fe3+ (ferrico) a Fe2+
• DMT1 trasporta il Fe2+ (ferroso) nell’enterocita
Enterocita
• Fe2+ viene
- immagazzinato nei depositi di ferritina
- riversato dalla ferroportina nel plasma
Versante plasmatico
•
Ferroportina (basolateral transporter) trasporta Fe2+ dal
citoplasma dell’enterocita ai vasi della sottomucosa
• Efestina ossida il Fe2+ a Fe3+
• Fe3+ viene legato a proteine trasportatrici (transferrina,
NTBI)
IPOTESI DELLA CRIPTA
Regolazione maturazione enterocitaria:
1. HFE / TfR1 basocellulare attivato da Tf-S
DMT1 (apicocellulare)
2. Epcidina
3. Citochine
4. Eritropiesi
SITI CHIAVE DEL METABOLISMO DEL Fe
ENTEROCITA DEL VILLO DUODENALE
Versante luminale
• DcytB1 riduce Fe3+ (ferrico) a Fe2+ (ferroso)
• DMT1 trasporta il Fe2+ nell’enterocita
• HPC1 trasporta l’Eme (Hb e Mb) nell’enterocita
Enterocita
• OH degrada l’eme e libera Fe2+
• Fe2+ viene
- immagazzinato nei depositi di ferritina
- riversato dalla ferroportina nel plasma
Versante plasmatico
•
Efestina ossida il Fe2+ a Fe3+
•
Fe3+ viene legato a proteine trasportatrici
(transferrina, NTBI)
DcytB1: citocromo B duodenale (Fe-reduttasi)
DMT1: trasportatore metallico divalente 1
HCP1: proteina trasportatrice di eme 1
OH: eme-ossigenasi
FP: ferroportina
Efestina: Fe-ossidasi
CP: ceruloplasmina
SITI CHIAVE DEL METABOLISMO DEL Fe
MACROFAGI RETICOLOENDOTELIALI
• I macrofagi fagocitano i globuli rossi senescenti
ALL’INTERNO DEI MACROFAGI
• I fagolisosomi li lisano
• L’Hb viene degradata
• Il Fe2+ liberato dall’eme
DMT1: trasportatore metallico divalente 1
• Fe2+ viene
FP: ferroportina
- immagazzinato nei depositi di ferritina
OH: eme-reduttasi
- riversato da ferroportina o ceruloplasmina nel plasma
CP: ceruloplasmina
NEL VERSANTE PLASMATICO
• Il Fe2+ viene ossidato a Fe3+
•
Fe3+ viene legato alla transferrina
SITI CHIAVE DEL METABOLISMO DEL Fe: EPATOCITI
ALL’INTERNO DELL’EPATOCITA
(s)HJV: emo-juvelina (solubile)
• Fe2+ è rilasciato dalla degradazione
Tf: transferrina
NTBI: non-transferrina legante Fe
ES: emosiderina
FP: ferroportina
CP: ceruloplasmina
TfR: recetore per assorbimento transferrina
intraepatocitaria di ferritina, eme, Hb, Tf e NTBI
• Fe2+ viene
- immagazzinato nei depositi di ferritina
- riversato da FP nel plasma
NEL VERSANTE PLASMATICO
• Fe2+ ossidato a Fe3+ legato a transferrina o NTBI
SITI CHIAVE DEL METABOLISMO DEL Fe: EPATOCITI
EPCIDINA
• Gli epatociti producono epcidina (attraverso la fase
di pre-proepcidina e pro-epcdina); l’epcidina
(s)HJV: emo-juvelina (solubile)
Tf: transferrina
NTBI: non-transferrina legante Fe
ES: emosiderina
FP: ferroportina
CP: ceruloplasmina
TfR: recetore per assorbimento transferrina
immissione di Fe nel plasma
• L’espressione di epcidina è modulata da HFE, TfR2
e HJV che fungono da sensori del Fe
OMEOSTASI DEL Fe IN CONDIZIONI NORMALI
•
Fe plasmatico espressione di HFE, transferrin
receptor 2 (TfR2) e hemojuvelin (HJV) espressione di
hepcidin antimicrobial peptide (HAMP) codificante per
Epcidina
•
legame Epcidina + Ferroportina (Fpn)
Internalizzazione degradazione della Fpn
•
immissione di Fe nel plasma ad opera di enterociti e
macrofagi.
EMOCROMATOSI
Disordine del metabolismo del Fe con progressivo accumulo
intra-parenchimale e potenziale danno multiorgano
•
Emocromatosi secondaria:
sovraccarico di ferro secondario ad una patologia organica, sistemica,
metabolica o iatrogena
•
Emocromatosi ereditaria:
mutazione ereditaria di uno o più geni coinvolto nel metabolismo del Fe
CLASSIFICAZIONE EZIOLOGICA DELLE PATOLOGIE DA ACCUMULO DI Fe
EMOCROMATOSI SECONDARIA
Anemie da carico di Fe
EMOCROMATOSI EREDITARIA
HFE
•
C282Y omozigosi (95%)
•
C282Y/H63D eterozigosi (4%)
S. talassemiche, anemia sideroblastica,
•
H63D omozigosi (1%)
mielodisplasia, diseritropoiesi congenita
NON HFE
• Eritropoiesi inefficace
• Aumentata eritropoiesi
Anemia emolitica cronica
Terapia marziale o emotrasfusioni multiple
S. Metaboliche
•
Emocromatosi variante HJV
•
Emocromatosi variante epcidina
•
Emocromatosi variante TfR2
•
Emocromatosi variante ferroportina
ALTRE FORME
• Obesità / insulino-resistenza, ipertensione
•
S. da iperferritinemia – catarratta congenita
Epatopatie croniche
•
Deficit di eme-ossigenasi (OH)
• Epatiti, alcol, NASH, porfiria cutanea tarda
•
Accumulo neonatale di Fe
•
Aceruloplasminemia congenita
•
A-(ipo)transferrinemia congenita
•
Variante DMT1
Accumulo di Fe delle popolazioni africane
CLASSIFICAZIONE EZIOLOGICA DELLE PATOLOGIE DA ACCUMULO DI Fe
EMOCROMATOSI SECONDARIA
Anemie da carico di Fe
EMOCROMATOSI EREDITARIA
HFE
•
C282Y omozigosi (95%)
•
C282Y/H63D eterozigosi (4%)
S. talassemiche, anemia sideroblastica,
•
H63D omozigosi (1%)
mielodisplasia, diseritropoiesi congenita
NON HFE
• Eritropoiesi inefficace
• Aumentata eritropoiesi
Anemia emolitica cronica
Terapia marziale o emotrasfusioni multiple
S. Metaboliche
•
Emocromatosi variante HJV
•
Emocromatosi variante epcidina
•
Emocromatosi variante TfR2
•
Emocromatosi variante ferroportina
ALTRE FORME
• Obesità / insulino-resistenza, ipertensione
•
S. da iperferritinemia – catarratta congenita
Epatopatie croniche
•
Deficit di eme-ossigenasi (OH)
• Epatiti, alcol, NASH, porfiria cutanea tarda
•
Accumulo neonatale di Fe
•
Aceruloplasminemia congenita
•
A-(ipo)transferrinemia congenita
•
Variante DMT1
Accumulo di Fe delle popolazioni africane
STORIA NATURALE DELL’OMOZIGOSI C282Y
Danno
d’organo
Sintomi
Sovraccarico biochimico
Predisposizione genetica
Tempo
Fattori ambientali
Fattori genetici
EMOCROMATOSI – MANIFESTAZIONI CLINICHE
Adenoipofisi
Ipogonadismo ipogonadotropo
Infertilità, impotenza
Fegato
Cuore
Epatomegalia
Fibrosi (reversibile)
Cirrosi - HCC (x200)
Cardiomiopatia
Scompenso
Aritmie
Pancreas
Articolazioni
Diabete mellito
Artropatie
Altro
Cute
Astenia
Iperpigmentazione
EMOCROMATOSI - BIOPSIA EPATICA
Cirrosi epatica pressochè assente
con Ferritina <1.000 g/L
Enholm et al. Am J pathol 2003;163:827-32
Follow up senza salasso in
omozigoti C282Y diagnosticati da
adulti con ferritina normale o
scarsamente elevata ?
Gurrin et al. Gastroenterology 2008;135:1954-52
CLASSIFICAZIONE EZIOLOGICA DELLE PATOLOGIE DA ACCUMULO DI Fe
EMOCROMATOSI SECONDARIA
Anemie da carico di Fe
EMOCROMATOSI EREDITARIA
HFE
•
C282Y omozigosi (95%)
•
C282Y/H63D eterozigosi (5%)
S. talassemiche, anemia sideroblastica,
•
H63D omozigosi (1%)
mielodispia, diseritropoiesi congenita
NON HFE
• Eritropoiesi inefficace
• Aumentata eritropoiesi
Anemia emolitica cronica
Terapia marziale o emotrasfusioni multiple
S. Metaboliche
•
Emocromatosi variante HJV
•
Emocromatosi variante epcidina
•
Emocromatosi variante TfR2
•
Emocromatosi variante ferroportina
ALTRE FORME
• Obesità, ipertensione, insulino-resistenza
•
S. da iperferritinemia – catarratta congenita
Epatopatie croniche
•
Deficit di eme-ossigenasi (OH)
• Epatiti, alcol, NASH, porfiria cutanea tarda
•
Accumulo neonatale di Fe
•
Aceruloplasminemia congenita
•
A-(ipo)transferrinemia congenita
•
Variante DMT1
Accumulo di Fe delle popolazioni africane
DEFINIZIONE DELL’EMOCROMATOSI EREDITARIA
Disordine ereditario del metabolismo del Fe con progressivo accumulo
intra-parenchimale e potenziale danno multiorgano
Caratteristiche fondamentali
•
Natura ereditaria (generalmente trasmissione autosomica recessiva)
•
Fe nel distretto plasmatico ( sideremia e saturazione transferrina)
•
Fe nelle cellule parenchimali ( ferritina, danno d’organo)
•
Eritropoiesi generalmente non alterata, buona risposta al salasso
EPIDEMIOLOGIA EMOCROMATOSI EREDITARIA
• Irlanda: 1 / 83
• Nord Europa: 1 / 200-350
• Italia: 1 / 1500-2000
• + Rara tra i non caucasici
CLASSIFICAZIONE GENETICA (OMIM)
DELL’EMOCROMATOSI EREDITARIA
Tipo 1
HFE emocromatosi
Tipo 2A
Emocromatosi giovanile
“
Emocromatosi da epcidina
2B
Tipo 3
Emocromatosi da alterazione del recettore 2 della transferrina
Tipo 4
Emocromatosi da alterazione della ferroportina
CLASSIFICAZIONE GENETICA
DELL’EMOCROMATOSI EREDITARIA
TIPO
EREDITA’
GENE / LOCUS
1 (tipico)
AR
HFE / 6p21
95%
2A
AR
HJV / 1q21
PROTEINA / FUNZIONE
HFE/
Interazione con TfR1; Cofattore trascrizionei di epcidina
Emojuvelina /
Corecettore trascrizione di epcidina
2B
AR
HAMP / 19q13
Epcidina /
Ritenzione di Fe in macrofagi, enterociti e placenta
3
AR
TfR2 / 7q22
Transferrina-R2 /
Captazione di transferrina coniugata con Fe
Corecettore trascrizione di epcidina
4
AD
SCL40A1 / 2q32
Ferroportina /
Fuoriuscita di Fe da macrofagi, enterociti, epatociti, placenta
CLASSIFICAZIONE GENETICA
DELL’EMOCROMATOSI EREDITARIA
TIPO
EREDITA’
GENE / LOCUS
1 (tipico)
AR
HFE / 6p21
PROTEINA / FUNZIONE
HFE/
Interazione con TfR1; Cofattore trascrizione di epcidina
2A
AR
HJV / 1q21
Emojuvelina /
Corecettore trascrizione di epcidina
2B
AR
HAMP / 19q13
Epcidina /
Ritenzione di Fe in macrofagi, enterociti e placenta
3
AR
TfR2 / 7q22
Transferrina-R2 /
Captazione di transferrina coniugata con Fe
Corecettore trascrizione di epcidina
4
AD
SCL40A1 / 2q32
Ferroportina /
Fuoriuscita di Fe da macrofagi, enterociti, epatociti, placenta
GENE HFE
• Braccio corto cromosoma 6 (6p21)
• Sito adiacente al Major Histocompatibility Complex (MHC) – Classe 1
• Come le molecole MHC – Classe 1 necessita legame con
-microglobulina x esprimersi sulla superficie cellulare
• Duplice ruolo:
HFE epatico: lega TfR1 HAMP / epcidina ferroportina
•
HFE enterocitario: lega TfR1 (basocellulare) DMT1
(DcytB1) assorbimento di Fe (apicale)
PRINCIPALI MUTAZIONI DEL GENE HFE
C282Y
Omozigozi per mutazioni di questo gene
90-95% emocromatosi / HFE
H63D
Eterozigosi per mutazioni di questo gene + C282Y
4-5%
emocromatosi / HFE
GENE HFE EPATICO ED ENTEROCITARIO
Trapianto di fegato e intestino tenue da donatore omozigote C282Y EMOCROMATOSI
Trapianto di fegato isolato da donatore omozigote C282Y NO EMOCROMATOSI
Step patogenetici e
alterazioni biochimiche
Fattori non correlati al
gene HFE
STORIA NATURALE DELL’OMOZIGOSI C282Y
Fattori ambientali
Fattori genetici
Mutazione HFE
Crescita, mestruazioni,
gravidanza, dieta, perdite
ematiche
Abuso etilico, malattie con
sovraccarico di Fe: talassemia,
porfiria, infezioni, HCV, NASH
Geni codificanti per epcidina,
TfR2, aptoglobina, emopessina,
ceruloplasmina, emeossigenasi 1
Fe
plasmatico
Fe
tessutale
Saturazione
transferrina
Ferritina
Geni implicati in
antiossidanti, fibrogenesi,
riparazione tissutale
Danno
d’organo
Ferritina > 1000 ng/ml
Alterazione test epatici,
endocrini e glicemici
CLASSIFICAZIONE GENETICA
DELL’EMOCROMATOSI EREDITARIA
TIPO
EREDITA’
GENE / LOCUS
1 (tipico)
AR
HFE / 6p21
PROTEINA / FUNZIONE
HFE/
Interazione con TfR1; Cofattore trascrizione di epcidina
2A
AR
HJV / 1q21
Emojuvelina /
Corecettore trascrizione di epcidina
2B
AR
HAMP / 19q13
Epcidina /
Ritenzione di Fe in macrofagi, enterociti e placenta
3
AR
TfR2 / 7q22
Transferrina-R2 /
Captazione di transferrina coniugata con Fe
Corecettore trascrizione di epcidina
4
AD
SCL40A1 / 2q32
Ferroportina /
Fuoriuscita di Fe da macrofagi, enterociti, epatociti, placenta
GENE HJV / HAMP
2A
• Mutazioni HJV – cromosoma 1 (1q21) – omozigosi G320V (50% dei casi)
• Emogiuvelina – proteina di superficie con funzioni di co-recettore
• Forma clinicamente severa ad insorgenza precoce (>30 aa); M=F
• Interessamento epatico simile a HH-1, ma ipogonadismo e cardiomiopatia
2B
• Mutazioni HAMP – cromosoma 19 (19q13)
• Pro- Pre- Epcidina – proteina sintetizzata nel fegato in risposta a
sovraccarico sideremico (sovraespressione anemia o previene
emocromatosi in caso di mutazioni C282Y)
• Forma clinicamente severa =2A
CARATTERISTICHE CLINICHE
DELL’EMOCROMATOSI EREDITARIA: TIPO 2a e 2b
•
Localizzazione cuore, apparato endocrino, fegato
•
Sintomi e segni clinici esordio dopo i 10 anni; dolore addominale,
ipogonadismo ipogonadotropo, aritmie e insufficianza cardiaca
intrattabile, ridotta tolleranza glucidica; transferrina e ferritina.
•
Manifestazione clinica principale cardiopatia, ipogonadismo, diabete
•
Accumulo di Fe epatociti, cuore, ghiandole endocrine, muscolo
scheletrico
•
Decorso clinico estremamente severo
•
Risposta a salassoterapia aggressiva buona
CLASSIFICAZIONE GENETICA
DELL’EMOCROMATOSI EREDITARIA
TIPO
EREDITA’
GENE / LOCUS
1 (tipico)
AR
HFE / 6p21
PROTEINA / FUNZIONE
HFE/
Interazione con TfR1; Cofattore trascrizione di epcidina
2A
AR
HJV / 1q21
Emojuvelina /
Corecettore trascrizione di epcidina
2B
AR
HAMP / 19q13
Epcidina /
Ritenzione di Fe in macrofagi, enterociti e placenta
3
AR
TfR2 / 7q22
Transferrina-R2 /
Captazione di transferrina coniugata con Fe
Corecettore trascrizione di epcidina
4
AD
SCL40A1 / 2q32
Ferroportina /
Fuoriuscita di Fe da macrofagi, enterociti, epatociti, placenta
GENE TfR2
3
• Mutazioni TfR2 – cromosoma 7 (7q22)
• Proteina TfR2 espressa soprattutto dal fegato con affinità per Fe < rispetto
al comune recettore TfR (a livello delle cripte intestinali si ritiene
interferisca con HFE nel segnalare i livelli di Fe circolante)
• Fenotipicamente simile a HH-1, ma generalmente + severa e ad insorgenza +
precoce ; popolazioni mediterranee
CARATTERISTICHE CLINICHE
DELL’EMOCROMATOSI EREDITARIA: TIPO 1 E 3
•
Localizzazione fegato, apparato endocrino, cuore
•
Sintomi e segni clinici esordio dopo i 40 anni; astenia, artralgie,
impotenza, inferitilità, epatomegalia, diabete mellito, pigmentazione
cutanea, cirrosi, scompenso cadiaco, aritmie; transferrina e ferritina.
•
Manifestazione clinica principale epatopatia
•
Accumulo di Fe epatociti
•
Decorso clinico moderato per il tipo 1, severo per il tipo 3
•
Risposta a salassoterapia buona
CLASSIFICAZIONE GENETICA
DELL’EMOCROMATOSI EREDITARIA
TIPO
EREDITA’
GENE / LOCUS
1 (tipico)
AR
HFE / 6p21
PROTEINA / FUNZIONE
HFE/
Interazione con TfR1; Cofattore trascrizione di epcidina
2A
AR
HJV / 1q21
Emojuvelina /
Corecettore trascrizione di epcidina
2B
AR
HAMP / 19q13
Epcidina /
Ritenzione di Fe in macrofagi, enterociti e placenta
3
AR
TfR2 / 7q22
Transferrina-R2 /
Captazione di transferrina coniugata con Fe
Corecettore trascrizione di epcidina
4
AD
SCL40A1 / 2q32
Ferroportina /
Fuoriuscita di Fe da macrofagi, enterociti, epatociti, placenta
GENE FERROPORTINA
4
• Mutazioni Ferroportina (FPN1) (iron exporter) – cromosoma 2 (2q32)
• Proteina FPN1 espressa da epatociti e macrofagi – se mutata “sigilla” Fe
all’interno dei macrofagi Fe circolante assorbimento intestinale
• Fenotipicamente caratterizzata da ferritina (accumulo di Fe nei macrofagi
con relativo risparmio degli epatociti) e o normali livelli di transferrina –
4/1: saturazione di transferrina e deposito epatocitario –
4/2: (+ frequente) saturazione di trasferrina e minimo interessamento
epatocitario con andamento clinico benigno
• Caucasici, Asiatici, Africani
EMOCROMATOSI NON-HFE – 4
Mutazione del gene per la ferroportina (FPN1)
• efflusso di Fe dai macrofagi
• Fe intratissutale ( Ferritina)
• Fe circolante ( sat transferrina)
L’assorbimento intestinale di Fe è normale
CARATTERISTICHE CLINICHE
DELL’EMOCROMATOSI EREDITARIA: TIPO 4
•
Localizzazione (fegato) milza
•
Sintomi e segni clinici esordio dopo i 40 anni; sintomi simili al tipo 1
+ anemia lieve; ferritina >> transferrina.
•
Manifestazione clinica principale epatopatia
•
Accumulo di Fe cellule reticolo-endoteliali
•
Decorso clinico lieve
•
Risposta al salasso scarsa
OMEOSTASI DEL Fe IN CONDIZIONI NORMALI
Eritrociti circolanti
2500 mg
Emolisi
(monociti/macrofagi):
20 mg/die
Assorbimento
(intestino)
1-2 mg/die
Eritropoiesi
(midollo osseo)
20 mg/die
Pool plasmatico
4 mg
Deposito corporeo totale
macrofagi tessutali, epatociti : 4g
(fegato: 300mg –1g)
Eliminazione
(intestino)
1-2 mg/die
METABOLISMO DEL Fe NELL’EMOCROMATOSI
Eritrociti circolanti
Fe: 2500 mg
Monociti/macrofagi
Fe: 20 mg/die
Intestino
Assorbimento
Fe: 3-5 mg/die
Midollo osseo
Eritropoiesi
Fe: 20 mg/dì
Pool plasmatico
Deposito corporeo totale Fe:
25 –30 g
Intestino
Eliminazione
Fe: 2-3 mg/die
ALGORITMO DIAGNOSTICO NEL SOSPETTO DI EMOCROMATOSI EREDITARIA (EE)
Sat. Transferrina (>45%)
Ferritina
Escludere malattie epatiche o ematologiche ed
altre cause (flogosi cronica, infezioni)
Test genetici: mutazione
C282Y e H63D
• Omozigosi C282Y
• C282Y / H63D
• C282Y eterozigosi
H63D eterozigosi/omozigosi
• No mutazioni HFE
Ferritina < 500g/L
Follow-up
EE tipo 1
Ferritina >500 g/L
Ferritina >1000 g/L
e/o GOT-GPT
RM (Fe epatico)
Nella norma
Fe
NO- HFE-EE
NO- EE
epcidina / ferritina ratio
Biopsia epatica: Fe
CEF>4000 g/g di peso secco
IEF>1.9 (CEF/età)
Salasso ( ferritina = 50g/L)
Valutazione genetica
Studi sulla famiglia
Follow-up
EE tipo 2-4
NO-EE tipo 2-4
Test tipo 4
Test tipo 3
Test tipo 2a/2b